QUMICA Conceptos Fundamentales Temas a desarrollar Conceptos de














- Slides: 17

QUÍMICA Conceptos Fundamentales

Temas a desarrollar Conceptos de: n n n n n Átomos Moléculas uma Peso Atómico Peso Molecular Mol Número de Avogadro Volumen Molar Fórmulas: Molecular, Estructural, Desarrollada

Átomo Es la menor porción de materia capaz de combinarse para formar moléculas

Molécula Es la partícula más pequeña de una sustancia (simple o compuesta), formada por átomos que puede existir libre y presenta todas las propiedades de dicha sustancia

Clasificación de las Moléculas MOLÉCULAS SIMPLES Monoatómicas Biatómicas Poliatómicas COMPUESTAS

Molécula Simple Monoatómica Ej. : Helio

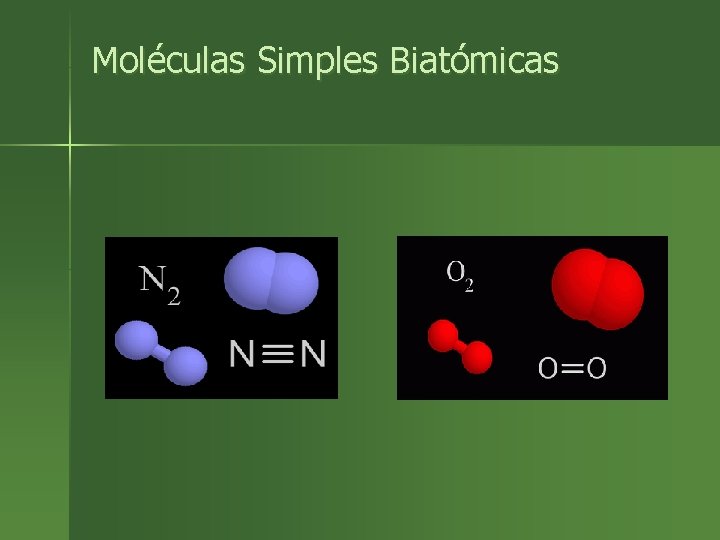
Moléculas Simples Biatómicas

Moléculas Simples Poliatómicas n Ej. : Fósforo

Moléculas Compuestas Ejemplos: Agua Bicarbonato de Sodio Amoníaco

Atomicidad Es el número de átomos que contiene la molécula de una sustancia Formas de representación de moléculas

Fórmulas n Fórmula Molecular: Indica el número real de átomos presentes en una molécula. n Fórmula Estructural: Permite distinguir la posición de los átomos en el espacio mediante gráficos que simulan figuras tridimensionales. n Fórmula Desarrollada: Esclarece el tipo de enlace entre los distintos átomos dentro de la molécula.

Masa o Peso Atómico Es la cantidad de materia que constituye un átomo. Se representa con la letra A. PA = Masa absoluta del elemento UMA

Unidad de Masa Atómica Es la doceava parte de la masa del átomo del carbono. u. m. a. = masa del átomo de C 12 12

Masa o Peso Molecular La masa de una molécula es igual a la suma de las masas de los átomos que la constituyen. Se representa con la letra M. Fe O 2 H 2 O HNO 3

Número de Avogadro: Es la cantidad de partículas elementales que existen en un mol de cualquier sustancia 23 Número de Avogadro = 6, 023 x 10

Mol Es la cantidad de una sustancia que contiene exactamente 6, 023 x 10 23 partículas elementales

Volumen Molar: Es el volumen ocupado por un mol de moléculas de cualquier sustancia en estado gaseoso y en CNTP. Su valor es 22, 4 L. 1 mol de moléculas = 6, 02 x 1023 moléculas = 22, 4 L