QUMICA BIOLGICA PROPIEDADES DEL AGUA Y SOLUCIONES 4

QUÍMICA BIOLÓGICA PROPIEDADES DEL AGUA Y SOLUCIONES 4º QUÍMICA ESCUELA ORT

Propiedades del agua ● Es líquida en un amplio rango de temperaturas (0 - 100º C). Permite que pueda existir vida en zonas con diferentes condiciones climáticas. ● �� = 1 g/m. L. El hielo tiene menor densidad y flota en el agua líquida. ● Dipolo: disolución de sales, solvatación de moléculas polares.

Propiedades de las soluciones El soluto modifica las propiedades que tenía el solvente puro: densidad, color, p. H. Algunas propiedades no se deben a la naturaleza del soluto y del número de partículas disueltas: propiedades coligativas.

Propiedades coligativas ● DESCENSO CRIOSCÓPICO La temperatura de fusión de un sólido puro es mayor que la temperatura de fusión de un sólido impuro. Ejemplos: Pf agua de mar = -2º C Pf leche = 0, 5º C Anticongelante para el auto?

Propiedades coligativas ● DESCENSO DE LA PRESIÓN DE VAPOR La presión de vapor es la presión que ejerce la fase gaseosa sobre la fase líquida. Aumenta con la temperatura. Evaporación: es el proceso del pasaje de la fase líquida a la fase gaseosa. Ebullición: ocurre cuando la presión de vapor de un líquido iguala a la presión atmosférica.
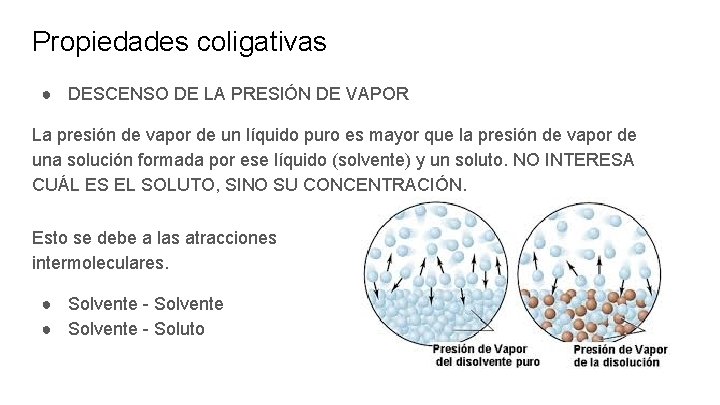
Propiedades coligativas ● DESCENSO DE LA PRESIÓN DE VAPOR La presión de vapor de un líquido puro es mayor que la presión de vapor de una solución formada por ese líquido (solvente) y un soluto. NO INTERESA CUÁL ES EL SOLUTO, SINO SU CONCENTRACIÓN. Esto se debe a las atracciones intermoleculares. ● Solvente - Solvente ● Solvente - Soluto

Propiedades coligativas ● ASCENSO EBULLOSCÓPICO La temperatura de ebullición de un líquido puro es menor que la temperatura de ebullición de un líquido impuro. Ejemplos: Almíbar punto hilo: 105 -110º C Almíbar punto bola: 116 -119º C
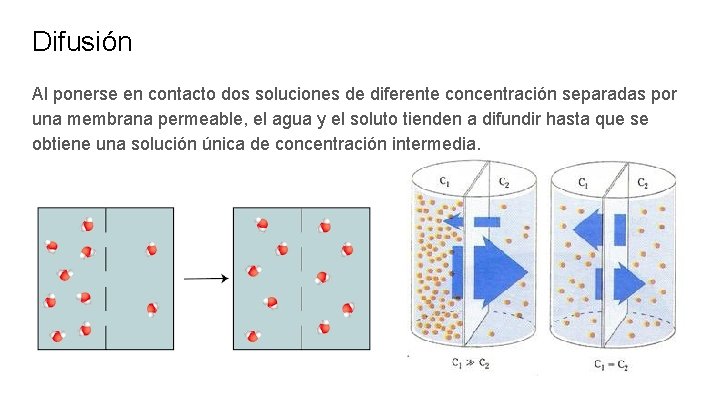
Difusión Al ponerse en contacto dos soluciones de diferente concentración separadas por una membrana permeable, el agua y el soluto tienden a difundir hasta que se obtiene una solución única de concentración intermedia.
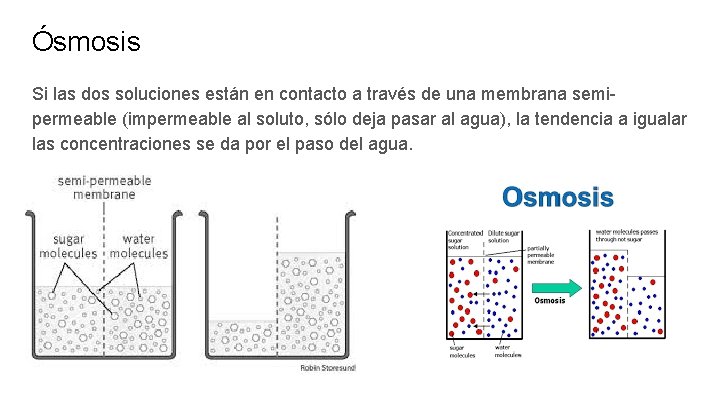
Ósmosis Si las dos soluciones están en contacto a través de una membrana semipermeable (impermeable al soluto, sólo deja pasar al agua), la tendencia a igualar las concentraciones se da por el paso del agua.
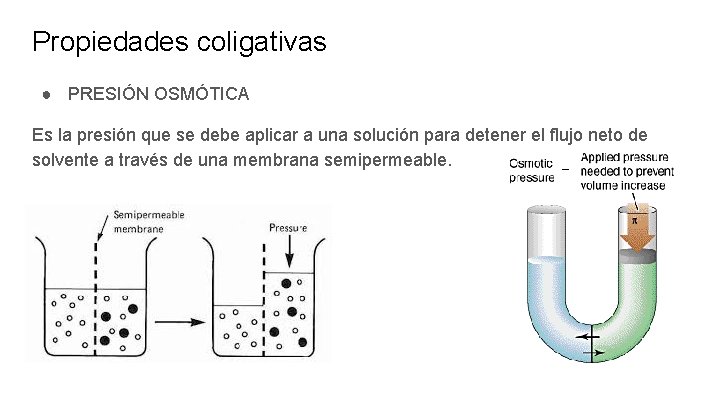
Propiedades coligativas ● PRESIÓN OSMÓTICA Es la presión que se debe aplicar a una solución para detener el flujo neto de solvente a través de una membrana semipermeable.

Tonicidad ● Medio isotónico: una solución es isotónica respecto a una célula cuando tiene la misma concentración de solutos que dicha célula. ● Medio hipotónico: una solución es hipotónica respecto a una célula cuando tiene menor concentración de solutos que dicha célula. ● Medio hipertónico: una solución es hipertónica respecto a una célula cuando tiene mayor concentración de solutos que dicha célula.
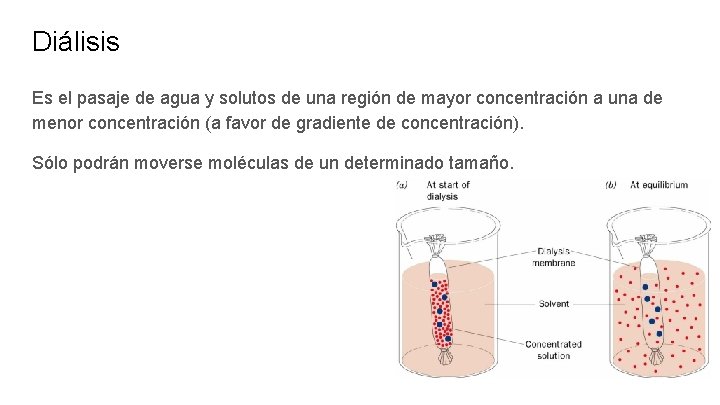
Diálisis Es el pasaje de agua y solutos de una región de mayor concentración a una de menor concentración (a favor de gradiente de concentración). Sólo podrán moverse moléculas de un determinado tamaño.
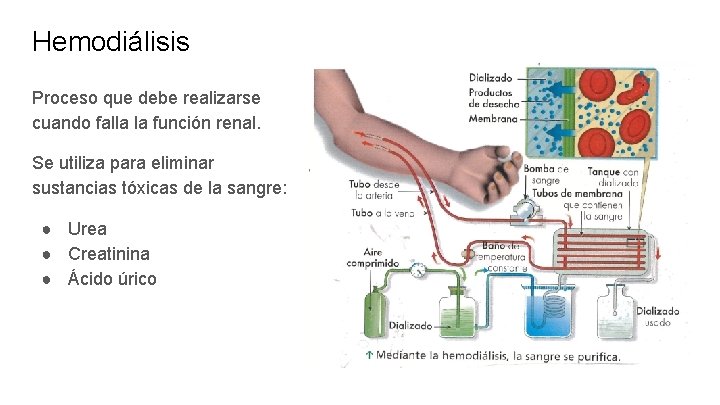
Hemodiálisis Proceso que debe realizarse cuando falla la función renal. Se utiliza para eliminar sustancias tóxicas de la sangre: ● Urea ● Creatinina ● Ácido úrico
- Slides: 13