Qumica Biolgica Patolgica Tcnicas de Biologa Molecular aplicadas

Química Biológica Patológica Técnicas de Biología Molecular aplicadas a Bioquímica Clínica 2016 Tema 2 Dra. Silvia Varas curso. tecmol@gmail. com

Tema 2 PCR n Historia n Bases n Optimización de una reacción de PCR n

APLICACIONES DE PCR n n n n MUTAGENESIS RT-PCR PRODUCCION DE SONDAS DETECCIÓN DE INFECCIONES BACTERIANAS Y VIRALES DIAGNÓSTICO DE ENFERMEDADES HEREDITARIAS ESTUDIOS DE EVOLUCIÓN MOLECULAR ESTUDIOS DE MEDICINA FORENSE ESTUDIOS DE FILIACIÓN

n Un poco de historia…



n n n La reacción en cadena de la polimerasa (PCR): no fué un descubrimiento pero fué mas que una invención Una ADN polimerasa especial (Taq) es usada para hacer muchas copias de una corta longitud de ADN (0, 1 -10 Kb) y que esta definida por cebadores o primers Kary Mullis, el inventor de la PCR fue premiado en 1993 con el Premio Nobel en Química


Camino Biotecnológico Life at High Temperatures by Thomas D. Brock Biotechnology in Yellowstone © 1994 Yellowstone Association for Natural Science nhttp: //www. bact. wisc. edu/Bact 303/b 27 En el año 1960, el microbiólogo Dr. n n n Steamboat Geyser: Thermus aquaticus Taq DNA polymerase Thomas Brock viaja al Parque Yellowstone National (Wyoming) para investigar a los microorganismos termófilos que viven en el calor de los géiser. El descubrió una bacteria de la especie de la Eubacterias que vivía a altas temperaturas en los géiser Barco de vapor (Steamboat Geyser) del parque: Thermus aquaticus En 1976 se purificó la Taq DNA polymerasa desde Thermus aquaticus. En 1983 la empresa Cetus Corporation patentó la técnica y el uso de la enzima DNA polimerasa de Thermus aquaticus y sentó las bases para el desarrollo de esta tecnología Hubo en paralelo un desarrollo de un blocks de calentamiento programables (termocicladores)

Termocicladores para PCR

CUIDADOS!
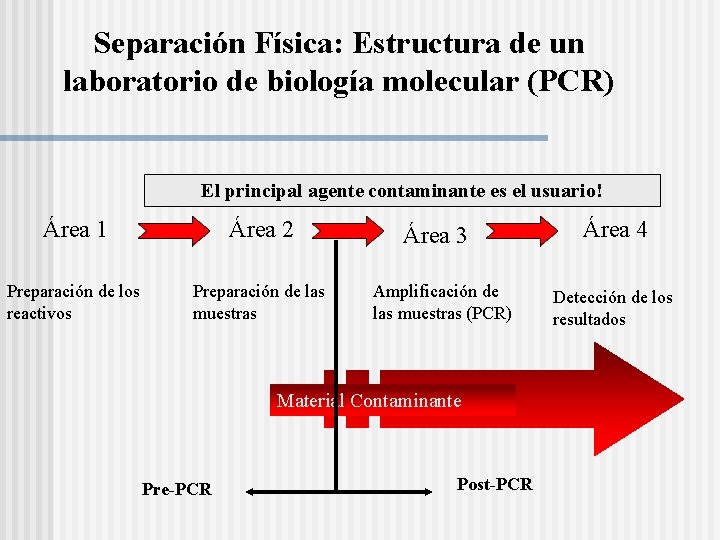
Separación Física: Estructura de un laboratorio de biología molecular (PCR) El principal agente contaminante es el usuario! Área 1 Área 2 Preparación de los reactivos Preparación de las muestras Área 3 Amplificación de las muestras (PCR) Material Contaminante Pre-PCR Post-PCR Área 4 Detección de los resultados
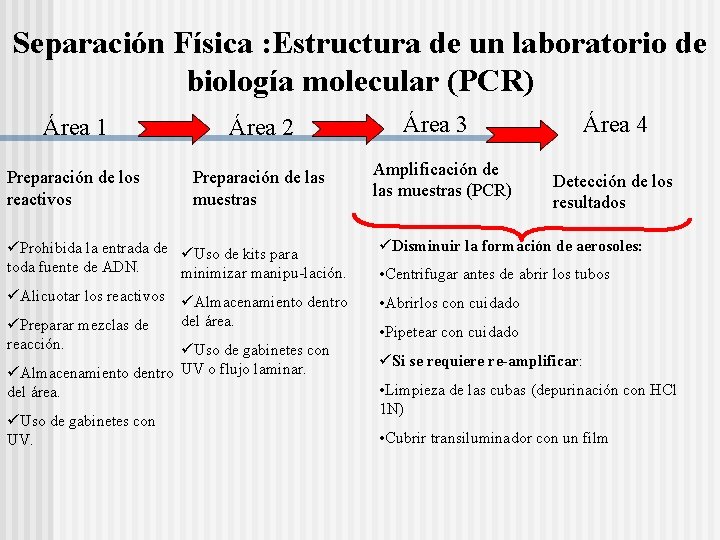
Separación Física : Estructura de un laboratorio de biología molecular (PCR) Área 1 Área 2 Preparación de los reactivos Preparación de las muestras üProhibida la entrada de üUso de kits para toda fuente de ADN. minimizar manipu-lación. üAlicuotar los reactivos üAlmacenamiento dentro üPreparar mezclas de reacción. del área. üUso de gabinetes con üAlmacenamiento dentro UV o flujo laminar. del área. üUso de gabinetes con UV. Área 3 Amplificación de las muestras (PCR) Área 4 Detección de los resultados üDisminuir la formación de aerosoles: • Centrifugar antes de abrir los tubos • Abrirlos con cuidado • Pipetear con cuidado üSi se requiere re-amplificar: • Limpieza de las cubas (depurinación con HCl 1 N) • Cubrir transiluminador con un film

Contaminación: Riesgos y Mecanismos ü Cuando la PCR se realiza en un laboratorio común(sin sala separadas para cada etapa). ü No existe un conjunto de pipetas dedicadas a cada etapa (preparación, PCR, análisis). ü Uso de material no estéril o contaminado. ü Formación de aerosoles (pipeteo o centrifugación). ü Contaminación humana (secreciones, saliva, cabellos, etc. ) ü Arrastre de muestra o carryover.

Control de Contaminación Buenas prácticas de laboratorio Movimiento unidireccional (no transportar elementos de post a pre PCR). Uso de elementos específicos para cada área. Uso de consumibles de alta calidad Uso de tips con filtro o de desplazamiento positivo. Evitar el uso de baños de agua o de hielo.

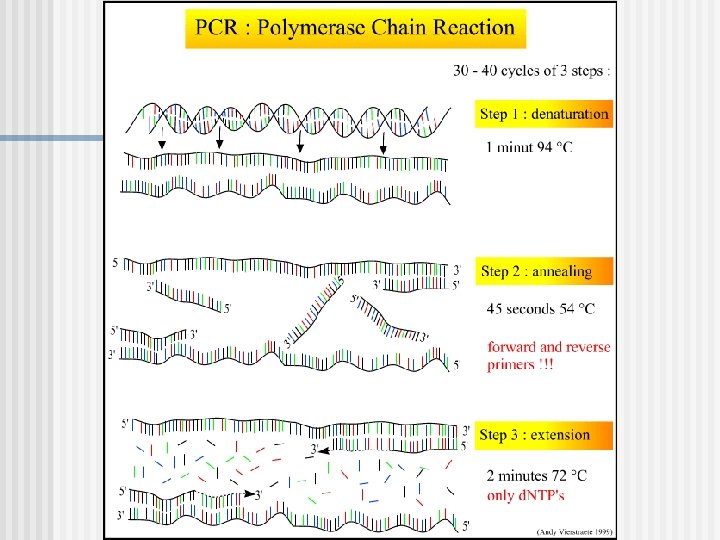
El ciclo de amplificación de PCR Cada ciclo requiere tres pasos de temperaturas para completar un ronda de la síntesis de ADN.
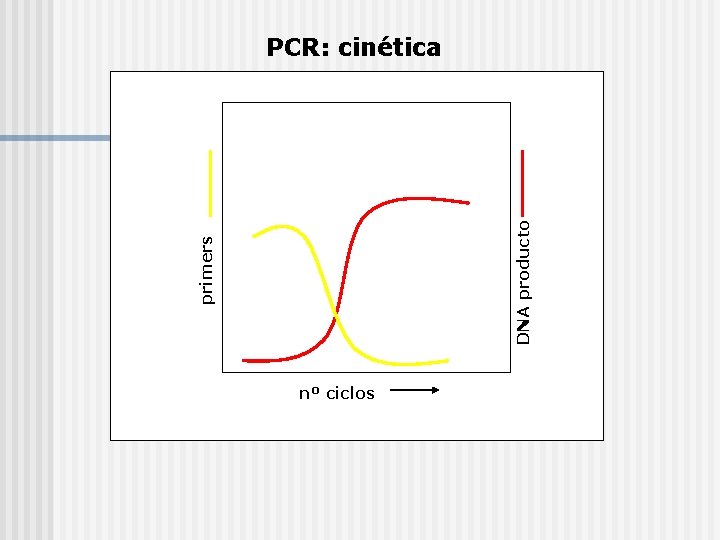
primers DNA producto PCR: cinética nº ciclos
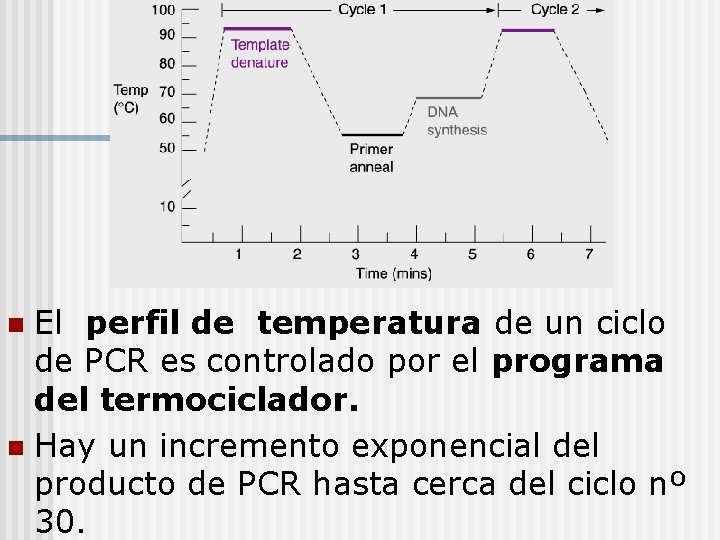
El perfil de temperatura de un ciclo de PCR es controlado por el programa del termociclador. n Hay un incremento exponencial del producto de PCR hasta cerca del ciclo nº 30. n
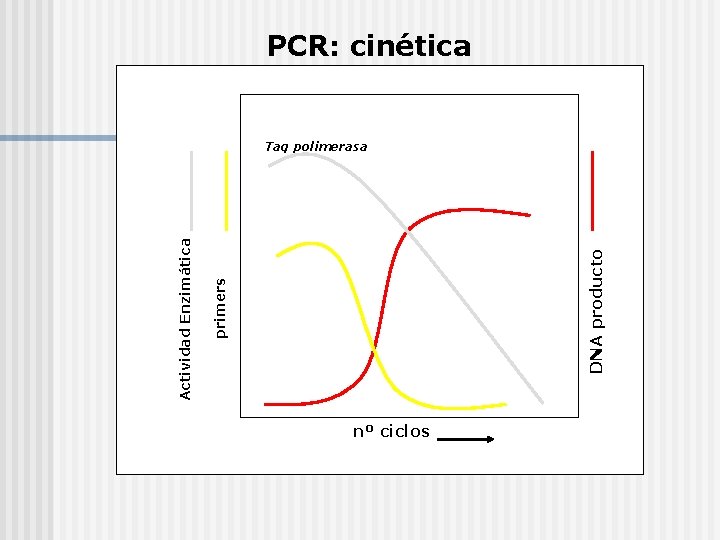
DNA producto primers Actividad Enzimática PCR: cinética Taq polimerasa nº ciclos
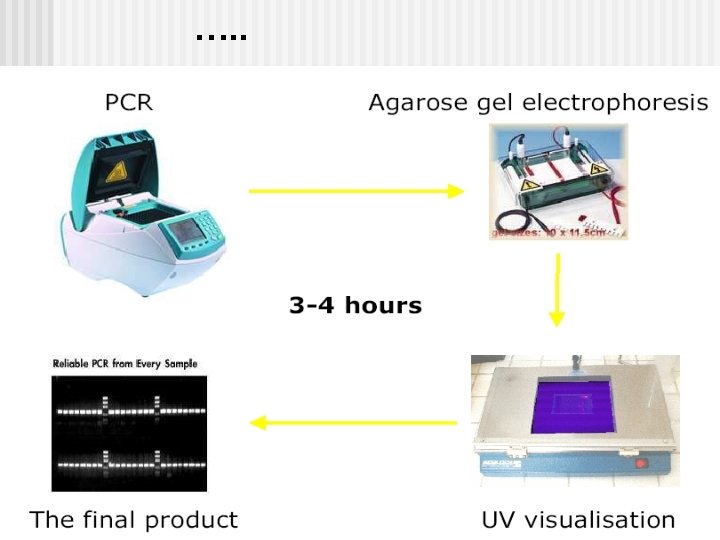

n. PCR: PRINCIPIOS

La Reacción en Cadena de la Polimerasa (PCR) n PCR es una técnica la cual es usada para amplificar un numero de copias de una región específica del ADN hasta producir una cantidad de ADN que sea adecuadamente testeada. n El propósito de la PCR es hacer un alto número de copias de un gen. Como resultado es posible y caracterizar fragmentos de ADN hallados en una gota de sangre, en una escena de crimen o de un dinosaurio extinguido.

Definición n PCR es un sistema no celular de clonado del ADN Es un método de amplificación selectiva de secuencia específicas. A partir de una población heterogénea de moléculas, como puede ser ADN genómico o c. DNA. PCR es un proceso de replicación in vitro.

Ventajas y Desventajas VENTAJAS: Rapidez Sensibilidad Fortaleza n DESVENTAJA DE PCR COMO METODO DE CLONADO: Se debe conocer la secuencia Producto generalmente pequeño Infidelidad de la replicación del ADN n

CONCEPTOS BASICOS: n EFICIENCIA: MAXIMA PRODUCCION DE AMPLIFICACION EN FUNCION DEL NUMERO DE CICLOS n ESPECIFICIDAD: GENERACION DE UN UNICO PRODUCTO DE AMPLIFICACION n FIDELIDAD: NUMERO DE ERRORES QUE COMETE LA DNA POLIMERASA DURANTE LA COPIA n SENSIBILIDAD: MINIMA CANTIDAD DE DNA QUE SE NECESITA PARA OBTENER UNA GRAN CANTIDAD DE COPIAS
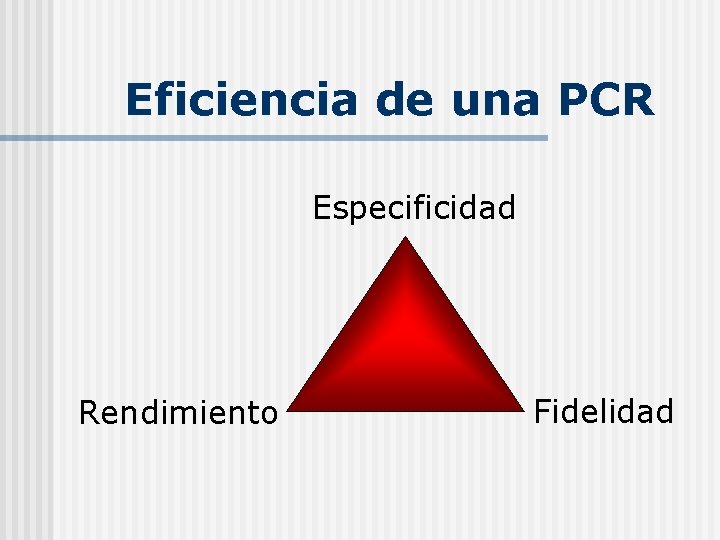
Eficiencia de una PCR Especificidad Rendimiento Fidelidad

Fidelidad vs Eficiencia Infidelidad: n Errores cometidos por la enzima: Eficiencia: n Taq pol 1 error / 2 x 104 pb incorporadas 88 % n Tli pol (Thermococcus litoralis) 1 error/ 4 x 105 pb incorporadas 70% n Pfu pol (Pyrococcus furiosus): 1 error/ 7 x 107 pb incorporadas 60% n In vivo ADN polimerasa: 1 error/ 3 x 109 pb incorporadas fidelidad eficiencia Procesividad Tiempo de extensión: Taq polimerasa: 2 Kb/min Tli polimerasa: 1 Kb/min Pfu polimerasa: 0. 5 Kb/ min

PCR En un tubo de PCR con una mezcla de DNA genómico, DNA polimerasa, buffer, nucleósido trifosfatos y primers Termociclador
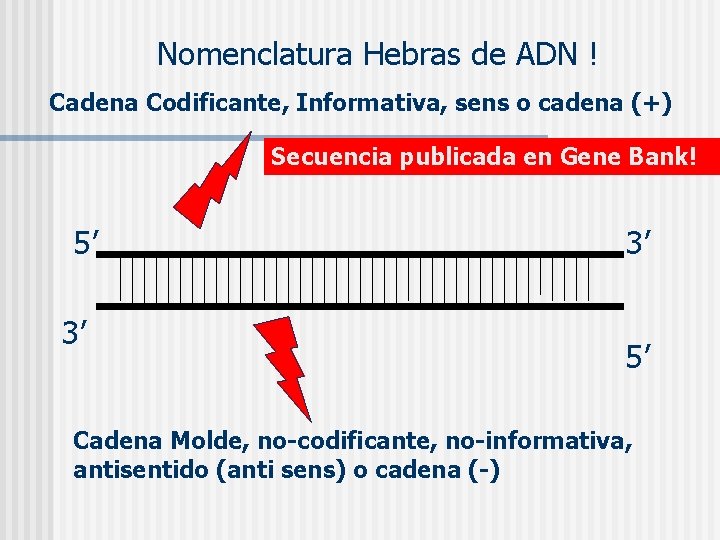
Nomenclatura Hebras de ADN ! Cadena Codificante, Informativa, sens o cadena (+) Secuencia publicada en Gene Bank! 5’ 3’ 3’ 5’ Cadena Molde, no-codificante, no-informativa, antisentido (anti sens) o cadena (-)
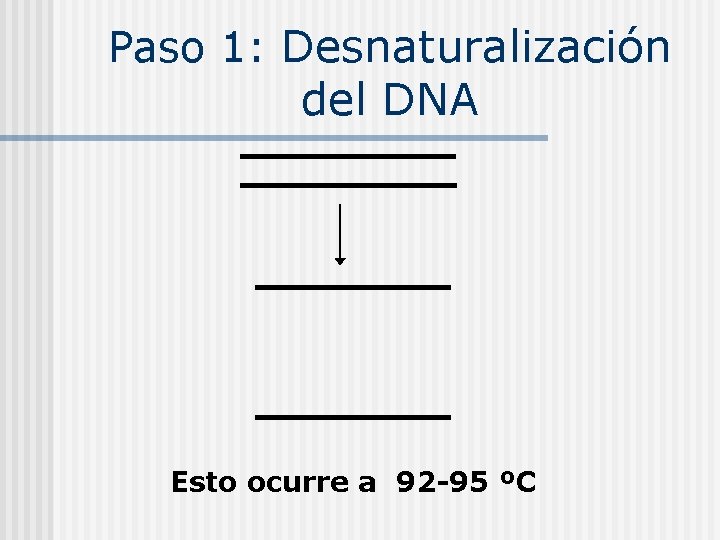
Paso 1: Desnaturalización del DNA Esto ocurre a 92 -95 ºC
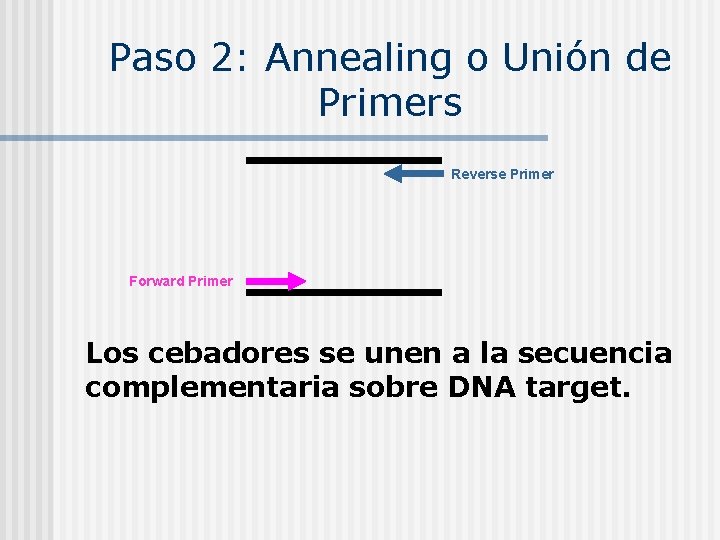
Paso 2: Annealing o Unión de Primers Reverse Primer Forward Primer Los cebadores se unen a la secuencia complementaria sobre DNA target.
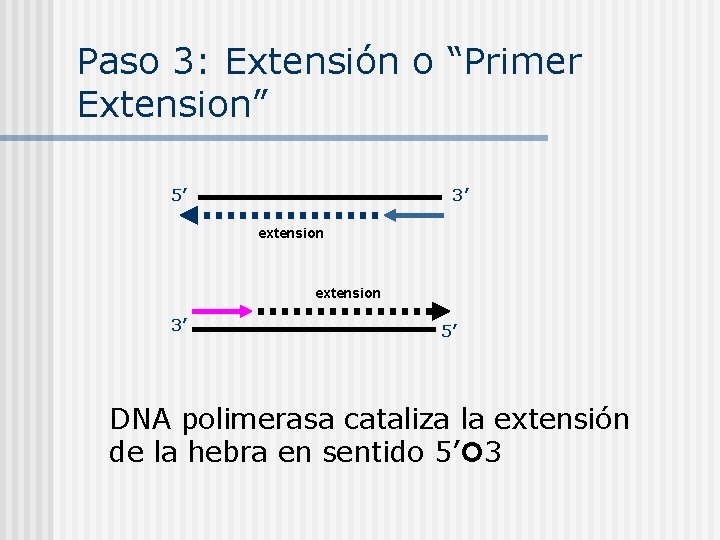
Paso 3: Extensión o “Primer Extension” 5’ 3’ extension 3’ 5’ DNA polimerasa cataliza la extensión de la hebra en sentido 5’ 3
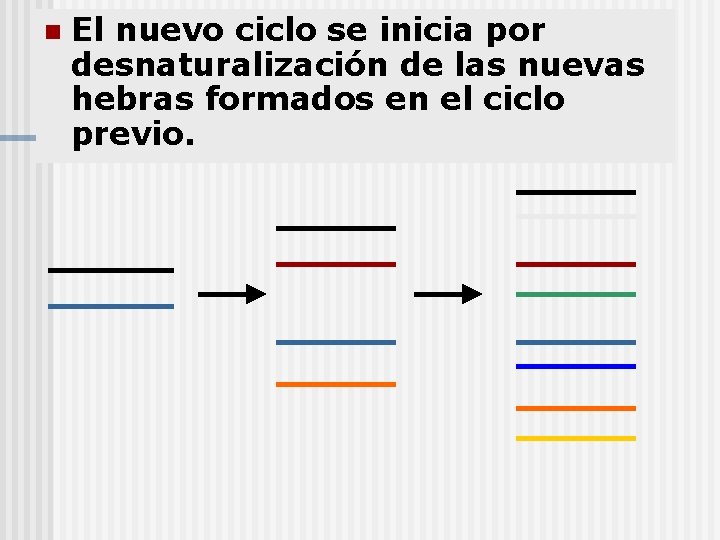
n El nuevo ciclo se inicia por desnaturalización de las nuevas hebras formados en el ciclo previo.
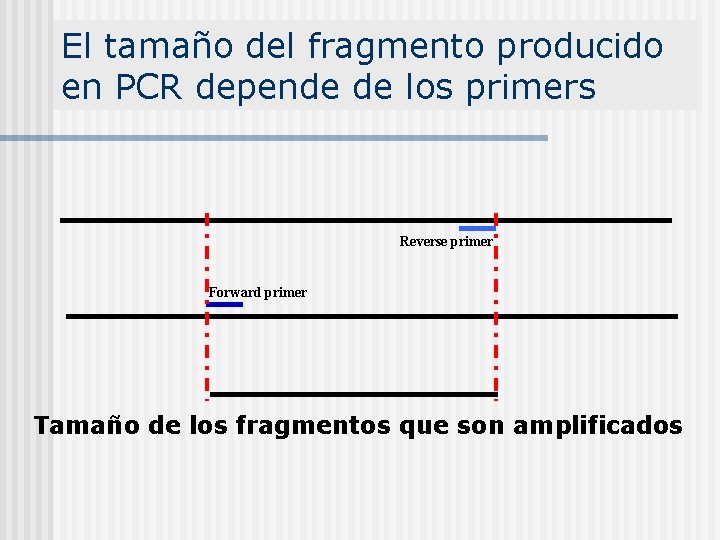
El tamaño del fragmento producido en PCR depende de los primers Reverse primer Forward primer Tamaño de los fragmentos que son amplificados

Elementos de una PCR especifica 1) 2) 3) 4) 5) 6) 7) 8) Calidad Templado Concentración Enzima Secuencia Iniciadores Concentración, pureza y estabilidad Temperatura de anneling Concentración de Magnesio Concentración de Nucleótidos Condiciones del medio: Buffer, p. H, etc. Aditivos: Formamida, DMSO, glicerol, etc.


1)Templado ADN genómico n n CALIDAD: CONCENTRACION: 10 pg-1μg Templados: Sangre, sangre seca, exudado vaginal, cabellos, frotis nasofaríngeo, etc.

2) Enzima

DNA Polimerase de Taq (Thermus aquaticus ) n Esta enzima tolerante al calor y sobrevive a los distintos ciclos de desnaturalización
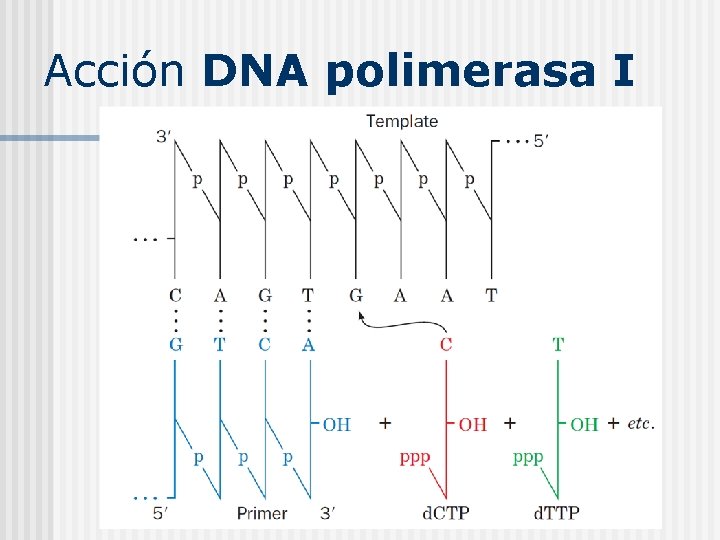
Acción DNA polimerasa I

DNA polimerasas termoestables: características n Procesividad: Actividad de polimerasa 5’ 3’ actividad de síntesis n Fidelidad: Actividad 3’ 5’ exonucleasa (correctora) n Actividad de Transferasa Terminal: Agrega un nucleótido de adenina (A) en extremo 3’. n (-) actividad transferasa terminal: extremos romos (blunt) 5’ 3’ A A 3’ 5’
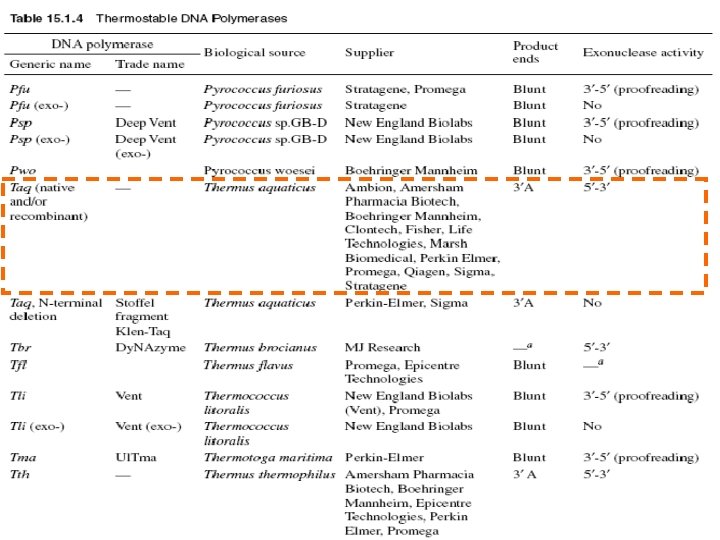
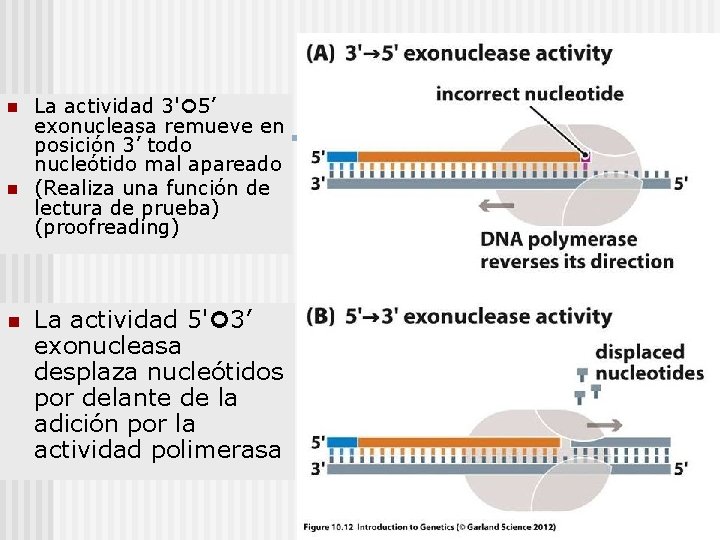
n n n La actividad 3' 5’ exonucleasa remueve en posición 3’ todo nucleótido mal apareado (Realiza una función de lectura de prueba) (proofreading) La actividad 5' 3’ exonucleasa desplaza nucleótidos por delante de la adición por la actividad polimerasa
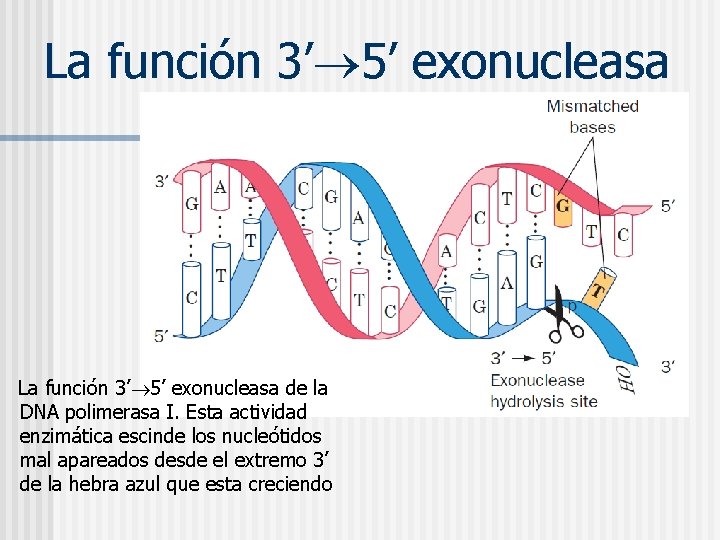
La función 3’ 5’ exonucleasa de la DNA polimerasa I. Esta actividad enzimática escinde los nucleótidos mal apareados desde el extremo 3’ de la hebra azul que esta creciendo
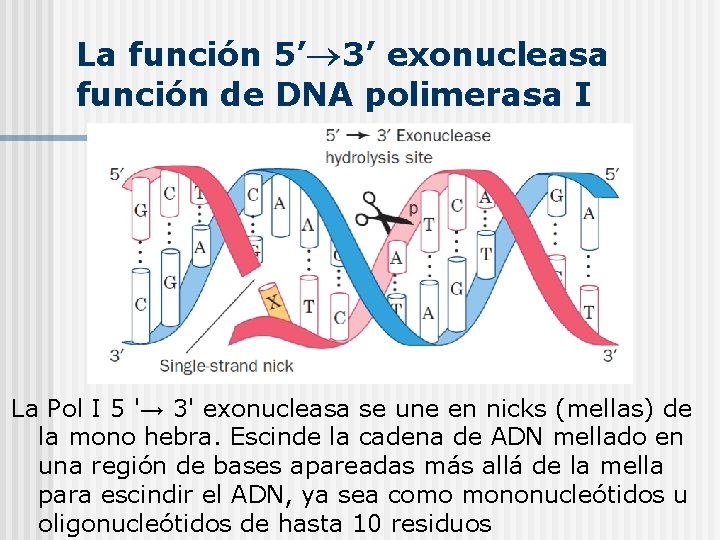
La función 5’ 3’ exonucleasa función de DNA polimerasa I La Pol I 5 '→ 3' exonucleasa se une en nicks (mellas) de la mono hebra. Escinde la cadena de ADN mellado en una región de bases apareadas más allá de la mella para escindir el ADN, ya sea como mononucleótidos u oligonucleótidos de hasta 10 residuos

n La actividad 3' 5’ exonucleasa (proofreading) In vivo 1 base en 3 x 109 nt es copiado incorrectamente

Diferencias entre 2 polimerasas n n Velocidad de síntesis n Termoestabilidad n n Taq Mas rápida (2000 nt/min) n Menos de 1 h a 95ºC n n n Pfu Más lenta (500 nt/min) Vida media 18 -25 h a 95ºC 98ºC GC
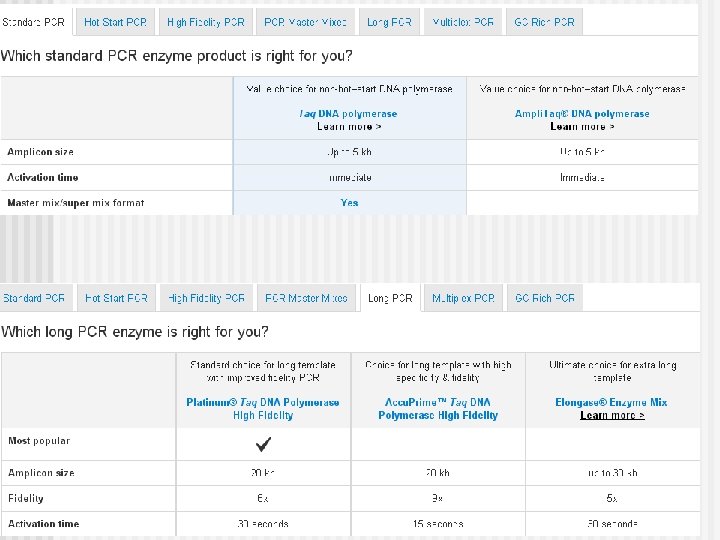

3) Elección de los Primers o Iniciadores I 1. Tamaño: generalmente cerca de 20 nt. Si son muy largos problemas annealing y inespecificos. 2. Tº de anneling semejante 3. Tm= 4(G+C) + 2 (A+T) ºC 4. Evitar repeticiones, buscar regiones con una distribución homogeneas de bases 5. Contenido de GC (40 -60%) 6. Elección de primers para c. DNA

3) Elección de los Primers o Iniciadores II 7. Elegir iniciadores con residuos G o C en 3’ o en la zona central 8. Evitar secuencias complementarias en el extremo 3’ 9. Evitar secuencias que formen estructuras secundarias. 10. CONCENTRACION : 20 -50 p. M/ul 11. Proporción molecular: Iniciadores/ADN molde = 108: 1 12. Si es disminuye la eficiencia 13. Si es disminuye el rendimiento
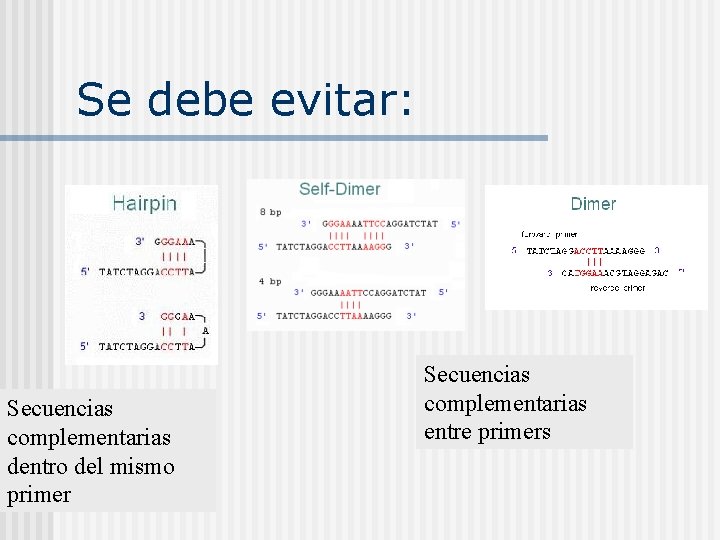
Se debe evitar: Secuencias complementarias dentro del mismo primer Secuencias complementarias entre primers

3) Primers o Iniciadores: Resumen 1. Específicos de la secuencia de interés 2. Longitud 18 -30 nucleótido 3. Tº Annealing 50 o. C-70 o. C Idealmente 58 o. C-63 o. C 4. GC contenido 40 -60% 5. Extremo 3’ critico G o C en extremo 3’ terminal aumenta la eficiencia de la reacción. 4. Secuencia Complementarias entre si mismas y con otros Hairpins <5, dimers <9

4) Temperatura de anneling n n n Temperatura de Annealing: Tmprimer = ∆H [∆S+ R ln (c/4)] – 273. 15°C + 16. 6 log 10 [K+] H: entalpia, S entropia para la formación helix; R constante molar y c es la concentración primer Tm = 4(G + C) + 2(A + T)o. C n Para 18– 24 bases ~ 5 o. C menos que la Tm de los primers en la tº anneling resulta en una union noespecífica. en la tº annealing resulta en reducción en el rendimiento

G: · 3 ; A: 11 C: 5 T: 7 ; TOTAL= 26 nt Tm= 4. 8+2. 18=32+36=68ºC
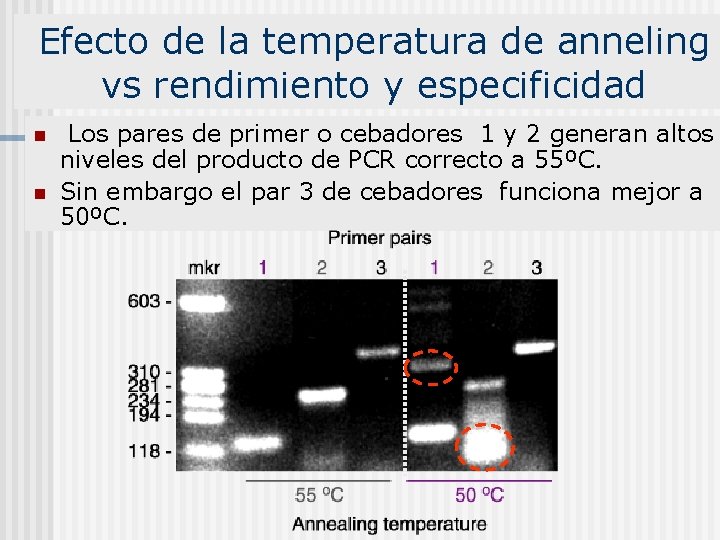
Efecto de la temperatura de anneling vs rendimiento y especificidad n n Los pares de primer o cebadores 1 y 2 generan altos niveles del producto de PCR correcto a 55ºC. Sin embargo el par 3 de cebadores funciona mejor a 50ºC.

RESUMEN: n n n n n LONGITUD DE 18 a 24 nucleótidos ESPECIFICOS Tm = 55 a 75 C, CON Tm SIMILARES ENTRE SI DISEÑAR PRIMERS CON CANTIDAD APROXIMADAMENTE 50% DE GC Y DISTRIBUCION AL AZAR EVITAR PRIMERS CON SECUENCIAS DE POLIPURINAS Y/O POLIPIRIMIDINAS (Poly GC: DISMINUYE ESPECIFICIDAD Poly AT: DISMINUYE EFICIENCIA) EVITAR SECUENCIAS QUE FORMEN ESTRUCTURAS SECUNDARIAS CONTROLAR QUE LOS PRIMERS NO HIBRIDICEN ENTRE SI EVITAR MAS DE 3 CG SEGUIDAD EN EL EXTREMO 3´ COMENZAR Y TERMINAR CON PURINAS EXISTEN PROGRAMAS PARA DISEÑO DE PRIMERS
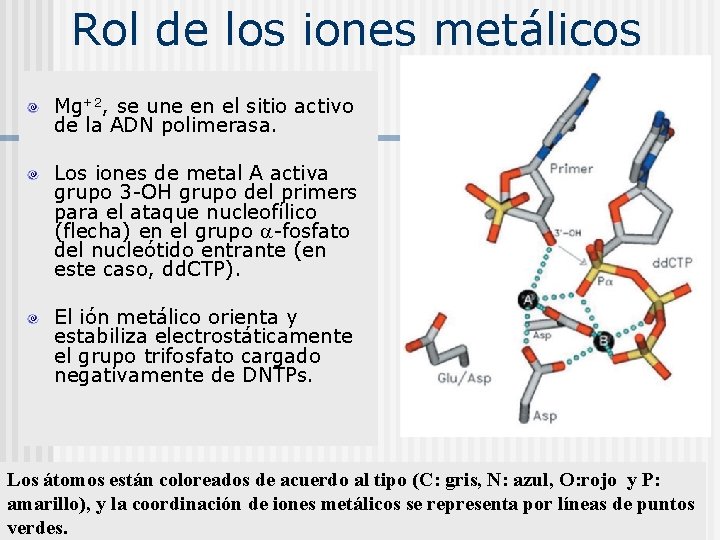
Rol de los iones metálicos Mg+2, se une en el sitio activo de la ADN polimerasa. Los iones de metal A activa grupo 3 -OH grupo del primers para el ataque nucleofílico (flecha) en el grupo -fosfato del nucleótido entrante (en este caso, dd. CTP). El ión metálico orienta y estabiliza electrostáticamente el grupo trifosfato cargado negativamente de DNTPs. Los átomos están coloreados de acuerdo al tipo (C: gris, N: azul, O: rojo y P: amarillo), y la coordinación de iones metálicos se representa por líneas de puntos verdes.

5) Concentración de Mg 2+ 1. Importante para la actividad de la enzima. 2. Debe hacerse una curva de titulación 1 -3 m. M con incrementos de 0, 5 m. M. 3. Mg. Cl 2: se requiere para la unión del primer

5) Concentración de Mg 2+ - II n Mg. Cl 2 afecta la union de los cebadores, Tm del templado del ADN, actividad de la enzima y fidelidad n Los d. NTPs, cebadores y el templado quelan y secuestran ion Mg su concentración debe ser mayor que los d. NTPs n Exceso de Mg 2+ aumenta la inespecificidad n Pequeñas cantidades de Mg 2+ reduce el rendimiento

6) Concentración de d. NTPS 1. Debe variar según el tamaño de la secuencia target a amplificar. 2. Por ejemplo: para un rendimiento de 1012 moléculas de 100 pb, se necesitan 1014 moléculas. 3. Generalmente la mix que se prepara son de 2 -2, 5 m. M

7) Mezcla de reacción 1. El buffer, p. H y concentración de Mg 2+ óptimos de acuerdo a la secuencia y al par de iniciadores elegidos 2. Uso de estabilizantes de la enzima: gelatina, Tritón X-100, Tween 20, BSA 3. Elementos que facilitan la desnaturalización del ADN molde: glicerol, dimetilsulfóxido y formamida

7) Mezcla de reacción II La mayoría de los buffers tienen KCl (50 m. M) y Tris (10 m. M): 1. Estas concentraciones pueden ser alteradas, KCl facilita la unión de los cebadores pero a concentraciones 50 m. M inhiben la Taq 2. Los buffer pueden tener: DMSO, BSA, gelatina, glicerol, Tween-20, Nonidet P-40, Triton X-100, DTT. la especificidad de la reacción pero tambien pueden ser inhibitorios.

Coadyuvantes: BSA: estabiliza la polimerasa y secuestra inhibidores no especifícos n Formamida: Baja la temperatura de desnaturalización (templado ricos en GC) n DMSO: Ayuda la elongación en templados ricos en GC Mezcla de polimerasas Hot start n n n

8) Típica reacción de PCR: 1. El

Optimización: número de ciclos n 25 -40 ciclos n El tiempo de vida media de Taq es de 30 minutes a 95 o. C n Si se usa mas de 30 ciclos con un tiempo de desnaturalización de 1 minuto, la eficiencia de la Taq será menor. n No caer en la fase de Plateau
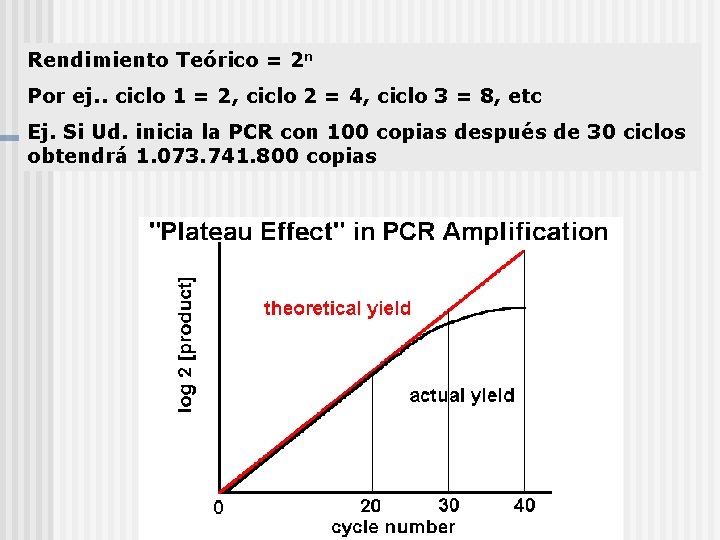
Rendimiento Teórico = 2 n Por ej. . ciclo 1 = 2, ciclo 2 = 4, ciclo 3 = 8, etc Ej. Si Ud. inicia la PCR con 100 copias después de 30 ciclos obtendrá 1. 073. 741. 800 copias
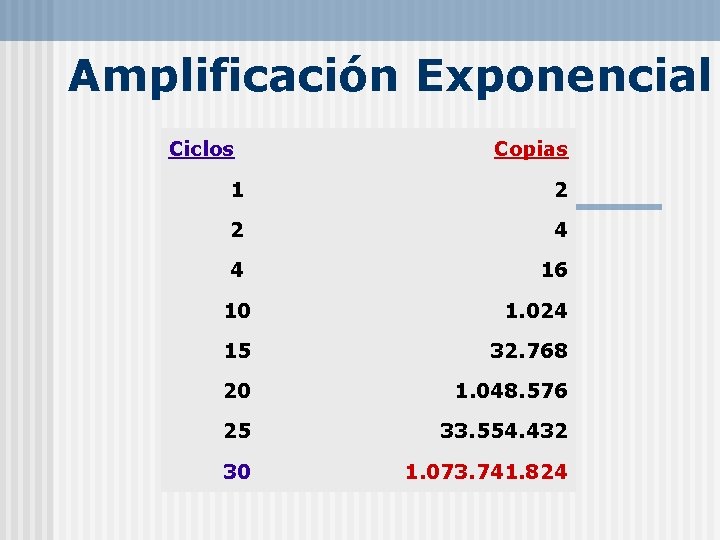
Amplificación Exponencial Ciclos Copias 1 2 2 4 4 16 10 1. 024 15 32. 768 20 1. 048. 576 25 33. 554. 432 30 1. 073. 741. 824
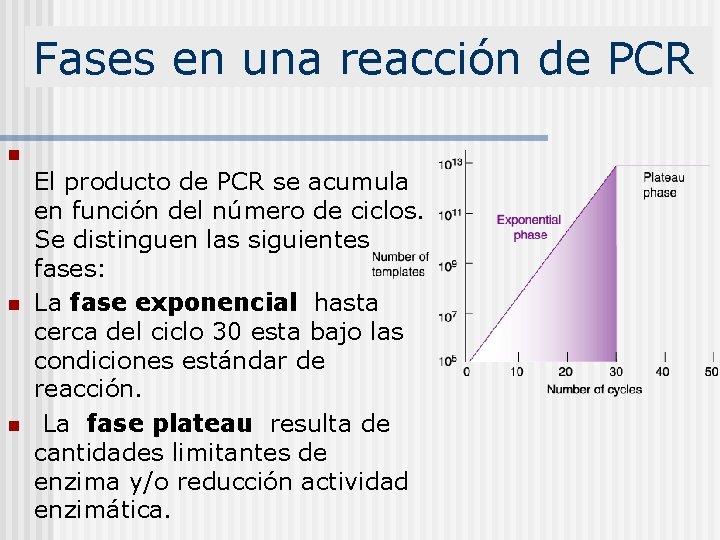
Fases en una reacción de PCR n n n El producto de PCR se acumula en función del número de ciclos. Se distinguen las siguientes fases: La fase exponencial hasta cerca del ciclo 30 esta bajo las condiciones estándar de reacción. La fase plateau resulta de cantidades limitantes de enzima y/o reducción actividad enzimática.

Causas de Efecto Plateau Agotamiento de los sustratos (d. NTPs o primers). n Estabilidad de los reactivos (d. NTPs o enzima) particularmente a la tº de desnaturalización. n Inhibición por los productos finales generados (pirofosfato, duplex de DNA). n Competición de los reactivos por productos no específicos o dímeros de cebadores. n Incompleta desnaturalización / separación de hebras a altas concentraciones del producto. n
![CONDICIONES PARA MEJORAR LA ESPECIFICIDAD DISMINUIR: n Mg++ n [d NTP] n LARGO DE CONDICIONES PARA MEJORAR LA ESPECIFICIDAD DISMINUIR: n Mg++ n [d NTP] n LARGO DE](http://slidetodoc.com/presentation_image_h2/1e83b36de3817d5777ae97f371661bf9/image-71.jpg)
CONDICIONES PARA MEJORAR LA ESPECIFICIDAD DISMINUIR: n Mg++ n [d NTP] n LARGO DE LOS CICLOS n NUMERO DE CICLOS n CONCENTRACION DE PRIMER AUMENTAR: n Tº DE ANNEALING

RESUMEN: n MENOR TIEMPO Y MAYOR Tº DE ANNEALING: MAYOR ESPECIFICIDAD CICLOS EXTRAS: MENOR ESPECIFICIDAD PARA OBTENER MASA DE AMPLIFICACION SE REALIZA REAMPLIFICACION n CONTROL NEGATIVO: n n n SIN ADN MUESTRA CON ADN QUE NO CONTIENE SECUENCIA TARGET SOLUCION DE EXTRACCION DE ADN

VARIANTES DE PCR PARA MEJORAR ESPECIFICIDAD n HOT START PCR: EVITA PRODUCTOS INESPECIFICOS GENERADOS INICIALMENTE CUANDO AUMENTA LA Tº
- Slides: 73