QUMICA AMBIENTAL Prof Ana Flvia Suzana Cincia Ambiental

QUÍMICA AMBIENTAL Prof. Ana Flávia Suzana

Ciência Ambiental “Estudo interdisciplinar que usa informações das ciências físicas e sociais para aprender como a Terra funciona, como interagimos com ela e como lidar com os problemas ambientais. ” Miller Jr. ; G. T. ; Ciência Ambiental, 1ª Ed. São Paulo: CENCAGE Learning, 2011. Química Biologia Geologia Ciências Ambientais Física Política Ética Antropologia Economia
Química Ambiental Interações entre as substâncias químicas e os diferentes compartimentos ambientais e como o ciclo desses podem ser afetados de acordo com as atividades antrópicas; Biota Atmosfera Água Solos

ÁGUA Composição da água • • Moléculas de H 2 O; Sais minerais; Gases Dissolvidos (O 2, N 2, CO 2, entre outros); Outras substâncias; % da superfície planeta Água Terra • Cerca de 71, 8% da superfície terrestre; A distribuição da água no planeta • Oceanos e mares - 97% • Geleiras inacessíveis - 2% • Rios, lagos e fontes subterrâneas - 1%
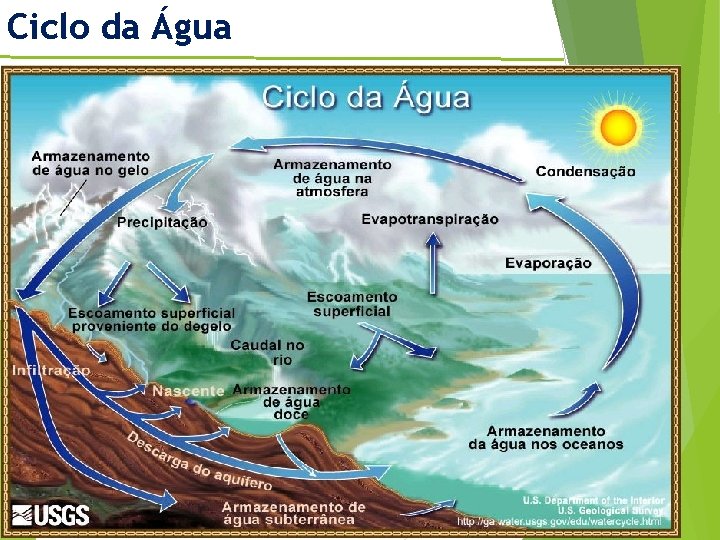
Ciclo da Água
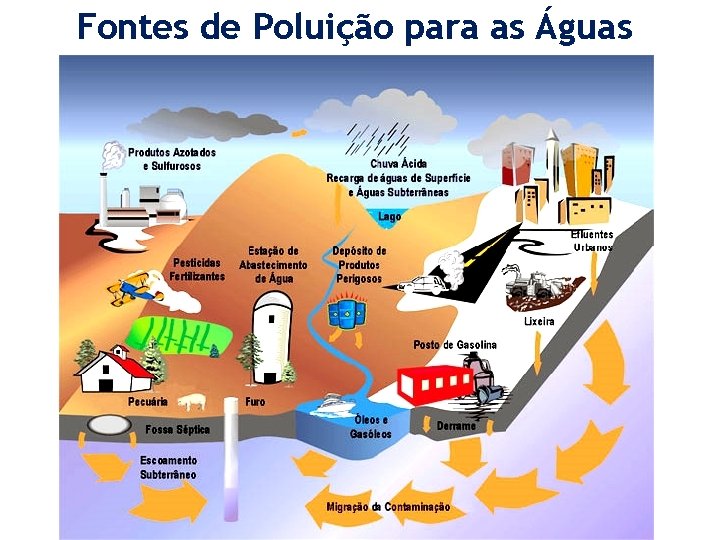
Fontes de Poluição para as Águas

Detergentes e a poluição Os detergentes no Brasil são feitos a partir da mistura de alquilbenzeno-sulfonatos de sódio e recebem a classificação de detergente biodegradável ou não biodegradável. A diferença entre eles começa na cadeia carbônica que os constitui. Os micro-organismos existentes na água produzem enzimas capazes de quebrar as moléculas de cadeias lineares presentes nos detergentes biodegradáveis, mas elas não reconhecem as cadeias ramificadas presentes nos detergentes não biodegradáveis, por esse motivo eles permanecem na água sem sofrer decomposição.

Efeitos da poluição da Água Eutrofização da água; Excesso de nutrientes nas águas (C, N e P, principalmente) gera a proliferação excessiva de algas; Hipóxia; Algas em quantidade excessiva consomem o O 2 dissolvido na água e impossibilitam a vida de outras espécies que necessitariam desse gás; Contaminação com substâncias extremamente tóxicas; Ácidos, metais, substâncias orgânicas e diversas outras! Proliferação de malefícios e doenças a saúde humana e ambiental;

A que ponto chegamos …
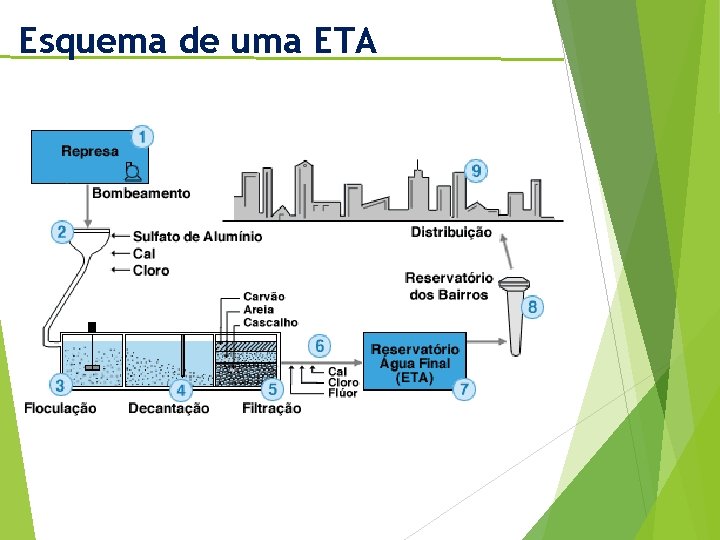
Esquema de uma ETA

E o que deve ser feito? 1. Começar a implantar programas de redução de consumo de água; 2. Monitoramento e manutenção dos corpos hídricos! Fonte: CONAMA, Resolução 357 de 2005. Disponível em <http: //www. mma. gov. br/port/conama/res 05/res 35705. pdf> 3. Investigar a presença de contaminantes em concentrações excessivas nos corpos hídricos e demais compartimentos ambientais; 4. Incentivar e apoiar a criação de legislações mais rigorosas e a criação de mais ETE e ETA, bem como implantação de técnicas melhores de saneamento básico; 5. Colaborar na fiscalização da poluição.

(Enem) A falta de água doce no planeta será, possivelmente, um dos mais graves problemas deste século. Prevê-se que, nos próximos vinte anos, a quantidade de água doce disponível para cada habitante será drasticamente reduzida. Por meio de seus diferentes usos e consumos, as atividades humanas interferem no ciclo da água, alterando: a) a quantidade total, mas não a qualidade da água disponível no planeta. b) a qualidade da água e sua quantidade disponível para o consumo das populações. c) a qualidade da água disponível, apenas no subsolo terrestre. d) apenas a disponibilidade de água superficial existente nos rios e lagos. e) o regime de chuvas, mas não a quantidade de água disponível no Planeta.

Nos últimos 60 anos, a população mundial duplicou, enquanto o consumo de água foi multiplicado por sete. Da água existente no planeta, 97% são de água salgada (mares e oceanos), 2% formam geleiras inacessíveis e apenas 1% corresponde à água doce, armazenada em lençóis subterrâneos, rios e lagos. A poluição pela descarga de resíduos municipais e industriais, combinada com a exploração excessiva dos recursos hídricos disponíveis, ameaça o meio ambiente, comprometendo a disponibilidade de água doce para o abastecimento das populações humanas. Se esse ritmo se mantiver, em alguns anos a água potável tornar-se-á um bem extremamente raro e caro. MORAES, D. S. L. ; JORDAO, B. Q. Degradação de recursos hídricos e seus efeitos sobre a saúde humana. Saúde Pública São Paulo, v. 36, n. 3, Jun. 2002 (adaptado). Considerando o texto, uma proposta viável para conservar o meio ambiente e a água doce seria a) fazer uso exclusivo da água subterrânea, pois ela pouco interfere na quantidade de água dos rios. b) desviar a água dos mares para os rios e lagos, de maneira a aumentar o volume de água doce nos pontos de captação. c) promover a adaptação das populações humanas ao consumo da água do mar, diminuindo assim a demanda sobre a água doce. d) reduzir a poluição e a exploração dos recursos naturais, otimizar o uso da água potável e aumentar captação da água da chuva. e) realizar a descarga dos resíduos municipais e industriais diretamente nos mares, de maneira a não afetar a água doce disponível.

Poluição do Ar Refere-se ao lançamento de gases na atmosfera que alterem sua composição original; Composição original: Gases % em volume Nitrogênio 78, 0 Oxigênio 21, 0 Vapor d’água Argônio Dióxido de Carbono Neônio Hélio Metano 1, 0
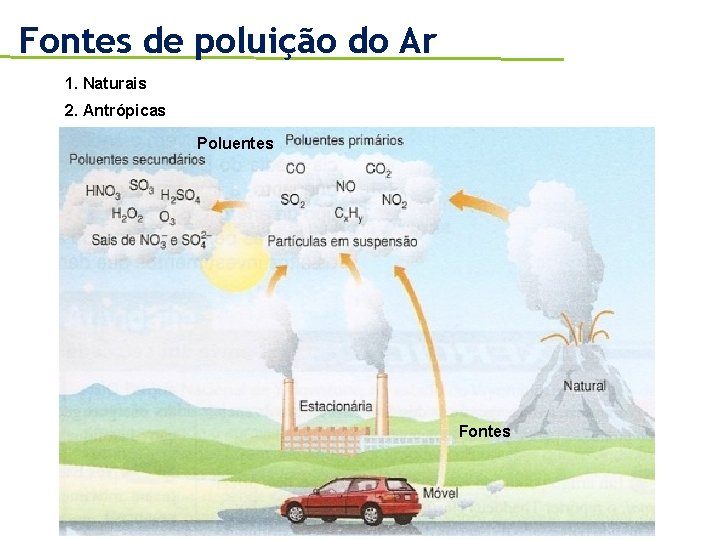
Fontes de poluição do Ar 1. Naturais 2. Antrópicas Poluentes Fontes

DIÓXIDO DE CARBONO (CO 2) FONTES ü respiração, decomposição de plantas e animais e queimadas de florestas; ü queima de combustíveis fósseis, atividade humana (principalmente indústrias) e erupções vulcânicas. CONCENTRAÇÃO ü antes 1750 - 280 ppmv (partes por milhão por volume) ü em 1992 – 355 ppmv ü atualmente – 400 ppmv • EFEITOS ü Principal gás do “efeito estufa”

METANO (CH 4) FONTES Matéria orgânica em decomposição; ü Queima de biomassa, queima de combustíveis fósseis e rúmen de ruminantes. ü CONCENTRAÇÃO Atual – 1, 72 ppmv ü Antes Revolução Industrial – 0, 8 ppmv ü • EFEITOS ü Ao ser inalado, o gás pode causar asfixia e perda de consciência, parada cardíaca e, em caso extremo, danos no sistema nervoso central.

HALOCARBONOS (CFCs, HFCs) FONTES ü Produção de aerossóis, espuma, indústria de ar condicionado CONCENTRAÇÃO ü Em 1992 - CFC 11 – 280 pptv (partes por trilhão por volume) - CFC 12 – 484 pptv - CFC 113 – 60 pptv • EFEITOS ü Destruição da camada de ozônio (CFCs e HCFCs) ü Efeito estufa

MONÓXIDO DE CARBONO (CO) FONTES ü Tráfego (veículos) ü Indústrias CONCENTRAÇÃO üA partir dos anos 80, a emissão de CO pelos automóveis passou de 33 g. CO/Km para 0, 43 g. CO/Km o que resultou numa queda progressiva na poluição, mesmo com o aumento da frota de veículos. Contudo em 2000 apresentou um pequeno crescimento. • EFEITOS ü Perda de consciência; morte.
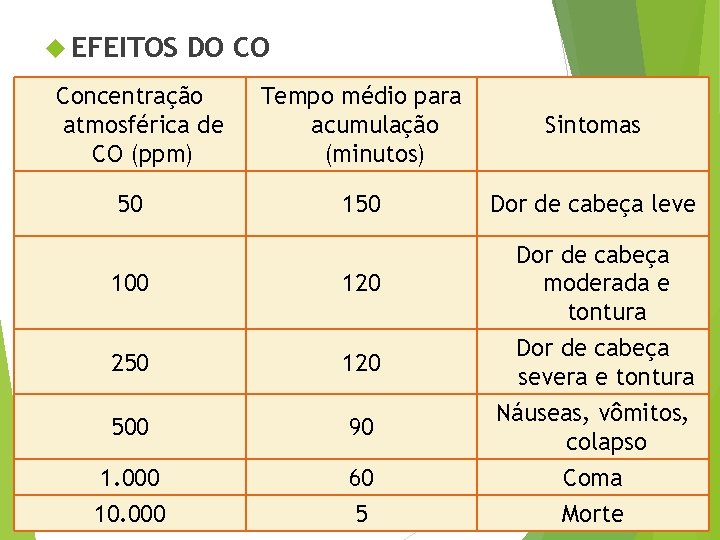
EFEITOS DO CO Concentração atmosférica de CO (ppm) Tempo médio para acumulação (minutos) Sintomas 150 Dor de cabeça leve 100 120 Dor de cabeça moderada e tontura 250 120 Dor de cabeça severa e tontura 500 90 Náuseas, vômitos, colapso 1. 000 60 Coma 10. 000 5 Morte 50

ÓXIDOS DE NITROGÊNIO (NO, NO 2) FONTES ü As fontes naturais incluem incêndios florestais, calor gerado pelos relâmpagos e atividade microbiana nos solos. ü Produção de nylon, ácido nítrico, atividades agrícolas, queima de biomassa e queima de combustíveis fósseis CONCENTRAÇÃO ü Em 1993 – 310 ppbv (partes por bilhão por volume) ü Antes Revolução Industrial – 275 ppbv • EFEITOS ü Inflamações do sistema respiratório ü Chuva ácida

DIÓXIDO DE ENXOFRE (SO 2) FONTES Combustão (petróleo e carvão mineral) ü Veículos à diesel ü Erupções vulcânicas ü EFEITOS Sistema respiratório ü Problemas cardiovasculares ü Chuva ácida ü

Poluição do solo É qualquer alteração provocada nas suas características, pela introdução de produtos químicos ou resíduos, de forma que ele se torne prejudicial ao homem e a outros organismos ou tenha os seus usos prejudicados. Fertilizantes artificiais Aplicação de pesticidas Deposição de resíduos sólidos Deposição de esgotos

DESTRUIÇÃO DA CAMADA DE OZÔNIO COMO A CAMADA DE OZÔNIO PROTEGE A TERRA? • absorve a radiação ultravioleta (UVA, UVB, UVC) do Sol, impedindo que a maior parte dela atinja a superfície terrestre

CFCs (clorofluorcarbonos)

QUIMICAMENTE TEMOS: Formação do Ozônio: Destruição do Ozônio: Equilíbrio natural entre formação e destruição do ozônio • EFEITOS ü Irritação dos olhos e vias respiratórias ü Envelhecimento precoce e corrosão dos tecidos
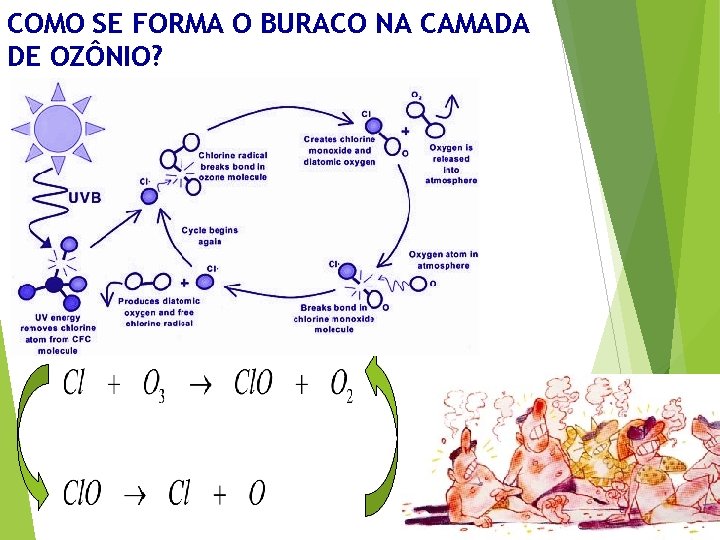
COMO SE FORMA O BURACO NA CAMADA DE OZÔNIO?

Buraco na camada de ozônio: ESTAMOS PERDENDO PROTEÇÃO

CONHEÇA AS RADIAÇÕES ULTRAVIOLETAS radiação UV λ (em nm) UVA 320 - 400 UVB 280 - 320 UVC < 280 efeitos • Não são absorvidos pela camada de O 3; • Não possuem efeitos maléficos ao ser humano; • Parcialmente absorvidos pela camada de ozônio; • Vermelhidão na pele e diferentes tipos de câncer de pele; • Totalmente absorvidos pela camada de O 3 ; • Podem danificar a córnea e outros tecidos.

OS EFEITOS DA DIMINUIÇÃO DA CAMADA DE OZÔNIO ATINGEM O HEMISFÉRIO SUL: üaumento nos casos de câncer de pele e catarata em regiões do hemisfério sul, como a Austrália, Nova Zelândia, África do Sul e Patagônia. üO Ministério da Saúde do Chile informou que desde o aparecimento do buraco na camada de ozônio sobre o pólo Sul, os casos de câncer de pele no Chile cresceram 133%; ü Atualmente o governo faz campanhas para a população utilizar cremes protetores para a pele e não ficar exposta ao sol durante as horas mais críticas do dia.

ü Em Queensland, no nordeste da Austrália, mais de 75% dos cidadãos acima de 65 anos apresentam alguma forma de câncer de pele; ü A lei local obriga as crianças a usarem grandes chapéus e cachecóis quando vão à escola, para se protegerem das radiações ultravioletas. ü A Academia de Ciências dos Estados Unidos calcula que apenas na Austrália, estejam surgindo anualmente 10 mil casos de carcinoma de pele por causa da redução da camada de ozônio.

(Enem-2012) O rótulo de um desodorante aerossol informa ao consumidor que o produto possui em sua composição os gases isobutano, butano e propano, dentre outras substâncias. Além dessa informação, o rótulo traz, ainda, a inscrição “Não contém CFC”. As reações a seguir, que ocorrem na estratosfera, justificam a não utilização de CFC (clorofluorcarbono ou Freon) nesse desodorante: I) CF 2 Cℓ 2 + UV → CF 2 Cℓ • + Cℓ • II) Cℓ • + O 3 → O 2 + CℓO • A preocupação com as possíveis ameaças à camada de ozônio (O 3) baseia-se na sua principal função: proteger a matéria viva na Terra dos efeitos prejudiciais dos raios solares ultravioleta. A absorção da radiação ultravioleta pelo ozônio estratosférico é intensa o suficiente para eliminar boa parte da fração de ultravioleta que é prejudicial à vida. A finalidade da utilização dos gases isobutano, butano e propano neste aerossol é: a) substituir o CFC, pois não reagem com o ozônio, servindo como gases propelentes em aerossóis. b) servir como propelentes, pois, como são muito reativos, capturam o Freon existente livre na atmosfera, impedindo a destruição do ozônio. c) reagir com o ar, pois se decompõem espontaneamente em dióxido de carbono (CO 2) e água (H 2 O), que não atacam o ozônio. d) impedir a destruição do ozônio pelo CFC, pois os hidrocarbonetos gasosos reagem com a radiação UV, liberando hidrogênio (H 2), que reage com o oxigênio do ar (O 2), formando água (H 2 O). e) destruir o CFC, pois reagem com a radiação UV, liberando carbono (C), que reage com o oxigênio do ar (O 2), formando dióxido de carbono (CO 2), que é inofensivo para a camada de ozônio.

(Fuvest-SP) Entidades ligadas à preservação ambiental têm exercido fortes pressões para a redução da produção de gases CFC (clorofluorcarbonos). Isto se deve principalmente ao fato de os CFCs: a) reagirem com H 2 O, produzindo ácidos e chuva ácida. b) reagirem espontaneamente com O 2, produzindo CO 2 e agravando o efeito estufa. c) escaparem para o espaço provocando o fenômeno da inversão térmica. d) reagirem com oxigênio a baixas pressões, produzindo ozônio. e) produzirem, sob a ação da luz, átomos livres, que reagem com o ozônio.

EFEITO ESTUFA
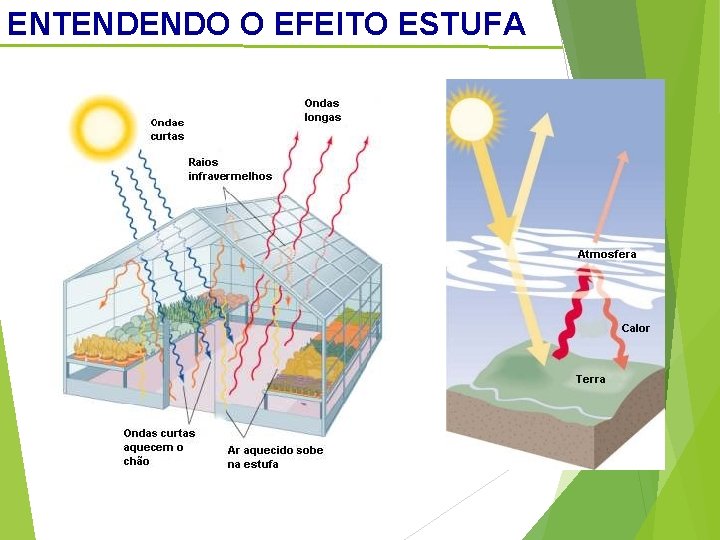
ENTENDENDO O EFEITO ESTUFA

A TERRA: UMA GRANDE ESTUFA Efeito Estufa natural: natural grande parte se deve a presença de água na atmosfera (em forma de vapor, 85% e água líquida 12%) Em conseqüência da poluição: poluição Se deve principalmente pelo (CO 2), (CH 4), (N 2 O), clorofluorcarbonetos (CFCs), hidroclorofluorcarbonetos (HCFCs) e (SF 6)

O que potencializa esse fenômeno? Queima de combustíveis fósseis Desperdício de alimentos Emprego de certos fertilizantes Desmatamento AQUECIMENTO GLOBAL

O SUPERAQUECIMENTO GLOBAL E SUAS CONSEQÜÊNCIAS
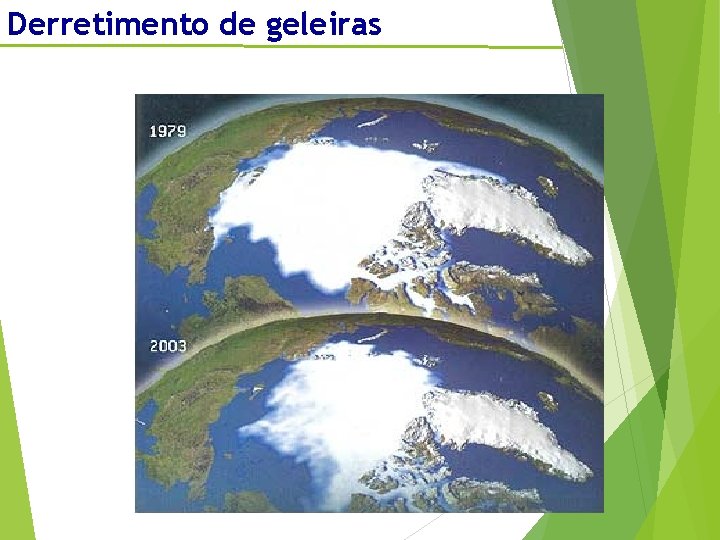
Derretimento de geleiras

Derretimento de geleiras

Inundações

Desertificação Sistema Cantareira - SP Mar do Aral

Furacões

O PROTOCOLO DE KYOTO (1997) ü entre 2008 e 2012, os países industrializados devem diminuir a emissão de gases poluentes a um nível 5, 2% menor que a média de 1990. ü E. U. A. se recusam a ratificar o acordo em 2001 üProrrogado para 2020. METAS DE REDUÇÃO Países da União Européia – 8% Estados Unidos – 7% Japão – 6% Para a China e os países em desenvolvimento, como Brasil, Índia e México, ainda não foram estabelecidos níveis de redução.

E a chuva ácida? ?

A CHUVA É, NATURALMENTE, UM POUCO ÁCIDA! • Os animais e o homem, ao respirarem, liberam gás carbônico (CO 2) na atmosfera. Então quando chove: CO 2(g) + H 2 O(l) H 2 CO 3(aq) • deixando a chuva ligeiramente ácida (p. H = 5, 7), já que se trata de um ácido fraco
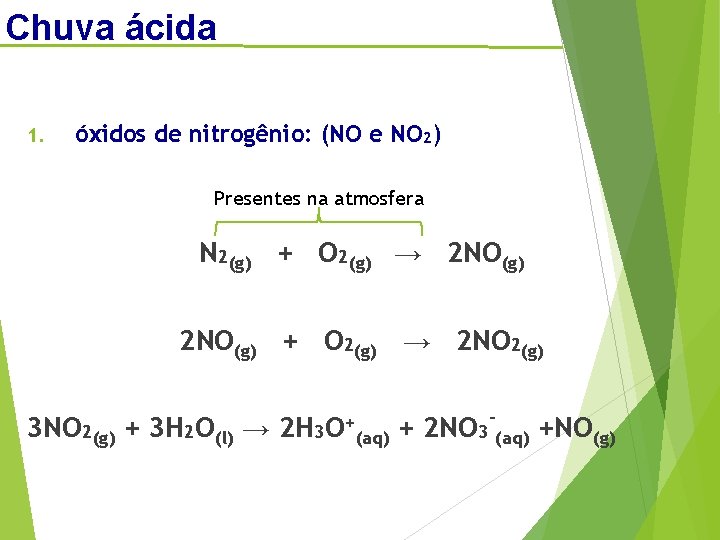
Chuva ácida 1. óxidos de nitrogênio: (NO e NO 2) Presentes na atmosfera N 2(g) + O 2(g) → 2 NO(g) + O 2(g) → 2 NO 2(g) 3 NO 2(g) + 3 H 2 O(l) → 2 H 3 O+ (aq) - + 2 NO 3 (aq) +NO(g)

Chuva ácida 2. Óxidos de enxofre: (SO 2) SO 2(g) + H 2 O(l) → H 2 SO 3(aq) 2 SO 2(g) + O 2(g) → 2 SO 3(g) + H 2 O(l) → H 2 SO 4(aq) Consequências: ü A água dos rios e lagos se torna ácida e, conseqüentemente, imprópria para a vida de peixes e outras espécies.

ü corrosão do ferro pelo ácido sulfúrico Fe(s) + H 2 SO 4(aq) H 2(g) + Fe. SO 4(s) ü corrosão do mármore pelo ácido sulfúrico H 2 SO 4(aq) + Ca. CO 3(s) Ca. SO 4(aq) + H 2 CO 3(aq)


CONTROLE DE EMISSÃO DE POLUENTES POR VEÍCULOS AUTOMOTORES üUso de combustíveis menos poluidores, o gás natural por exemplo; üInstalação de catalisadores; üOperação e manutenção adequadas do veículo; üRodízio de carros; üUtilização de transportes públicos.

CONTROLE DE EMISSÃO DE POLUENTES PELAS INDÚSTRIAS üAltura adequada das chaminés de indústrias, facilitando a dispersão dos poluentes üUso de matérias primas e combustíveis que resultem em resíduos gasosos menos poluidores üMelhoria da combustão: quanto mais completa a combustão, “menor a emissão de poluentes” üInstalação de filtros nas chaminés üTratamento de resíduos químicos

O QUE PODEMOS FAZER PARA CONTRIBUIR COM A DIMINUIÇÃO DE POLUENTES? üEvitar queimar compostos orgânicos ou lixo de modo geral üPlantar mais árvores üReduzir e reciclar o lixo üFazer vistorias constantes em seus veículos e se empresário, em suas indústrias. üBuscar utilizar fontes renováveis de energia um
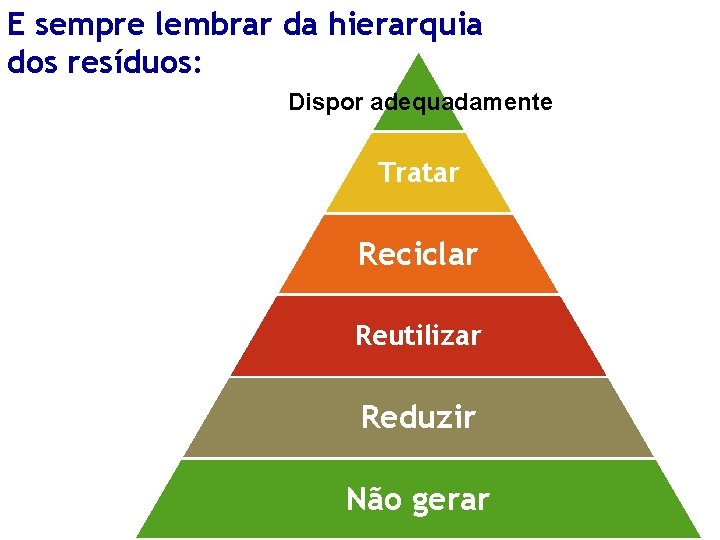
E sempre lembrar da hierarquia dos resíduos: Dispor adequadamente Tratar Reciclar Reutilizar Reduzir Não gerar
- Slides: 55