Qumica 2 Medio Profesor Bastin Crdenas G 2

Química 2º Medio Profesor Bastián Cárdenas G
2 Ruta de aprendizaje • Objetivo: Comprender y calcular las concentraciones físicas de diferentes mezclas • Contenido 1. 2. 3. 4. 5. 6. Concentraciones Tipos de concentraciones Moles Avogadro Nº de Avogadro Ejercitemos • Cierre de clases

3 Concentración ¿Qué son las concentraciones? la concentración de una disolución es la proporción o relación que hay entre la cantidad de soluto y la cantidad de disolución o, a veces, de disolvente.

1. Antes de comenzar ¿Qué son los moles?

“ El mol es la unidad utilizada para expresar la cantidad de una determinada sustancia en el SI el resultado de expresar la masa atómica de un elemento o la masa molecular de un compuesto en gramos. 5
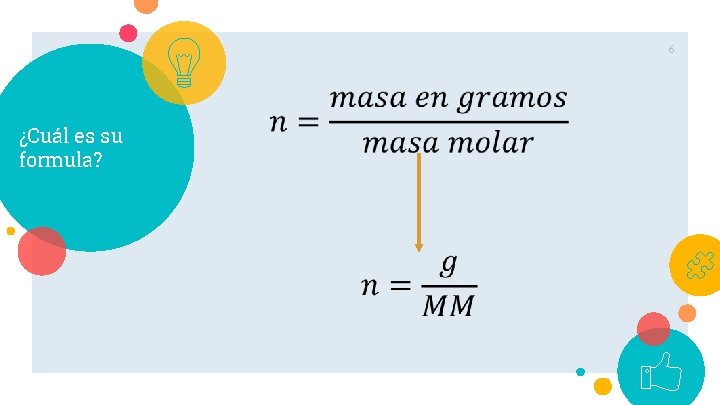
6 ¿Cuál es su formula?

7 Avogadro ¿Para qué sirve?
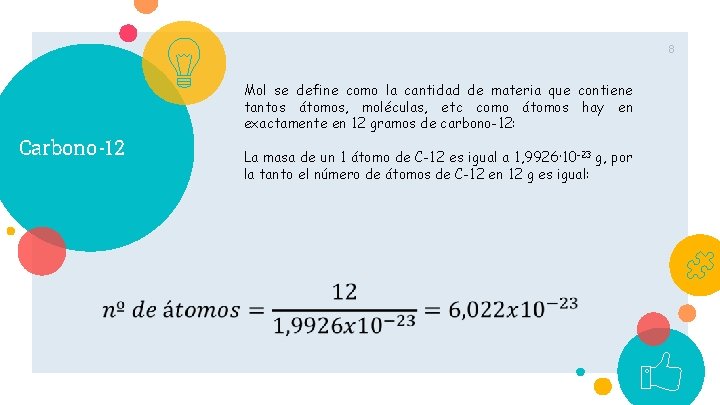
8 Mol se define como la cantidad de materia que contiene tantos átomos, moléculas, etc como átomos hay en exactamente en 12 gramos de carbono-12: Carbono-12 La masa de un 1 átomo de C-12 es igual a 1, 9926· 10 -23 g, por la tanto el número de átomos de C-12 en 12 g es igual:

9 1 mol de cualquier especie química (átomo, molécula, ión, etc. ) = 6, 022· 1023 especies. In two or three columns Esto es, el número de partículas por mol es 6, 022· 1023 y este número se denomina número de Avogadro, NA. NA permite realizar conversiones entre número de moles (n) y número de átomos, iones, moléculas, etc. (es decir, número de partículas. Importante considerar las siguientes relaciones: • 1 mol de molécula de H 2 O= 6, 02· 1023 moléculas de H 2 O • 1 mol de átomos de Carbono (C) = 6, 02· 1023 átomos de carbono (C) • 1 mol de iones CO 3 -2= 6, 02· 1023 iones CO 3 -2
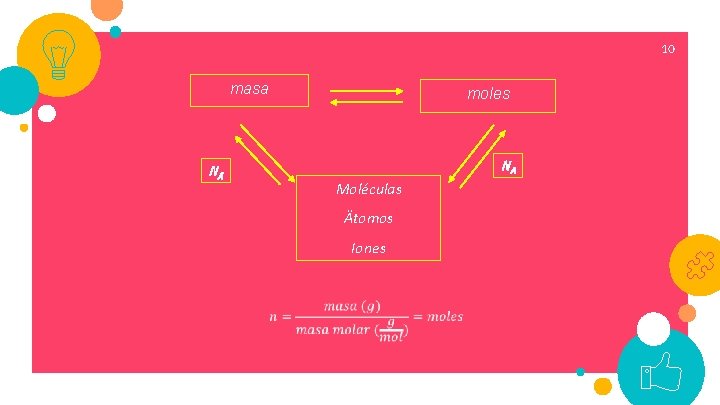
10 masa NA moles NA Moléculas Ätomos Iones

11 Ejemplo 1: Calcular el número de átomos de Carbono ( C ) que hay en 0, 350 mol de glucosa (C 6 H 12 O 6). La estrategia es saber la relación entre : moles de glucosa moléculas de glucosa 1 mol de C 6 H 12 O 6 0, 350 mol de C 6 H 12 O 6 átomos de C 6, 02 x 1023 moléculas de C 6 H 12 O 6 X= 2, 11 x 10 23 moléculas de C 6 H 12 O 6 1 molécula de C 6 H 12 O 6 2, 11 x 1023 moléculas de C 6 H 12 O 6 6 átomos de C X= 1, 26 x 10 24 átomos de C

12 Ejemplo 2: cuántos átomos de oxígeno hay en 0, 25 mol de Ca(NO 3)2 Resp. : 9, 0 x 1023 átomos de oxígeno Ejemplo 3: cuántos átomos de nitrógeno hay en 1, 50 mol de Ca(NO 3)2 Resp. : 1, 81 x 1024 átomos de nitrógeno Ejemplo 3: cuántos átomos de calcio hay en 2, 36 mol de Ca(NO 3)2 Resp. : 1, 42 x 1024 átomos de calcio Ejemplo 3: cuántas moléculas de nitrato de calcio hay en 0, 85 mol de Ca(NO 3)2 Resp. : 5, 12 x 1023 moléculas de nitrato de calcio.
13 Cierre Moles Moléculas Átomos
- Slides: 13