Qumica 2 Bachillerato Estructura de la materia Configuraciones

Química 2. º Bachillerato Estructura de la materia Configuraciones electrónicas Los sistemas evolucionan hasta alcanzar situaciones de mínima energía. La disposición de los electrones alrededor del núcleo en un átomo es de la forma más estable posible, y se denomina configuración electrónica. Se cumplen tres reglas: Principio de Aufbau. Los electrones entran en los orbitales de energía más bajos disponibles. Principio de exclusión de Pauli. En un orbital atómico solo caben, como mucho, dos electrones. Estos deben tener espines opuestos y entonces se dice que están apareados y se representan mediante flechas verticales y . Segunda regla de Hund. Cuando varios electrones ocupan orbitales de la misma energía (es decir, de un mismo subnivel), se disponen de modo que tenga el máximo número de electrones desapareados (con el mismo espín) Una forma habitual de representar la configuración electrónica de un átomo consiste en escribir los subniveles indicando en un superíndice el número de electrones que los ocupan. Por ejemplo, para el sodio, que posee 11 electrones, la configuración es 1 s 1 2 s 2 2 p 6 3 s 1.
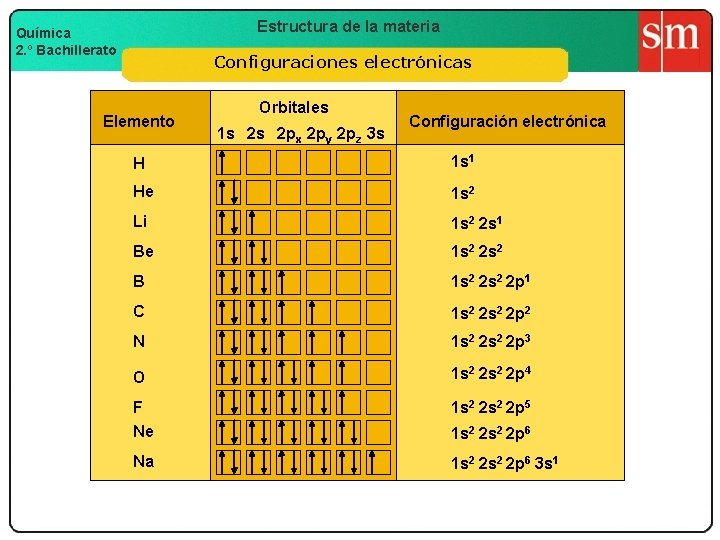
Estructura de la materia Química 2. º Bachillerato Configuraciones electrónicas Elemento Orbitales 1 s 2 s 2 px 2 py 2 pz 3 s Configuración electrónica H 1 s 1 He 1 s 2 Li 1 s 2 2 s 1 Be 1 s 2 2 s 2 B 1 s 2 2 p 1 C 1 s 2 2 p 2 N 1 s 2 2 p 3 O 1 s 2 2 p 4 F Ne 1 s 2 2 p 5 Na 1 s 2 2 p 6 3 s 1 1 s 2 2 p 6
- Slides: 2