Qumica 2 BAC U 1 Estructura atmica Sistema

Química 2º BAC U. 1 Estructura atómica. Sistema periódico Configuración electrónica

Ahora, teniendo en cuenta el orden creciente de energía de los orbitales (usaremos el diagrama de ocupación de los orbitales que nos da el orden de llenado) y sabiendo el número de electrones disponibles, que para un átomo neutro coincide con el valor del número atómico, Z, podemos escribir cualquier configuración electrónica. La notación usualmente empleada comienza con un número entero, que nos indica el nivel energético (valor de n), seguida de una letra (s, p, d, f, etc. ), que muestra el subnivel que ocupa el electrón. Por último, un número, que va como superíndice de la citada letra, que indica el número de electrones incluidos en dicho subnivel.
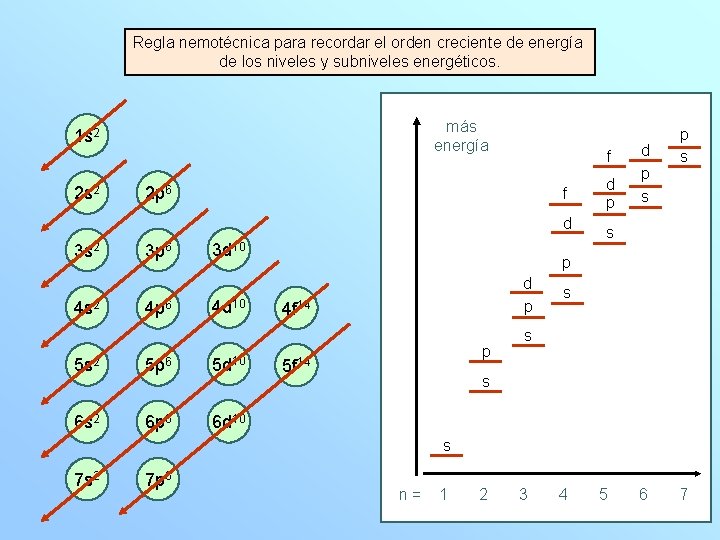
Regla nemotécnica para recordar el orden creciente de energía de los niveles y subniveles energéticos. más energía 1 s 2 2 s 2 f 2 p 6 f d 3 s 2 4 s 2 3 p 6 4 p 6 3 d 10 4 d 10 5 s 2 5 p 6 5 d 10 6 s 2 6 p 6 6 d 10 d p s p s s p d p 4 f 14 p 5 f 14 s s 7 s 2 7 p 6 n= 1 2 3 4 5 6 7
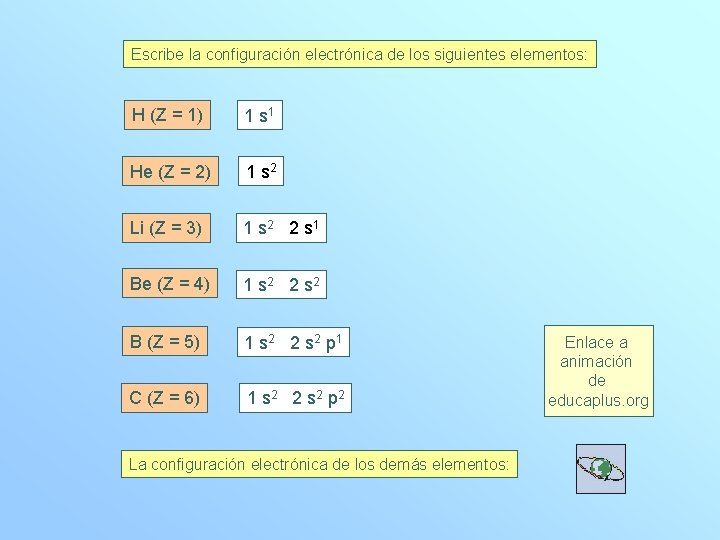
Escribe la configuración electrónica de los siguientes elementos: H (Z = 1) 1 s 1 He (Z = 2) 1 s 2 Li (Z = 3) 1 s 2 2 s 1 Be (Z = 4) 1 s 2 2 s 2 B (Z = 5) 1 s 2 2 s 2 p 1 C (Z = 6) 1 s 2 2 s 2 p 2 La configuración electrónica de los demás elementos: Enlace a animación de educaplus. org
- Slides: 4