Qumica 2 BAC U 1 Estructura atmica Sistema

Química 2º BAC U. 1 Estructura atómica. Sistema periódico Descripción del Sistema Periódico actual
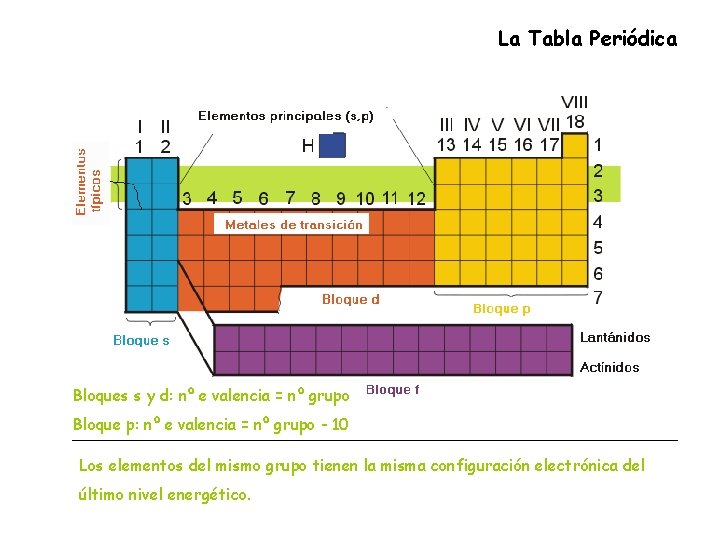
La Tabla Periódica Bloques s y d: nº e valencia = nº grupo Bloque p: nº e valencia = nº grupo - 10 Los elementos del mismo grupo tienen la misma configuración electrónica del último nivel energético.
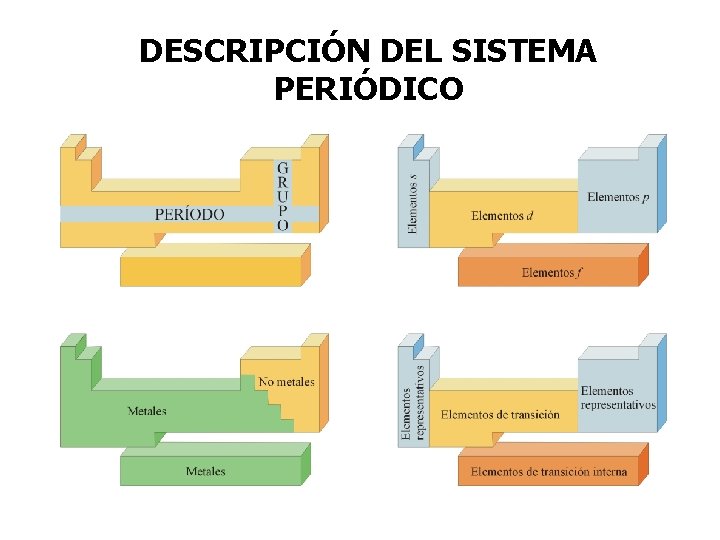
DESCRIPCIÓN DEL SISTEMA PERIÓDICO
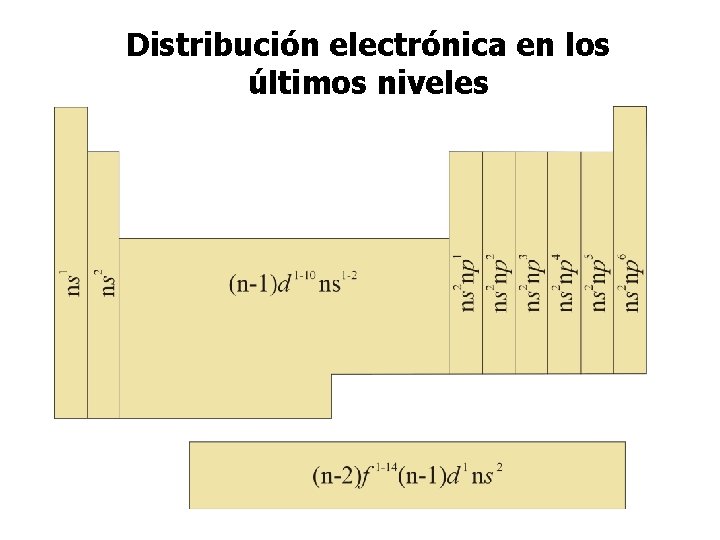
Distribución electrónica en los últimos niveles
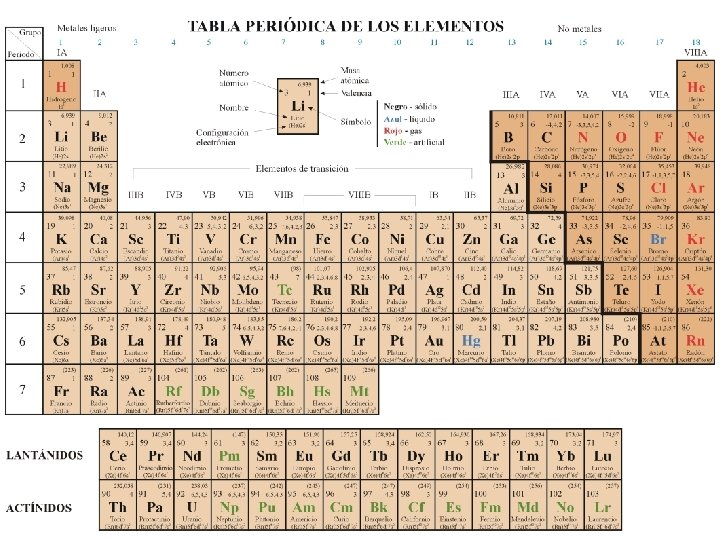
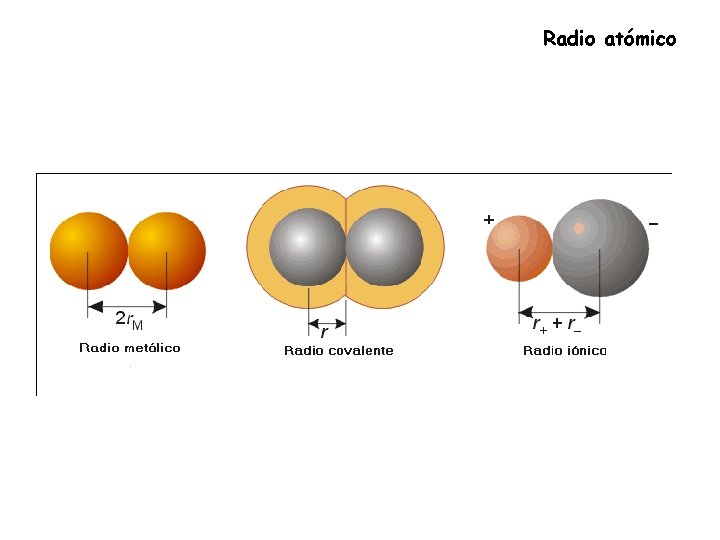
Radio atómico
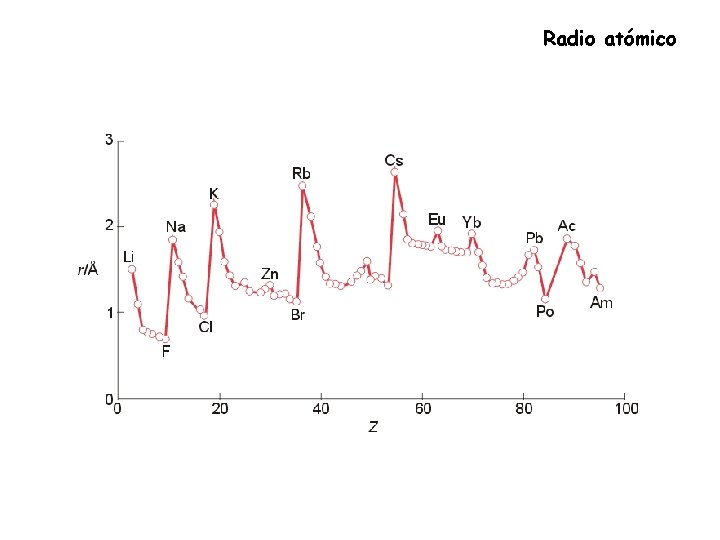
Radio atómico
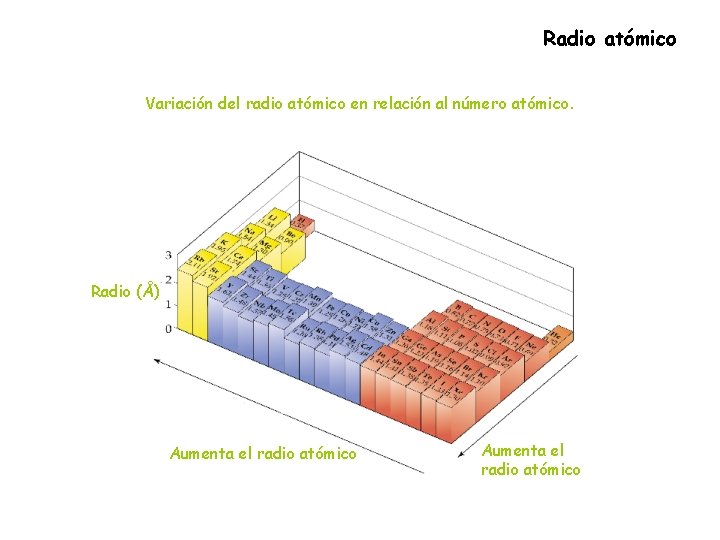
Radio atómico Variación del radio atómico en relación al número atómico. Radio (Å) Aumenta el radio atómico

Radio atómico
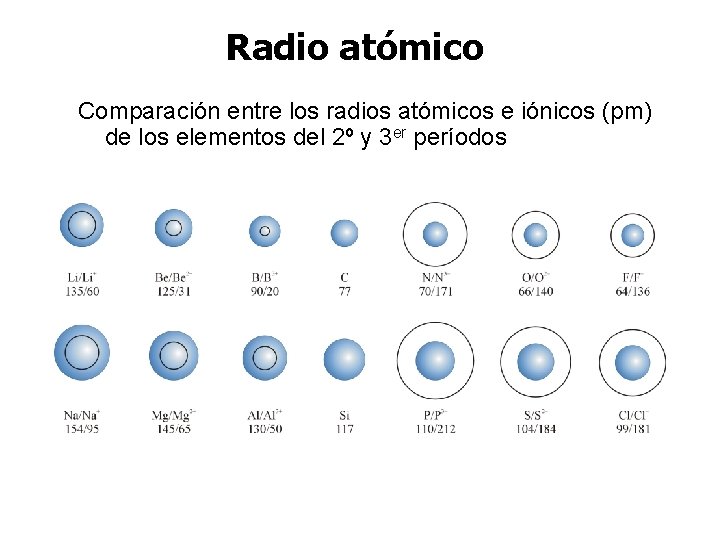
Radio atómico Comparación entre los radios atómicos e iónicos (pm) de los elementos del 2º y 3 er períodos
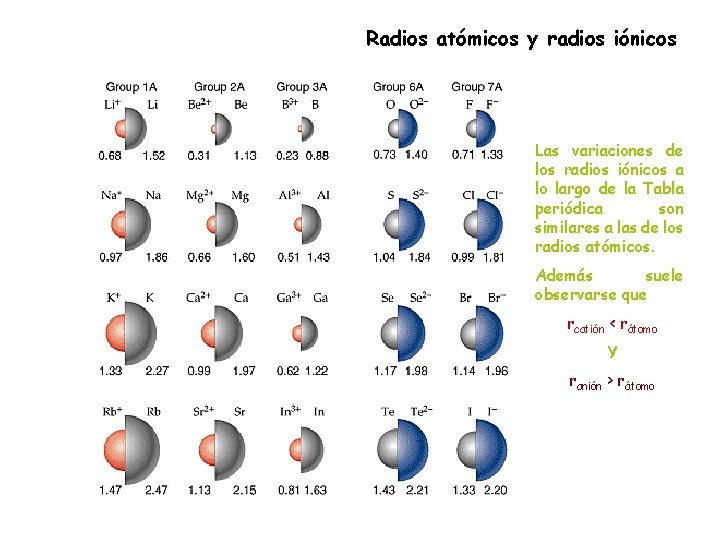
Radios atómicos y radios iónicos Las variaciones de los radios iónicos a lo largo de la Tabla periódica son similares a las de los radios atómicos. Además suele observarse que rcatión < rátomo Y ranión > rátomo
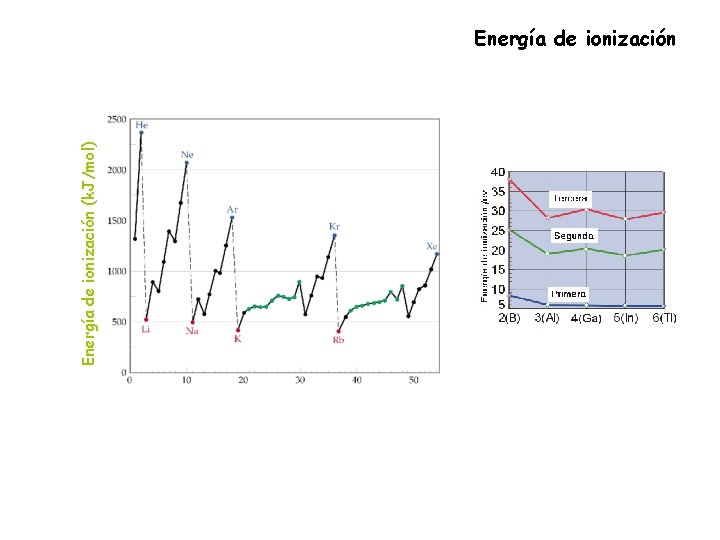
Energía de ionización (k. J/mol) Energía de ionización
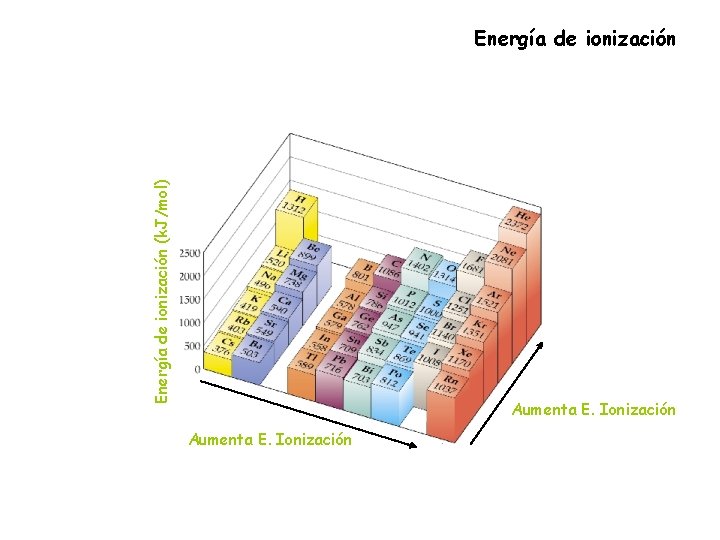
Energía de ionización (k. J/mol) Energía de ionización Aumenta E. Ionización
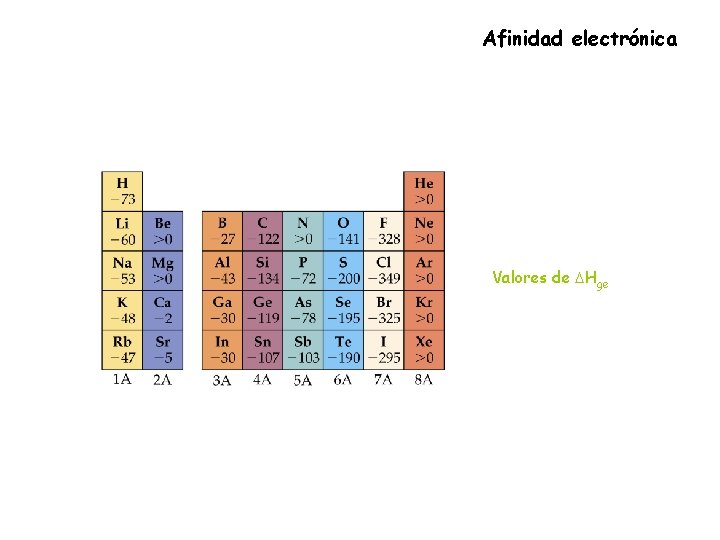
Afinidad electrónica Valores de DHge
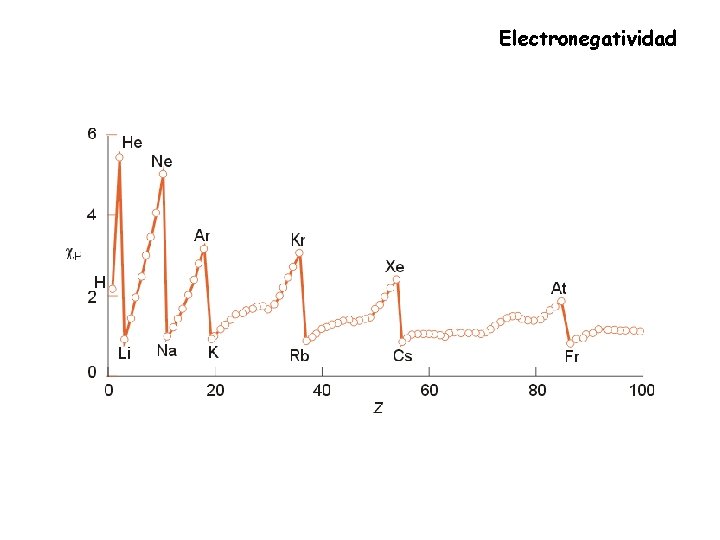
Electronegatividad
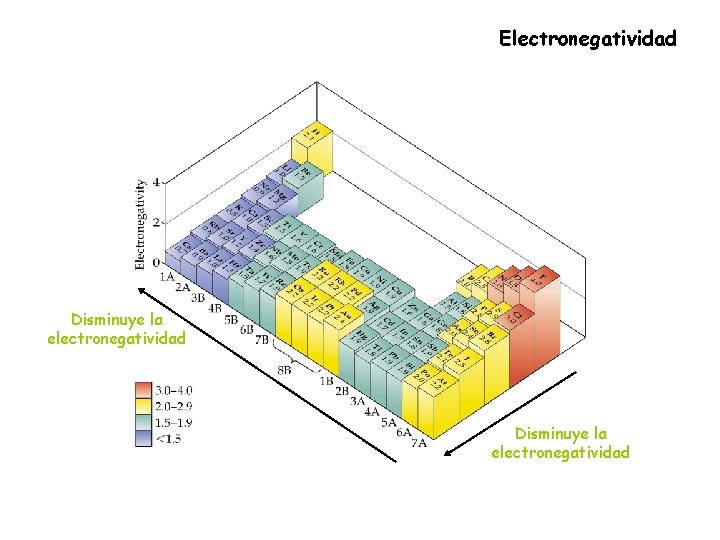
Electronegatividad Disminuye la electronegatividad
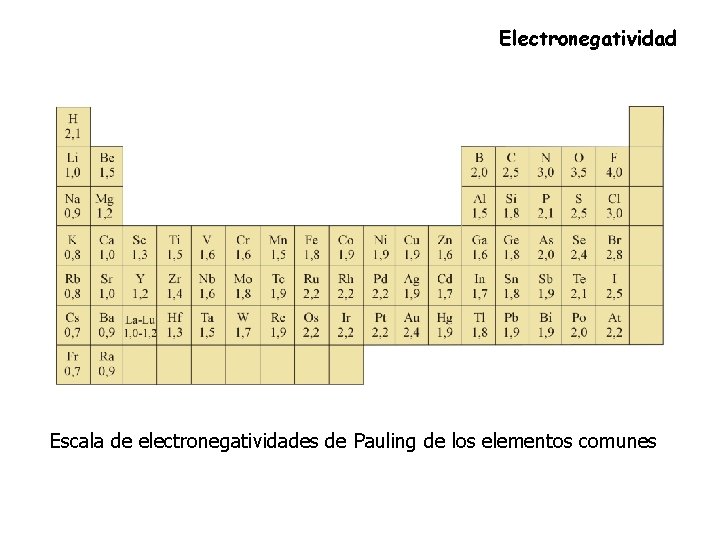
Electronegatividad Escala de electronegatividades de Pauling de los elementos comunes
- Slides: 17