Quiz Het ideaal gas en de toestandsgrootheden van




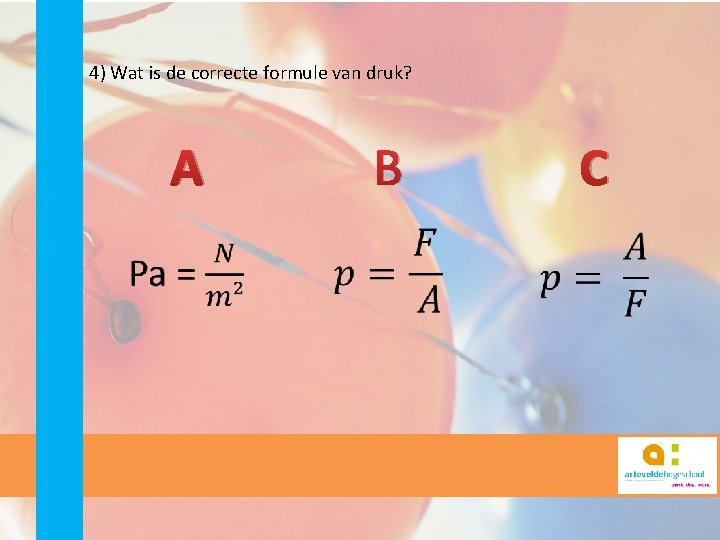





- Slides: 10

Quiz Het ideaal gas en de toestandsgrootheden van een gas

1) Welk van onderstaande modellen geeft de voorstelling van een gas weer? A B C

2) Welke van onderstaande mogelijkheden zijn regels waaraan een ideaal gas moet voldoen? A B C De deeltjes oefenen een kracht uit op elkaar De deeltjes veranderen na een botsing niet van gemiddelde snelheid De deeltjes hebben zelf geen volume. D E F De deeltjes botsen niet De deeltjes oefenen geen krachten uit op elkaar. De deeltjes bewegen enkel naar rechts

3) Wat is de betekenis van druk in het deeltjesmodel? A B C Deeltjes die botsen Deeltjes die verdwijnen Deeltjes die versnellen
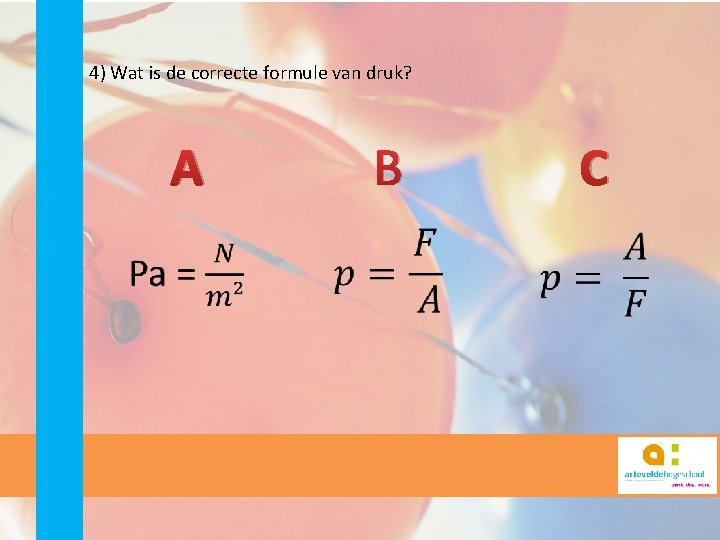
4) Wat is de correcte formule van druk? A B C

5) Hoe zie je aan het deeltjesmodel als de temperatuur van een gas stijgt? A B C De deeltjes bewegen zich sneller voort De deeltjes bewegen zich trager voort Je kan geen verschil zien aan het deeltjesmodel D E F Het gas vertraagt Het gas versnelt De deeltjes worden groter

6) Kan een ideaal gas een vaste stof worden? A B C Ja Neen Enkel als je het afkoelt

7) Waarom kan een ideaal gas geen vloeistof worden? A B C Omdat de deeltjes geen volume hebben Omdat de deeltjes Niet van Gemiddelde snelheid Veranderen Als ze botsen Omdat de deeltjes elkaar niet aantrekken

8) Wat zijn de toestandsfactoren van een ideaal gas? A B C Het aantal deeltjes Snelheid van het gas Druk van het gas D E F Temperatuur van het gas De aantrekkingskracht tussen de deeltjes Het volume van het gas

Bibliografie Bedian, K. (2010, Mei 15). photos/hyekab 25/4609697710. Opgeroepen op April 28, 2015, van flickr: https: //www. flickr. com/photos/hyekab 25/4609697710 Pjetter. (2014, November 4). Fysica/Deeltjesmodel. Opgeroepen op April 28, 2015, van Wikibooks: http: //nl. wikibooks. org/wiki/Fysica/Deeltjesmodel