QUIMIOTERAPIA INTRAPERITONEAL HIPEC DRA CHRISTIAN YAHOSKA COREA URBINA

QUIMIOTERAPIA INTRAPERITONEAL/ HIPEC DRA. CHRISTIAN YAHOSKA COREA URBINA R 2 GO COORDINADOR DRA. ROSA SALCEDO
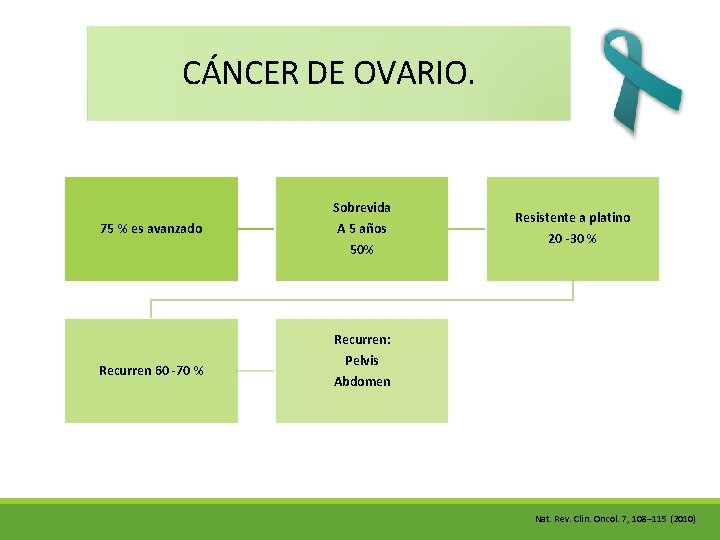
CÁNCER DE OVARIO. Sobrevida 75 % es avanzado Recurren 60 -70 % A 5 años 50% Resistente a platino 20 -30 % Recurren: Pelvis Abdomen Nat. Rev. Clin. Oncol. 7, 108– 115 (2010)

QUIMIOTERAPIA INTRAPERITONEAL EN CÁNCER DE OVARIO
PERITONEO
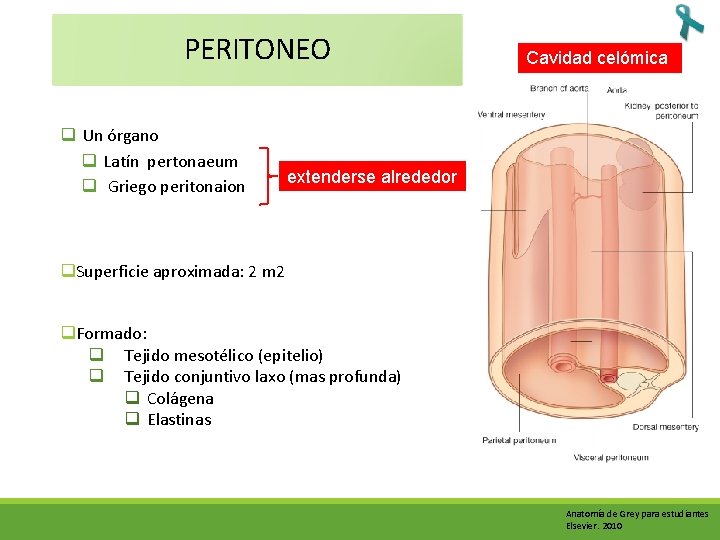
PERITONEO q Un órgano q Latín pertonaeum q Griego peritonaion Cavidad celómica extenderse alrededor q. Superficie aproximada: 2 m 2 q. Formado: q Tejido mesotélico (epitelio) q Tejido conjuntivo laxo (mas profunda) q Colágena q Elastinas Anatomía de Grey para estudiantes Elsevier. 2010
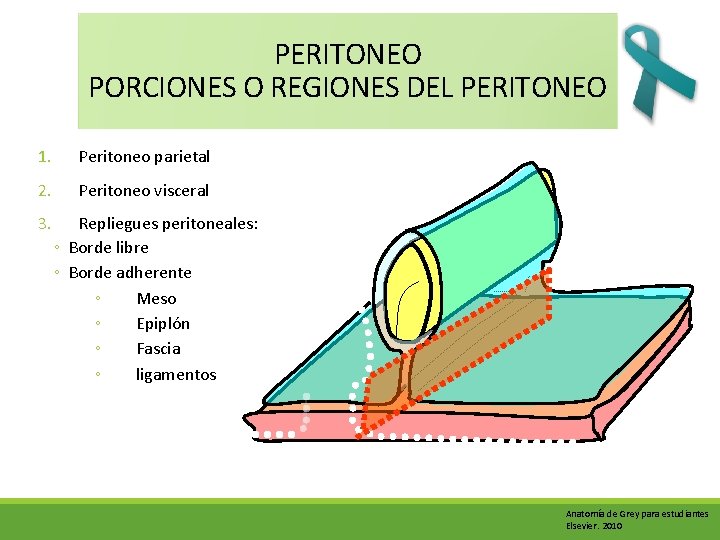
PERITONEO PORCIONES O REGIONES DEL PERITONEO 1. Peritoneo parietal 2. Peritoneo visceral 3. Repliegues peritoneales: ◦ Borde libre ◦ Borde adherente ◦ Meso ◦ Epiplón ◦ Fascia ◦ ligamentos Anatomía de Grey para estudiantes Elsevier. 2010
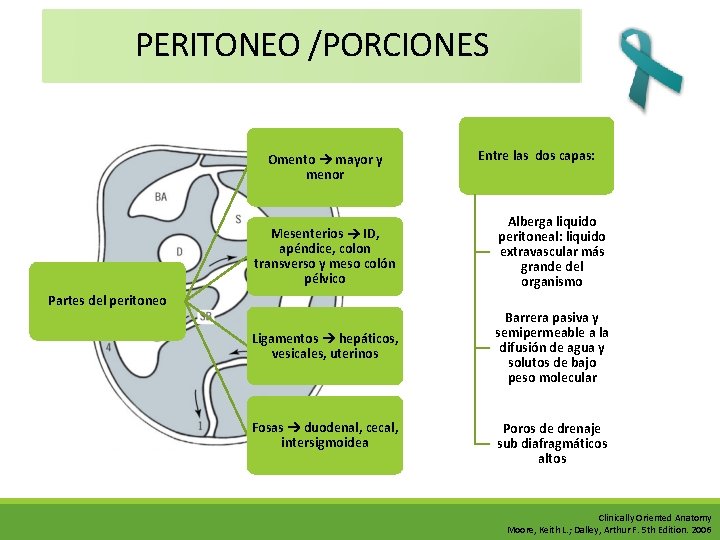
PERITONEO /PORCIONES Omento mayor y menor Entre las dos capas: Mesenterios ID, apéndice, colon transverso y meso colón pélvico Alberga liquido peritoneal: liquido extravascular más grande del organismo Ligamentos hepáticos, vesicales, uterinos Barrera pasiva y semipermeable a la difusión de agua y solutos de bajo peso molecular Partes del peritoneo Fosas duodenal, cecal, intersigmoidea Poros de drenaje sub diafragmáticos altos Clinically Oriented Anatomy Moore, Keith L. ; Dalley, Arthur F. 5 th Edition. 2006

LIQUIDO PERITONEAL Ø 100 cc q Proteínas 3 g q Electrolitos q Densidad 1016 q Antimicrobiana ØPelícula protectora de movimiento ØCélulas 2000 a 2500 x cm 3 q Macrófagos q Mastocitos q Fibroblastos q Linfocitos Ascitis � Liquido >300 cc � Clínicamente >1000 ml � Desequilibrio �Producción a nivel de capilar �Reabsorción (poros linfáticos, manchas lácteas) Skandalakis' Surgical Anatomy Chapter 10. Peritoneum, Omenta. MG Hill thirth edition 2006
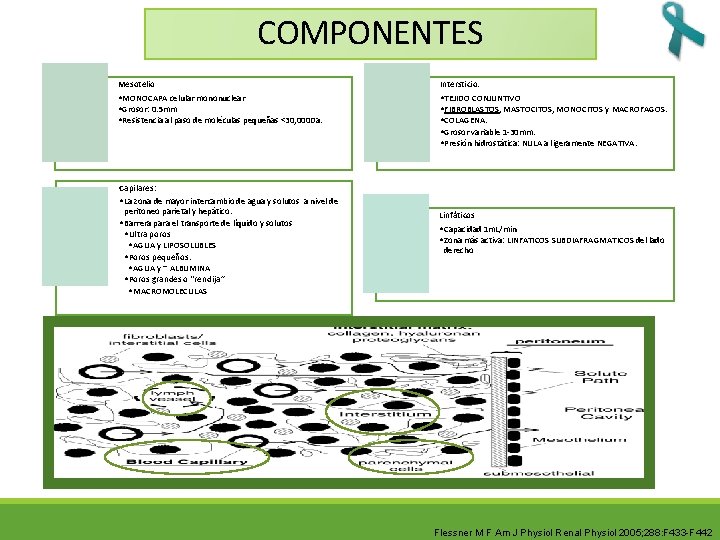
COMPONENTES Mesotelio Intersticio: • MONOCAPA celular mononuclear • Grosor: 0. 5 mm • Resistencia al paso de moléculas pequeñas <30, 000 Da. • TEJIDO CONJUNTIVO • FIBROBLASTOS, MASTOCITOS, MONOCITOS y MACROFAGOS. • COLAGENA. • Grosor variable 1 -30 mm. • Presión hidrostática: NULA a ligeramente NEGATIVA. Capilares: • La zona de mayor intercambio de agua y solutos a nivel de peritoneo parietal y hepático. • Barrera para el transporte de líquido y solutos • Ultra poros • AGUA y LIPOSOLUBLES • Poros pequeños: • AGUA y ~ ALBUMINA • Poros grandes o “rendija” • MACROMOLECULAS Linfáticos • Capacidad 1 m. L/min • Zona más activa: LINFATICOS SUBDIAFRAGMATICOS del lado derecho Flessner M F Am J Physiol Renal Physiol 2005; 288: F 433 -F 442
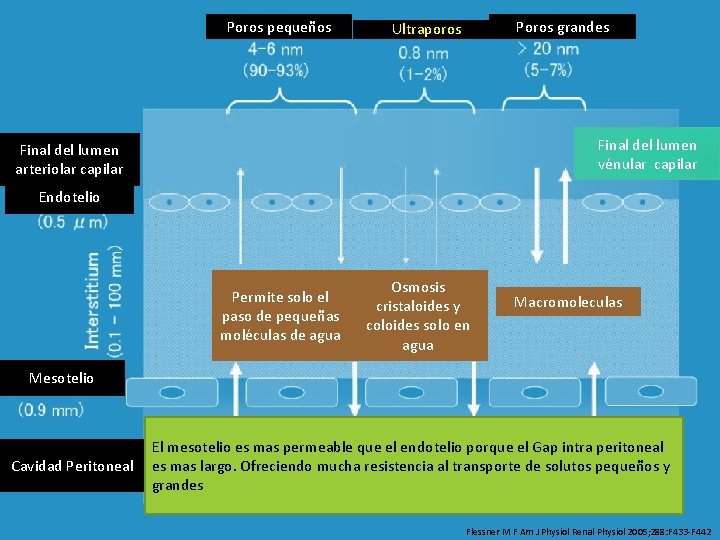
Poros pequeños Poros grandes Ultraporos FISIOLOGIA PERITONEAL Final del lumen vénular capilar Final del lumen arteriolar capilar Endotelio Permite solo el paso de pequeñas moléculas de agua Osmosis cristaloides y coloides solo en agua Macromoleculas Mesotelio Cavidad Peritoneal El mesotelio es mas permeable que el endotelio porque el Gap intra peritoneal es mas largo. Ofreciendo mucha resistencia al transporte de solutos pequeños y grandes Flessner M F Am J Physiol Renal Physiol 2005; 288: F 433 -F 442
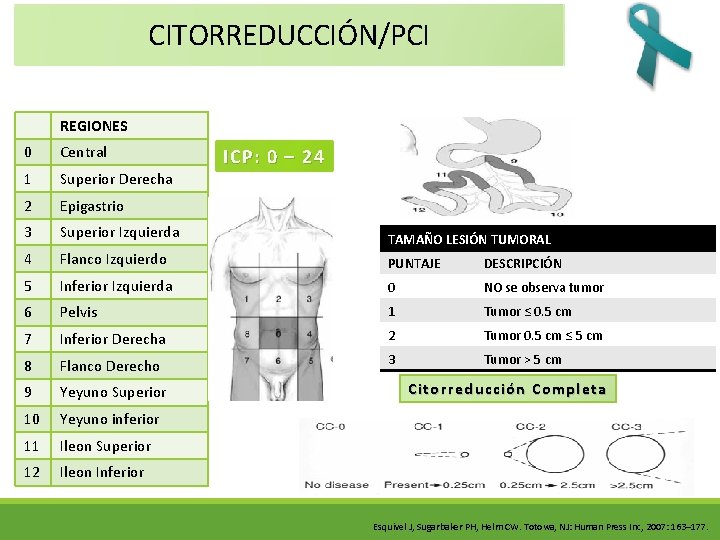
CITORREDUCCIÓN/PCI REGIONES 0 Central 1 Superior Derecha 2 Epigastrio 3 Superior Izquierda TAMAÑO LESIÓN TUMORAL 4 Flanco Izquierdo PUNTAJE DESCRIPCIÓN 5 Inferior Izquierda 0 NO se observa tumor 6 Pelvis 1 Tumor ≤ 0. 5 cm 7 Inferior Derecha 2 Tumor 0. 5 cm ≤ 5 cm 8 Flanco Derecho 3 Tumor ˃ 5 cm 9 Yeyuno Superior 10 Yeyuno inferior 11 Ileon Superior 12 Ileon Inferior ICP: 0 – 24 Citorreducción Completa Esquivel J, Sugarbaker PH, Helm CW. Totowa, NJ: Human Press Inc, 2007: 163– 177.
BASES DE MANEJO IP

CARCINOMATOSIS q 1931 Sampson q. Diseminación regional del cáncer en el carcinoma ovárico • 10 -20% - Mesotelioma • 7 -14% - CA peritoneal primario • 73% diseminación de tumores intraabdominales COMPLICACIONES ORIGEN q“Forma de diseminación del cáncer sobre la superficie del peritoneo. ” • Ascitis • Obstrucción intestinal Sugarbaker PH. Peritonectomy Procedures. Ann Surg 1995; 221: 29 -42 •

CONCEPTOS CLAVE La diseminación peritoneal no es un proceso uniforme. La descripción de la barrera peritoneal (espacio – plasma) “Ineficiencia metastásica” • Células neoplásicas libres: • Peritoneo - casi siempre progresan = impacto en SG • Circulantes o MO – rara vez progresan = poco o nulo impacto SG • Manejo efectivo de carcinomatosis = impacto en SG • Grandes moleculas en cavidad peritoneal se mantienen secuestradas por horas y lentamente se absorben. Sugarbaker PH. Int J Hyperthermia. 2007; 23 (5): 431 -442
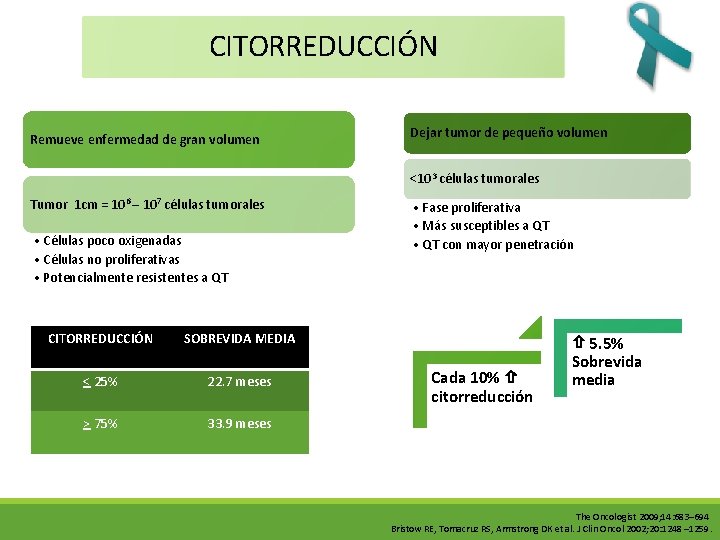
CITORREDUCCIÓN Remueve enfermedad de gran volumen Dejar tumor de pequeño volumen ˂103 células tumorales Tumor 1 cm = 106 – 107 células tumorales • Células poco oxigenadas • Células no proliferativas • Potencialmente resistentes a QT CITORREDUCCIÓN SOBREVIDA MEDIA ˂ 25% 22. 7 meses ˃ 75% 33. 9 meses • Fase proliferativa • Más susceptibles a QT • QT con mayor penetración Cada 10% citorreducción 5. 5% Sobrevida media The Oncologist 2009; 14: 683– 694 Bristow RE, Tomacruz RS, Armstrong DK et al. J Clin Oncol 2002; 20: 1248 – 1259.
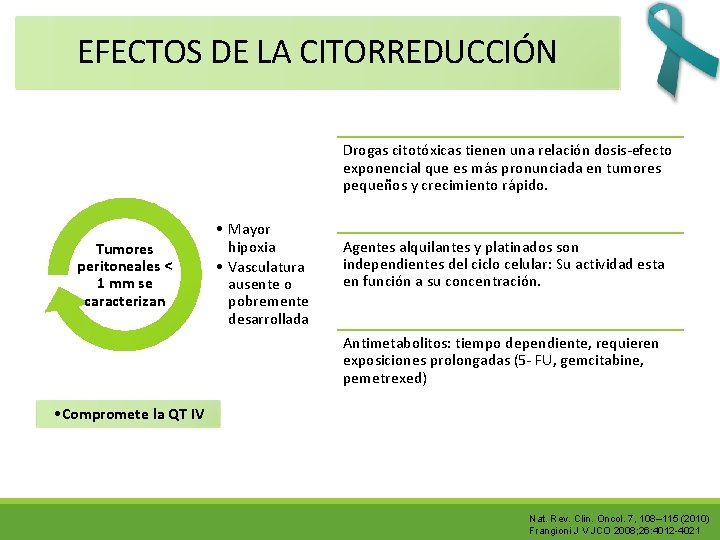
EFECTOS DE LA CITORREDUCCIÓN Drogas citotóxicas tienen una relación dosis-efecto exponencial que es más pronunciada en tumores pequeños y crecimiento rápido. Tumores peritoneales ˂ 1 mm se caracterizan • Mayor hipoxia • Vasculatura ausente o pobremente desarrollada Agentes alquilantes y platinados son independientes del ciclo celular: Su actividad esta en función a su concentración. Antimetabolitos: tiempo dependiente, requieren exposiciones prolongadas (5 - FU, gemcitabine, pemetrexed) • Compromete la QT IV Nat. Rev. Clin. Oncol. 7, 108– 115 (2010) Frangioni J V JCO 2008; 26: 4012 -4021
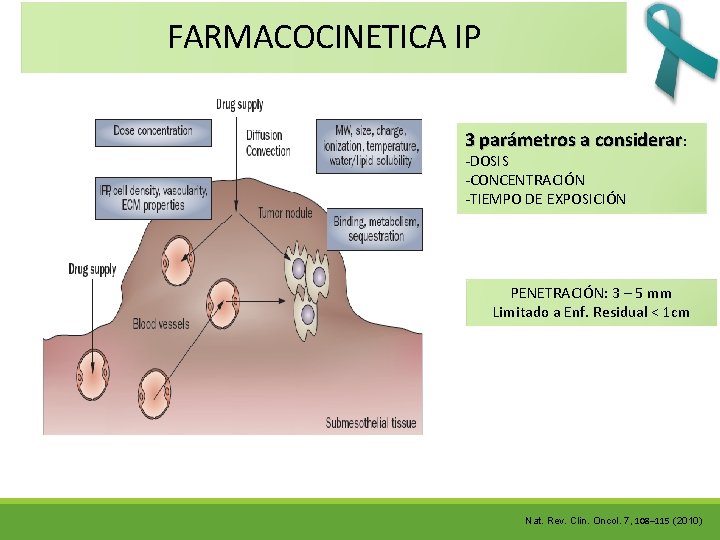
FARMACOCINETICA IP 3 parámetros a considerar: -DOSIS -CONCENTRACIÓN -TIEMPO DE EXPOSICIÓN PENETRACIÓN: 3 – 5 mm Limitado a Enf. Residual ˂ 1 cm Nat. Rev. Clin. Oncol. 7, 108– 115 (2010)
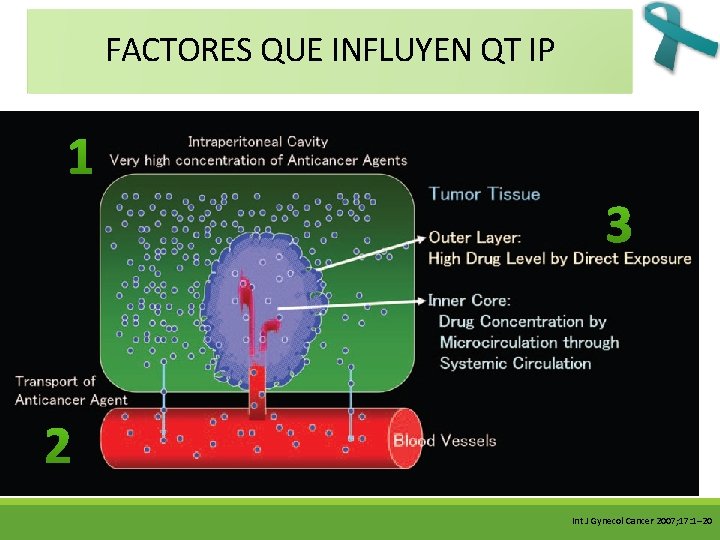
FACTORES QUE INFLUYEN QT IP 1 3 2 Int J Gynecol Cancer 2007; 17: 1– 20
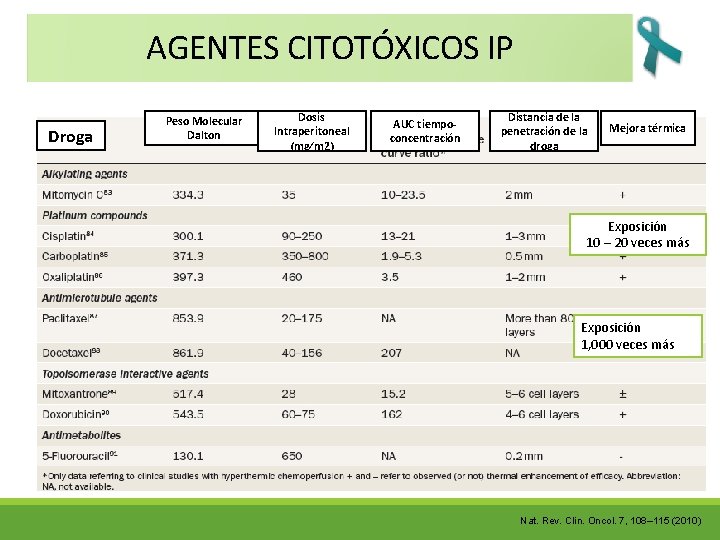
AGENTES CITOTÓXICOS IP Droga Peso Molecular Dalton Dosis Intraperitoneal (mg∕m 2) AUC tiempoconcentración Distancia de la penetración de la droga Mejora térmica Exposición 10 – 20 veces más Exposición 1, 000 veces más Nat. Rev. Clin. Oncol. 7, 108– 115 (2010)
QT INTRAPERITONEAL
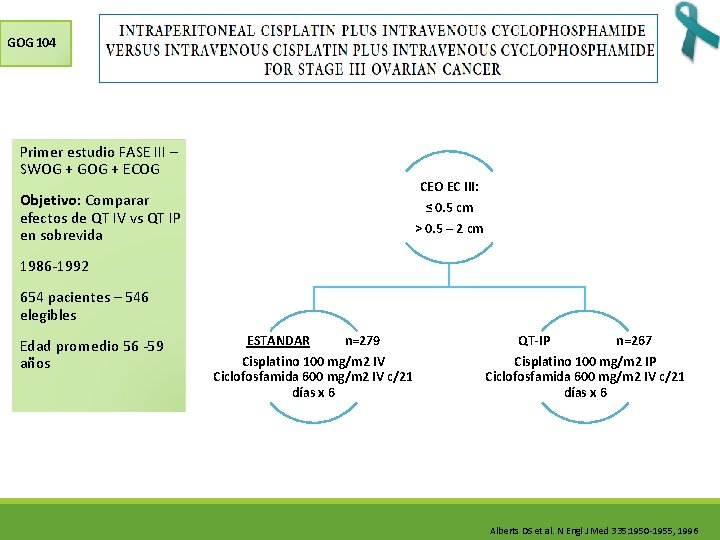
GOG 104 Primer estudio FASE III – SWOG + GOG + ECOG CEO EC III: ≤ 0. 5 cm Objetivo: Comparar efectos de QT IV vs QT IP en sobrevida ˃ 0. 5 – 2 cm 1986 -1992 654 pacientes – 546 elegibles Edad promedio 56 -59 años ESTANDAR n=279 Cisplatino 100 mg/m 2 IV Ciclofosfamida 600 mg/m 2 IV c/21 días x 6 QT-IP n=267 Cisplatino 100 mg/m 2 IP Ciclofosfamida 600 mg/m 2 IV c/21 días x 6 Alberts DS et al. N Engl J Med 335: 1950 -1955, 1996
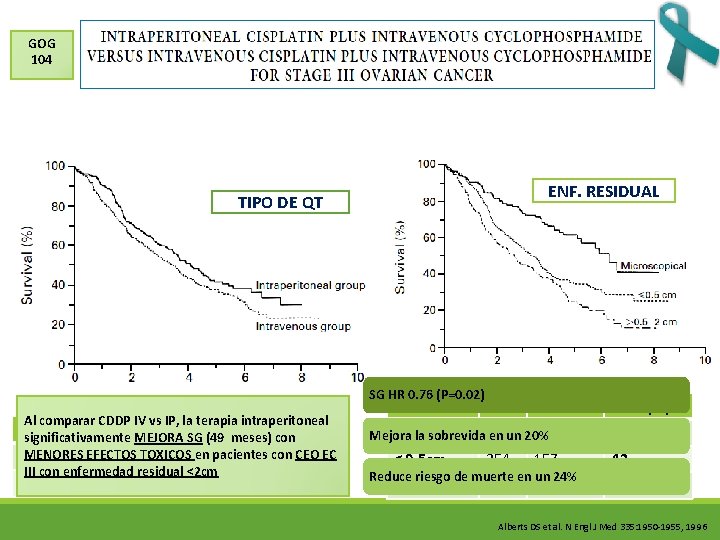
GOG 104 ENF. RESIDUAL TIPO DE QT SG HR 0. 76 (P=0. 02) Al comparar CDDP IV vs IP, la terapia intraperitoneal Grupo N Muertes SGM (m) significativamente MEJORA SG (49 meses) con MENORES EFECTOS TOXICOS en pacientes con CEO EC IP 267 147 49 III con enfermedad residual <2 cm IV 279 174 41 Residual N Muertes Microsc. 139 53 Mejora la sobrevida en un 20% SGM (m) 76 < 0. 5 cm 254 157 42 >0. 5 -2 cm 153 111 32 Reduce riesgo de muerte en un 24% Alberts DS et al. N Engl J Med 335: 1950 -1955, 1996
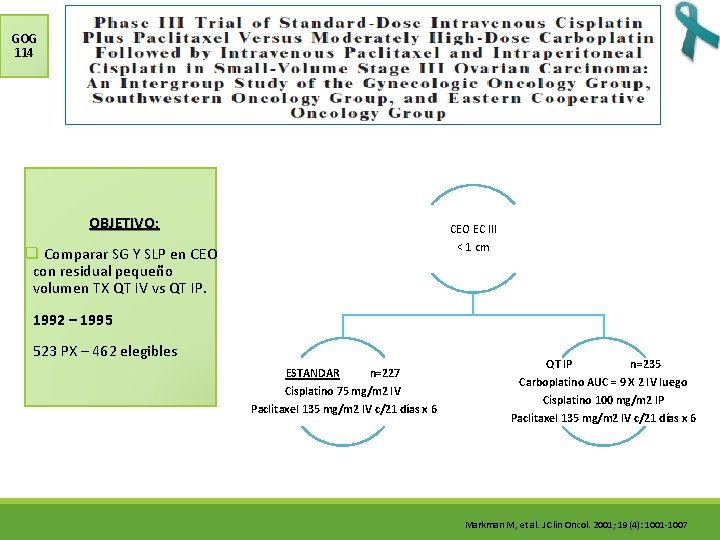
GOG 114 OBJETIVO: CEO EC III ˂ 1 cm q Comparar SG Y SLP en CEO con residual pequeño volumen TX QT IV vs QT IP. 1992 – 1995 523 PX – 462 elegibles ESTANDAR n=227 Cisplatino 75 mg/m 2 IV Paclitaxel 135 mg/m 2 IV c/21 días x 6 QT IP n=235 Carboplatino AUC = 9 X 2 IV luego Cisplatino 100 mg/m 2 IP Paclitaxel 135 mg/m 2 IV c/21 días x 6 Markman M, et al. J Clin Oncol. 2001; 19(4): 1001 -1007
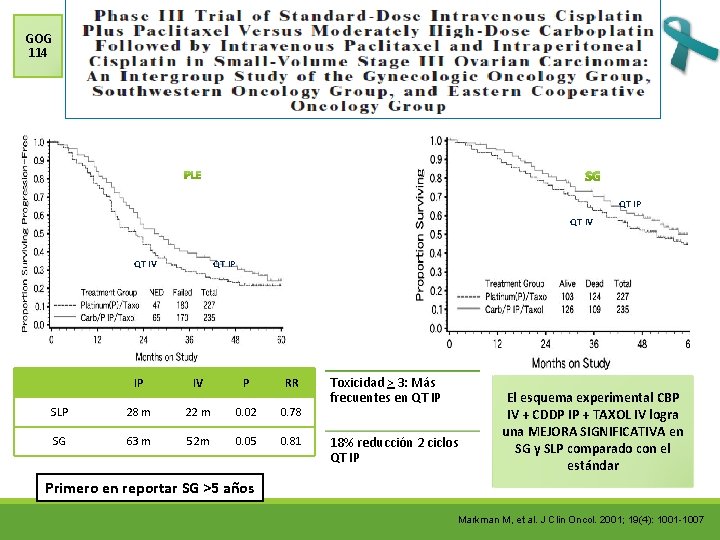
GOG 114 QT IP QT IV QT IP IP IV P RR SLP 28 m 22 m 0. 02 0. 78 SG 63 m 52 m 0. 05 0. 81 Toxicidad ˃ 3: Más frecuentes en QT IP 18% reducción 2 ciclos QT IP El esquema experimental CBP IV + CDDP IP + TAXOL IV logra una MEJORA SIGNIFICATIVA en SG y SLP comparado con el estándar Primero en reportar SG >5 años Markman M, et al. J Clin Oncol. 2001; 19(4): 1001 -1007
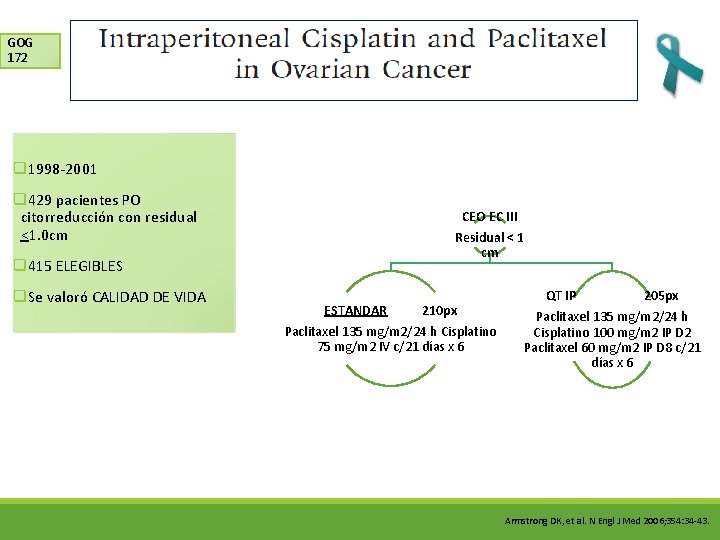
GOG 172 q 1998 -2001 q 429 pacientes PO citorreducción con residual <1. 0 cm q 415 ELEGIBLES q. Se valoró CALIDAD DE VIDA CEO EC III Residual ˂ 1 cm ESTANDAR 210 px Paclitaxel 135 mg/m 2/24 h Cisplatino 75 mg/m 2 IV c/21 días x 6 QT IP 205 px Paclitaxel 135 mg/m 2/24 h Cisplatino 100 mg/m 2 IP D 2 Paclitaxel 60 mg/m 2 IP D 8 c/21 días x 6 Armstrong DK, et al. N Engl J Med 2006; 354: 34 -43.
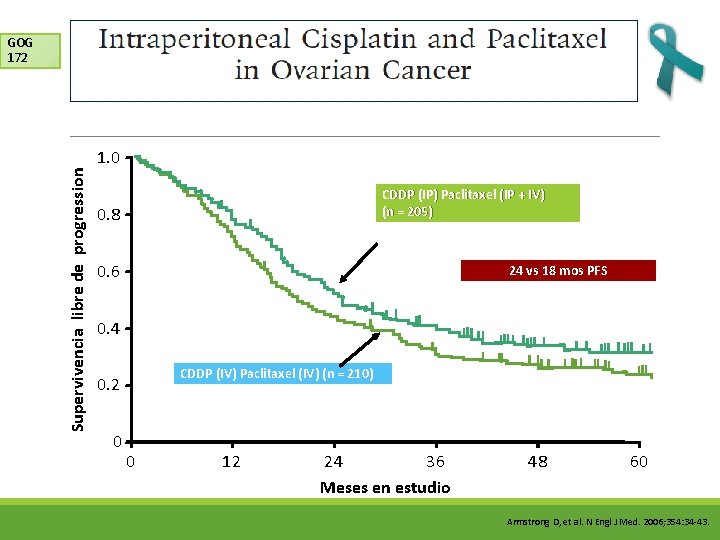
Supervivencia libre de progression GOG 172 1. 0 CDDP (IP) Paclitaxel (IP + IV) (n = 205) 0. 8 0. 6 24 vs 18 mos PFS 0. 4 CDDP (IV) Paclitaxel (IV) (n = 210) 0. 2 0 0 12 24 36 Meses en estudio 48 60 Armstrong D, et al. N Engl J Med. 2006; 354: 34 -43.
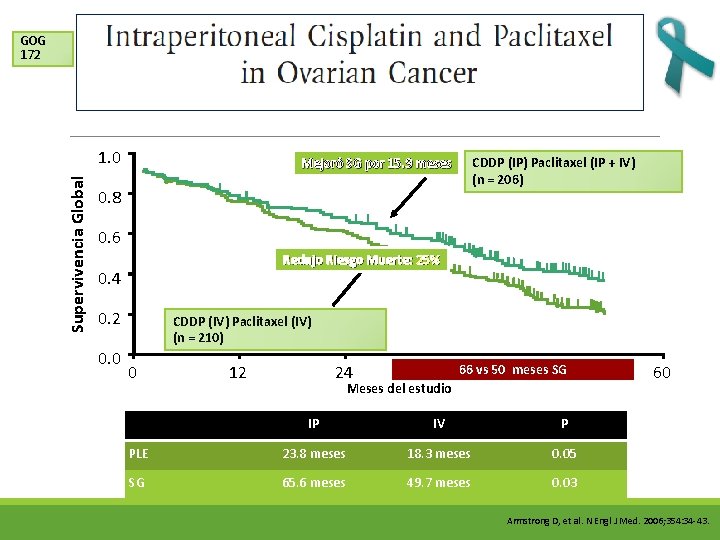
GOG 172 Supervivencia Global 1. 0 Mejoró SG por 15. 9 meses 0. 8 CDDP (IP) Paclitaxel (IP + IV) (n = 206) 0. 6 Redujo Riesgo Muerte: 25% 0. 4 0. 2 0. 0 CDDP (IV) Paclitaxel (IV) (n = 210) 0 12 24 3666 vs 50 meses SG 48 Meses del estudio IP IV P PLE 23. 8 meses 18. 3 meses 0. 05 SG 65. 6 meses 49. 7 meses 0. 03 60 Armstrong D, et al. N Engl J Med. 2006; 354: 34 -43.
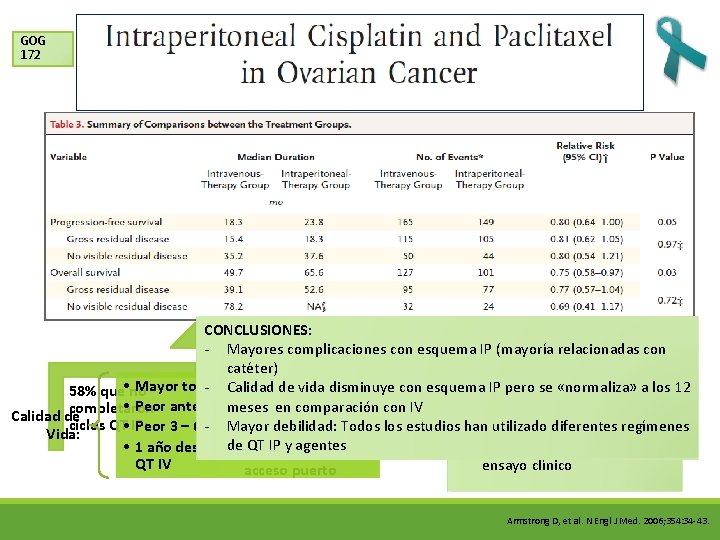
GOG 172 CONCLUSIONES: - Mayores complicaciones con esquema IP (mayoría relacionadas con • QT IP utilizó dosis más altas y 34% se relacionó frecuentes al CATÉTER: catéter) • Mayor toxicidad QT IP (P ≤ 0. 001) - Calidad de vida disminuye con esquema IP pero se «normaliza» a los 12 • Toxicidad mayor en QT IP 58% que no • Infección • Peor antes de ciclo 4 meses en comparación con IV completaron • Mejora PLE y SG en QT IP • Obstrucción Calidad de ciclos QT IP: - Mayor debilidad: Todos los estudios han utilizado diferentes regímenes • Peor 3 – 6 semanas después TX • La SG 65. 6 meses en QT IP es • Fuga Vida: de QT IP y agentes • 1 año después TX NO diferencia con lo más largo reportado en un • Problemas QT IV ensayo clínico acceso puerto Armstrong D, et al. N Engl J Med. 2006; 354: 34 -43.
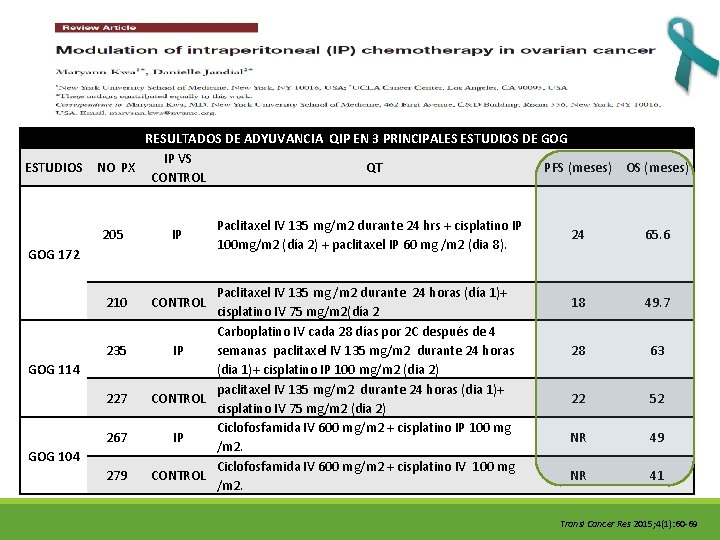
RESULTADOS DE ADYUVANCIA QIP EN 3 PRINCIPALES ESTUDIOS DE GOG IP VS ESTUDIOS NO PX QT PFS (meses) OS (meses) CONTROL 205 IP 210 CONTROL GOG 172 235 GOG 114 227 267 GOG 104 279 Paclitaxel IV 135 mg/m 2 durante 24 hrs + cisplatino IP 100 mg/m 2 (día 2) + paclitaxel IP 60 mg /m 2 (dia 8). Paclitaxel IV 135 mg /m 2 durante 24 horas (día 1)+ cisplatino IV 75 mg/m 2(día 2 Carboplatino IV cada 28 días por 2 C después de 4 IP semanas paclitaxel IV 135 mg/m 2 durante 24 horas (dia 1)+ cisplatino IP 100 mg/m 2 (dia 2) paclitaxel IV 135 mg/m 2 durante 24 horas (dia 1)+ CONTROL cisplatino IV 75 mg/m 2 (dia 2) Ciclofosfamida IV 600 mg/m 2 + cisplatino IP 100 mg IP /m 2. Ciclofosfamida IV 600 mg/m 2 + cisplatino IV 100 mg CONTROL /m 2. 24 65. 6 18 49. 7 28 63 22 52 NR 49 NR 41 Transl Cancer Res 2015; 4(1): 60 -69
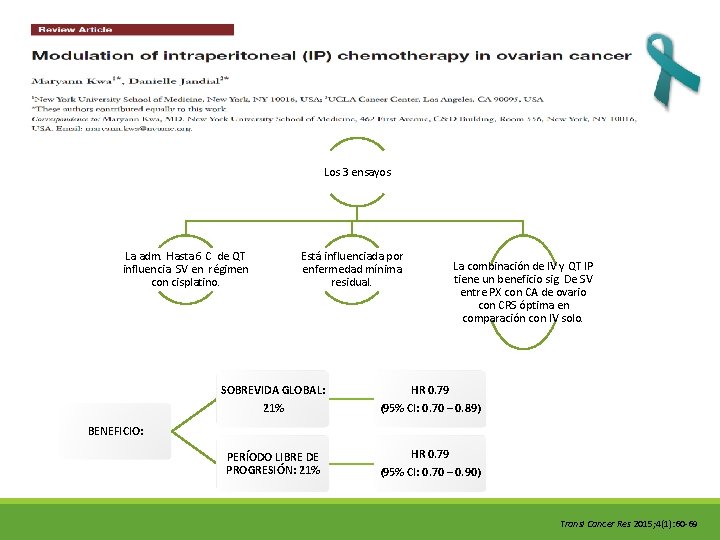
Los 3 ensayos La adm. Hasta 6 C de QT influencia SV en régimen con cisplatino. Está influenciada por enfermedad mínima residual. La combinación de IV y QT IP tiene un beneficio sig. De SV entre PX con CA de ovario con CRS óptima en comparación con IV solo. SOBREVIDA GLOBAL: 21% HR 0. 79 (95% CI: 0. 70 – 0. 89) PERÍODO LIBRE DE PROGRESIÓN: 21% HR 0. 79 (95% CI: 0. 70 – 0. 90) BENEFICIO: Transl Cancer Res 2015; 4(1): 60 -69
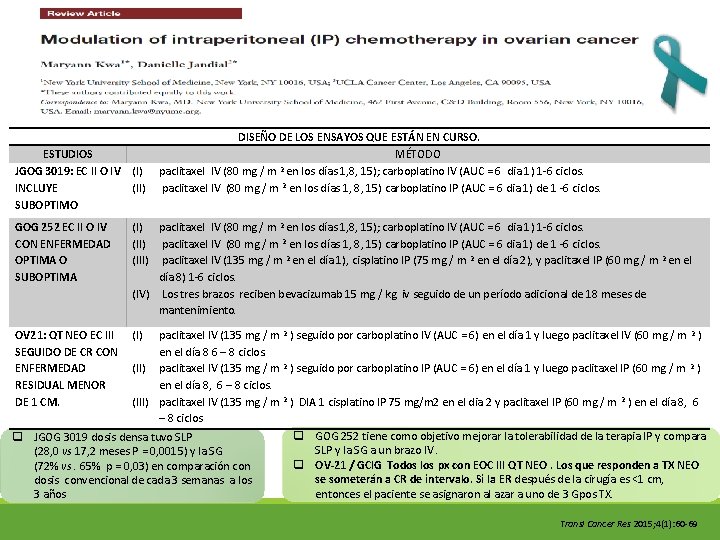
ESTUDIOS JGOG 3019: EC II O IV (I) INCLUYE (II) SUBOPTIMO GOG 252 EC II O IV CON ENFERMEDAD OPTIMA O SUBOPTIMA DISEÑO DE LOS ENSAYOS QUE ESTÁN EN CURSO. MÉTODO 2 paclitaxel IV (80 mg / m en los días 1, 8, 15); carboplatino IV (AUC = 6 dia 1) 1 -6 ciclos. paclitaxel IV (80 mg / m 2 en los días 1, 8, 15) carboplatino IP (AUC = 6 dia 1) de 1 -6 ciclos. (I) paclitaxel IV (80 mg / m 2 en los días 1, 8, 15); carboplatino IV (AUC = 6 dia 1) 1 -6 ciclos. (II) paclitaxel IV (80 mg / m 2 en los días 1, 8, 15) carboplatino IP (AUC = 6 dia 1) de 1 -6 ciclos. (III) paclitaxel IV (135 mg / m 2 en el día 1), cisplatino IP (75 mg / m 2 en el día 2), y paclitaxel IP (60 mg / m 2 en el día 8) 1 -6 ciclos. (IV) Los tres brazos reciben bevacizumab 15 mg / kg iv seguido de un período adicional de 18 meses de mantenimiento. OV 21: QT NEO EC III (I) SEGUIDO DE CR CON ENFERMEDAD (II) RESIDUAL MENOR DE 1 CM. (III) paclitaxel IV (135 mg / m 2 ) seguido por carboplatino IV (AUC = 6) en el día 1 y luego paclitaxel IV (60 mg / m 2 ) en el día 8 6 – 8 ciclos. paclitaxel IV (135 mg / m 2 ) seguido por carboplatino IP (AUC = 6) en el día 1 y luego paclitaxel IP (60 mg / m 2 ) en el día 8, 6 – 8 ciclos. paclitaxel IV (135 mg / m 2 ) DIA 1 cisplatino IP 75 mg/m 2 en el dia 2 y paclitaxel IP (60 mg / m 2 ) en el día 8, 6 – 8 ciclos q GOG 252 tiene como objetivo mejorar la tolerabilidad de la terapia IP y compara q JGOG 3019 dosis densa tuvo SLP y la SG a un brazo IV. (28, 0 vs 17, 2 meses P = 0, 0015) y la SG q OV-21 / GCIG Todos los px con EOC III QT NEO. Los que responden a TX NEO (72% vs. 65% p = 0, 03) en comparación con se someterán a CR de intervalo. Si la ER después de la cirugía es <1 cm, dosis convencional de cada 3 semanas a los entonces el paciente se asignaron al azar a uno de 3 Gpos TX. 3 años Transl Cancer Res 2015; 4(1): 60 -69
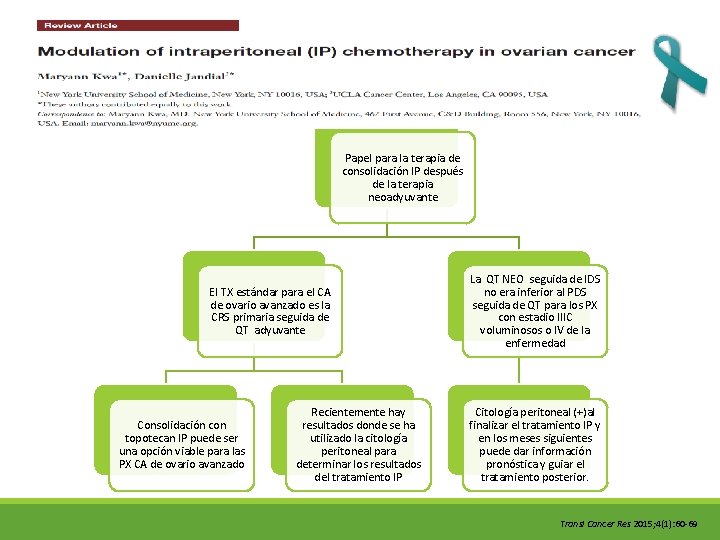
Papel para la terapia de consolidación IP después de la terapia neoadyuvante El TX estándar para el CA de ovario avanzado es la CRS primaria seguida de QT adyuvante Consolidación con topotecan IP puede ser una opción viable para las PX CA de ovario avanzado Recientemente hay resultados donde se ha utilizado la citología peritoneal para determinar los resultados del tratamiento IP La QT NEO seguida de IDS no era inferior al PDS seguida de QT para los PX con estadio IIIC voluminosos o IV de la enfermedad Citología peritoneal (+)al finalizar el tratamiento IP y en los meses siguientes puede dar información pronóstica y guiar el tratamiento posterior. Transl Cancer Res 2015; 4(1): 60 -69

SUSPENSION DE QT IP Toxicidad QT Complicaciones relacionadas al catéter 33% • • • Fuga Ruptura Oclusión Infección Abscesos abdominales Peritonitis Fistula Dolor Perforación intestinal • Paclitaxel 2. 3% • Adherencias intestinales Commun Oncol 2010; 7: 67– 72
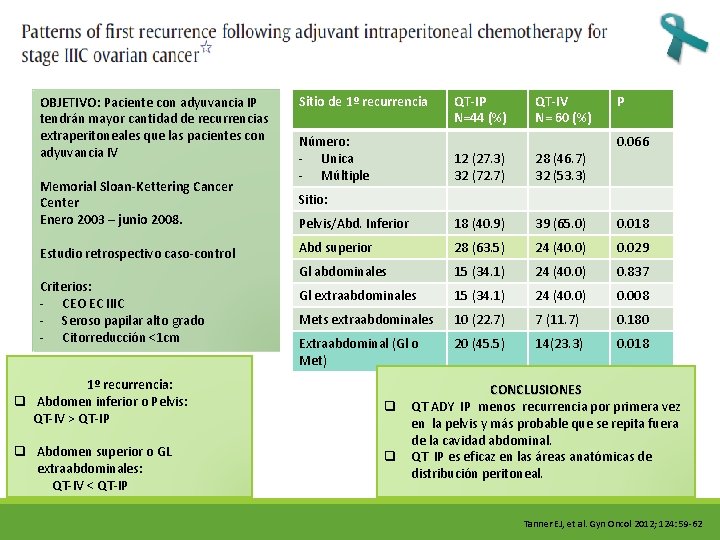
OBJETIVO: Paciente con adyuvancia IP tendrán mayor cantidad de recurrencias extraperitoneales que las pacientes con adyuvancia IV Memorial Sloan-Kettering Cancer Center Enero 2003 – junio 2008. Estudio retrospectivo caso-control Criterios: - CEO EC IIIC - Seroso papilar alto grado - Citorreducción <1 cm 1º recurrencia: q Abdomen inferior o Pelvis: QT-IV > QT-IP q Abdomen superior o GL extraabdominales: QT-IV < QT-IP Sitio de 1º recurrencia Número: - Unica - Múltiple QT-IP N=44 (%) QT-IV N= 60 (%) P 0. 066 12 (27. 3) 32 (72. 7) 28 (46. 7) 32 (53. 3) Pelvis/Abd. Inferior 18 (40. 9) 39 (65. 0) 0. 018 Abd superior 28 (63. 5) 24 (40. 0) 0. 029 Gl abdominales 15 (34. 1) 24 (40. 0) 0. 837 Gl extraabdominales 15 (34. 1) 24 (40. 0) 0. 008 Mets extraabdominales 10 (22. 7) 7 (11. 7) 0. 180 Extraabdominal (Gl o Met) 20 (45. 5) 14(23. 3) 0. 018 Sitio: q q CONCLUSIONES QT ADY IP menos recurrencia por primera vez en la pelvis y más probable que se repita fuera de la cavidad abdominal. QT IP es eficaz en las áreas anatómicas de distribución peritoneal. Tanner EJ, et al. Gyn Oncol 2012; 124: 59 -62
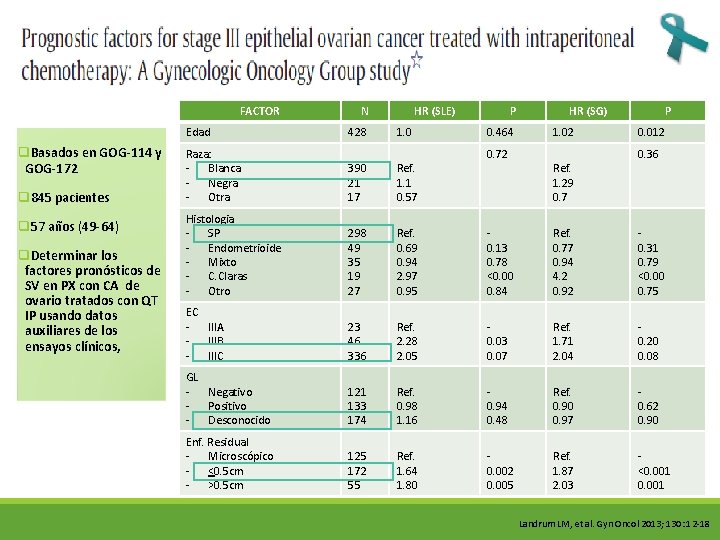
FACTOR Edad q. Basados en GOG-114 y GOG-172 q 845 pacientes q 57 años (49 -64) q. Determinar los factores pronósticos de SV en PX con CA de ovario tratados con QT IP usando datos auxiliares de los ensayos clínicos, N 428 HR (SLE) 1. 0 P 0. 464 0. 72 HR (SG) 1. 02 P 0. 012 Raza: - Blanca - Negra - Otra 390 21 17 Ref. 1. 1 0. 57 Histologia - SP - Endometrioide - Mixto - C. Claras - Otro 298 49 35 19 27 Ref. 0. 69 0. 94 2. 97 0. 95 0. 13 0. 78 <0. 00 0. 84 Ref. 0. 77 0. 94 4. 2 0. 92 0. 31 0. 79 <0. 00 0. 75 EC - IIIA - IIIB - IIIC 23 46 336 Ref. 2. 28 2. 05 0. 03 0. 07 Ref. 1. 71 2. 04 0. 20 0. 08 GL - Negativo - Positivo - Desconocido 121 133 174 Ref. 0. 98 1. 16 0. 94 0. 48 Ref. 0. 90 0. 97 0. 62 0. 90 Enf. Residual - Microscópico - <0. 5 cm - >0. 5 cm 125 172 55 Ref. 1. 64 1. 80 0. 002 0. 005 Ref. 1. 87 2. 03 <0. 001 Ref. 1. 29 0. 7 0. 36 Landrum LM, et al. Gyn Oncol 2013; 130: 12 -18
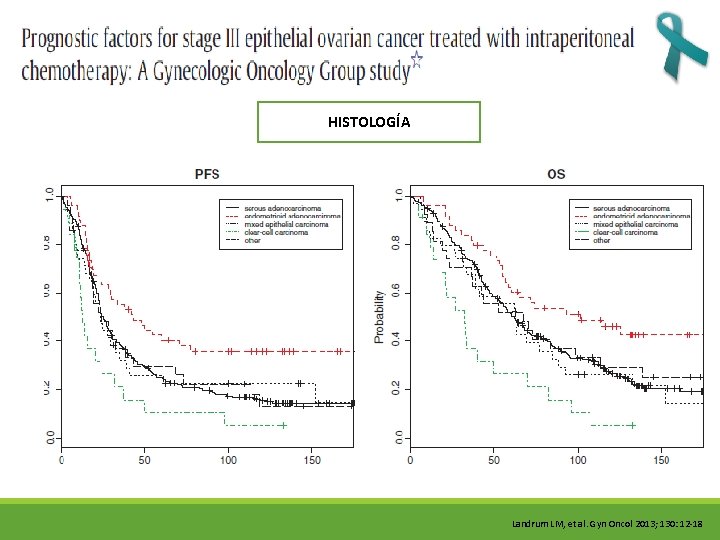
HISTOLOGÍA Landrum LM, et al. Gyn Oncol 2013; 130: 12 -18
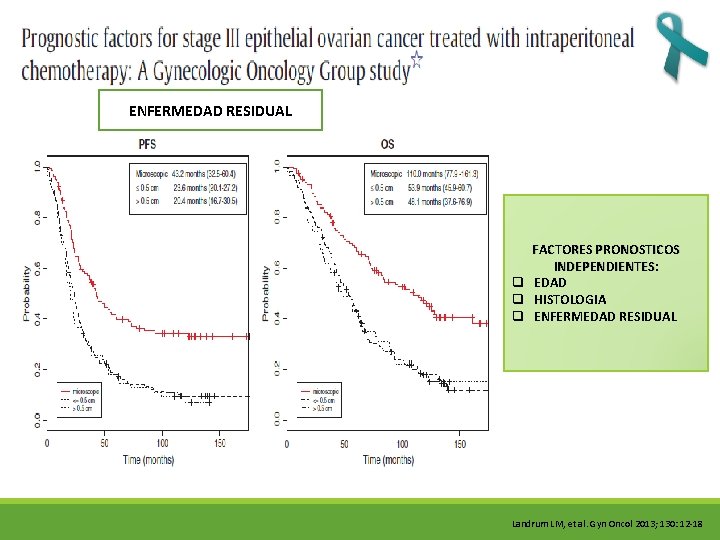
ENFERMEDAD RESIDUAL FACTORES PRONOSTICOS INDEPENDIENTES: INDEPENDIENTES q EDAD q HISTOLOGIA q ENFERMEDAD RESIDUAL Landrum LM, et al. Gyn Oncol 2013; 130: 12 -18
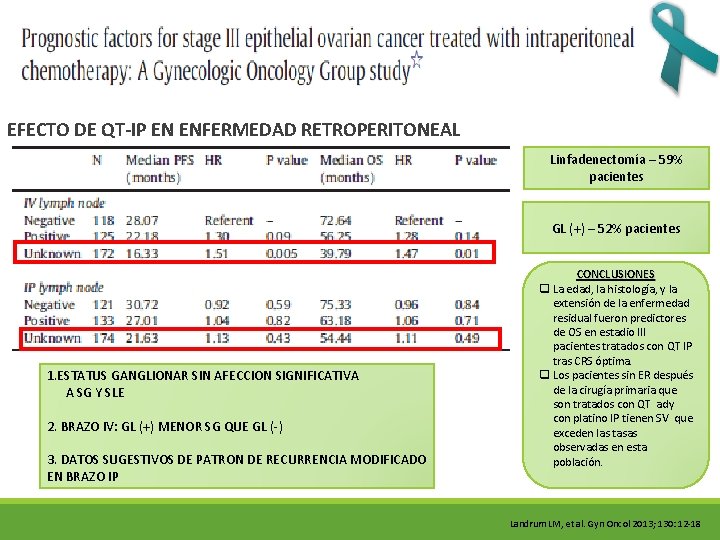
EFECTO DE QT-IP EN ENFERMEDAD RETROPERITONEAL Linfadenectomía – 59% pacientes GL (+) – 52% pacientes 1. ESTATUS GANGLIONAR SIN AFECCION SIGNIFICATIVA A SG Y SLE 2. BRAZO IV: GL (+) MENOR SG QUE GL (-) 3. DATOS SUGESTIVOS DE PATRON DE RECURRENCIA MODIFICADO EN BRAZO IP CONCLUSIONES q La edad, la histología, y la extensión de la enfermedad residual fueron predictores de OS en estadio III pacientes tratados con QT IP tras CRS óptima. q Los pacientes sin ER después de la cirugía primaria que son tratados con QT ady con platino IP tienen SV que exceden las tasas observadas en esta población. Landrum LM, et al. Gyn Oncol 2013; 130: 12 -18
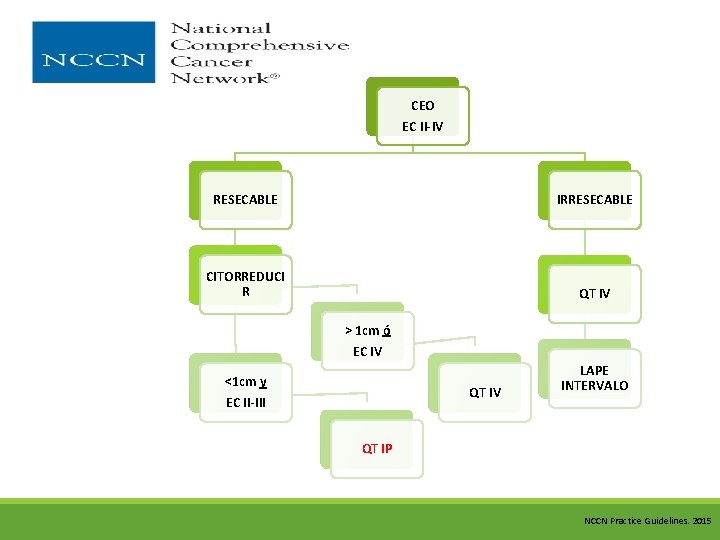
CEO EC II-IV RESECABLE IRRESECABLE CITORREDUCI R QT IV > 1 cm ó EC IV <1 cm y QT IV EC II-III LAPE INTERVALO QT IP NCCN Practice Guidelines. 2015

Paclitaxel 135 mg/m 2 IV en 24 hrs D 1 Cisplatino 75 – 100 mg/m 2 IP D 2 después paclitaxel IV Paclitaxel 60 mg/m 2 IP D 8 Repetir cada 3 meses por 6 ciclos NCCN Practice Guidelines. 2015

CONCLUSIONES – QT IP Opción terapéutica para el manejo de CARCINOMATOSIS PERITONEAL Útil en pacientes seleccionados: EC III, Citoreducción de inicio óptima, Buen estado funcional Comprometidos a tratamiento (incluido cuidados de catéter)

HIPEC

ANTECEDENTES • 1980 John S. Spratt y cols. • Primer caso: • Masculino 35 años • PSEUDOMIXOMA PERITONEAL 1994 Loggie y cols: Primer reporte de paciente con CEO tratada con HIPEC Procedimiento: • LAPE + Lavado (mucina) + exploración (foco primario: cistadeocarcinoma del páncreas) • Infusión 2. 5 L Ringer Lactato con técnica cerrada • Temperatura: 42°C (1. 5 h) • QT IP: Thiotepa (intraoperatorio) + Metotrexato (5 días postqx, con hipertermia) Spratt JS, et al. Cancer Res. 1980; 40: 256 -260
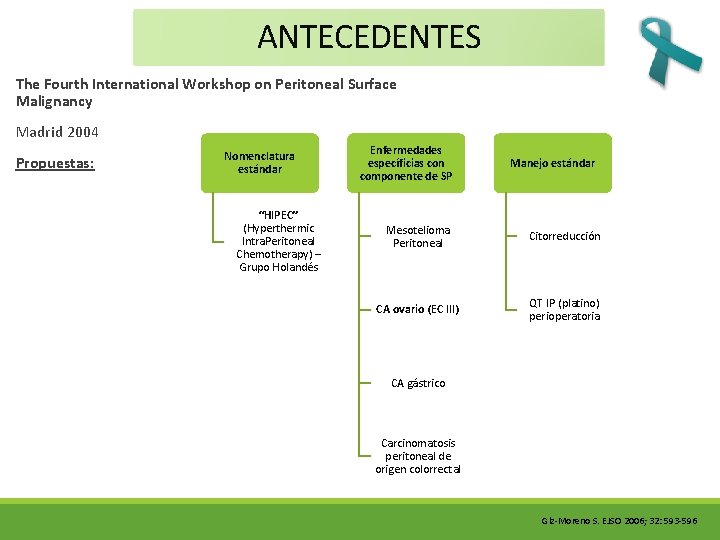
ANTECEDENTES The Fourth International Workshop on Peritoneal Surface Malignancy Madrid 2004 Propuestas: Nomenclatura estándar “HIPEC” (Hyperthermic Intra. Peritoneal Chemotherapy) – Grupo Holandés Enfermedades específicias con componente de SP Manejo estándar Mesotelioma Peritoneal Citorreducción CA ovario (EC III) QT IP (platino) perioperatoria CA gástrico Carcinomatosis peritoneal de origen colorrectal Glz-Moreno S. EJSO 2006; 32: 593 -596

INDICACIONES Pseudomixoma peritoneal Cáncer de colon carcinomatosis limitada Mesotelioma peritoneal (excepto histología sarcomatoide) HIPEC idealmente se debe realizar en un protocolo de investigación q q CARCINOMATOSIS CEO EC III y IV (CC<2) CEO recurrente (abdomen) Paliación Sin indicación para limítrofes Sugarbaker PH. Peritonectomy Procedures. Ann Surg 1995; 221: 29 -42 Surg Oncol Clin N Am 2012; 21: 645 -663
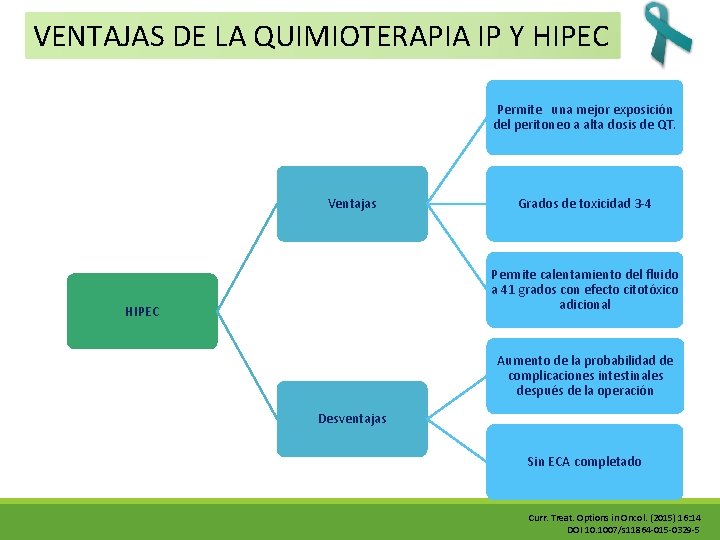
VENTAJAS DE LA QUIMIOTERAPIA IP Y HIPEC Permite una mejor exposición del peritoneo a alta dosis de QT. Ventajas Grados de toxicidad 3 -4 Permite calentamiento del fluido a 41 grados con efecto citotóxico adicional HIPEC Aumento de la probabilidad de complicaciones intestinales después de la operación Desventajas Sin ECA completado Curr. Treat. Options in Oncol. (2015) 16: 14 DOI 10. 1007/s 11864 -015 -0329 -5
HIPERTERMIA
EFECTOS TEORICOS • • Tumoricida Inhibe angiogenesis Induce apoptosis Desnaturalización de proteínas • Falla reparación ADN • Aumento de citotoxicidad de algunos agentes • Aumenta flujo sanguíneo y oxigenación • Aumenta penetración de tumores sólidos (hasta 5 mm) 1. Propios 2. Sobre QT 3. Hemodinámicos Nat. Rev. Clin. Oncol. 7, 108– 115 (2010) Christophi et al, 1999; Dahl et al, 1999
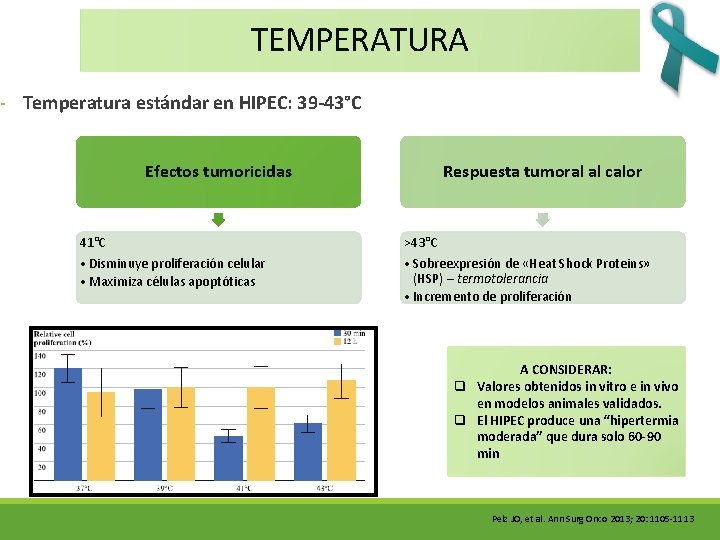
TEMPERATURA - Temperatura estándar en HIPEC: 39 -43°C Efectos tumoricidas Respuesta tumoral al calor 41°C >43°C • Disminuye proliferación celular • Maximiza células apoptóticas • Sobreexpresión de «Heat Shock Proteins» (HSP) – termotolerancia • Incremento de proliferación A CONSIDERAR: q Valores obtenidos in vitro e in vivo en modelos animales validados. q El HIPEC produce una “hipertermia moderada” que dura solo 60 -90 min Pelz JO, et al. Ann Surg Onco 2013; 20: 1105 -1113

AUMENTO DE CITOTOXICIDAD Engelhardt 1987 • Compila una lista de drogas que modifican comportamiento al interactuar con calor • Revisa distintas vías para aplicar calor: Sistémica – Local – Regional - Perfusión aislada Dahl 1988 • Interacción de calor con citotóxicos • La falla en aumento de citotoxicidad proviene de una baja en el flujo sanguíneo (estasis en tumores) Meyer 1989 • Valora efectos de RT-hipertermia y QT : “Heat Shock Proteins” Urano 1999 • Las drogas de elección en temperatura fisiológica no necesariamente lo serán en condiciones de hipertermia Sugarbaker PH. Int J Hyperthermia. 2007; 23 (5): 431 -442
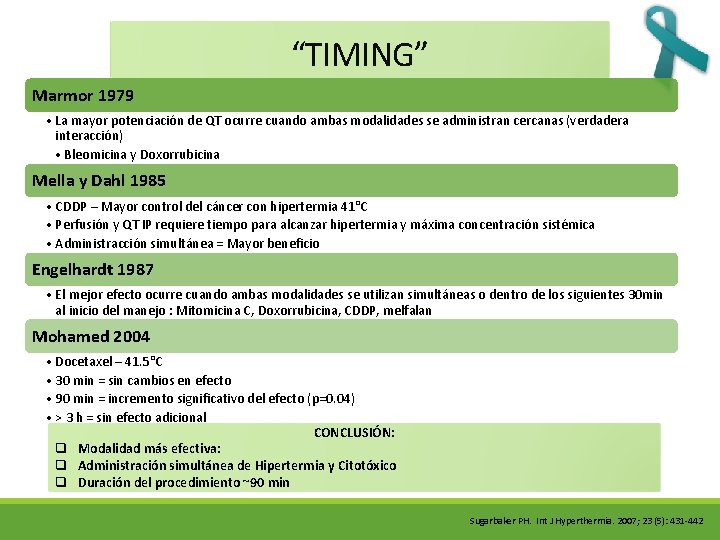
“TIMING” Marmor 1979 • La mayor potenciación de QT ocurre cuando ambas modalidades se administran cercanas (verdadera interacción) • Bleomicina y Doxorrubicina Mella y Dahl 1985 • CDDP – Mayor control del cáncer con hipertermia 41°C • Perfusión y QT IP requiere tiempo para alcanzar hipertermia y máxima concentración sistémica • Administracción simultánea = Mayor beneficio Engelhardt 1987 • El mejor efecto ocurre cuando ambas modalidades se utilizan simultáneas o dentro de los siguientes 30 min al inicio del manejo : Mitomicina C, Doxorrubicina, CDDP, melfalan Mohamed 2004 • Docetaxel – 41. 5°C • 30 min = sin cambios en efecto • 90 min = incremento significativo del efecto (p=0. 04) • > 3 h = sin efecto adicional CONCLUSIÓN: q Modalidad más efectiva: q Administración simultánea de Hipertermia y Citotóxico q Duración del procedimiento ~90 min Sugarbaker PH. Int J Hyperthermia. 2007; 23 (5): 431 -442

PENETRACION EN TUMORES Hahn y Li 1982 • El alcohol de la membrana lipídica y las lecitinas de superficie celular intensifican la destrucción celular por QT y calor Dahl 1988 • Revisa mecanismos de interección y concluye: daño a la membrana por calor = aumento de penetración de la droga • Doxorrubicina – Melfalan - CDDP Jaquet 1998 • Hipertermia aumenta la penetración de doxorrubicina en todos los tejidos directamente expuestos: Intestino delgado, vejiga, SP • No aumenta concentración en corazón o hígado Los 2006 QT QUE AUMENTA SU ACTIVIDAD CON HIPERTERMIA • Penetración de QT en tejidos cancerosos c/s calor Cisplatino Irinotecan • Incremento de CBP administrada IP e IV en hipertermia CONCLUSIÓN: Carboplatino Melfalan q Puede utilizarse QT Ciclofosfamida Mitomicina C Doxetacel Mitoxantrone Doxirrubicina Oxaliplatino Gemcitabine a Topotecan ifosfamida Vinorelbine bidireccional (IV + IP) en combinación con hipertermia q QT IV incrementa acceso sistémico q QT IP incrementa penetración directa A Si se da antes de hipertermia Sugarbaker PH. Int J Hyperthermia. 2007; 23 (5): 431 -442
• INTRODUCCIÓN • La QT IP + CRS ha demostrado eficacia para el tratamiento de PC en diversos tumores malignos, tales como cáncer de ovario , el cáncer colorrectal , pseudomixoma peritoneal y el mesotelioma • OBJETIVO. • Esta revisión pretende resaltar la situación actual y las perspectivas futuras de la QT IP en pacientes con PC, centrándose especialmente en la farmacocinética de los fármacos administrados IP • La hipertermia puede aumentar la citotoxicidad en la cavidad peritoneal, sin un aumento en la toxicidad sistémica Surgical Oncology 23 (2014) 99 e 106
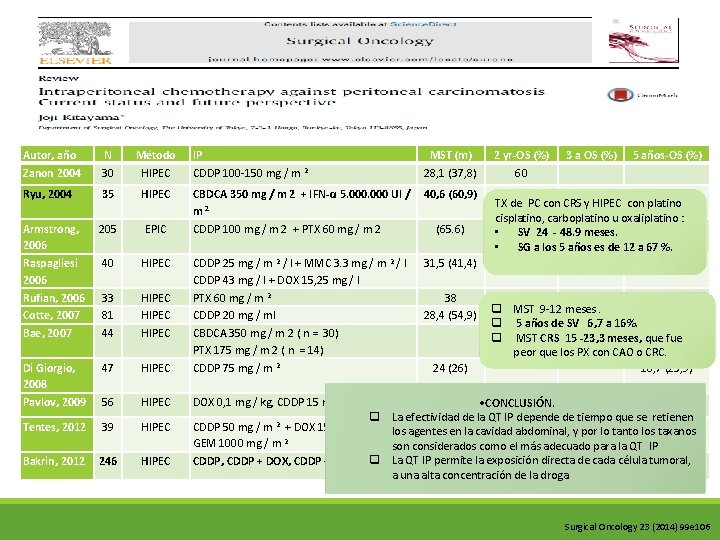
Autor, año Zanon 2004 N 30 Método HIPEC IP CDDP 100 -150 mg / m 2 Ryu, 2004 35 HIPEC Armstrong, 2006 Raspagliesi 2006 Rufian, 2006 Cotte, 2007 Bae, 2007 205 EPIC 40 HIPEC 33 81 44 HIPEC Di Giorgio, 2008 Pavlov, 2009 47 HIPEC CDDP 75 mg / m 2 56 HIPEC DOX 0, 1 mg / kg, CDDP 15 mg / m 2 Tentes, 2012 39 HIPEC Bakrin, 2012 246 HIPEC MST (m) 28, 1 (37, 8) CBDCA 350 mg / m 2 + IFN-α 5. 000 UI / 40, 6 (60, 9) m 2 CDDP 100 mg / m 2 + PTX 60 mg / m 2 (65. 6) CDDP 25 mg / m 2 / l + MMC 3. 3 mg / m 2 / l CDDP 43 mg / l + DOX 15, 25 mg / l PTX 60 mg / m 2 CDDP 20 mg / ml CBDCA 350 mg / m 2 ( n = 30) PTX 175 mg / m 2 ( n = 14) 31, 5 (41, 4) 38 28, 4 (54, 9) 24 (26) 2 yr-OS (%) 60 3 a OS (%) 5 años-OS (%) 53, 8 (65, 6) TX de PC con CRS y HIPEC con platino cisplatino, carboplatino u oxaliplatino : • SV 24 - 48. 9 meses. • SG a los 5 años es de 12 a 67 %. (15) 46 37 (60) q MST 9 -12 meses. q 5 años de SV 6, 7 a 16%. 63 (CBDCA) 84, 6 q MST CRS 15 -23, 3 meses, que fue (PTX) peor que los PX con CAO o CRC. 16, 7 (25, 9) 38. 1 • CONCLUSIÓN. 67 q La efectividad de la QT IP depende de tiempo que se retienen CDDP 50 mg / m 2 + DOX 15 mg / m 2 los agentes en la cavidad abdominal, y por lo tanto los taxanos 37 54 (62. 5) 2 GEM 1000 mg / m son considerados como el más adecuado para la QT IP CDDP, CDDP + DOX, CDDP + MMC q La QT IP permite la exposición directa de cada célula tumoral, 48. 9 60 35 a una alta concentración de la droga. Surgical Oncology 23 (2014) 99 e 106

EFECTOS SECUNDARIOS 39 -41. 5°C Efectos mínimos en función cardiopulmonar 43 -44°C Elevación de TA Aumenta uresis Sd distrés respiratorio del adulto (postqx) Sugarbaker PH. Int J Hyperthermia. 2007; 23 (5): 431 -442
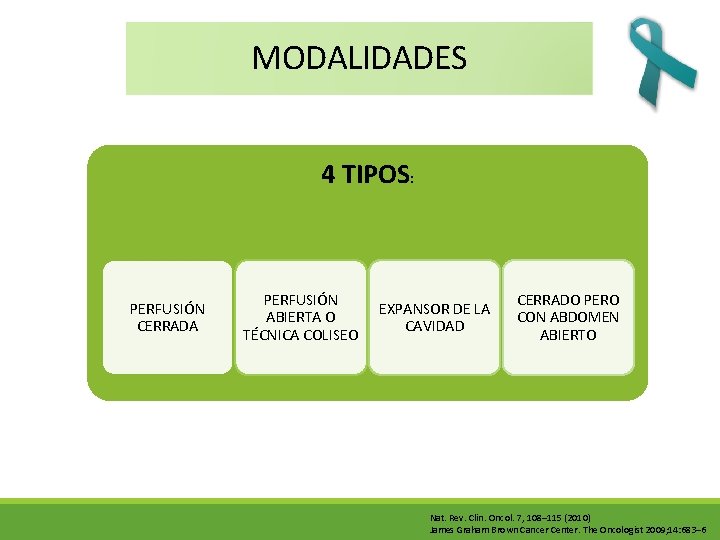
MODALIDADES 4 TIPOS: PERFUSIÓN CERRADA PERFUSIÓN ABIERTA O TÉCNICA COLISEO EXPANSOR DE LA CAVIDAD CERRADO PERO CON ABDOMEN ABIERTO Nat. Rev. Clin. Oncol. 7, 108– 115 (2010) James Graham Brown Cancer Center. The Oncologist 2009; 14: 683– 6
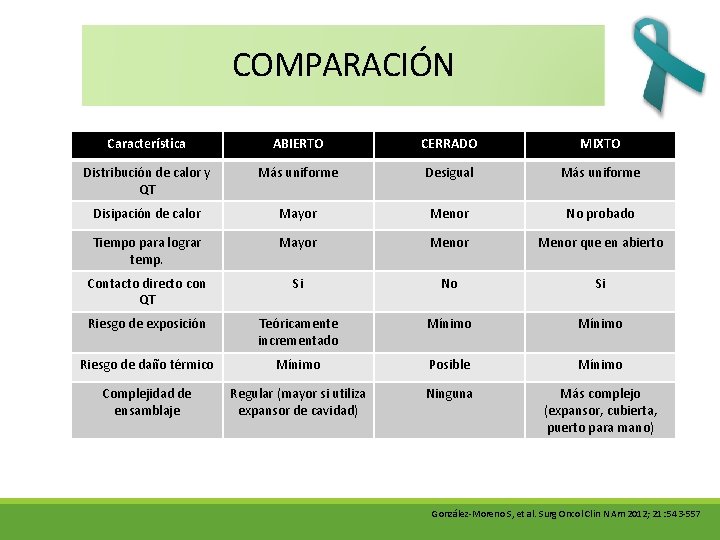
COMPARACIÓN Característica ABIERTO CERRADO MIXTO Distribución de calor y QT Más uniforme Desigual Más uniforme Disipación de calor Mayor Menor No probado Tiempo para lograr temp. Mayor Menor que en abierto Contacto directo con QT Si No Si Riesgo de exposición Teóricamente incrementado Mínimo Riesgo de daño térmico Mínimo Posible Mínimo Complejidad de ensamblaje Regular (mayor si utiliza expansor de cavidad) Ninguna Más complejo (expansor, cubierta, puerto para mano) González-Moreno S, et al. Surg Oncol Clin N Am 2012; 21: 543 -557

COMPLICACIONES Trastorno hidroelectrolitico Toxicidad gastrica, renal, neurologica, hematológica Alteraciones metabólicas Íleo prolongado Edema dependiente a temperatura Fatiga Infección Dolor Mortalidad: 3 – 8% Morbilidad postoperatoria: 20 – 50% González-Moreno S, et al. Surg Oncol Clin N Am 2012; 21: 543 -557

JUSTIFICACIÓN DE LA QUIMIOTERAPIA INTRAPERITONEAL HIPERTÉRMICA (HIPEC) EN EL CÁNCER DE OVARIO INTRODUCCIÓN • 4 ta causa en Francia. • En el momento del dx con carcinomatosis peritoneal. • El estándar de tratamiento es CX CR Y QT sistémica. • Con remisión completa de 60 – 80% y SV 35 a 38 meses. • 20 – 30 % son resistente a platino. • 75% de los que responden a platino recaen a los 5 años. La administración se lleva a cabo inmediatamente después de la citorreducción quirúrgica un tratamiento temprano de la enfermedad peritoneal residual, Hay beneficios teóricos comparables para HIPEC como terapia intervalo. LA MORBILIDAD Y LA MORTALIDAD DE HIPEC Riesgo de insuficiencia renal Complicaciones hematológicas. Mortalidad postoperatoria 0 -10% : 0. 8% de origen ginecológico en el registro francés. 4. 1% en PC no ginecológico. Journal of Visceral Surgery (2014) 151, 347— 353
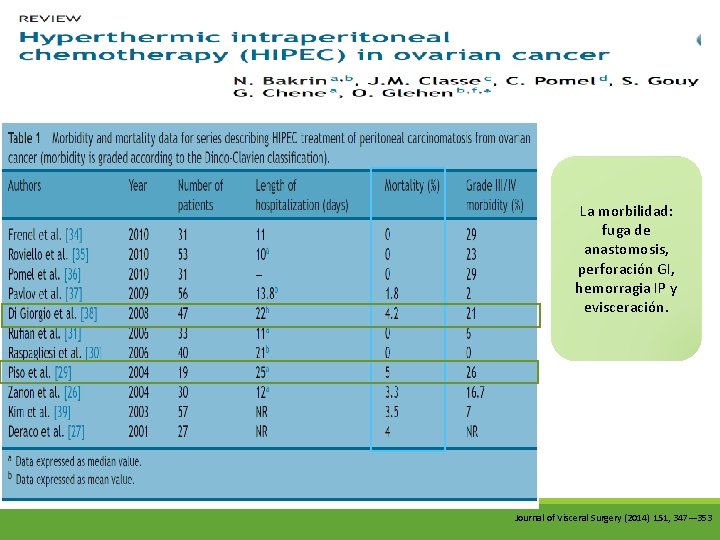
La morbilidad: fuga de anastomosis, perforación GI, hemorragia IP y evisceración. Journal of Visceral Surgery (2014) 151, 347— 353
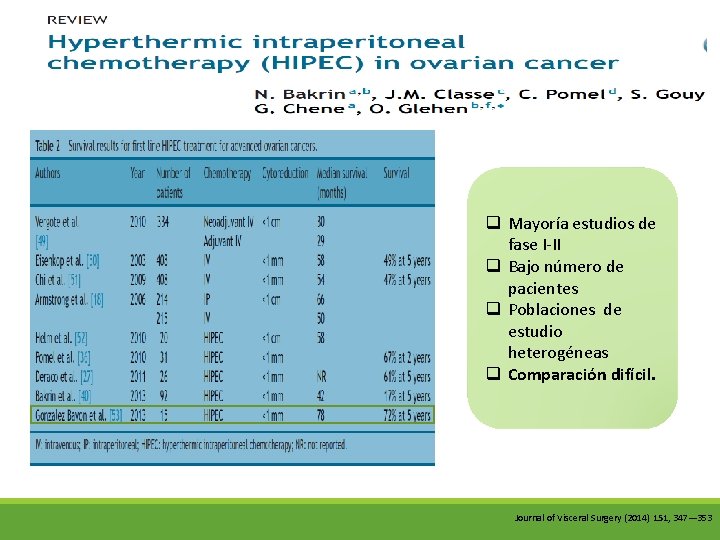
q Mayoría estudios de fase I-II q Bajo número de pacientes q Poblaciones de estudio heterogéneas q Comparación difícil. Journal of Visceral Surgery (2014) 151, 347— 353
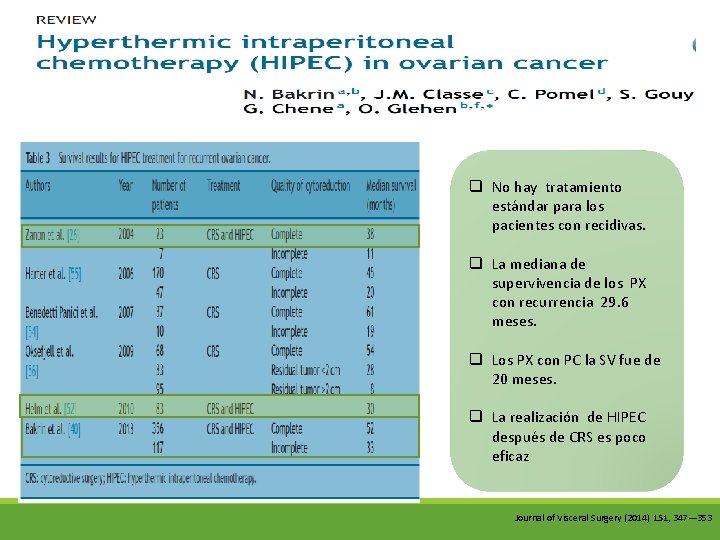
q No hay tratamiento estándar para los pacientes con recidivas. q La mediana de supervivencia de los PX con recurrencia 29. 6 meses. q Los PX con PC la SV fue de 20 meses. q La realización de HIPEC después de CRS es poco eficaz Journal of Visceral Surgery (2014) 151, 347— 353
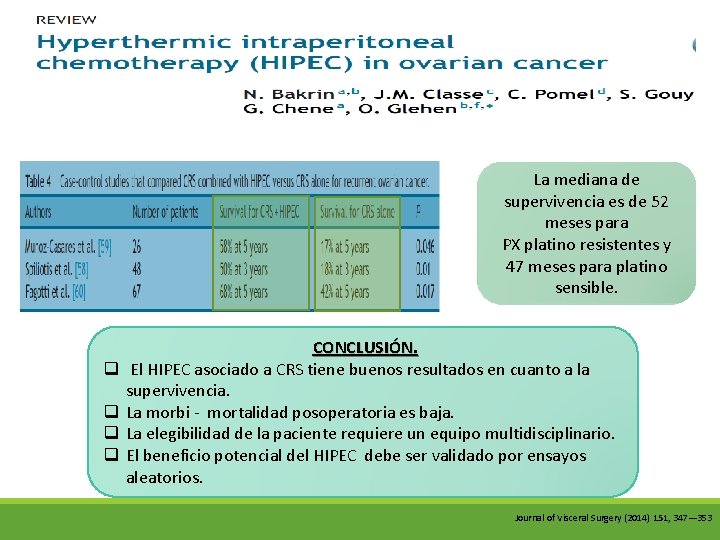
La mediana de supervivencia es de 52 meses para PX platino resistentes y 47 meses para platino sensible. q q CONCLUSIÓN. El HIPEC asociado a CRS tiene buenos resultados en cuanto a la supervivencia. La morbi - mortalidad posoperatoria es baja. La elegibilidad de la paciente requiere un equipo multidisciplinario. El beneficio potencial del HIPEC debe ser validado por ensayos aleatorios. Journal of Visceral Surgery (2014) 151, 347— 353
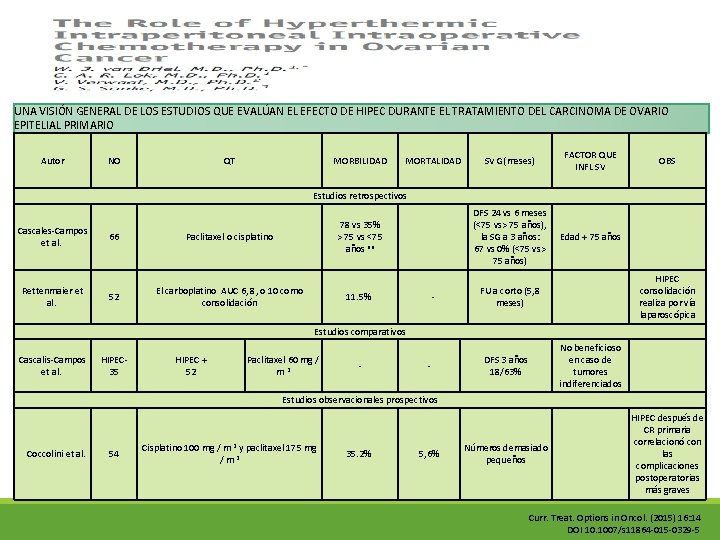
UNA VISIÓN GENERAL DE LOS ESTUDIOS QUE EVALÚAN EL EFECTO DE HIPEC DURANTE EL TRATAMIENTO DEL CARCINOMA DE OVARIO EPITELIAL PRIMARIO Autor NO QT MORBILIDAD SV G(meses) FACTOR QUE INFL SV OBS DFS 24 vs 6 meses (<75 vs> 75 años), la SG a 3 años: 67 vs 0% (<75 vs> 75 años) Edad + 75 años - FU a corto (5, 8 meses) HIPEC consolidación realiza por vía laparoscópica No beneficioso en caso de tumores indiferenciados HIPEC después de CR primaria correlacionó con las complicaciones postoperatorias más graves MORTALIDAD Estudios retrospectivos Cascales-Campos et al. Rettenmaier et al. 78 vs 35% > 75 vs <75 años un 66 Paclitaxel o cisplatino 52 El carboplatino AUC 6, 8, o 10 como consolidación 11. 5% Estudios comparativos Cascalis-Campos et al. HIPEC 35 HIPEC + 52 Paclitaxel 60 mg / m 2 - - DFS 3 años 18/63% Estudios observacionales prospectivos Coccolini et al. 54 Cisplatino 100 mg / m 2 y paclitaxel 175 mg / m 2 35. 2% 5, 6% Números demasiado pequeños Curr. Treat. Options in Oncol. (2015) 16: 14 DOI 10. 1007/s 11864 -015 -0329 -5
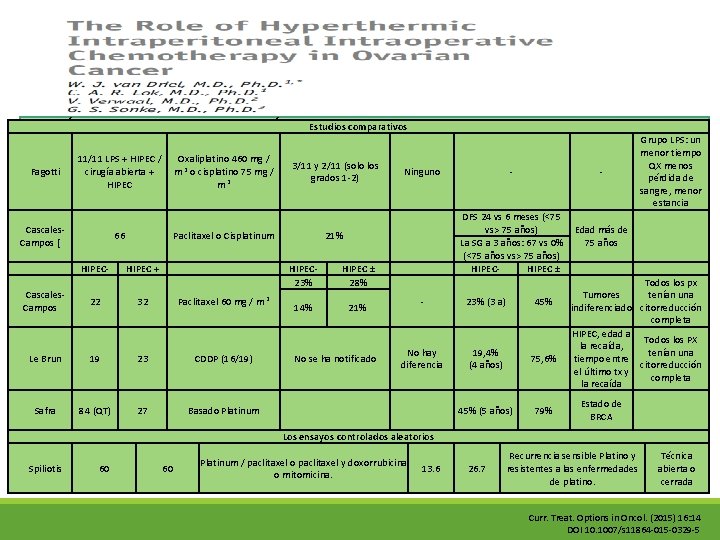
UNA VISIÓN GENERAL DE LOS ESTUDIOS QUE EVALÚAN EL EFECTO DE HIPEC EN EL TRATAMIENTO DEL CARCINOMA DE OVARIO Estudios comparativos RECURRENTE Grupo LPS: un menor tiempo QX menos Fagotti Ninguno pérdida de sangre, menor Autor PX QT MORBILIDAD MORTALIDAD SV G FACTORES QUE INFL. SV estancia OBS DFS 24 vs 6 meses (<75 vs> 75 años) Cascales. Edad más de 66 Paclitaxel o Cisplatinum 21% Campos [ 75 años La SG a 3 años: 67 vs 0% Estudios retrospectivos (<75 años vs> 75 años) HIPEC + HIPECHIPEC ± Koningsrain 90 Cisplatino 50 mg / m 2 38 (42%) 0 14 -35 c Tasa completa CR 23% 28% Todos los px er Cascales. Tumores tenían una 22 32 Paclitaxel 60 mg / m 2 23% (3 a) 45% Campos indiferenciado citorreducción 14% 21% completa Cisplatino 100 mg / m 2 y doxorrubicina 15, 2 Tasa de citorreducción Robella 25/70 35, 7% 7, 1% 47 HIPEC, edad a mg / l completa; PCI Todos los PX la recaída, No hay 19, 4% tenían una Le Brun 19 23 CDDP (16/19) No se ha notificado 75, 6% tiempo entre diferencia (4 años) citorreducción el último tx y completa Cripe 32 Varios fármacos 65, 6% 0 -la recaída 11/11 LPS + HIPEC / Oxaliplatino 460 mg / cirugía abierta + m 2 o cisplatino 75 mg / HIPEC m 2 Safra Fagotti Spiliotis 84 (QT) 10 60 27 Basado Platinum 3/11 y 2/11 (solo los grados 1 -2) 45% (5 años) Los ensayos controlados aleatorios Cisplatino 75 mg / m 2 o oxaliplatino 460 mg / Ninguno m 2 60 Platinum / paclitaxel o paclitaxel y doxorrubicina o mitomicina. 13. 6 26. 7 79% Estado de BRCA HIPEC laparoscópica para la enfermedad Recurrencia sensible Platino y Técnica recurrente resistentes a las enfermedades abierta o aislada de platino. cerrada Curr. Treat. Options in Oncol. (2015) 16: 14 DOI 10. 1007/s 11864 -015 -0329 -5
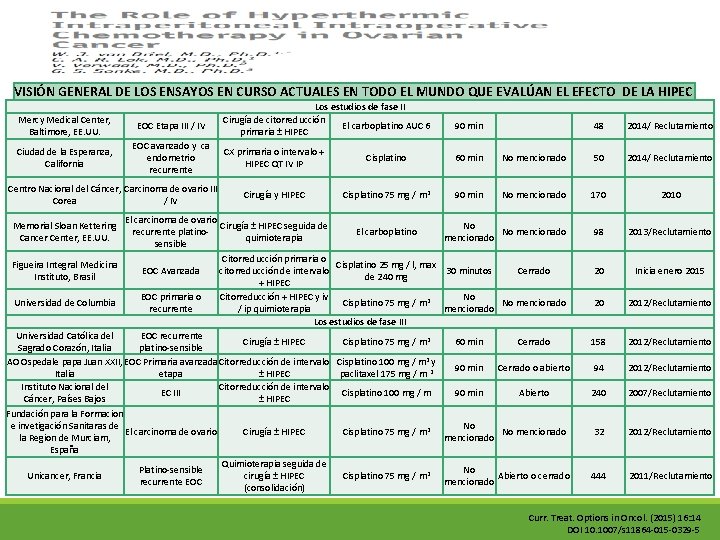
VISIÓN GENERAL DE LOS ENSAYOS EN CURSO ACTUALES EN TODO EL MUNDO QUE EVALÚAN EL EFECTO DE LA HIPEC Los estudios de fase II EN EL TRATAMIENTO DE PACIENTES CON CARCINOMA EPITELIAL DE OVARIO Mercy Medical Center, Baltimore, EE. UU. EOC Etapa III / IV Cirugía de citorreducción primaria ± HIPEC ETAPA DE LA ENFERMEDAD EOC avanzado y ca Ciudad de la Esperanza, California endometrio recurrente BRAZOS El carboplatino AUC 6 QT HIPEC CX primaria o intervalo + Cisplatino HIPEC QT IV IP Estudio observacional Malignidades superficie Centro Nacional del Cáncer, Carcinoma de ovario III Hospital de la Cirugía y HIPEC Cisplatino 75 mg / m 2 peritoneal (EOC, carcinoma Corea / IV Universidad de Cirugía + HIPEC No enlistado 90 min DURACIÓN DE TÉCNICA LA HIPEC UTILIZADA 48 2014/ Reclutamiento N FECHA DE INICIO 60 min No mencionado 50 2014/ Reclutamiento 90 min No mencionado No 170 2010 No mencionado colorrectal, el mesotelioma, mencionado El carcinoma de ovario pseudomixoma)Cirugía ± HIPEC seguida de Memorial Sloan Kettering No El carboplatino No mencionado 98 2013/Reclutamiento recurrente platino. Cancer Center, EE. UU. quimioterapia Los estudios de fase I mencionado sensible Hospital 60 dosis, 80, 100 mg Citorreducción primaria o 2011 hasta Figueira Integral Medicina Platino-sensible recurrente Cisplatino 25 mg / l, max Cirugía + HIPEC 90 min Cerrado 20 9 Inicia enero 2015 Universitario de / m EOC Avanzada 30 minutos citorreducción de intervalo Instituto, Brasil de 240 mg EOC julio 2013 + HIPEC Bonn, Alemania Cisplatinumescalating EOC primaria o Citorreducción + HIPEC y iv Jules Bordet Citorreducción de Cisplatino 75 mg / m 2 2 No No Universidad de Columbia No mencionado 20 24 2012/Reclutamiento Etapa primaria III / IV EOC Cisplatino 50 mg / mmencionado No mencionado 2010 recurrente / ip quimioterapia Institute, Bélgica intervalo + HIPEC mencionado Oslo, Noruega Los estudios de fase III Masonic Cancer Platino-sensible recurrente Carboplatino 1000 Universidad Católica del EOC recurrente 2 Cirugía + HIPEC Cisplatino 75 mg / m 90 min Cerrado 158 Cirugía ± HIPEC 60 min Center, EE. UU. EOC mg / m 2 Sagrado Corazón, Italia platino-sensible AO Ospedale papa Juan XXII, EOC Primaria avanzada Citorreducción de intervalo Cisplatino 100 mg / m 2 y Citorreducción 90 min Cerrado o abierto 94 2 Italia etapa ± HIPEC paclitaxel 175 mg / m Universidad de Aumento de la dosis No Etapas primarias II-IV EOC 60 primaria o Instituto Nacional del Citorreducción de intervalo Irvin, EE. UU. de carboplatino mencionado 240 EC III Cisplatino 100 mg / m 90 min Abierto intervalo + HIPEC Cáncer, Países Bajos ± HIPEC Fundación para la Formacion QT 6 C + HIPEC e invetigación Sanitaras de No Cisplatino dosis El carcinoma de ovario Cirugía ± HIPEC 32 Gustave Roussy, completan con Cisplatino 75 mg / m 2 mencionado No la Region de Murciam, EOC avanzada Primaria escalada, 50, 60, 70, No mencionado bevacizumab por Francia mencionado España 80 mg / m 2 15 meses Quimioterapia seguida de Platino-sensible No Unicancer, Francia Cisplatino 75 mg / m 2 Abierto o cerrado 444 cirugía ± HIPEC recurrente EOC mencionado (consolidación) 10 2012/Reclutamiento 2010 30 30 2012/Reclutamiento 2014 2007/Reclutamiento 2012/Reclutamiento 2011/Reclutamiento Curr. Treat. Options in Oncol. (2015) 16: 14 DOI 10. 1007/s 11864 -015 -0329 -5

Conclusión q Los principales criterios para la selección de pacientes dependen de la posibilidad de cirugía citorreductora y la extensión de carcinomatosis (PCI), que son los principales factores pronósticos. q La elegibilidad de los pacientes para este tipo de tratamiento requiere una rigurosa selección y debe llevarse a cabo por equipos multidisciplinarios. Curr. Treat. Options in Oncol. (2015) 16: 14 DOI 10. 1007/s 11864 -015 -0329 -5

Principales variables en el momento de la cirugía 88% 93% q La gravedad de la enfermedad es mayor en cx primaria que el grupo de recurrencia. q En tiempo operatorio es similar en ambas cortes. q La morbilidad es mayor en los px con recurrencia. q En tiempo promedio de adm de QT es de 70 min. q Temp media es de 42. 7. Gynecologic Oncology 136 (2015) 130– 135
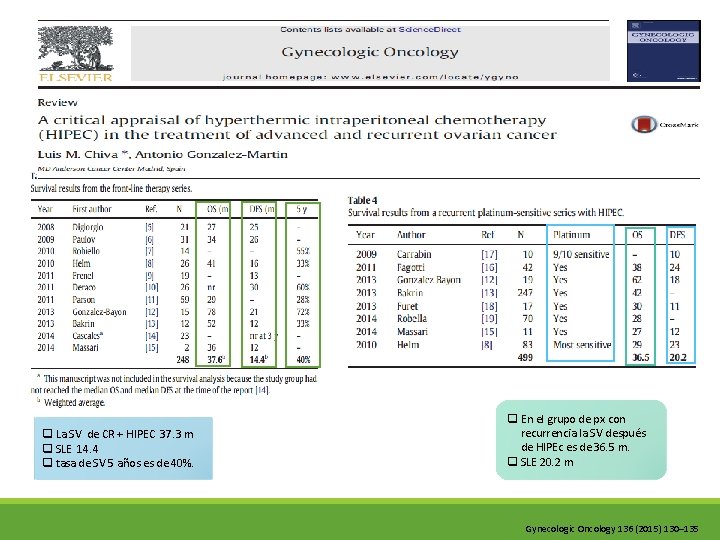
q La SV de CR + HIPEC 37. 3 m q SLE 14. 4 q tasa de SV 5 años es de 40%. q En el grupo de px con recurrencia la SV después de HIPEc es de 36. 5 m. q SLE 20. 2 m Gynecologic Oncology 136 (2015) 130– 135
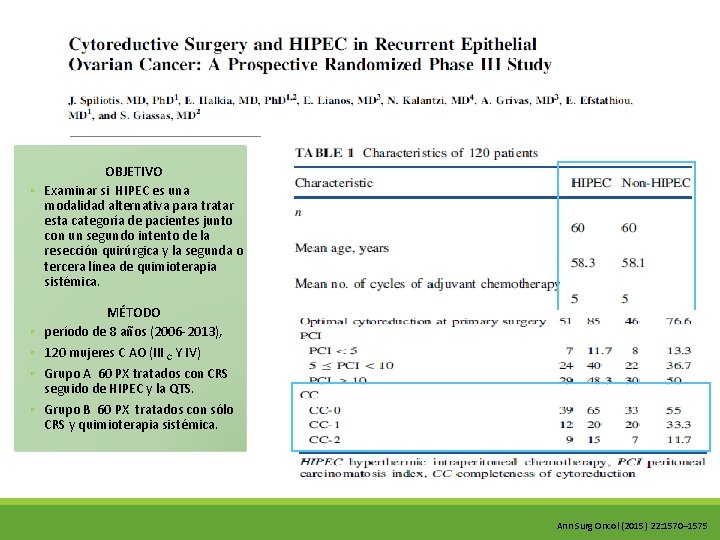
OBJETIVO ◦ Examinar si HIPEC es una modalidad alternativa para tratar esta categoría de pacientes junto con un segundo intento de la resección quirúrgica y la segunda o tercera línea de quimioterapia sistémica. ◦ ◦ MÉTODO período de 8 años (2006 -2013), 120 mujeres C AO (III C Y IV) Grupo A 60 PX tratados con CRS seguido de HIPEC y la QTS. Grupo B 60 PX tratados con sólo CRS y quimioterapia sistémica. Ann Surg Oncol (2015) 22: 1570– 1575
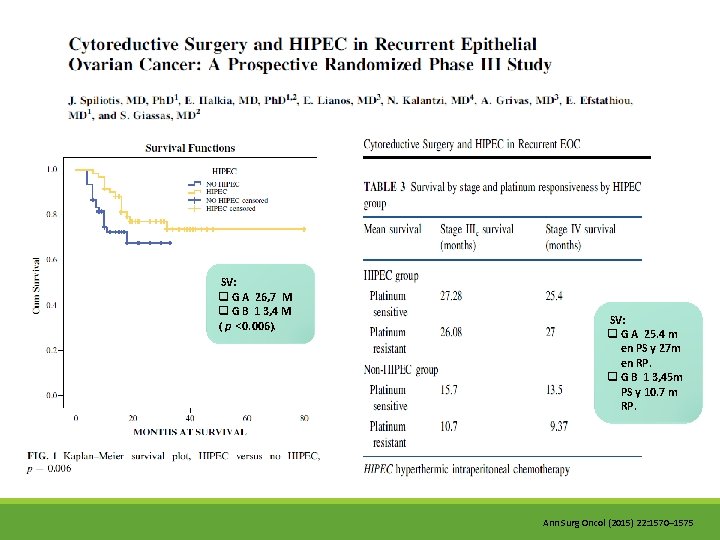
SV: q G A 26, 7 M q G B 1 3, 4 M ( p <0. 006). SV: q G A 25. 4 m en PS y 27 m en RP. q G B 1 3, 45 m PS y 10. 7 m RP. Ann Surg Oncol (2015) 22: 1570– 1575

GRUPO NO HIPEC: q EC III c SP la SV de 15, 7 meses frente a 10, 7 meses en PX RP. q EC IV 13, 5 meses PS VS a 9, 37 meses PR. q ENF RP 10, 7 meses EC III vs. 9, 37 meses EC IV. q SV EC III c (15, 7 meses) y EC IV (13, 5 meses) GRUPO HIPEC q EC III SV PS 27, 28 meses y PR 26, 08 meses. q EC IV, SP 25, 4 meses VS 27 RP. q LOS PX RP tuvieron una supervivencia similar, independientemente del estadio de la enfermedad 26, 8 meses para EC III vs. 27 meses EV IV. q Los resultados fueron similares para los pacientes con enfermedad SP 27, 28 EC III vs 25, 4 meses EC IV CONCLUSIONES q CRS y HIPEC ofrecen un beneficio en supervivencia para los pacientes con EOC recurrente, se aplica tanto a la enfermedad sensible al platino y platino-esistentes. q Eficacia máxima de HIPEC se observa cuando se logra una citorreducción completa. Ann Surg Oncol (2015) 22: 1570– 1575

TIEMPO DE APLICACIÓN Y RESULTADOS
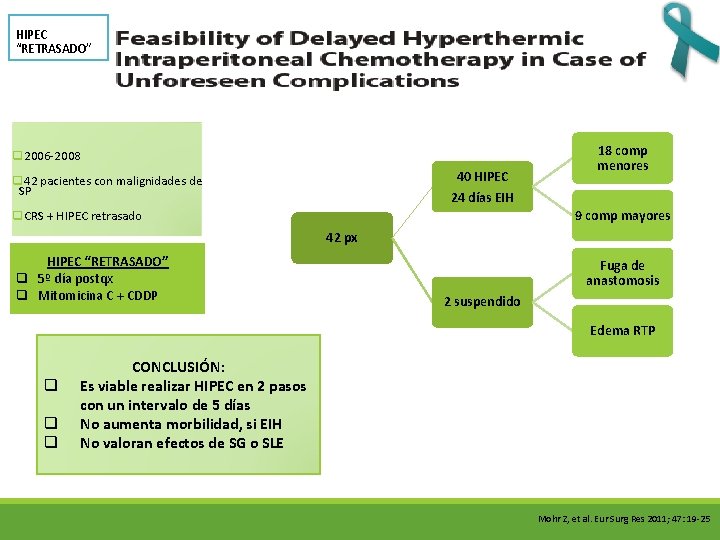
HIPEC “RETRASADO” q 2006 -2008 40 HIPEC 24 días EIH q 42 pacientes con malignidades de SP 18 comp menores 9 comp mayores q. CRS + HIPEC retrasado 42 px HIPEC “RETRASADO” q 5º día postqx q Mitomicina C + CDDP Fuga de anastomosis 2 suspendido Edema RTP q q q CONCLUSIÓN: Es viable realizar HIPEC en 2 pasos con un intervalo de 5 días No aumenta morbilidad, si EIH No valoran efectos de SG o SLE Mohr Z, et al. Eur Surg Res 2011; 47: 19 -25

HIPEC “ITERATIVO” Objetivo: La presencia de recurrencias aisladas puede ser tratada con procesos iterativos. 1990 -2010. Hosp. Civiles Lyon 30 pacientes Inclusión: q. CRS + HIPEC previo en mismo hospital q. Bajas comorbilidades q< 65 años q. Recurrencia documentada por RHP o TAC+MT RESULTADOS: q 19 px presentaron 2ª recurrencia (63%) q 12 fue intraabdominal (63%) q PLE tras 2º procedimiento: mediana 15 meses q Factores pronósticos significativos: q Invasión ganglionar (p=0. 021) q CC 0 -1 vs >1 (p=0. 049) q Aplasia medular grado ¾ (p=0. 016) q Complicaciones principales: q Indice de reoperación= 26. 7% q EIH 19. 5 días (P=0. 01) Golse N, et al. J Surg Oncol. 2012; 106: 197 -203

EXPERIENCIA INCan
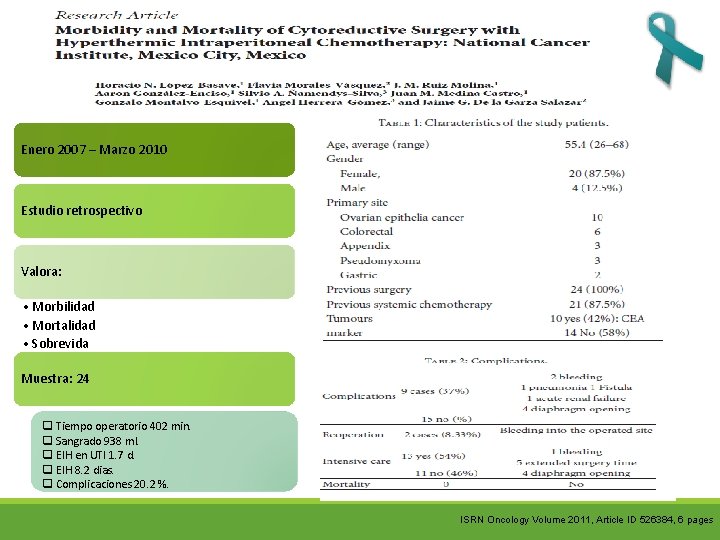
Enero 2007 – Marzo 2010 Estudio retrospectivo Valora: • Morbilidad • Mortalidad • Sobrevida Muestra: 24 q Tiempo operatorio 402 min. q Sangrado 938 ml. q EIH en UTI 1. 7 d. q EIH 8. 2 dias. q Complicaciones 20. 2 %. ISRN Oncology Volume 2011, Article ID 526384, 6 pages
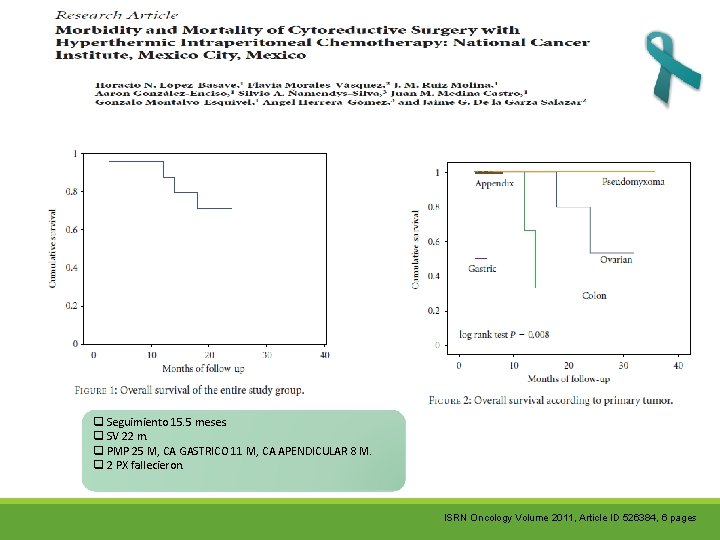
q Seguimiento 15. 5 meses. q SV 22 m. q PMP 25 M, CA GASTRICO 11 M, CA APENDICULAR 8 M. q 2 PX fallecieron. ISRN Oncology Volume 2011, Article ID 526384, 6 pages

CONCLUSIONES: q Con un enfoque riguroso para CRS y HIPEC se puede desarrollar un nuevo servicio con baja mortalidad y morbilidad aceptable con buenos resultados de SV. q Se debe hacer una buen selección de px. ISRN Oncology Volume 2011, Article ID 526384, 6 pages

CONCLUSIONES – HIPEC La cavidad peritoneal es el sitio preferido para la extensión local y para la recaída del cáncer de ovario, y por lo tanto la meta teórica ideal para el tratamiento loco-regional (CRS además HIPEC). Los resultados de morbilidad y mortalidad de CRS con HIPEC son comparables en los que solo se les CRS. La selección de los pacientes elegibles debe ser rigurosa y debe realizarse por un equipo multidisciplinario. El PCI desarrollado por Sugarbaker es un importante factor pronóstico para todos los casos de carcinomatosis, y se debe utilizar en la selección de indicaciones terapéuticas. Los resultados de supervivencia reportados por los estudios de casos y controles retrospectivos son particularmente prometedores, especialmente para las enfermedades quimiorresistente. Varios ensayos de fase III están actualmente en curso para evaluar el papel real de HIPEC en el manejo del cáncer de ovario en diferentes etapas (primera línea, consolidación, recurrencia).

GRACIAS POR SU ATENCIÓN.
- Slides: 81