QUIMICA ORGANICA Rama de la qumica que estudia











- Slides: 18


QUIMICA ORGANICA: • Rama de la química que estudia los compuestos orgánicos es decir tienen en su estructura el C. • Se pensó que los compuestos orgánicos no se podían sintetizar en el laboratorio porque tenían una fuerza vital que impedían su formación, sin embargo el químico Alemán Friedrich Wöhler logro tener urea un compuesto presente en la orina a partir de cianato de amonio lo que presento una conversión de sustancia inorgánica en orgánica • La química orgánica la encontramos en el diario vivir, como alimentos, ropa, madera, plásticos, gasolina, etc.

EL ATOMO DE CARBONO: • Hoy día se conocen mas de tres millones del compuesto del carbono y su numero aumenta constantemente. Esto se debe a las propiedades que posee el carbono. • Se encuentra en el grupo cuarto de la tabla periódica, tiene 4 electrones de Valencia • Notación Espectral: 1 S², 2 P² GRUPO: IVA PERIODO: 2 • Estado excitado del carbono: 1 S² 2 S¹ 2 PX¹ 2 PY¹ 2 PZ¹

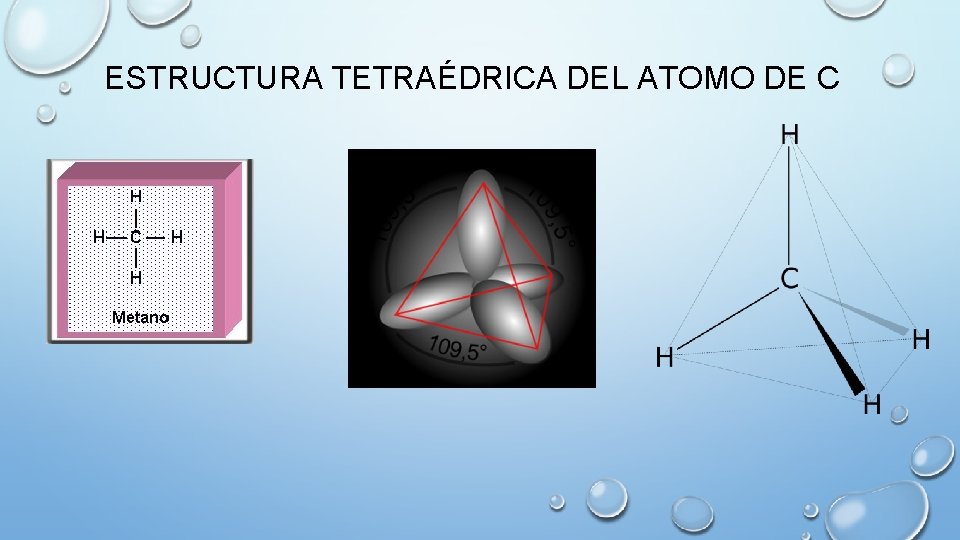
ESTRUCTURA TETRAÉDRICA DEL ATOMO DE C

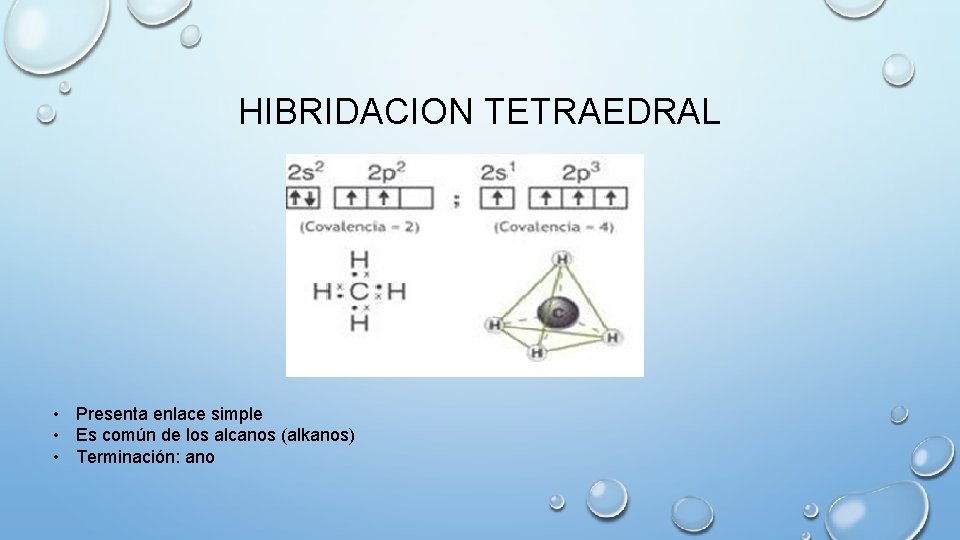
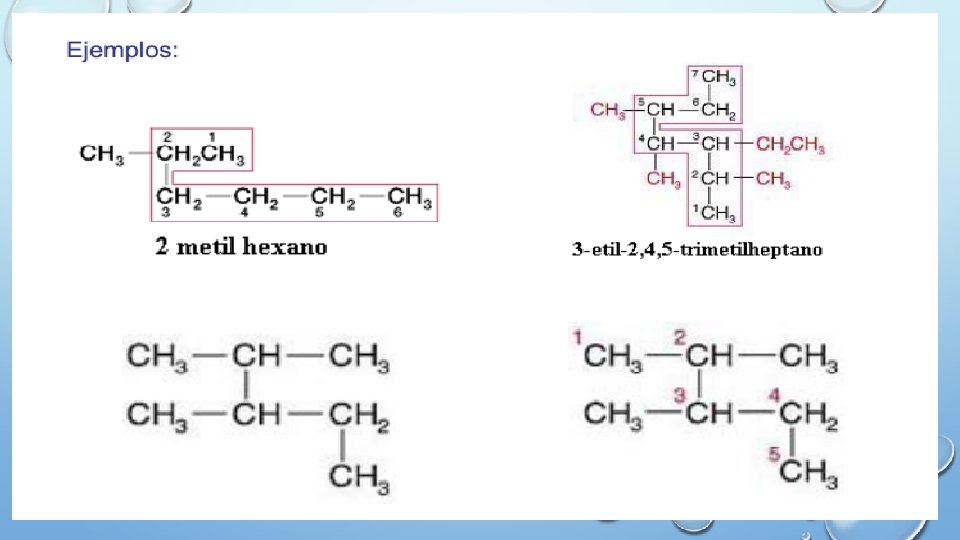
HIBRIDACION TETRAEDRAL • Presenta enlace simple • Es común de los alcanos (alkanos) • Terminación: ano

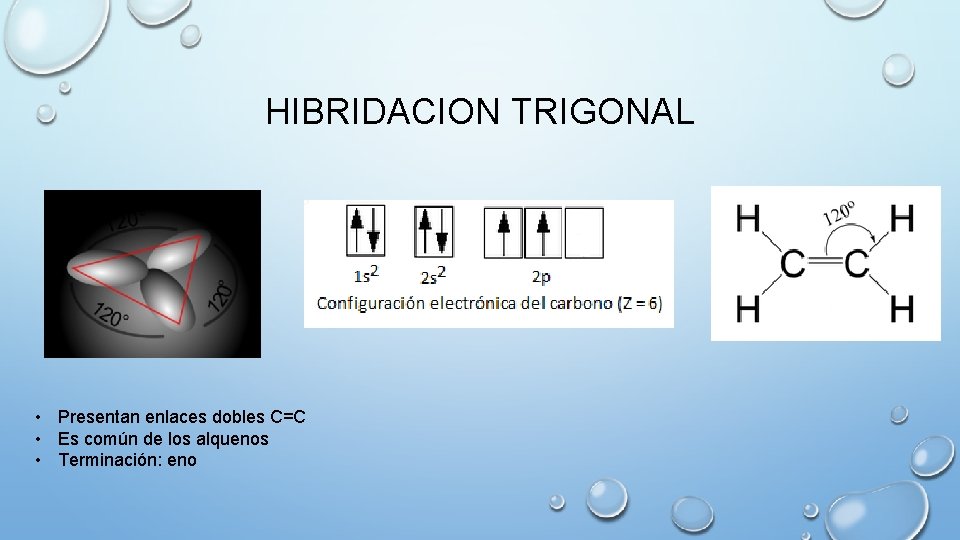
HIBRIDACION TRIGONAL • Presentan enlaces dobles C=C • Es común de los alquenos • Terminación: eno

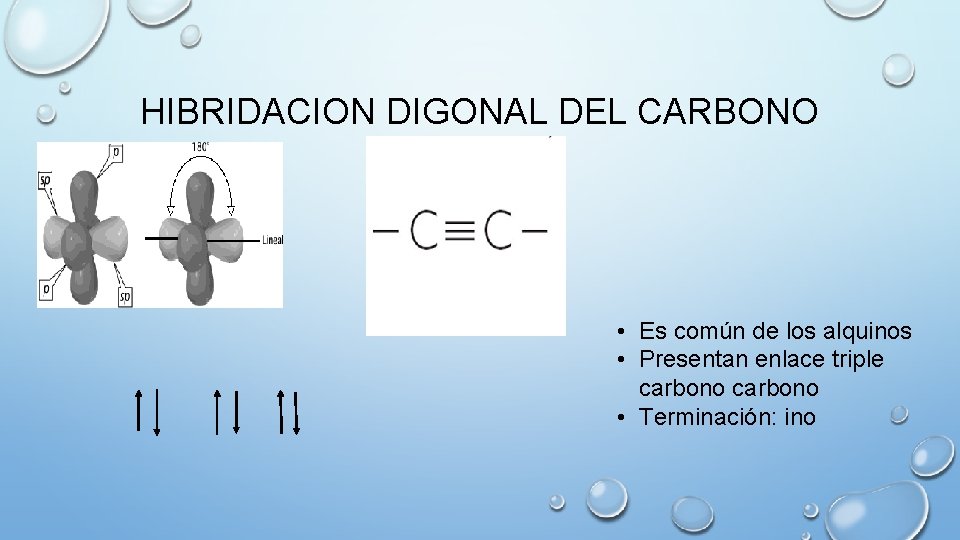
HIBRIDACION DIGONAL DEL CARBONO • Es común de los alquinos • Presentan enlace triple carbono • Terminación: ino

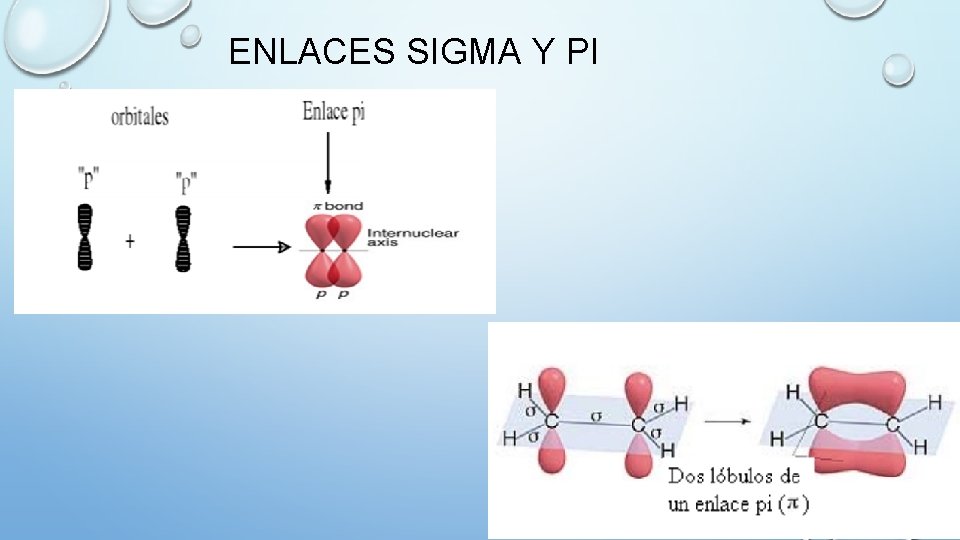
ENLACES SIGMA Y PI ENLACE SIGMA (σ) Se forman entre dos átomos de un compuesto covalente, debido a la superposición directa o frontal de los orbitales; es más fuerte y determina la geometría de la molécula. Dos átomos enlazados comparten un par de electrones de enlace, aportando cada uno de ellos, un electrón al par electrónico de enlace. Enlace sigma s ( s ) se manifiesta cuando se recubren dos orbitales s. ENLACE Pi ( π ) Se forma después del enlace sigma; es el segundo o tercer enlace formado entre dos átomos, debido a la superposición lateral de los orbitales p. Sus electrones se encuentran en constante movimiento.

ENLACES SIGMA Y PI








