QUIMICA GENERAL E INORGANICA I Ernesto J Calvo























- Slides: 42

QUIMICA GENERAL E INORGANICA I Ernesto J. Calvo • • calvo@qi. fcen. uba. ar www. q 1. fcen. uba. ar/grupos/laboeq http: //www. q 1. fcen. uba. ar/materias/qi 1/doc/ http: //www. q 1. fcen. uba. ar/

¿Qué es la Química? • Gran parte de las ciencias experimentales y naturales están basadas en el lenguaje molecular de la química cuya capacidad es construir, comprender y manejar “moléculas”, medir, predecir sus propiedades, modelar su comportamiento y aplicarlo al ensamblado en bloques para lograr materiales de propiedades predefinidas, reconocimiento molecular y diseñar dispositivos para la detección e identificación de especies químicas.

QUIMICA GENERAL E INORGANICA I Aspectos Microscópico Átomos (De los griegos al Microscopio de Efecto Túnel) Moléculas: Ladrillos de la química (menor porción de una sustancia). Uniones (entre átomos) químicas Forma de las moléculas (olfato, reconocimiento molecular) Energías en las moléculas (interacción con la radiación) Interacciones moleculares: gases, líquidos y sólidos Aspectos Macroscópico Termodinámica (relaciones entrevariables macroscópicas) Principios Equilibrio de Fases Equilibrio químico, de cargas Cinética Química (introducimos la variable tiempo)

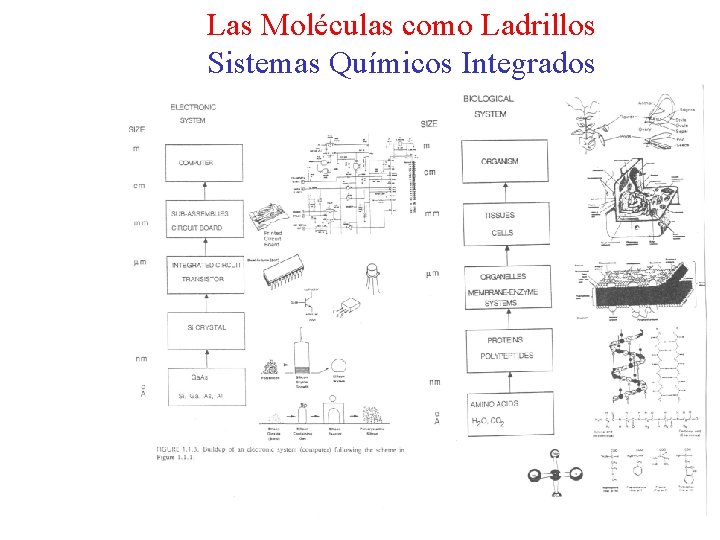
Las Moléculas como Ladrillos Sistemas Químicos Integrados

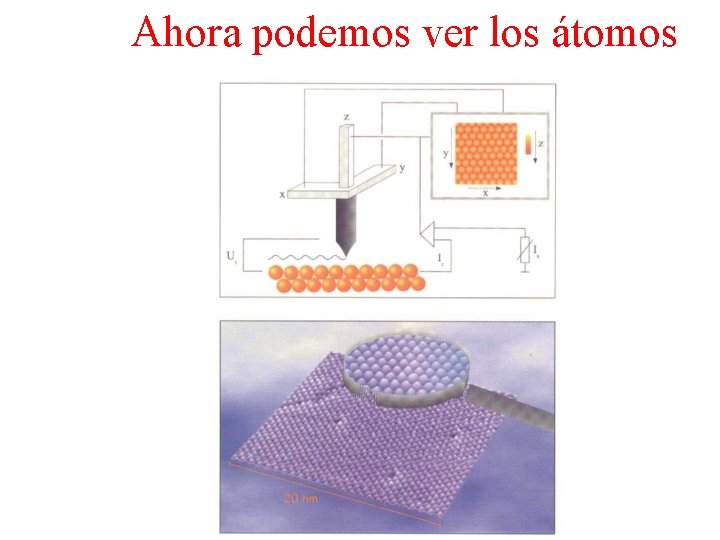
Ahora podemos ver los átomos

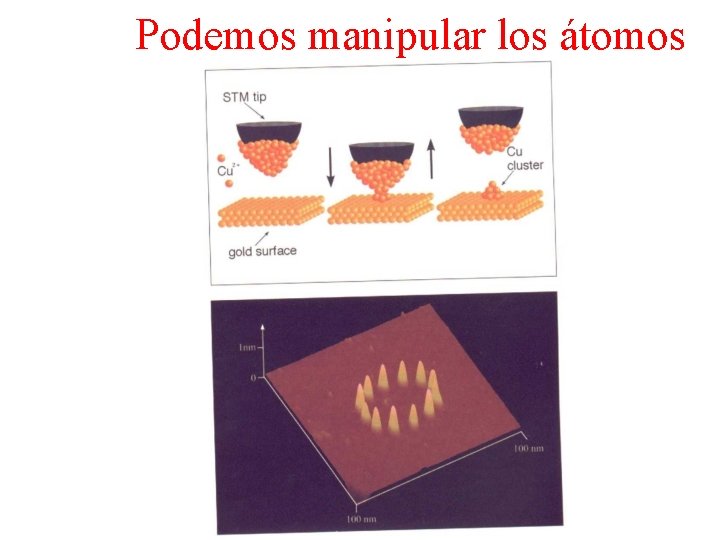
Podemos manipular los átomos

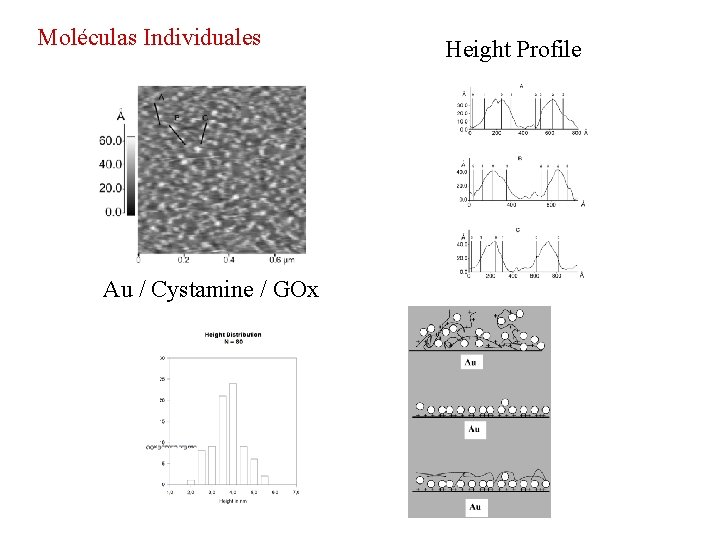
Moléculas Individuales Au / Cystamine / GOx Height Profile

STM de monocapa de dodecanotiol sobre terrazas de Au (Victoria Flexer, estudiante de quimica)

QUIMICA Propiedades de las sustancias (desde la estructura y propiedades de sus moléculas) Síntesis (colorantes, antibióticos, fertilizantes, armas químicas, etc. ) Análisis (composición ¿qué y cuánto? Un químico trata de responder preguntas como: ¿Porqué el H 2 O es líquida a temperatura ambiente mientras que H 2 S es gas? ¿Porqué el hielo flota sobre el agua si tienen la misma composición molecular, H 2 O? ¿Porqué el grafito es un lubricante y conduce la electricidad mientras que el diamante uno de los materiales más duros y aislante? ¿Porqué algunas sustancias causan el cáncer y otras sustancias lo curan? ¿Porqué el AZT interfiere en la copia del ADN y detiene el avance del SIDA?

ESTRUCTURA DEL ATOMO 1. 1897 J. J. Thomsom descubre el electrón en un tubo de rayos catódicos, con carga negativa independiente del metal con que se construye el cátodo. e. V = ½mv 2 e/m = 1, 75880 x 1011 Coul/ Kg 2. 1912 Robert Millikan determina la carga del electrón e = 1, 60 x 10 -19 Coul y por tanto me = 9, 1 x 10 -31 Kg

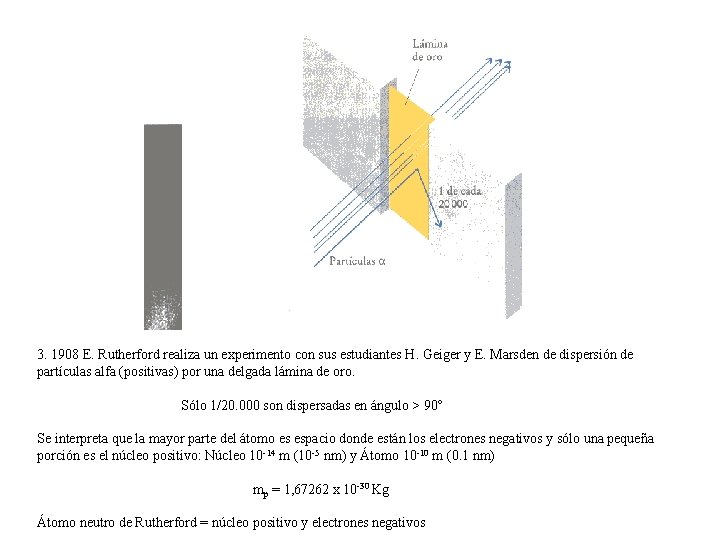
3. 1908 E. Rutherford realiza un experimento con sus estudiantes H. Geiger y E. Marsden de dispersión de partículas alfa (positivas) por una delgada lámina de oro. Sólo 1/20. 000 son dispersadas en ángulo > 90 Se interpreta que la mayor parte del átomo es espacio donde están los electrones negativos y sólo una pequeña porción es el núcleo positivo: Núcleo 10 -14 m (10 -5 nm) y Átomo 10 -10 m (0. 1 nm) mp = 1, 67262 x 10 -30 Kg Átomo neutro de Rutherford = núcleo positivo y electrones negativos

4. 1913 H. Moseley (electrones núcleo producen Rayos X) Determina que los números atómicos aumentan en una carga positiva entre elementos consecutivos

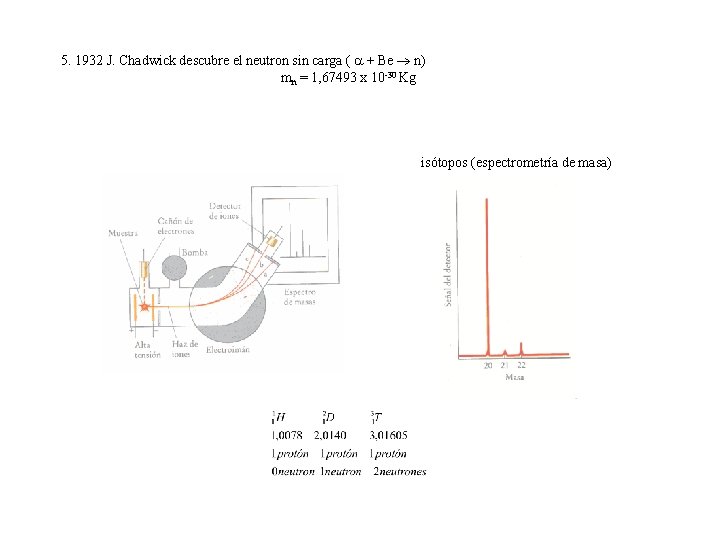
5. 1932 J. Chadwick descubre el neutron sin carga ( + Be n) mn = 1, 67493 x 10 -30 Kg isótopos (espectrometría de masa)

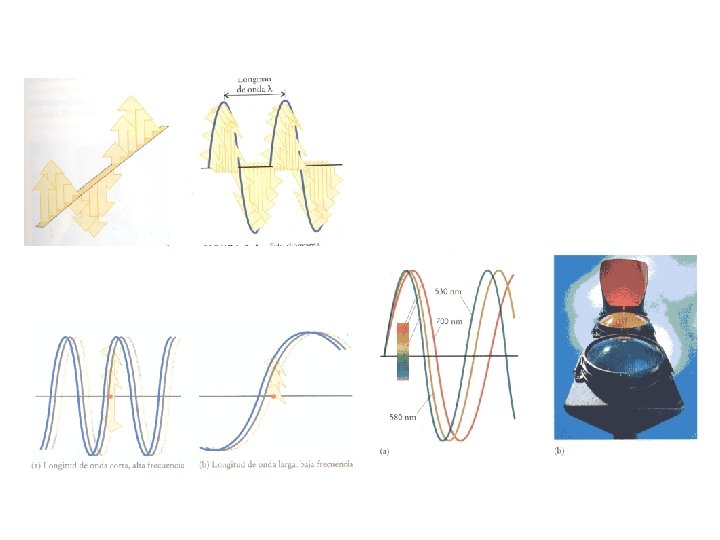
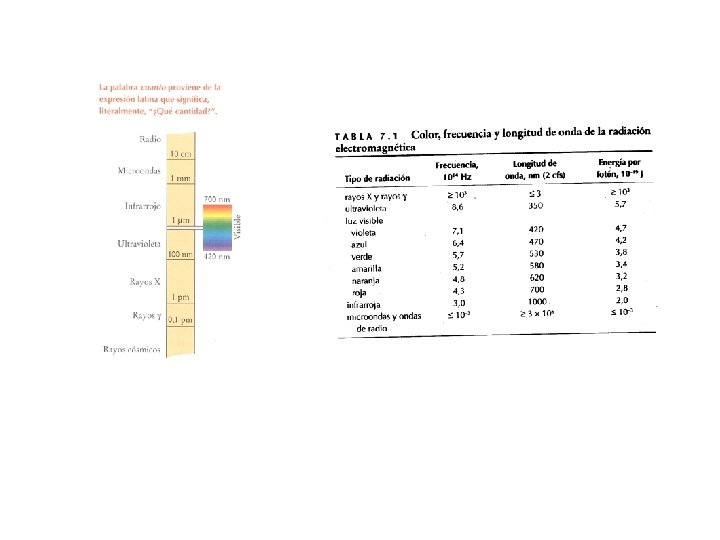
La luz encierra información química



ONDAS N=1 0 nodo N=2 1 nodo N=3, 2 nodos


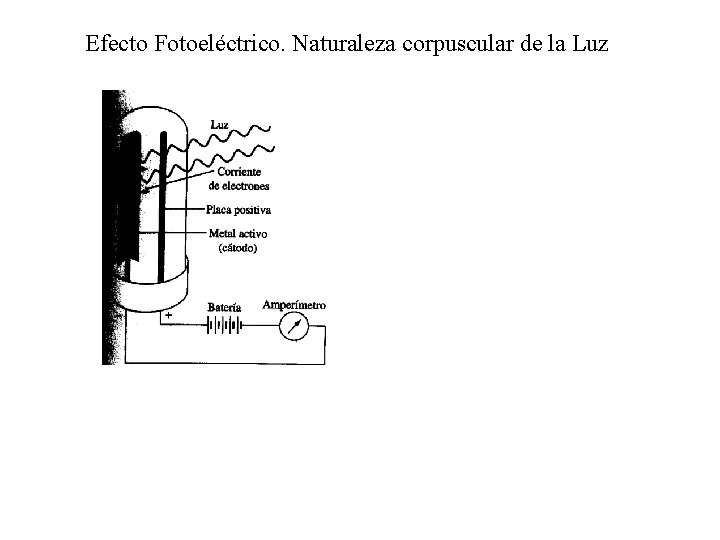
Efecto Fotoeléctrico. Naturaleza corpuscular de la Luz

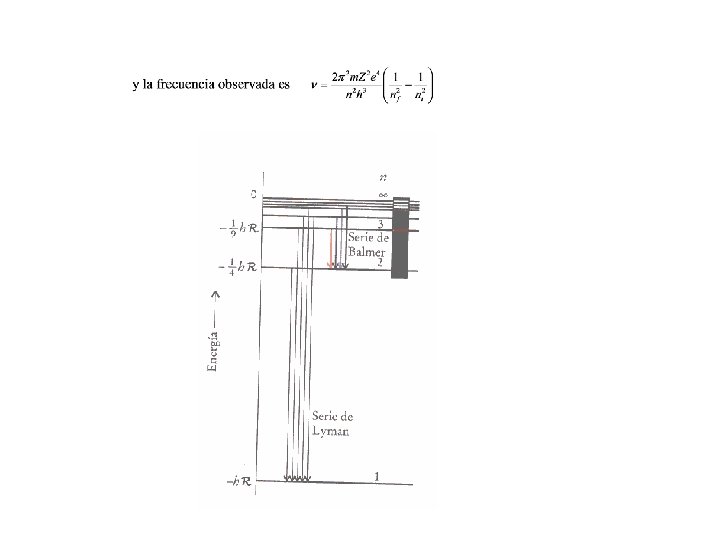
Los espectros de emisión de los àtomos nos dan información del mapa de energías posibles. Series espectrales del hidrógeno: Balmer Paschen Bracket Lyman





Mecánica Clásica (Newton)

Mecánica Cuántica o Mecánica Ondulatoria



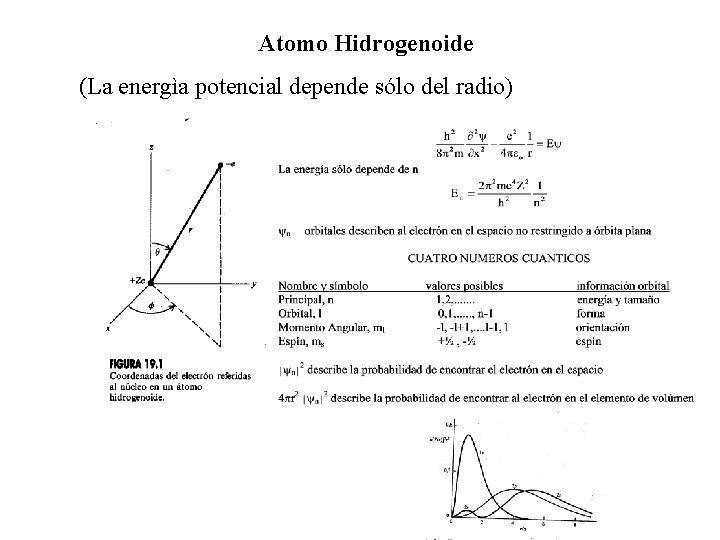
Atomo Hidrogenoide (La energìa potencial depende sólo del radio)



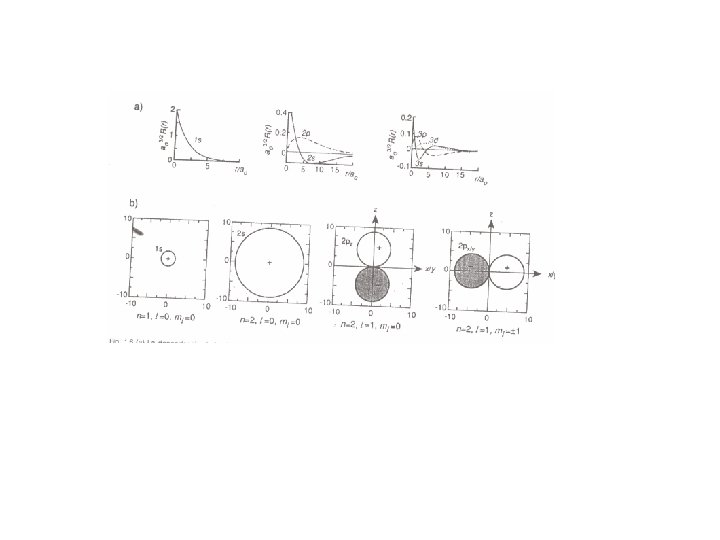
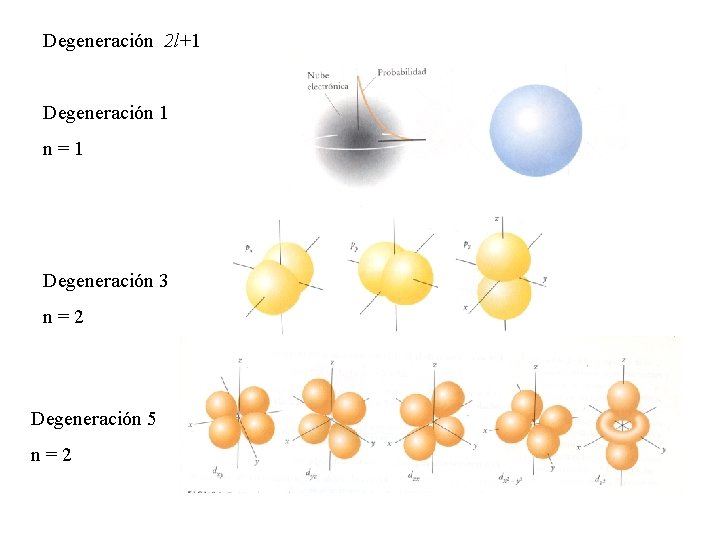
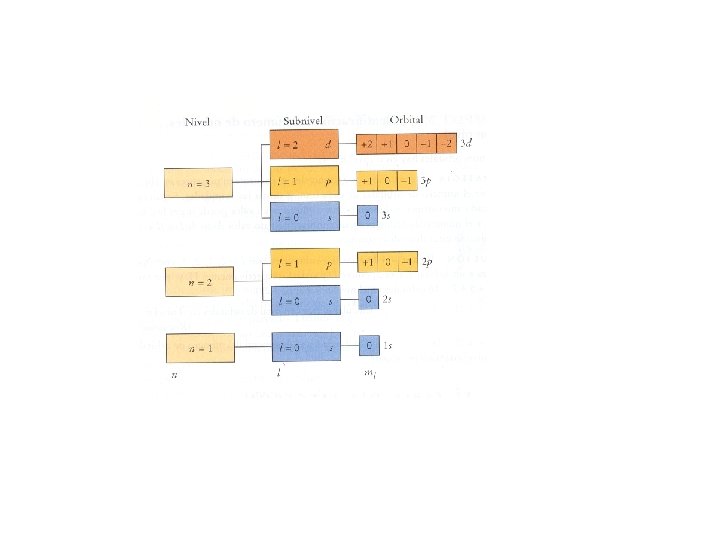
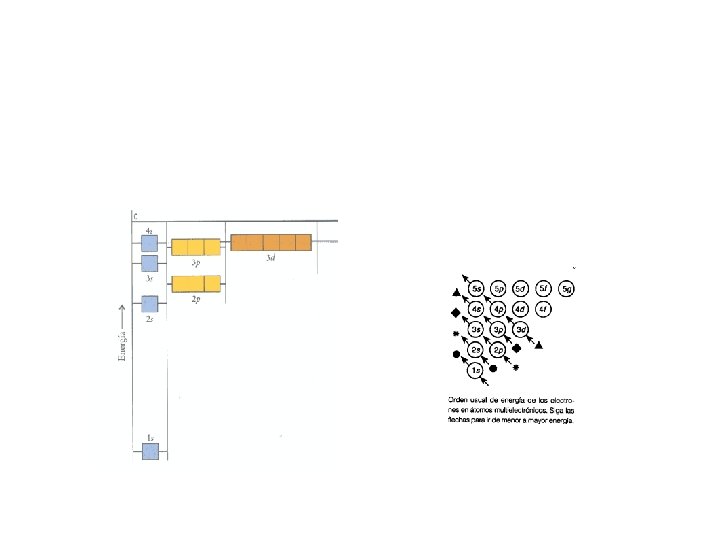
Degeneración 2 l+1 Degeneración 1 n=1 Degeneración 3 n=2 Degeneración 5 n=2




Espín (spin) a) Experimento de Stern-Gerlach b) Efecto Zeeman c) 1928 P. Dirac: Cuántica Relativística s=½ ms = ½ (2 s +1)


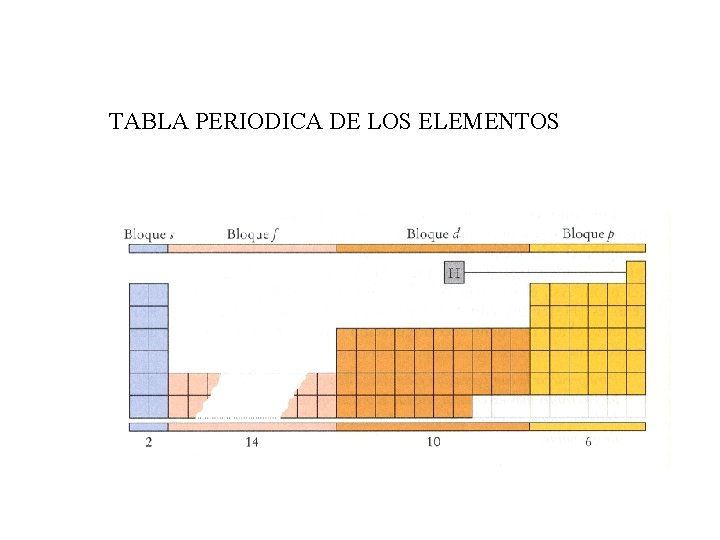
TABLA PERIODICA DE LOS ELEMENTOS


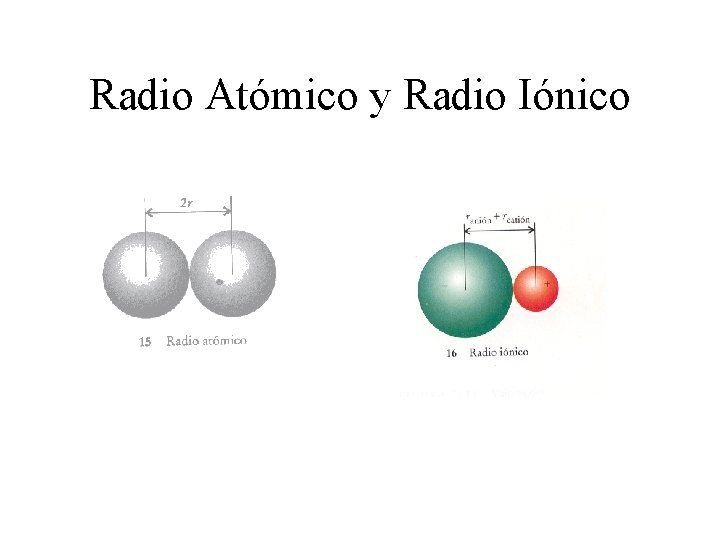
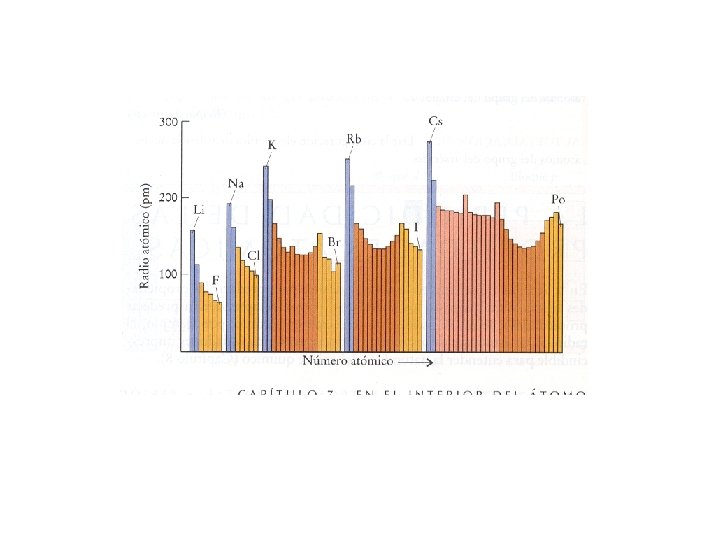
Radio Atómico y Radio Iónico

