QUIMICA BASICA PARA PRIMERO DE BACHILLERATO PROCEDIMIENTOS Problemas

QUIMICA BASICA PARA PRIMERO DE BACHILLERATO. PROCEDIMIENTOS. _

Problemas de conversión Para trasformar 5 km a mm se hace los siguiente: colocamos 1 km debajo de 5 km para que estos se puedan simplificar y como 1 km equivale a 1000 m lo colocamos en la parte superior los 1000 m para poder simplificar colocamos 1 m en la parte de abajo para que de igual manera se pueda simplificar , 1 m equivale a 100 cm colocando este valor en la parte superior para poder simplificar colocamos 1 cm en la parte de abajo 1 cm equivale a 10 mm. Seguido de esto multiplicamos todos las cantidades que se encuentran en la parte superior y dividimos para todas las cantidades de abajo obteniendo como resultado 5. 000 mm 5 km 1000 m 100 cm 10 mm R: 5. 000 mm 1 km 1 cm

Para transformar 78 km a cm : Los 78 km se encuentran ubicados en la parte superior para que se puedan simplificar colocamos 1 km en la parte inferior, como 1 km equivale a 1000 m ese resultado ira en la parte superior , para poder simplificar colocamos 1 m en la parte inferior y esto equivale a 100 cm de igual manera multiplicamos lo de arriba y ese resultado le dividimos para el resultado de abajo dándonos como resultado 7800000 cm. 78 km 1000 m 100 cm R: 780000 cm 1 km 100 cm Para transformar 300 cm a m : Los 300 cm son simplificados con 100 cm y los de 100 cm equivalen a 1 m dándonos como resultado 3 m 300 cm 1 m R: 3 m 100 cm

Para transformar 300 cm a mm : en la parte superior esta los 300 cm para poder simplificar colocamos 100 cm , estos 100 cm equivalen a 1 m de igual forma para poder simplificar en la parte inferior y 1 m equivale a 1000 mm de igual manera multiplicamos lo de arriba y ese resultado le dividimos para el resultado de abajo dándonos como resultado 300 mm 300 cm 1 m 1000 mm R: 300 mm 100 cm 1 m Para transformar 300 cm a “in” : Los 300 cm son simplificados con 2, 54 cm y los de 2, 54 cm equivalen a 1 “in” dándonos como resultado 118, 11 “in” 300 cm “in” R: 118, 11 “in” 2, 54 cm

Para transformar 5 cm a mm : Los 5 cm son simplificados con 1 cm y los de 1 cm equivalen a 10 mm dándonos como resultado 50 mm 5 cm 10 mm R: 50 mm 1 cm Para transformar 5 m a mm : en la parte superior esta los 5 m para poder simplificar colocamos 1 m, este 1 m equivalen a 100 cm de igual forma para poder simplificar en la parte inferior y 1 cm equivale a 10 mm de igual manera multiplicamos lo de arriba y ese resultado le dividimos para el resultado de abajo dándonos como resultado 5000 mm 5 m 100 cm 10 mm R: 5000 mm 1 m 1 cm

Para trasformar 5 km a mm se hace los siguiente: colocamos 1 km debajo de 5 km para que estos se puedan simplificar y como 1 km equivale a 1000 m lo colocamos en la parte superior los 1000 m para poder simplificar colocamos 1 m en la parte de abajo para que de igual manera se pueda simplificar , 1 m equivale a 100 cm colocando este valor en la parte superior para poder simplificar colocamos 1 cm en la parte de abajo 1 cm equivale a 10 mm. Seguido de esto multiplicamos todos las cantidades que se encuentran en la parte superior y dividimos para todas las cantidades de abajo obteniendo como resultado 5. 000 mm 5 km 1000 m 100 cm 10 mm R: 5000000 1 km 1 cm Para transformar 5 ft a mm : en la parte superior esta los 5 ft para poder simplificar colocamos 1 ft, este 1 ft equivalen a 30. 48 cm de igual forma para poder simplificar en la parte inferior y 1 cm equivale a 10 mm de igual manera multiplicamos lo de arriba y ese resultado le dividimos para el resultado de abajo dándonos como resultado 1. 524 mm 5 ft 30. 48 cm 10 mm R: 1. 524 mm 1 ft 1 cm

Para transformar 6 lb a onz : Las 6 lb son simplificados con 1 lb y los de 1 lb equivalen a 16 onz dándonos como resultado 96 onz 6 lb 16 onz R: 96 onz 1 lb Para transformar 6 lb a @ : Las 6 lb son simplificados con 25 lb y los de 25 lb equivalen a 1 @ dándonos como resultado 0, 24 @ 6 lb 1 @ R: 0. 24 @ 25 lb Para transformar 6 lb a qq : Las 6 lb son simplificados con 100 lb y los de 100 lb equivalen a 1 qq dándonos como resultado 0, 06 qq 6 lb qq R: 0. 06 qq 100 lb

Para transformar 6 lb a kg : Las 6 lb son simplificados con 2, 2 lb y los de 2, 2 lb equivalen a 1 kg dándonos como resultado 2, 72 kg 6 lb 1 kg R: 2. 72 Kg 2. 2 lb Para transformar 14, 4 cm a A° : en la parte superior esta los 14, 4 cm para poder simplificar colocamos 100 cm, estos 100 cm equivalen a 1 m de igual forma para poder simplificar en la parte inferior y 〖 1*10〗^(-10)m equivale a 1 A ° de igual manera multiplicamos lo de arriba y ese resultado le dividimos para el resultado de abajo dándonos como resultado 1440000000 A ° 14. 4 cm 1 A° R: 1440000000 100 cm 〖 1*10〗^(-10)m

Para transformar 14, 4 cm a pm : en la parte superior esta los 14, 4 cm para poder simplificar colocamos 100 cm, estos 100 cm equivalen a 1 m de igual forma para poder simplificar en la parte inferior y 〖 1*10〗^(-12)m equivale a 1 pm de igual manera multiplicamos lo de arriba y ese resultado le dividimos para el resultado de abajo dándonos como resultado 〖 1. 44*10〗^11 pm 14. 4 cm 1 pm R: 〖 1. 44*10〗^11 pm 100 cm 〖 1*10〗^(-12)m Para transformar 14, 4 cm a nm : en la parte superior esta los 14, 4 cm para poder simplificar colocamos 100 cm, estos 100 cm equivalen a 1 m de igual forma para poder simplificar en la parte inferior y 〖 1*10〗^(-9)m equivale a 1 nm de igual manera multiplicamos lo de arriba y ese resultado le dividimos para el resultado de abajo dándonos como resultado 〖 14. 4*10〗^6 nm 14. 4 cm 1 m 1 nm R: 〖 14. 4*10〗^6 nm 100 cm 〖 1*10〗^(-9)m



La celulosa es una biomolécula que se encuentra en un porcentaje del 50% en la madera, supongamos que una industria procesa diariamente 123500 kg de laurel, 25000 kg de eucalipto y 78400 kg de cedro. Calcular: a)la cantidad total de celulosa b)la relación de celulosa entre el laurel y el cedro c) la cantidad total de celulosa de la madera de eucalipto producida en un año. Primeramente separamos las cantidades , seguido de esto para calcular la cantidad total de celulosa sumamos las tres , para calcular la diferencia entre en el laurel y el cedro se divide la cantidad de celulosa del Laurel para la cantidad de celulosa del cedro finalmente para calcular la cantidad de celulosa total de eucalipto al año , la cantidad de celulosa dividimos para dos porque dice el 50% y ese resultado multiplicamos por 365 que son los días que lleva el año. 123500 kg Laurel 25000 kg Eucalipto 78400 kg Cedro 113450 kg Cantidad total de Celulosa : 113450 kg La relación de la celulosa entre el Laurel y el Cedro 61750 kg Laurel R: 1. 5752/1. 58. 39. 200 kg Cedro Cantidad total de celulosa de eucalipto producida por un año 2500/2 = 12500*365= 456. 2500 kg al año.





PROPIEDADES ESPECIFICAS • Color: capacidad de los cuerpos de observar (luz) con mayor o menor intensidad por ejemplo: azufre elemento no metálico color amarillo • Olor: capacidad de captar emaciones de los cuerpos atreves del nervio olfativo por ejemplo: aroma a perfumes, aroma a flores • Sabor: lengua y papilas gustativas por ejemplo: sabores ácidos / cítricos • Punto de función: es la temperatura la cual un solido se transforma en liquido por el aumento de calor por ejemplo: (AU) oro • Punto de ebullición: es la temperatura a la cual los líquidos hierven, pasan del estado líquido a gaseoso el agua hierve a 100 grados • Dureza: capacidad de la materia de vapor o ser rayado de la escala Mons. 1 -10 por ejemplo: carbono cristalizado • Solubilidad: capacidad de formar una solución solido / soluto liquido • Densidad: es la relación entre masa y volumen • Ductilidad: capacidad de los metales de transformarse (hilos) al ser metidos a altas temperaturas • Maleabilidad: capacidad de los metales de deformarse en láminas o pinchos por ejemplo: planchas o laminas de ZN, AI

PROPIEDADESA BIOLOGICAS • Disolución: capacidad de mezclarse entre soluto y solvente • Absorción: capacidad de absorber a través de estructura de los seres vivos por ejemplo pelos absorbentes e la planta • Transpiración: eliminación de líquidos que realizan todos los seres vivos atreves de las hojas • Difusión: distribución de partículas en un disolvente capacidad de expandirse por ejemplo una gota de tinta de agua otra seria el aroma de un perfume se expanda en el aire • Diálisis: es un proceso que nos permite filtrar atraves de una membrana porosa • Osmosis: es la propiedad mediante el cual un disolvente pasa atraves de una membrana semipermeable de un sitio mayor a uno de menor concentración

CLASIFICACION DE LA MATERIA • • Se dividen en: Inorgánicos: elementos de la tabla periódica Bioelementos: indispensables C-N-O-H-P-S-K-CA-M-Na-Fe Complejas: combinación de dos o más sustancias complejas son compuestos binarios HCI acido clorhídrico C 6 H 12 O 6 compuestos ternario (glucosa) Cuerpo: es la porción limitada de la materia tiene masa, peso y volumen el cual ocupa lugar en el espacio por ejemplo silla, vaso, mesa Sustancia: es la calidad de materia de la que están hechos los cuerpos Especie química: son sustancias simples o compuestas que existen con alto grado de pureza en la naturaleza por ejemplo Na. CI cloruro de sodio
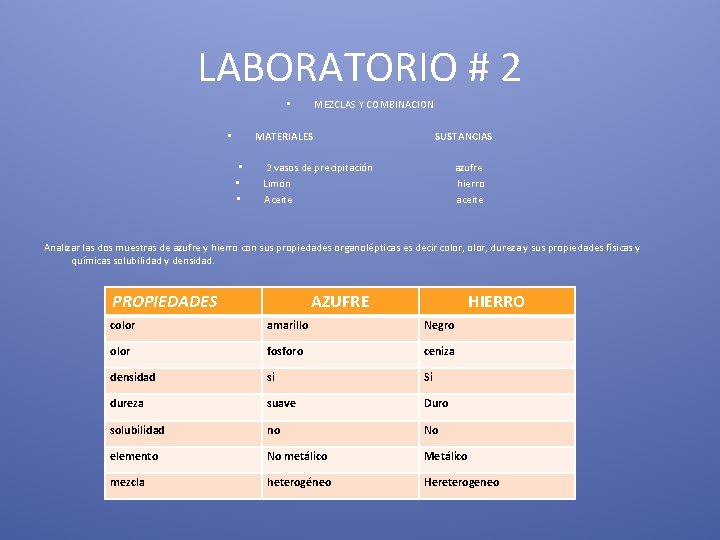
LABORATORIO # 2 MEZCLAS Y COMBINACION • MATERIALES • • SUSTANCIAS 2 vasos de precipitación azufre Limón hierro Aceite aceite Analizar las dos muestras de azufre y hierro con sus propiedades organolépticas es decir color, dureza y sus propiedades físicas y químicas solubilidad y densidad. PROPIEDADES AZUFRE HIERRO color amarillo Negro olor fosforo ceniza densidad si Si dureza suave Duro solubilidad no No elemento No metálico Metálico mezcla heterogéneo Hereterogeneo

HISTORIA DEL ATOMO 1 2 En 1808 propuso el primer modelo atómico con bases científicas. Surgió en su mente como un concepto puramente físico e inducido por el estudio de las propiedades físicas de la atmósfera y otros gases. Propuso la existencia del electrón, los cuales se distribuían en forma uniforme alrededor del átomo, este átomo se compone por los electrones de carga negativa y en el átomo positivo
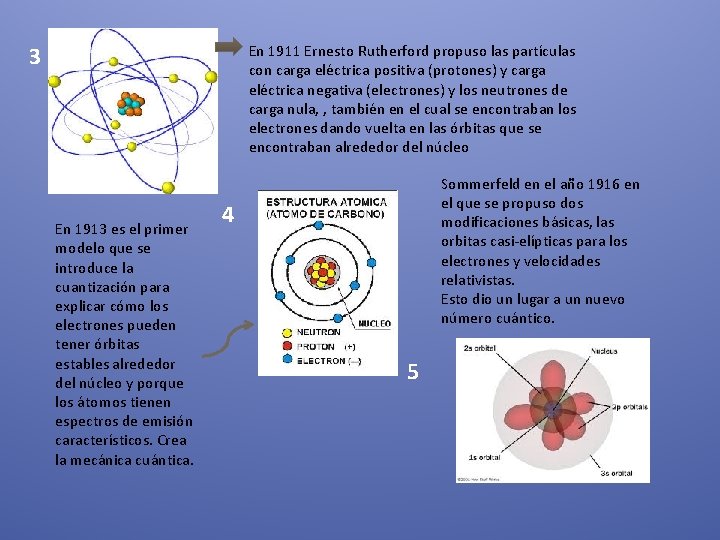
3 En 1911 Ernesto Rutherford propuso las partículas con carga eléctrica positiva (protones) y carga eléctrica negativa (electrones) y los neutrones de carga nula, , también en el cual se encontraban los electrones dando vuelta en las órbitas que se encontraban alrededor del núcleo En 1913 es el primer modelo que se introduce la cuantización para explicar cómo los electrones pueden tener órbitas estables alrededor del núcleo y porque los átomos tienen espectros de emisión característicos. Crea la mecánica cuántica. Sommerfeld en el año 1916 en el que se propuso dos modificaciones básicas, las orbitas casi-elípticas para los electrones y velocidades relativistas. Esto dio un lugar a un nuevo número cuántico. 4 5
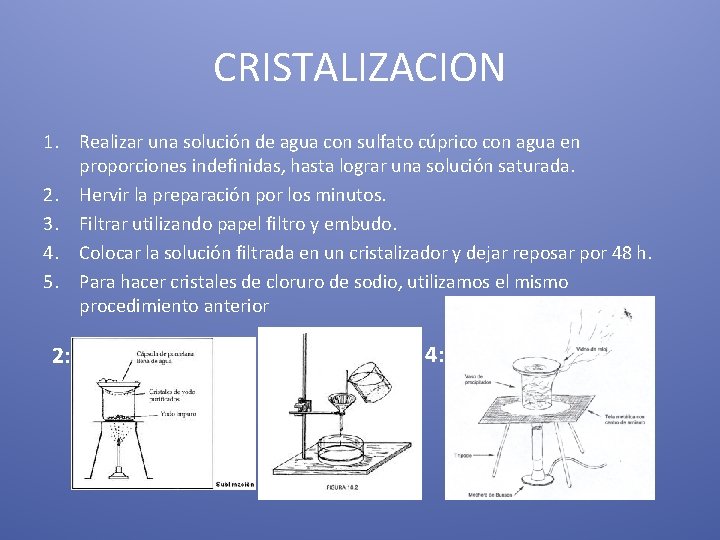
CRISTALIZACION 1. Realizar una solución de agua con sulfato cúprico con agua en proporciones indefinidas, hasta lograr una solución saturada. 2. Hervir la preparación por los minutos. 3. Filtrar utilizando papel filtro y embudo. 4. Colocar la solución filtrada en un cristalizador y dejar reposar por 48 h. 5. Para hacer cristales de cloruro de sodio, utilizamos el mismo procedimiento anterior 2: 3: 4:
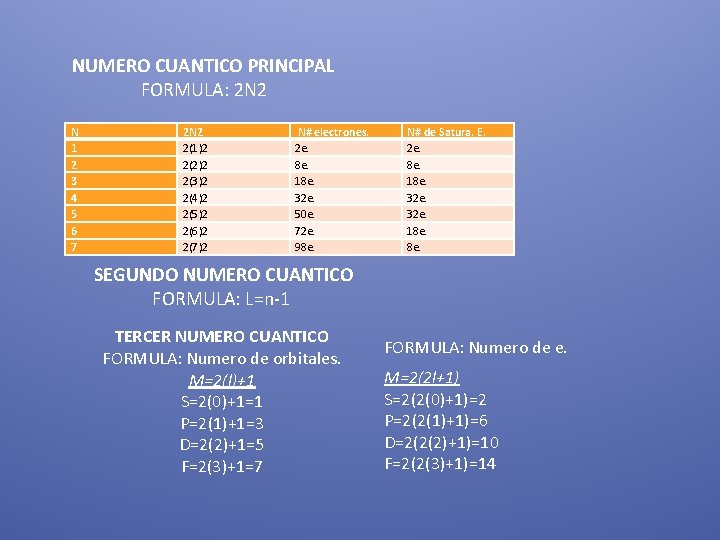
NUMERO CUANTICO PRINCIPAL FORMULA: 2 N 2 N 1 2 3 4 5 6 7 2 N 2 2(1)2 2(2)2 2(3)2 2(4)2 2(5)2 2(6)2 2(7)2 N# electrones. 2 e. 8 e. 18 e. 32 e. 50 e. 72 e. 98 e. N# de Satura. E. 2 e. 8 e. 18 e. 32 e. 18 e. SEGUNDO NUMERO CUANTICO FORMULA: L=n-1 TERCER NUMERO CUANTICO FORMULA: Numero de orbitales. M=2(l)+1 S=2(0)+1=1 P=2(1)+1=3 D=2(2)+1=5 F=2(3)+1=7 FORMULA: Numero de e. M=2(2 l+1) S=2(2(0)+1)=2 P=2(2(1)+1)=6 D=2(2(2)+1)=10 F=2(2(3)+1)=14

Tabla Periódica Grupos 6 A 7 A y 8 A

Grupo 6 A • Es llamado también anfígenos y calcogenos este grupo esta formado por Oxigeno (O), Azufre (S), Selenio (Se), Telurio (Te) y Polonio (Po). • Este grupo consiste en que: • Aunque todos ellos tienen seis electrones de valencia (última capa s 2 p 4), sus propiedades varían de no metálicas a metálicas en cierto grado, conforme aumenta su número atómico.

Oxigeno(O): • En su forma molecular más frecuente, O 2, es un gas a temperatura ambiente. Representa aproximadamente el 20, 9% en volumen de la composición de la atmósfera terrestre. Es uno de los elementos más importantes de la química orgánica y participa de forma muy importante en el ciclo energético de los seres vivos, esencial en la respiración celular de los organismos aeróbicos

Azufre(S): • Es un no metal abundante e insípido. El azufre se encuentra en forma nativa en regiones volcánicas y en sus formas reducidas formando sulfuros y sulfonales o bien en sus formas oxidadas como sulfatos.

El Selenio (Se): • El selenio se puede encontrar en varias formas alotrópicas. El selenio amorfo existe en dos formas, la vítrea, negra, obtenida al enfriar rápidamente el selenio líquido, funde a 180 °C y tiene una densidad de 4, 28 g/cm. • Es insoluble en agua y alcohol, ligeramente soluble en disulfuro de carbono y soluble en éter.

El Telurio (Te): • El telurio puede obtenerse combinado con oro en la calaverita, un mineral metálico relativamente poco abundante. • Se conocen 30 isótopos del telurio con masas atómicas que fluctúan entre 108 y 137. En la Naturaleza hay 8 isótopos del telurio, de los cuales tres son radiactivo.

El Polonio (Po): • El polonio es un elemento químico Se trata de un raro metaloide radioactivo, químicamente similar al telurio y al bismuto, presente en minerales de uranio. Esta sustancia radiactiva se disuelve con facilidad en ácidos, pero es sólo ligeramente soluble en alcalinos. Está químicamente relacionado a las dos sustancias nombradas en el apartado anterior. El polonio es un metal volátil.

Grupo 7ª: • También llamado halógenos este grupo esta formado por Flúor (F), Cloro(Cl), Bromo(Br), Yodo(I), Ástato (At). • Este grupo trata de : • En estado natural se encuentran como moléculas diatómica, X 2. Para llenar por completo su último nivel energético (s 2 p 5) necesitan un electrón más, por lo que tienen tendencia a formar un ion mononegativo, X-. Este anión se denomina haluro; las sales que lo contienen se conocen como haluros.

El Flúor (F): • El Flúor Es un gas a temperatura ambiente, de color amarillo pálido, formado por moléculas diatómicas F 2. Es el más electronegativo y reactivo de todos los elementos. En forma pura es altamente peligroso, causando graves quemaduras químicas en contacto con la piel.

El Cloro(Cl): • El Cloro en condiciones normales y en estado puro forma dicloro: un gas tóxico amarilloverdoso formado por moléculas diatómicas (Cl 2) unas 2, 5 veces más pesado que el aire, de olor desagradable y venenoso. Es un elemento abundante en la naturaleza y se trata de un elemento químico esencial para muchas formas de vida.

El bromo(Br): • El bromo a temperatura ambiente es un líquido rojo, volátil y denso. Su reactividad es intermedia entre el cloro y el yodo. En estado líquido es peligroso para el tejido humano y sus vapores irritan los ojos y la garganta. • El bromo se emplea en la fabricación de productos de fumigación, agentes ininflamables, productos para la purificación de aguas, colorantes Etc.

Yodo (I): • Este átomo puede encontrarse en forma molecular como iodo diatómico. • Es un oligoelemento y se emplea principalmente en medicina, fotografía y como colorante. Químicamente, el yodo es el halógeno menos reactivo y electronegativo.

Ástato (At): • Este elemento radiactivo, el más pesado de los halógenos, se produce a partir de la degradación de uranio y torio. El astato, seguido del francio, es el elemento más raro de la naturaleza, con una cantidad total sobre la superficie terrestre menor a 25 gramos en el mismo instante de tiempo. El comportamiento químico de este elemento altamente radiactivo es muy similar al de otros halógenos, especialmente el iodo.

Grupo 8 A: • Tambien llamado gases Nobles o gases inertes son un grupo de elementos químicos con propiedades muy similares: bajo condiciones normales, son gases monoatómicos inodoros, incoloros y presentan una reactividad química muy baja. • Este grupo esta formado por los siguientes elementos: Los seis gases nobles que se encuentran en la naturaleza son helio (He), neón (Ne), argón (Ar), kriptón (Kr), xenón (Xe) y el radioactivo radón (Rn). Hasta ahora el siguiente miembro del grupo, el ununoctio (Uuo), ha sido sintetizado en un acelerador de partículas, pero se conoce muy poco de sus propiedades debido a la pequeña cantidad producida.

Helio (He): • El Helio al tener el nivel de energía completo presenta las propiedades de un gas noble. Es decir, es inerte (no reacciona) y al igual que éstos, es un gas monoatómico incoloro e inodoro. El helio tiene el menor punto de ebullición de todos los elementos químicos y sólo puede ser solidificado bajo presiones muy grandes.

• El neón, argón, kriptón y xenón se obtienen del aire usando los métodos de licuefacción y destilación fraccionada. El helio es típicamente separado del gas natural y el radón se aísla normalmente a partir del decaimiento radioactivo de compuestos disueltos del radio. Los gases nobles tienen muchas aplicaciones importantes en industrias como iluminación, soldadura y exploración espacial. La combinación helio-oxígeno-nitrógeno (trimix) se emplea para respirar en inmersiones de profundidad para evitar que los buzos sufran el efecto narcótico del nitrógeno. Después de verse los riesgos causados por la inflamabilidad del hidrógeno, éste fue reemplazado por helio en los dirigibles y globos aerostáticos.

Neón (Ne): • Es un gas noble, incoloro, prácticamente inerte, presente en trazas en el aire, pero muy abundante en el universo, que proporciona un tono rojizo característico a la luz de las lámparas fluorescentes en las que se emplea. Es el segundo gas noble más ligero, y presenta un poder de refrigeración, por unidad de volumen, 40 veces mayor que el del helio líquido y tres veces mayor que el del hidrógeno líquido. En la mayoría de las aplicaciones el uso de neón líquido es más económico que el del helio.

Argón (Ar): • Es el tercero de los gases nobles, incoloro e inerte como ellos, constituye en torno al 1% del aire. Del griego Argos que significa perezoso (debido a que no reacciona). Se emplea como gas de relleno en lámparas incandescentes ya que no reacciona con el material del filamento incluso a alta temperatura y presión, prolongando de este modo la vida útil de la bombilla, y en sustitución del neón en lámparas fluorescentes cuando se desea un color verde-azul en vez del rojo del neón.

Kriptón (Kr): • El kriptón es un gas noble inoloro e insípido de poca reactividad caracterizado por un espectro de líneas verde y rojo-naranja muy brillantes. Es uno de los productos de la fisión nuclear del uranio. El kriptón sólido es blanco, de estructura cristalina cúbica centrada en las caras al igual que el resto de gases nobles

Ununoctio (Uuo): • Ununoctio conocido anteriormente como ekaradón o elemento 118 El átomo de ununoctio es radiactivo y altamente inestable. El ununocti es el elemento químico más pesado observado en laboratorio y su síntesis, junto a la del ununhexio, no estuvo exenta de polémica.

Xenon (Xe): • Gas noble inodoro, muy pesado, incoloro, el xenón está presente en la atmósfera terrestre sólo en trazas y fue parte del primer compuesto de gas noble sintetizado. El xenón es un miembro de los elementos de valencia cero llamados gases nobles o inertes.

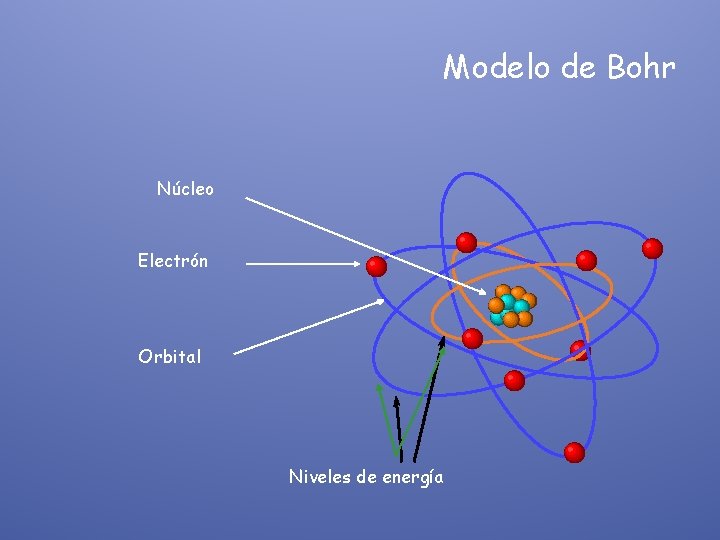
Modelo de Bohr Núcleo Electrón Orbital Niveles de energía
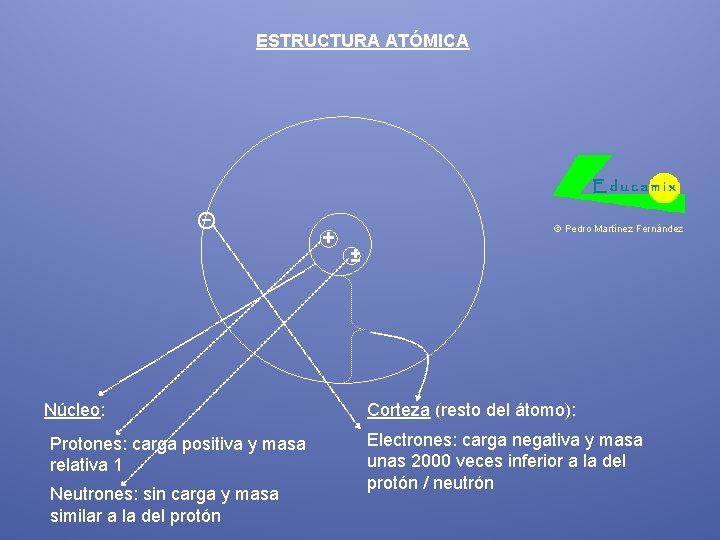
ESTRUCTURA ATÓMICA Θ Núcleo: Protones: carga positiva y masa relativa 1 Neutrones: sin carga y masa similar a la del protón + © Pedro Martínez Fernández ± Corteza (resto del átomo): Electrones: carga negativa y masa unas 2000 veces inferior a la del protón / neutrón

Desarrollo de la actual teoría atómica Números cuánticos y Niveles de energía. Un electrón que se mueve alrededor de núcleo puede considerarse ligado a él y podemos describir su movimiento ondulatorio mediante la ecuación de ondas. Con esta idea, Schrödinger realizó un estudio matemático del comportamiento del electrón en el átomo y obtuvo una expresión, conocida como ecuación de Schrödinger. Para que la ecuación de Schrödinger tenga significado físico es necesario imponerle unas restricciones que son conocidas como números cuánticos, que se simbolizan de la misma forma que los obtenidos en el modelo atómico de Bohr

n : número cuántico principal l : número cuántico del momento angular orbital m : número cuántico magnético s : número cuántico del spin electrónico Estos números cuánticos sólo pueden tomar ciertos valores permitidos: para n : números enteros 1, 2, 3, … para l : números enteros desde 0 hasta (n-1) para m : todos los números entre +l y -l incluido el 0 para s : sólo los números fraccionarios -1/2 y +1/2
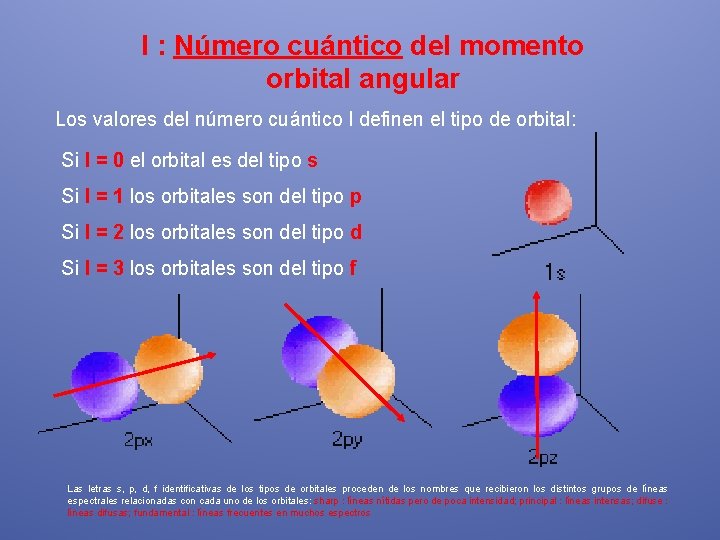
l : Número cuántico del momento orbital angular Los valores del número cuántico l definen el tipo de orbital: Si l = 0 el orbital es del tipo s Si l = 1 los orbitales son del tipo p Si l = 2 los orbitales son del tipo d Si l = 3 los orbitales son del tipo f Las letras s, p, d, f identificativas de los tipos de orbitales proceden de los nombres que recibieron los distintos grupos de líneas espectrales relacionadas con cada uno de los orbitales: sharp : líneas nítidas pero de poca intensidad; principal : líneas intensas; difuse : líneas difusas; fundamental : líneas frecuentes en muchos espectros
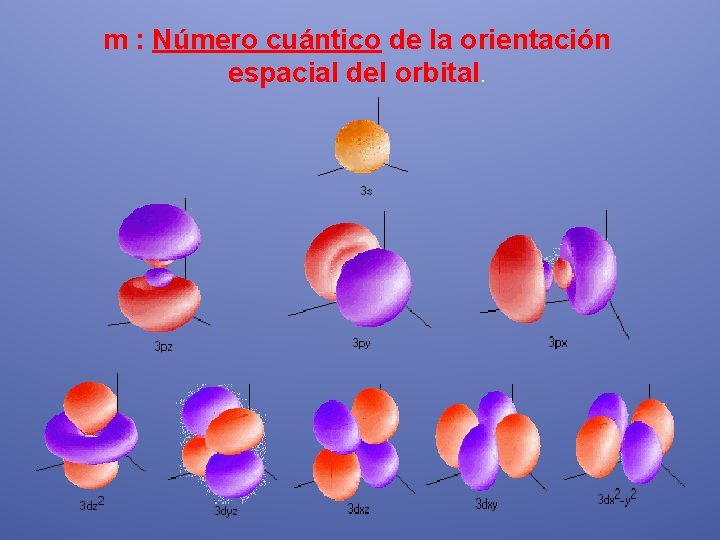
m : Número cuántico de la orientación espacial del orbital.
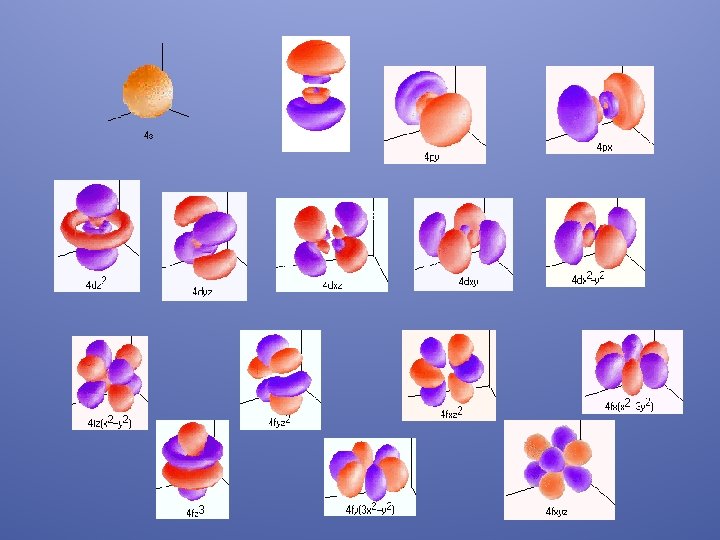
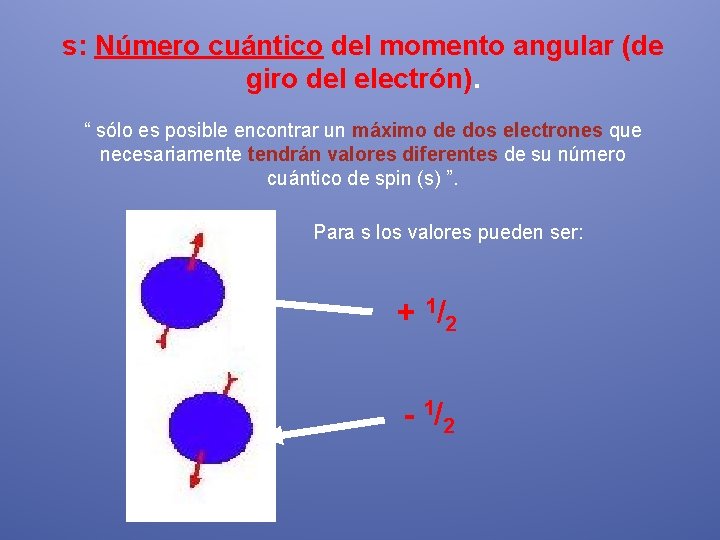
s: Número cuántico del momento angular (de giro del electrón). “ sólo es posible encontrar un máximo de dos electrones que necesariamente tendrán valores diferentes de su número cuántico de spin (s) ”. Para s los valores pueden ser: + 1/ 2 - 1/ 2

El conjunto de los cuatro números cuánticos definen a un electrón, no pudiendo existir en un mismo átomo dos electrones con los cuatro números cuánticos iguales, por lo que una vez definido el tamaño, el tipo y la orientación de un orbital con los tres primeros números cuánticos, es decir los valores de n, l y m, sólo es posible encontrar un máximo de dos electrones en dicha situación que necesariamente tendrán valores diferentes de su número cuántico de spin.
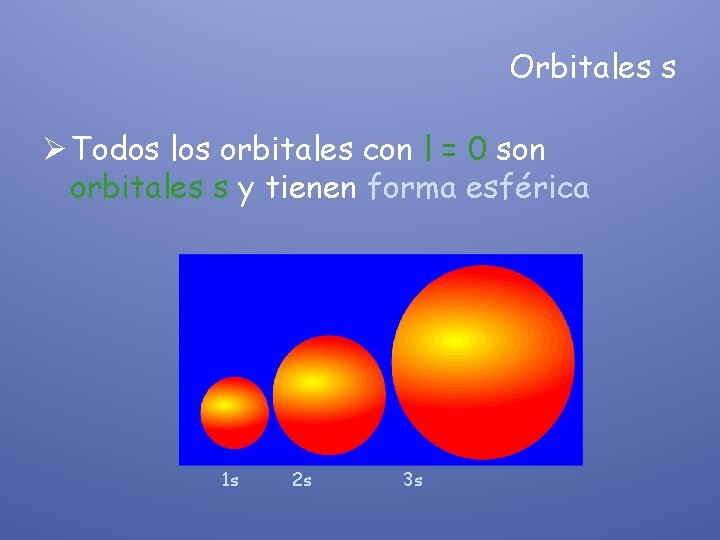
Orbitales s Ø Todos los orbitales con l = 0 son orbitales s y tienen forma esférica 1 s 2 s 3 s
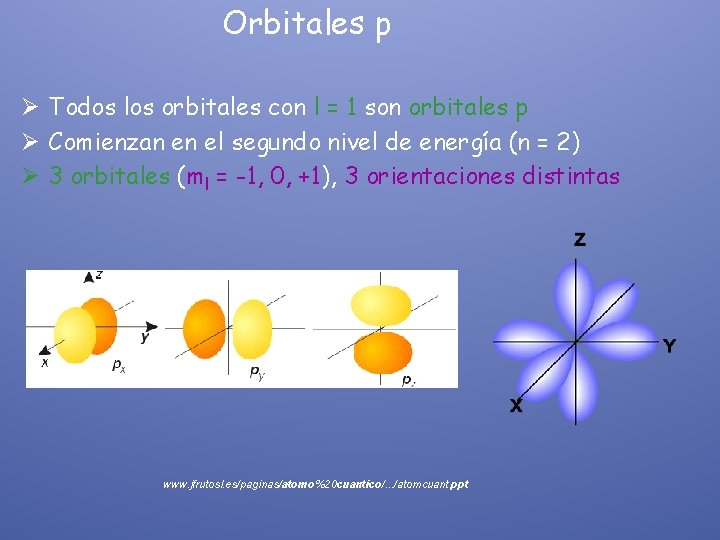
Orbitales p Ø Todos los orbitales con l = 1 son orbitales p Ø Comienzan en el segundo nivel de energía (n = 2) Ø 3 orbitales (ml = -1, 0, +1), 3 orientaciones distintas www. jfrutosl. es/paginas/atomo%20 cuantico/. . . /atomcuant. ppt

La ecuación de Schrödinger La ecuación predice una región tridimensional alrededor del núcleo atómico llamado ORBITAL ATÓMICO , donde hay probabilidad de encontrar al electrón
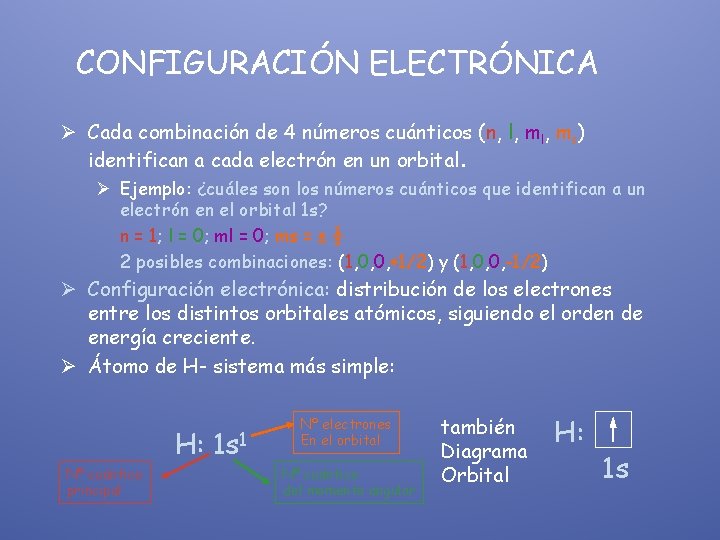
CONFIGURACIÓN ELECTRÓNICA Ø Cada combinación de 4 números cuánticos (n, l, ms) identifican a cada electrón en un orbital. Ø Ejemplo: ¿cuáles son los números cuánticos que identifican a un electrón en el orbital 1 s? n = 1; l = 0; ms = ± ½ 2 posibles combinaciones: (1, 0, 0, +1/2) y (1, 0, 0, -1/2) Ø Configuración electrónica: distribución de los electrones entre los distintos orbitales atómicos, siguiendo el orden de energía creciente. Ø Átomo de H- sistema más simple: H: Nº cuántico principal 1 s 1 Nº electrones En el orbital Nº cuántico del momento angular también Diagrama Orbital H: 1 s

PRINCIPIO DE EXCLUSIÓN DE PAULI Un máximo de dos electrones pueden ocupar un mismo orbital atómico pero solamente si los electrones tienes spin opuesto.

a) Todos los orbitales relacionados con un subnivel de energía son de igual energía = los tres orbitales 2 p tienen la misma energía. b) En átomos con múltiples electrones, los subniveles de energía dentro de un nivel principal tienen energía diferentes = los orbitales 2 p tienen energía más alta que el orbital 2 s.

DIAGRAMA DE SUBNIVEL 1 s 2 s 2 p 3 s 3 p 3 d 4 s 4 p 4 d 4 f 5 s 5 p 5 d 5 f 6 s 6 p 6 d 7 s 7 p
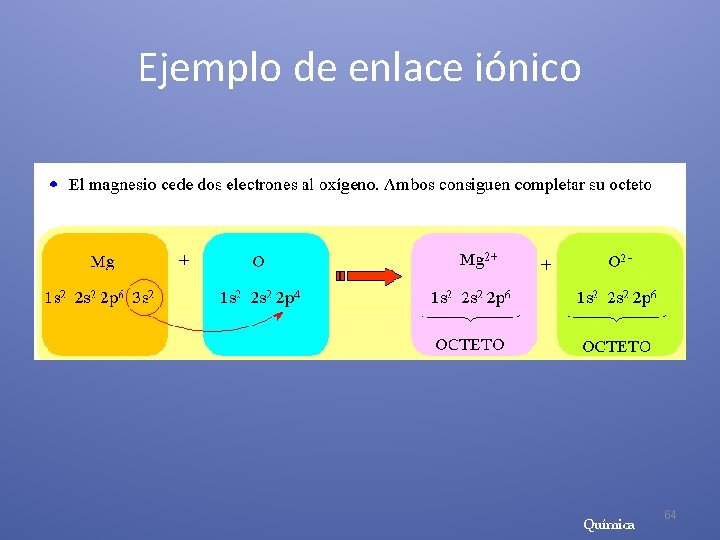
Ejemplo de enlace iónico Química 64
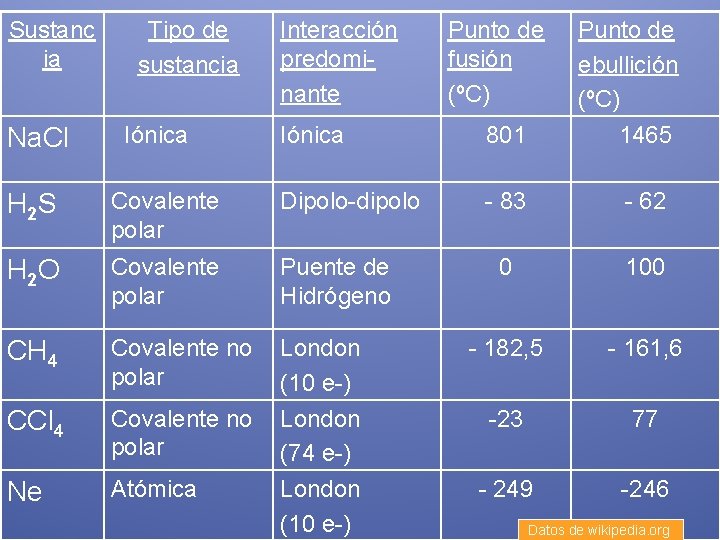
Sustanc ia Na. Cl Tipo de sustancia Iónica Interacción predominante Punto de fusión (ºC) Punto de ebullición (ºC) 1465 Iónica 801 - 83 - 62 0 100 - 182, 5 - 161, 6 -23 77 - 249 -246 H 2 S Covalente polar Dipolo-dipolo H 2 O Covalente polar Puente de Hidrógeno CH 4 Covalente no polar CCl 4 Covalente no polar Ne Atómica London (10 e-) London (74 e-) London (10 e-) Datos de wikipedia. org

CONFIGURACIÓN ELECTRÓNICA Consiste en distribuir a los electrones en los niveles, subniveles y orbitales del átomo. La finalidad es la de conocer cuántos electrones exteriores (en el último nivel de energía) tiene y de ese modo deducir las propiedades químicas del elemento en cuestión. Existen diferentes métodos para ordenar los electrones, pero antes de exponer el método a usar, daremos algunas recomendaciones que debemos tener siempre en cuenta. a) El número atómico siempre indica el número de electrones para cada elemento. b) Existe un número máximo de electrones en cada subnivel. c) Los subniveles se van llenando en forma que se van completando los subniveles de menor energía.
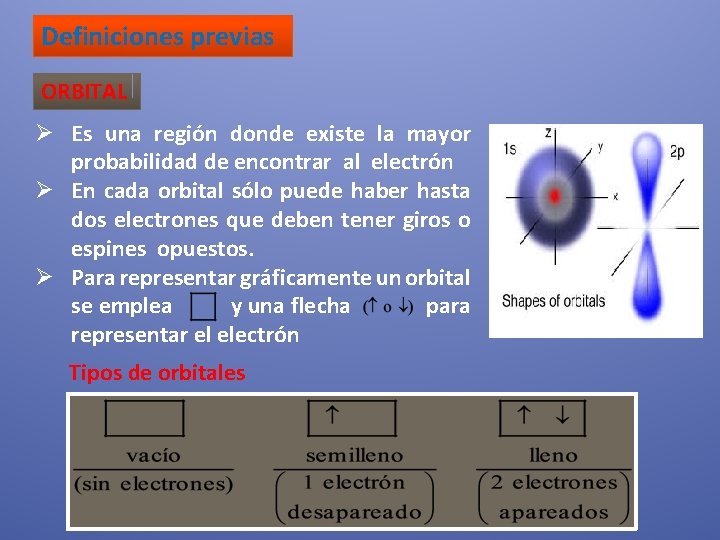
Definiciones previas ORBITAL Ø Es una región donde existe la mayor probabilidad de encontrar al electrón Ø En cada orbital sólo puede haber hasta dos electrones que deben tener giros o espines opuestos. Ø Para representar gráficamente un orbital se emplea y una flecha para representar el electrón Tipos de orbitales
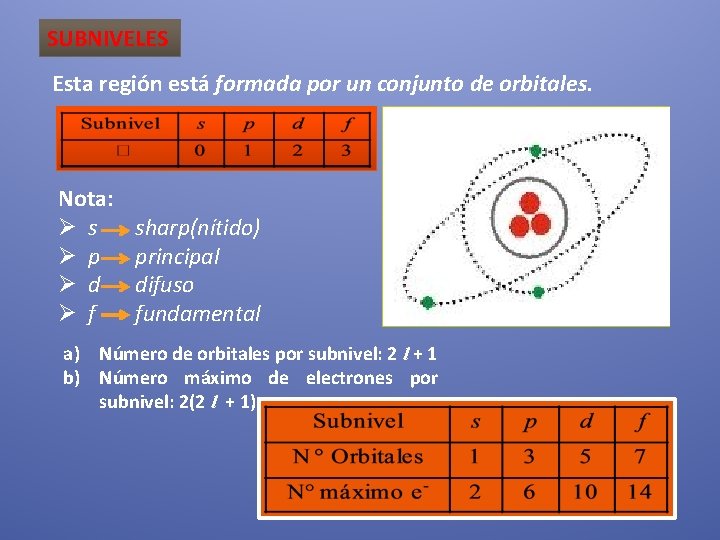
SUBNIVELES Esta región está formada por un conjunto de orbitales. Nota: Ø s Ø p Ø d Ø f sharp(nítido) principal difuso fundamental a) Número de orbitales por subnivel: 2 l + 1 b) Número máximo de electrones por subnivel: 2(2 l + 1)
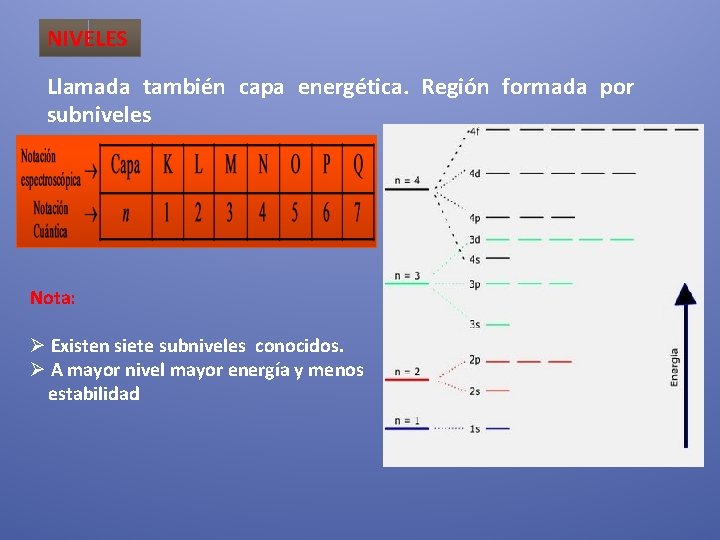
NIVELES Llamada también capa energética. Región formada por subniveles Nota: Ø Existen siete subniveles conocidos. Ø A mayor nivel mayor energía y menos estabilidad
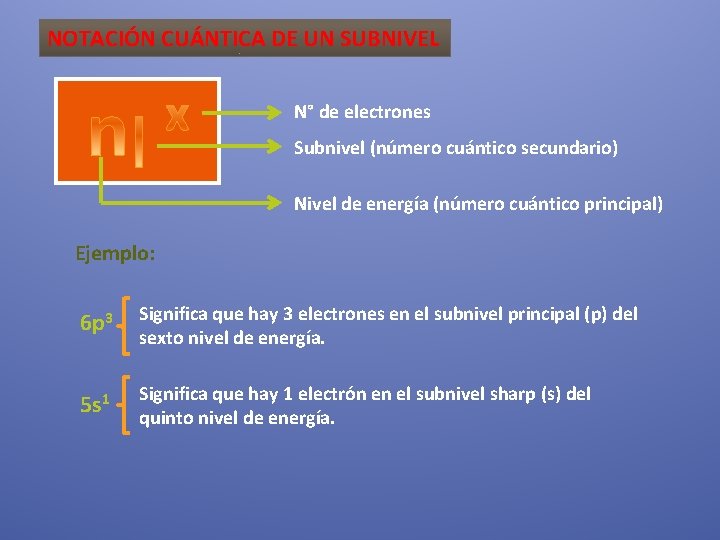
NOTACIÓN CUÁNTICA DE UN SUBNIVEL N° de electrones Subnivel (número cuántico secundario) Nivel de energía (número cuántico principal) Ejemplo: 6 p 3 Significa que hay 3 electrones en el subnivel principal (p) del sexto nivel de energía. 5 s 1 Significa que hay 1 electrón en el subnivel sharp (s) del quinto nivel de energía.

Principio de Construcción (Aufbau) Este principio establece que los electrones se distribuyen en los subniveles, en orden creciente a su energía relativa (E. R) Aufbau = palabra alemana : que significa construcción progresiva Energía Relativa (E. R) n: nivel de energía l: subnivel de energía Ejemplo: Subnivel n l E. R 2 p 5 2 1 3 4 d 8 5 s 1 4 f 11
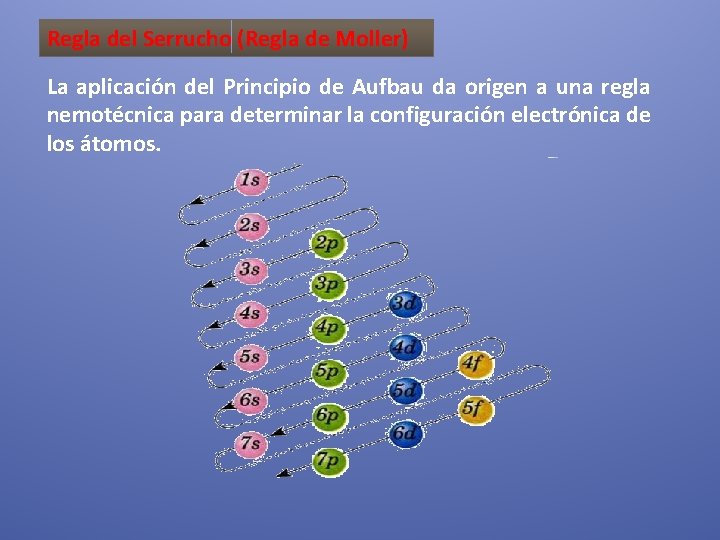
Regla del Serrucho (Regla de Moller) La aplicación del Principio de Aufbau da origen a una regla nemotécnica para determinar la configuración electrónica de los átomos.

Si empezamos por la línea superior y seguimos la flecha obtenemos el siguiente orden: 1 s 22 p 63 s 23 p 64 s 23 d 104 p 65 s 24 d 105 p 66 s 24 f 145 d 106 p 67 s 2 5 f 146 d 107 p 6 Ejemplo: Escribir las configuraciones electrónicas por subniveles para los siguientes átomos. Ø 9 F : 1 s 22 p 5 Ø 15 P : Ø 20 Ca: Ø 30 Zn: Ø 38 Sr :

Configuración Electrónica abreviada El método del Kernel, es una abreviación de la configuración de un gas noble. Los gases nobles son: helio (2 He), neón (10 Ne), argón (18 Ar), kriptón (36 Kr), xenón (54 Xe) y radón (86 Rn). Ejemplo: Realizar la C. E simplificada de los siguientes átomos. Ø 13 Al : [10 Ne] 3 s 2 3 p 1 Ø 34 Se : Ø 53 I : Ø 82 Pb :

Principio de Máxima Multiplicidad (Regla de Hund) La regla de Hund es una regla empírica obtenida por Friedrich Hund que enuncia lo siguiente: “ Al distribuir electrones en orbitales del mismo subnivel, primero se trata de ocupar todos estos orbitales antes de terminar de llenarlos, esto es, los electrones deben tener igual sentido de spin (espines paralelos) antes de aparearse. Ejemplo: Indique la C. E por orbitales para los siguientes átomos Ø 7 N : 1 s 22 p 3 => Ø 16 S :

Configuración Electrónica de iones 1. Para un anión Ø Primero se determina la cantidad de electrones. Ø Luego se realiza la configuración electrónica Ejemplo: Realizar la C. E de los siguientes aniones. Ø 8 O-2 : 1 s 22 p 6 e-=10 Ø 15 P-3 : 2. Para un catión Ø Primero se realiza la C. E para el átomo neutro. Ø Luego se quitan los electrones del nivel más externo. En caso que en el nivel más externo hayan varios subniveles, los electrones salen en orden: f, d, p, s

Ejemplo: Realizar la C. E de los siguientes cationes. Ø 20 Ca +2 Ø 26 Fe+3 Anomalías en la Configuración Electrónica Al desarrollar la configuración electrónica, encontramos una serie de excepciones, a las cuales consideramos como anomalías, entre estas tenemos los Antiserruchos. Se presenta en elementos de los grupos VIB y IB

Ejemplo: Realizar la C. E de los siguientes átomos. salta 1 electrón Ø 24 Cr [18 Ar] 4 s 2 3 d 4 (inestable) [18 Ar] 4 s 1 3 d 5 (estable) salta 1 electrón Ø 29 Cu [18 Ar] 4 s 2 3 d 9 (inestable) [18 Ar] 4 s 1 3 d 10 (estable)

Ácidos Hidrácidos En este caso el hidrogeno actúa con estado de oxidación 1+( ) , los halógenos con (1 -) y los anfígenos con (2 -) halógenos ( F, Cl, Br, I) anfígenos( S, Se, Te) • Ejemplos: La formula química del acido fluorhídrico es Hf su Reacción química es: 0 + 2 v El hidrogeno mas el flúor produce acido fluorhídrico v El hidrogeno tiene un estado de oxidación de 1+ mientras que el fluor de 1 - Entonces hacen que los dos se neutralicen dando como resultado 0 v Para que las cargas se equiparen ponemos el 2 adelante y asi tanto en los dos

Lados podemos observar 2 H y 2 F Ejemplo 2: • La formula química del acido clorhídrico es HCl su Reacción química es: 0 + 2 v El hidrogeno mas el cloro produce acido clorhídrico v El hidrogeno tiene un estado de oxidación de 1+ a diferencia del cloro que tiene un estado de 1 - Entonces hacen que los dos se neutralicen dando como resultado 0 v Para que las cargas se equiparen ponemos el 2 adelante y asi tanto en los dos lados podemos observar 2 H y 2 Cl Ejemplo 3: • La formula química del acido Bromhídrico es H Br su Reacción química es:

0 + 2 v El hidrogeno mas el bromo produce acido Bromhídrico v El hidrogeno tiene un estado de oxidación de 1+ mientras que el Bromo de 1 - Entonces hacen que los dos se neutralicen dando como resultado 0 v Para que las cargas se equiparen ponemos el 2 adelante y así tanto en los dos lados podemos observar 2 H y 2 Br Ejemplo 4 : • La formula química del acido sulfhídrico es 0 + S S su Reacción química es: v El hidrogeno mas el azufre produce acido sulfhídrico

v El hidrogeno tiene un estado de oxidación de 1+ en cambio el azufre tiene un estado de oxidación de 2 - v entonces dividimos 2/1 es igual a 2 v no se toma en cuenta los signos en el momento de dividir v Como 2/1 es =2 el 2 con signo positivo baja debajo del hidrogeno v Entonces ahí si podemos neutralizar porque el hidrogeno ahora tiene un estado de 2 y el azufre de -2 v Quedándonos como resultado 0 v Y tanto de los dos lados están equiparados Ejemplo 5: • La formula química del acido selenhídrico es Se su Reacción química es: 0 + Se v El hidrogeno mas el selenio produce acido selenhídrico

v El hidrogeno tiene un estado de oxidación de 1+ a diferencia del selenio tiene un estado de oxidación de 2 - v entonces dividimos 2/1 es igual a 2 v no se toma en cuenta los signos en el momento de dividir v Como 2/1 es =2 el 2 con signo positivo baja debajo del hidrogeno v Entonces ahí si podemos neutralizar porque el hidrogeno ahora tiene un estado de 2 y el selenio de -2 v Quedándonos como resultado 0 v Y tanto de los dos lados están equiparados Ejemplo 6: • La formula química del acido Telurhídrico es Te su Reacción química es: 0 + Te v El hidrogeno mas el selenio produce acido telurhídrico

v El hidrogeno tiene un estado de oxidación de 1+ a diferencia del telurio tiene un estado de oxidación de 2 - v entonces dividimos 2/1 es igual a 2 v no se toma en cuenta los signos en el momento de dividir v Como 2/1 es =2 el 2 con signo positivo baja debajo del hidrogeno v Entonces ahí si podemos neutralizar porque el hidrogeno ahora tiene un estado de 2 y el telurio de -2 v Quedándonos como resultado 0 v Y tanto de los dos lados están equiparados
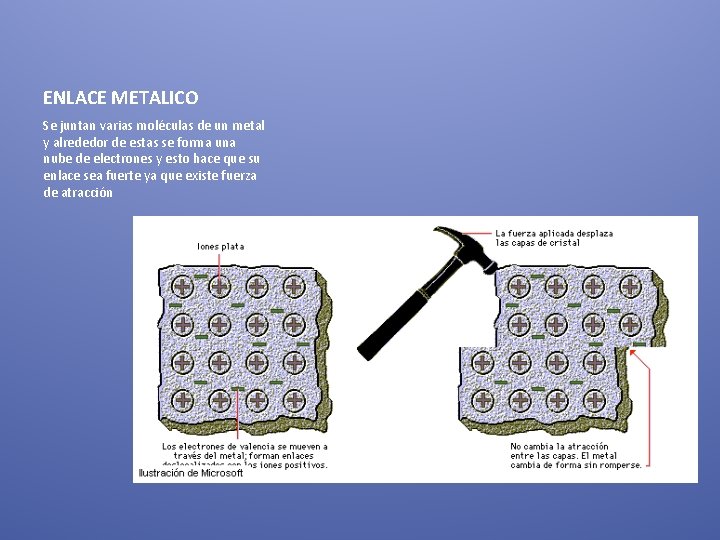
ENLACE METALICO Se juntan varias moléculas de un metal y alrededor de estas se forma una nube de electrones y esto hace que su enlace sea fuerte ya que existe fuerza de atracción
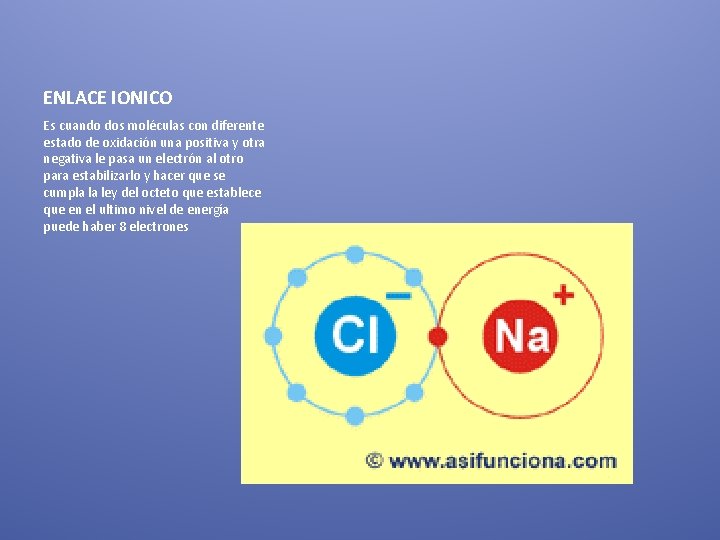
ENLACE IONICO Es cuando dos moléculas con diferente estado de oxidación una positiva y otra negativa le pasa un electrón al otro para estabilizarlo y hacer que se cumpla la ley del octeto que establece que en el ultimo nivel de energía puede haber 8 electrones

ENLACE COVALENTE SIMPLE covalente significa compartir cuando 2 moléculas con la misma electronegatividad se comparten un par de electrones para así estabilizarse los 2
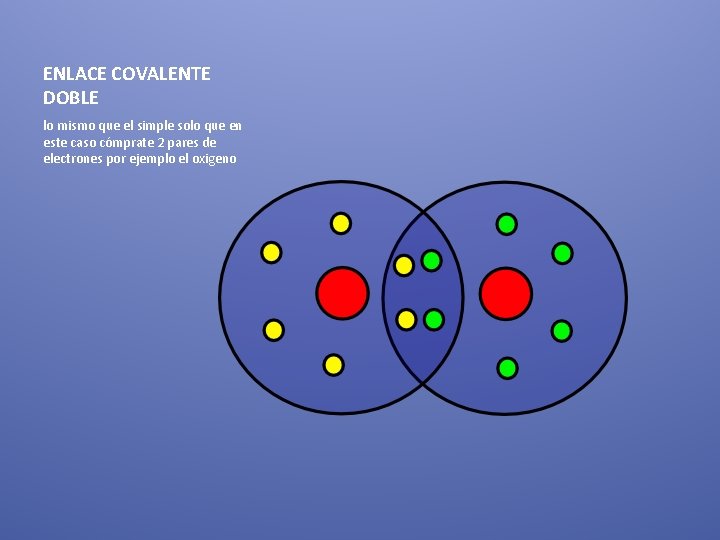
ENLACE COVALENTE DOBLE lo mismo que el simple solo que en este caso cómprate 2 pares de electrones por ejemplo el oxigeno
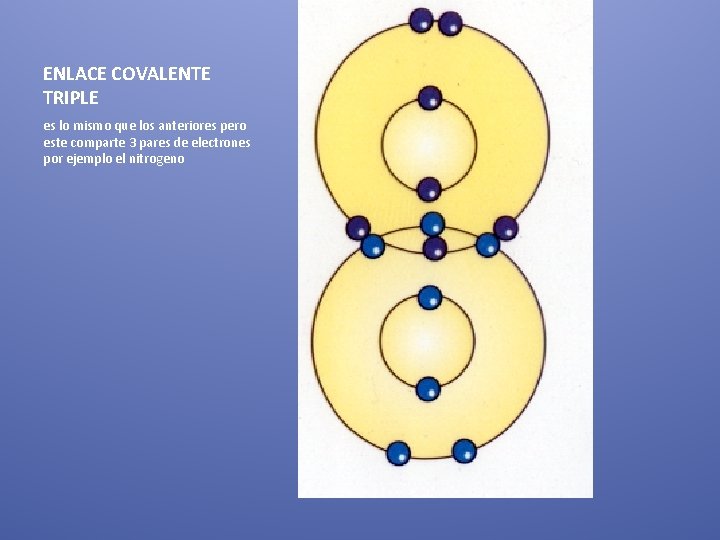
ENLACE COVALENTE TRIPLE es lo mismo que los anteriores pero este comparte 3 pares de electrones por ejemplo el nitrogeno

ENLACE APOLAR Es cuando 2 moléculas con diferentes cargas se juntan y forman una fuerza de atracción

ENLACE POLAR cuando 2 moléculas con la misma carga sea positiva o negativa se juntan y forman una fuerza de repulsión

PUENTES DE HIDROGENO Son muy débiles ya que los 2 de hidrogeno son positivos por lo que forman una fuerza de repulsión pero se estabiliza cuando se unen con el oxigeno ya que es negativo por lo tanto ahí se puede mantener unida la formula del agua y solo se forman con otras moléculas de agua

FIN.
- Slides: 93