quilibre chimique Il faut remplir 3 conditions pour
Équilibre chimique

Il faut remplir 3 conditions pour atteindre l’équilibre chimique: • 1. Système fermé; • 2. Réaction réversible; • 3. Propriétés macroscopiques constantes.

Le Principe de Le Châtelier Si nous avons un système déjà à l’équilibre et que l’on y fait un changement ou une modification, un changement ou une modification le système s’opposera au changement en favorisant la favorisant réaction opposée jusqu’à l’obtention d’un nouvel équilibre

Modification de la concentration: concentration Si au départ, la réaction est à l’équilibre, que se passera-t-il si on ajoute… Fe 3+(aq)?
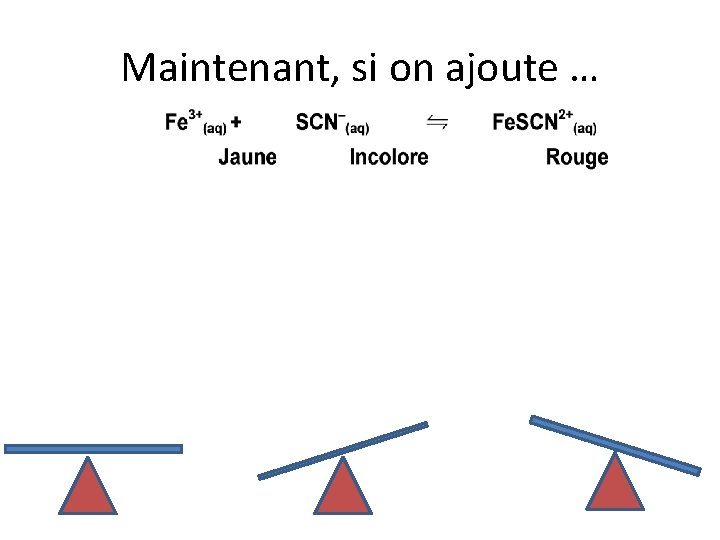
Maintenant, si on ajoute …
Déplacement de l’équilibre Éq. déplacé vers Changement

Ainsi, Substance ajoutée Changement de la concentration Couleur de la nouvelle solution Ajout de thiocyanate de potassium solide Augmentation de [SCN–] Rouge foncé Ajout de trinitrate de fer Augmentation de [Fe 3+] Rouge Ajout d’hydrogénophosphate de disodium solide Diminution de [Fe 3+] Jaune plus pâle

Quel est l’effet de l’augmentation de la concentration d’un réactif sur l’état d’équilibre ? Expliquez votre réponse . La réaction directe est favorisée ; c’est ce qui se produit dans les éprouvettes 2 et 3.

Quel est l’effet de la diminution de la concentration d’un réactif sur l’état d’équilibre ? Expliquez votre réponse. La réaction inverse est favorisée

Quel serait l’effet de l’augmentation de la concentration d’un produit sur l’état d’équilibre ? Expliquez votre réponse.

Maintenant, avec un autre exemple:

Le Principe de Le Châtelier dit que… En présence d’une réaction endothermique, une augmentation de la température favorise la réaction directe. Ainsi, pour cette même réaction, un diminution de température favorise la réaction inverse. A + B + Én. ↔ C + D En présence d’une réaction exothermique, une augmentation de température favorise la réaction inverse. Ainsi, pour cette même réaction, un diminution de température favorise la réaction directe. C + D ↔ A + B + Én.

Modification de la température: température Pour la même réaction, que se passera-t-il si on modifie la température?
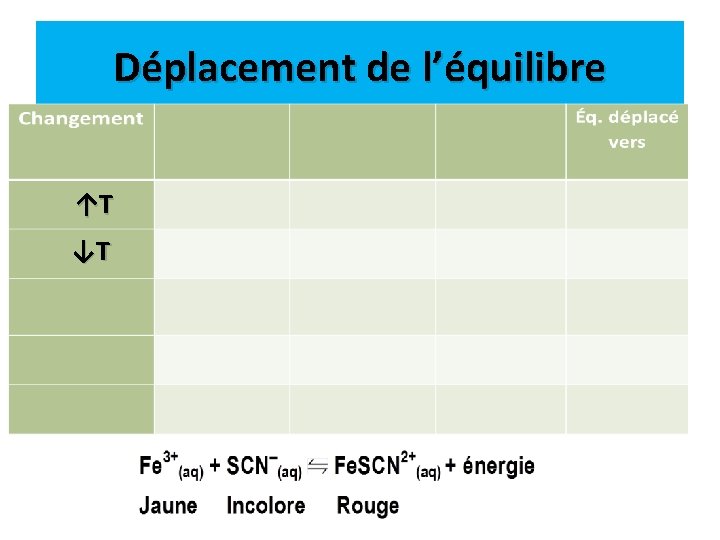
Déplacement de l’équilibre ↑T ↓T

Quelle réaction est favorisée par l’augmentation de la température ? Expliquez votre réponse.

Que peut-on dire des concentrations en ions Fe 3+, SCN– et Fe. SCN 2+ après l’augmentation de la température ? Expliquez votre réponse.

Quelle réaction est favorisée par la diminution de la température ? Expliquez votre réponse.

L’augmentation de la température a-t-elle favorisé la réaction endothermique ou la réaction exothermique ? Expliquez votre réponse.

Maintenant, avec un autre exemple:

Changement plus subtil… • • ↑P (en ↓ V) ↓ P (en ↑ V) Observez bien la vidéo: https: //youtu. be/s. Gbxx. Xx 32 i 4

Déplacement de l’équilibre
- Slides: 21