Quelques proprits de leau temprature dbullition leve la

Quelques propriétés de l’eau: -température d’ébullition élevée à la pression atmosphérique(100°C) -bon solvant des composés ioniques (comme le chlorure de sodium) et de certains composés moléculaires (comme le chlorure d’hydrogène) -propriétés ionisantes et hydratantes La structure de la molécule d’eau explique-t-elle ces propriétés?
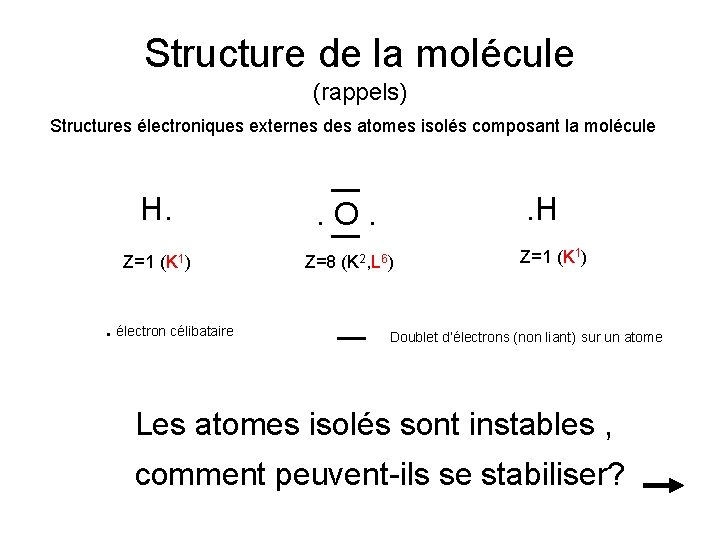
Structure de la molécule (rappels) Structures électroniques externes des atomes isolés composant la molécule H. . O. Z=1 (K 1) Z=8 (K 2, L 6) . électron célibataire . H Z=1 (K 1) Doublet d’électrons (non liant) sur un atome Les atomes isolés sont instables , comment peuvent-ils se stabiliser?
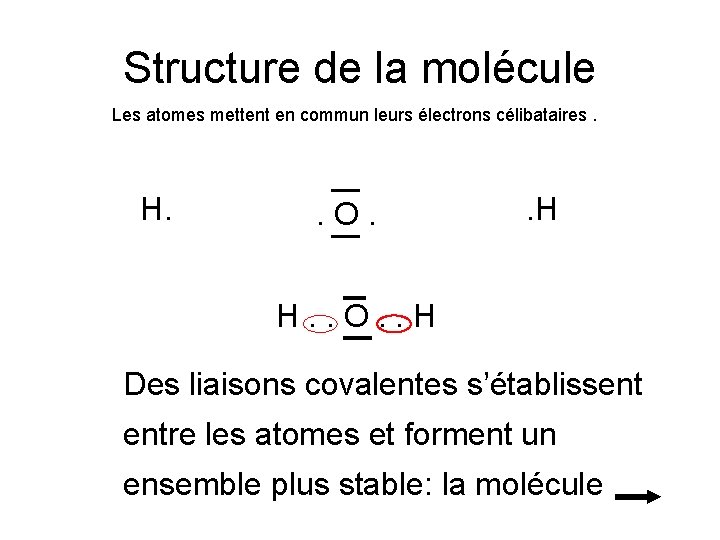
Structure de la molécule Les atomes mettent en commun leurs électrons célibataires. H. . O. . H Des liaisons covalentes s’établissent entre les atomes et forment un ensemble plus stable: la molécule
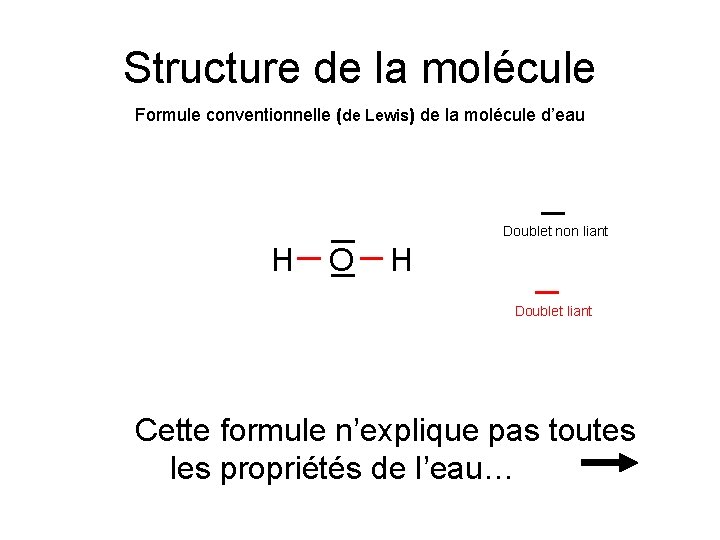
Structure de la molécule Formule conventionnelle (de Lewis) de la molécule d’eau Doublet non liant H O H Doublet liant Cette formule n’explique pas toutes les propriétés de l’eau…
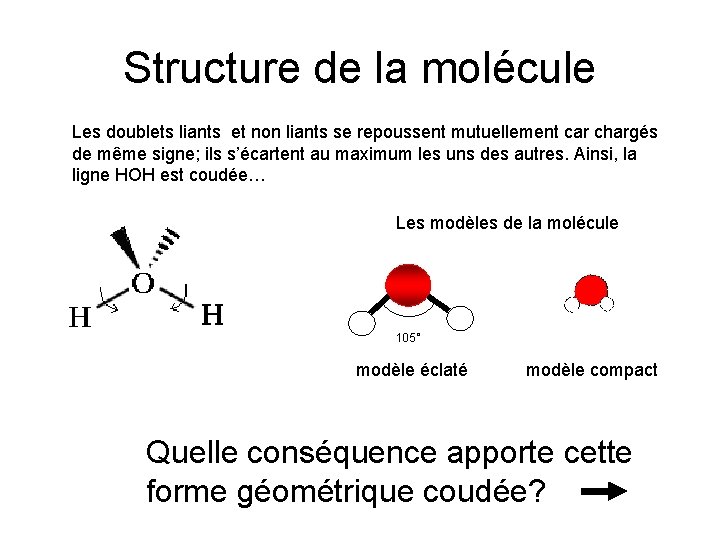
Structure de la molécule Les doublets liants et non liants se repoussent mutuellement car chargés de même signe; ils s’écartent au maximum les uns des autres. Ainsi, la ligne HOH est coudée… Les modèles de la molécule 105° modèle éclaté modèle compact Quelle conséquence apporte cette forme géométrique coudée?

Structure de la molécule Le doublet liant est statistiquement plus proche de l’oxygène que de l’hydrogène Les liaisons O-H sont donc polaires {symbolisation: O(-d)- H(+d) avec 0<d<e} (*) La forme coudée et la polarisation des liaisons H - O, entrainent une polarisation globale de la molécule (voir symbole ci-dessous) (*) on dit alors que O a une électronégativité plus forte que H La molécule d’eau se comporte comme un petit dipôle électrique

Les conséquences de cette structure: les propriétés de l’eau Dissolution et hydratation des composés ioniques Comment expliquer la solubilité dans l’eau du sulfate de cuivre anhydre et son changement de couleur?
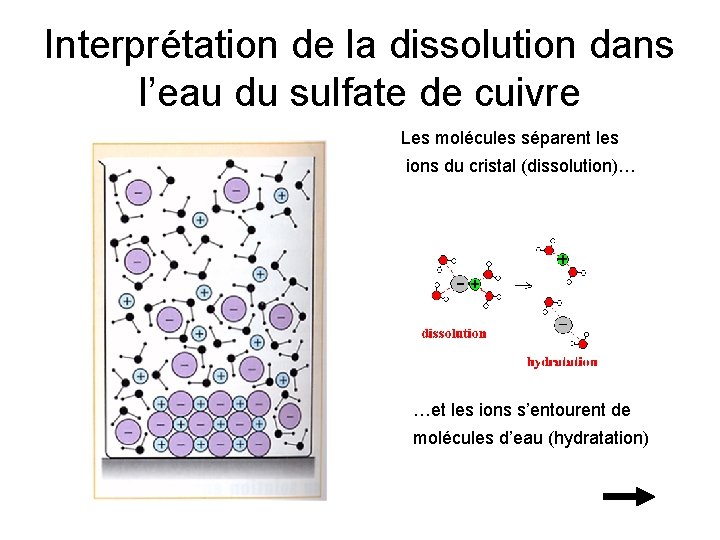
Interprétation de la dissolution dans l’eau du sulfate de cuivre Les molécules séparent les ions du cristal (dissolution)… …et les ions s’entourent de molécules d’eau (hydratation)
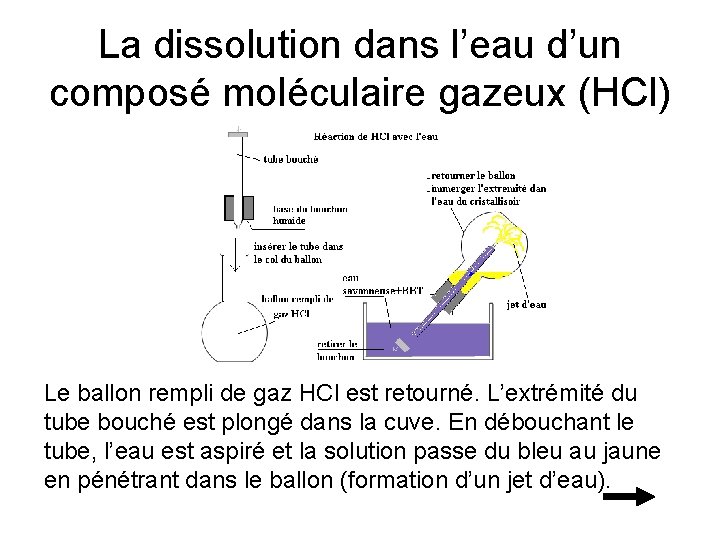
La dissolution dans l’eau d’un composé moléculaire gazeux (HCl) Le ballon rempli de gaz HCl est retourné. L’extrémité du tube bouché est plongé dans la cuve. En débouchant le tube, l’eau est aspiré et la solution passe du bleu au jaune en pénétrant dans le ballon (formation d’un jet d’eau).
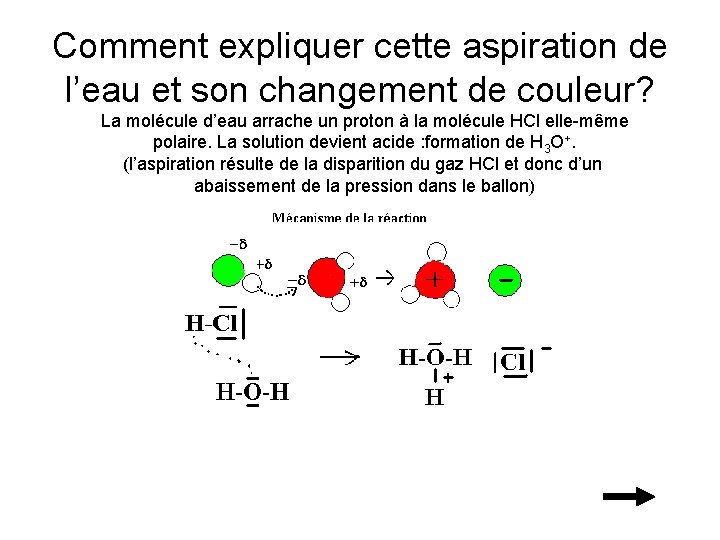
Comment expliquer cette aspiration de l’eau et son changement de couleur? La molécule d’eau arrache un proton à la molécule HCl elle-même polaire. La solution devient acide : formation de H 3 O+. (l’aspiration résulte de la disparition du gaz HCl et donc d’un abaissement de la pression dans le ballon)

Les propriétés de l’eau(suite) Pourquoi l’eau est-elle liquide et le dioxyde de carbone gazeux dans les conditions habituelles de température et pression?
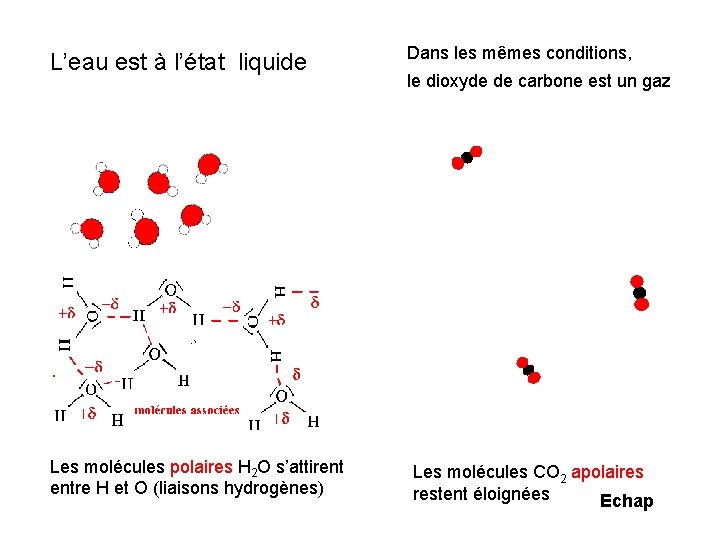
L’eau est à l’état liquide Les molécules polaires H 2 O s’attirent entre H et O (liaisons hydrogènes) Dans les mêmes conditions, le dioxyde de carbone est un gaz Les molécules CO 2 apolaires restent éloignées Echap
- Slides: 12