Qualification Validation Ralis par Equipe RD La mtrologie


















- Slides: 27

Qualification & Validation Réalisé par : Equipe R&D

ü La métrologie est la science des mesures et de ses applications. ü Etalonnage et vérification des systèmes et des instrumentation La Mésopotamie Poids, Distances et longueurs Bureau International des Poids et Mesures Sèvres en France 1875

Utilité La métrologie Qualité Réduction de cout Innovation Compétitivité Sécurité Protection de l’environnement Qualification ISO

Normalisation Une norme : des règles à appliquer pour garantir un niveau d’ordre optimal Les règles sont établis par un organisme de normalisation reconnu 14644 17025 21501 9001 8573 Organisme de Normalisation 14644: Salles propres et environnements maîtrisés apparentés 17025: exigences générales concernant la compétence des laboratoires d'étalonnages et d'essais 21501: Détermination de la distribution granulométrique 9001: système de management de la qualité 8573: Air comprimé

Salle Blanche Salle ZAC, salle propre où la concentration des particules dans l’air, la température, l’humidité et la pressionest bien maîtrisée pour des fabrications industriel ou recherche scientifique Centrale de traitement d‘air CTA

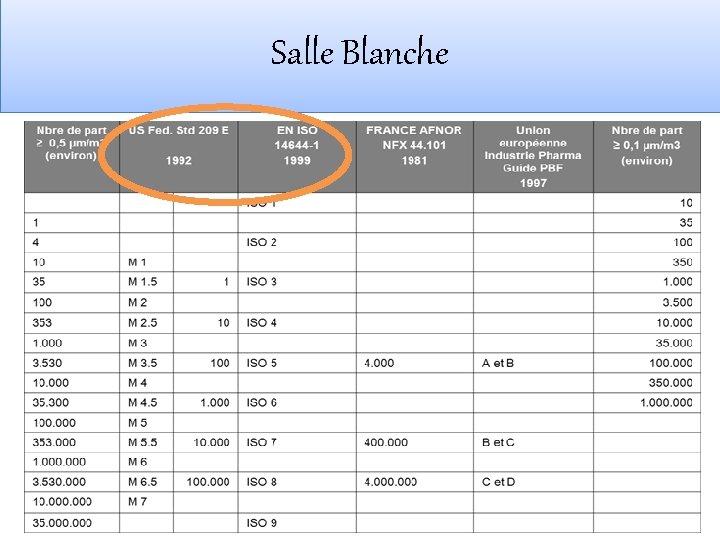
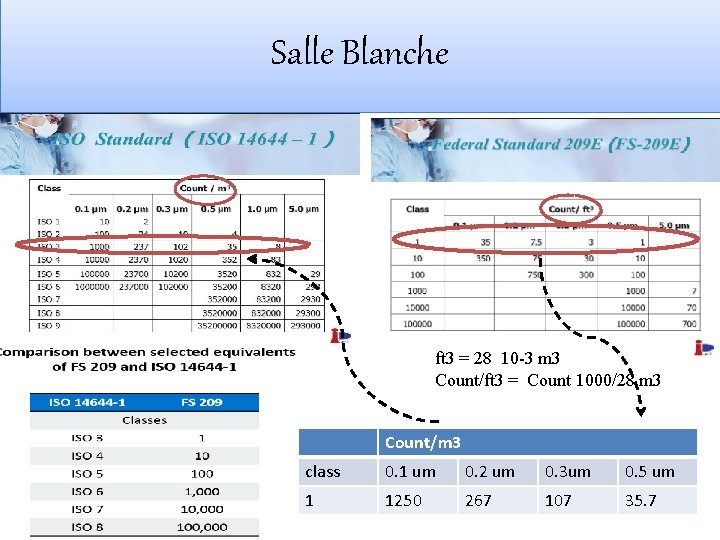
Salle Blanche ISO 14644 -1 Classification de la propreté particulaire de l'air Federal Standard Cleanroom and Work Station Requirements, Controlled Environments

Salle Blanche

Salle Blanche ft 3 = 28 10 -3 m 3 Count/ft 3 = Count 1000/28 m 3 Count/m 3 class 0. 1 um 0. 2 um 0. 3 um 0. 5 um 1 1250 267 107 35. 7

Validation La validation est une opération destinée à démontrer, documents à l'appui, qu'une procédure, un procédé ou une activité conduit effectivement aux résultats escomptés. Assurer convenablement : üLa qualité üLa Sécurité üEfficacité üRépondre aux spécifications définies üdiminuer les coûts üSurmonter les problèmes üRéduire les risques de production üRéduire les défaut üAlléger les contrôles

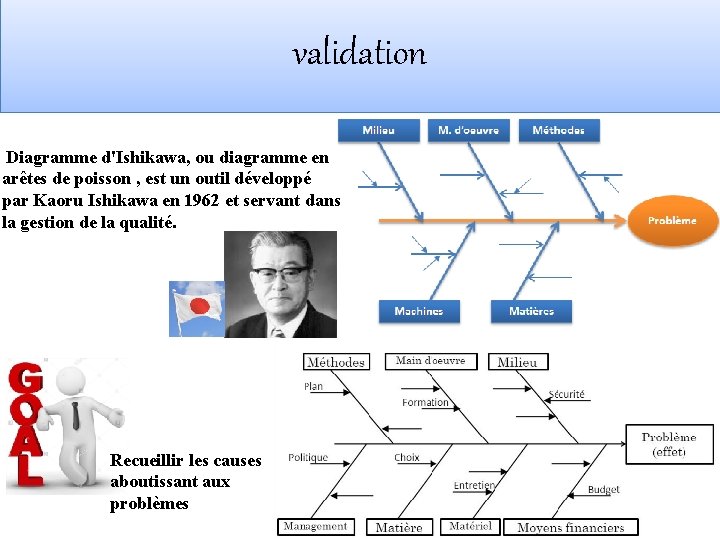
validation Diagramme d'Ishikawa, ou diagramme en arêtes de poisson , est un outil développé par Kaoru Ishikawa en 1962 et servant dans la gestion de la qualité. Recueillir les causes aboutissant aux problèmes

gmp La validation est définie par les BPF comme étant : « l’établissement de la preuve en conformité avec les principes de bonnes pratiques de fabrication, que la mise en œuvre ou l’application de tout processus, procédure, matériel, matière première, article de conditionnement ou produit, activité ou système permet réellement d’atteindre les résultats escomptés » BPF (GMP) est une notion d'assurance de la qualité: l'aptitude de la société ou de l'organisation à satisfaire le niveau de qualité désiré BPF est constitué de 9 chapitres généraux et de 20 Lignes Directrices particulières. GMP sont des normes de qualité pour garantir une production et un contrôle cohérent

gmp Les concepts de la validation sont décrits dans: üchapitre 5 : Production üla Ligne Directrice 15: Qualification et Validation Chapitre 5 : Production üLes études de validation doivent être menées conformément à des procédures définies üTout changement dans la formule de fabrication doit aboutir systématiquement à un produit de qualité requise, et toute modification dans le processus de fabrication doit être validé üDes validations critiques doivent être périodiquement réalisées sur les procédés et les procédures afin de confirmer la qualité du produit.

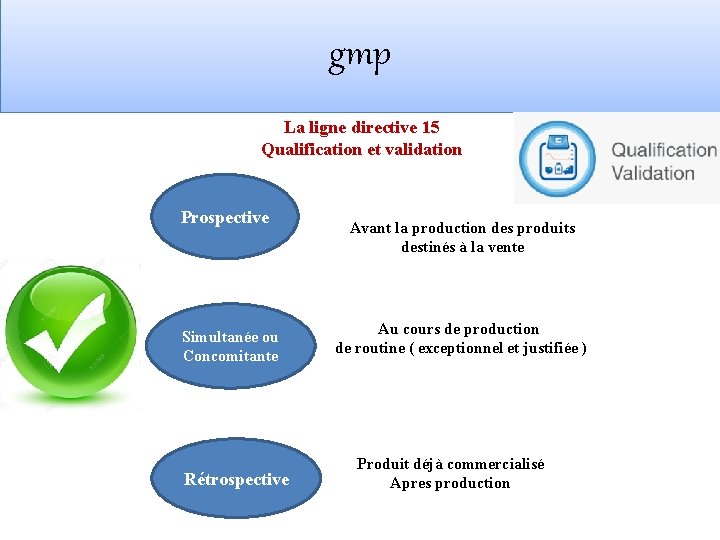
gmp La ligne directive 15 Qualification et validation Prospective Simultanée ou Concomitante Rétrospective Avant la production des produits destinés à la vente Au cours de production de routine ( exceptionnel et justifiée ) Produit déjà commercialisé Apres production

recommendation Les activités de qualification et de validation doivent être planifiées et prendre en considération le cycle de vie des installations, de l’équipement, et des produits. Les activités de qualification et de validation ne doivent être effectuées que par des personnes disposant d’une formation adéquate se conformant aux procédures approuvées. Des vérifications appropriées doivent être intégrées dans le travail de qualification et validation pour garantir l’intégrité de toutes les données obtenues

Plan Directeur de Validation (PDV) Le PDV ou document équivalent doit définir le système de qualification/validation et référencer des données au moins sur les éléments suivants : ü Politique de qualification et de validation ü Structure organisationnelle incluant des rôles et des responsabilités pour les activités de qualification et de validation ü Récapitulatif des installations, de l’équipement, des systèmes et des procédés sur site et statut de qualification et de validation ü Contrôle des changements et gestion des déviations pour le processus de qualification et de validation ü Recommandations sur le développement des critères d’acceptation ü Références à des documents existants ü Stratégie de qualification et validation

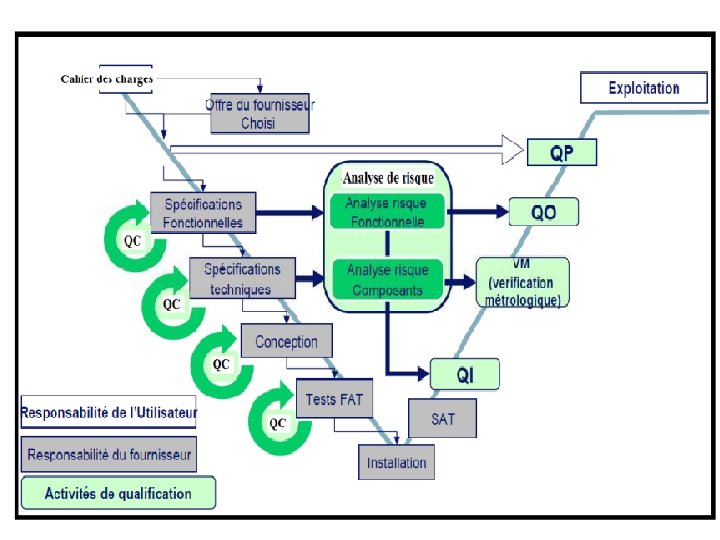
Qualification QC Concepteur ( fournisseur) QI Cahier de charge QP En activité ( réelle) QO Test a vide (Hors production)


Qualification On dit validé: ü Une démarche ü Un procédé ü Une méthode ü Une manière de faire. On dit qualifié ü Un équipement ü Une installation üUne ligne de production ü Un outil de production Les deux démarches sont complémentaires et visent à garantir que les opérations de production ne permettent pas de libérer un produit ne répondant pas aux critères de qualité

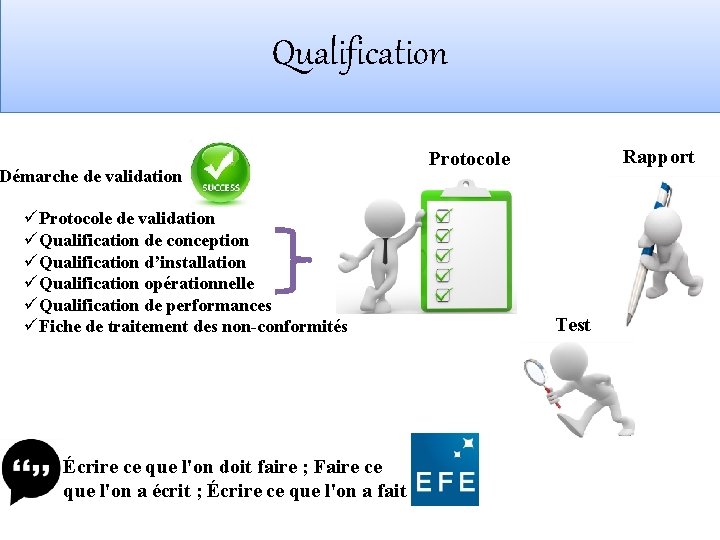
Qualification Démarche de validation üProtocole de validation üQualification de conception üQualification d’installation üQualification opérationnelle üQualification de performances üFiche de traitement des non-conformités Écrire ce que l'on doit faire ; Faire ce que l'on a écrit ; Écrire ce que l'on a fait Rapport Protocole Test

Qc Vérification documentée que la conception proposée des installations, systèmes et équipements convient aux usages auxquels ils sont destinés. NORME REGLEMENT -ATION BUDGET Qualification Conception PLANNING BESOINS

QI Vérification documentée que les installations, systèmes et équipements, tels qu’ils ont été installés ou modifiés, sont conformes à la conception approuvée et aux recommandations du fabricant Pratiquement: ü Le système est physiquement installé sur le lieu prévu de son utilisation üLes instruments de mesure et le matériel du système ont été vérifiés et sont conformes aux exigences spécifiées. üLe protocole de référence des documents de conformité aux normes en vigueur, les documents d’installation et de construction, ainsi que les documents d’exploitation sont présents

QI Documents fournis lors de la qualification d’installation Caractéristiques techniques et documentation : üDes éléments de production thermique, chauffage, production d’humidité üSchémas de fonctionnement. üDes systèmes de commandes et de puissance des installations, régulateurs de température et d’humidité, schémas électriques. ü Des capteurs de température, d’humidité, enregistreur de température et d’humidité. ü Principe de fonctionnement des enceintes climatiques, mode opératoire et procédure de mise en service. üListe des pièces détachées, procédure de maintenance des équipement

QO Vérification documentée que les installations, systèmes et équipements, tels qu’ils ont été installés ou modifiés, fonctionnent comme prévu sur toute la gamme d’exploitation Vérification des caractéristiques internes: pression, débit, étanchéité, intégrité des filtre Le protocole de qualification opérationnelle présente üles éléments à vérifier üla méthode retenue üles exigences (limite, tolérance) üles fréquences de requalification ütests de défaillance et maintenance curative avec indication des risques majeurs et mineurs üUne mise au point est effectuée par le fournisseur, en présence du personnel client üCette opération permet de déterminer et de valider les paramètres et les sécurités du process

QP Vérification documentée que les installations, systèmes et équipements, tels qu’ils ont été agencés, sont en mesure de fonctionner de manière efficace et reproductible, sur la base de la méthode opérationnelle approuvée et de la spécification du produit. Il s’agit d’établir ici la preuve documentée que l’appareil produit les résultats exigés de façon reproductible, à l’état chargé et dans les conditions de service

C/NC Traitement des non-conformités Fiche de non-conformité (Issue Sheet) Document précisant les détails observés permettant de relever la non-conformité Evaluation Correction Amélioration

C/NC SMART est une méthode de management par objectifs Objectifs SMART Traitement des non-conformités Il s’agit de répertorier les éléments du rapport qui ne sont pas conformes, d’évoquer la raison de la non conformité et de décrire les modifications envisagées. üDescription de la non conformité üDescription de la modification envisagée üRésultat obtenu üConformité après modification C / NC

MERCI