Puferi Koncentrovani rastvori jakih kiselina ili baza C

Puferi Koncentrovani rastvori jakih kiselina ili baza (C > 1· 10 -2 mol/dm 3) = „pseudo-puferi“ Ø Značajni samo u jako kiselim ili jako baznim rastvorima Rastvor slabe kiseline i njoj korespodentne baze, [k] ~ [b] Veliki značaj u AH Održavanje p. H = const pri izvođenju reakcija
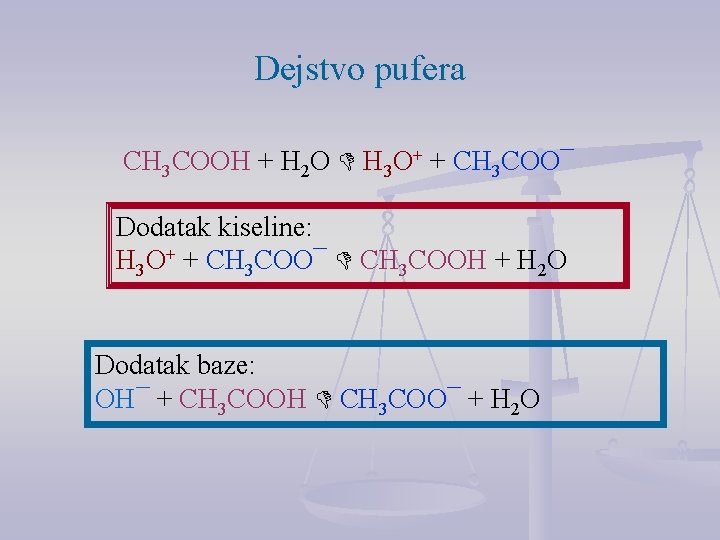
Dejstvo pufera CH 3 COOH + H 2 O H 3 O+ + CH 3 COO¯ Dodatak kiseline: H 3 O+ + CH 3 COO¯ CH 3 COOH + H 2 O Dodatak baze: OH¯ + CH 3 COOH CH 3 COO¯ + H 2 O
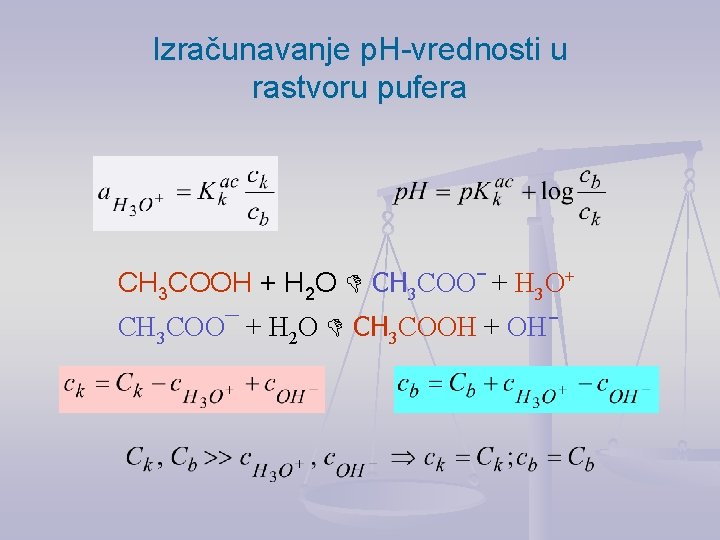
Izračunavanje p. H-vrednosti u rastvoru pufera CH 3 COOH + H 2 O CH 3 COOˉ + H 3 O+ CH 3 COO¯ + H 2 O CH 3 COOH + OHˉ

Primer 1. Izračunati p. H-vrednost rastvora koji sadrži mravlju kiselinu (p. Kka = 3, 75), C = 0, 1 mol/dm 3 i natrijum-formijat, C = 0, 1 mol/dm 3. Za koliko će se promeniti p. H-vrednost ako se u 100 cm 3 ovog rastvora doda 1 cm 3 rastvora Na. OH, C = 0, 1 mol/dm 3?



Puferski kapacitet CB = količina dodate jake baze Uvek β > 0: Dodatak baze: d. CB > 0 p. H dp. H > 0 Dodatak kiseline: d. CB < 0 p. H dp. H < 0
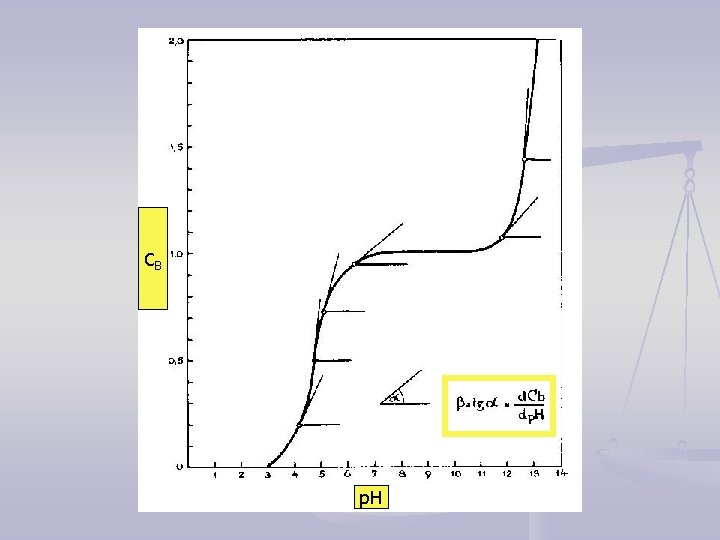
CB p. H
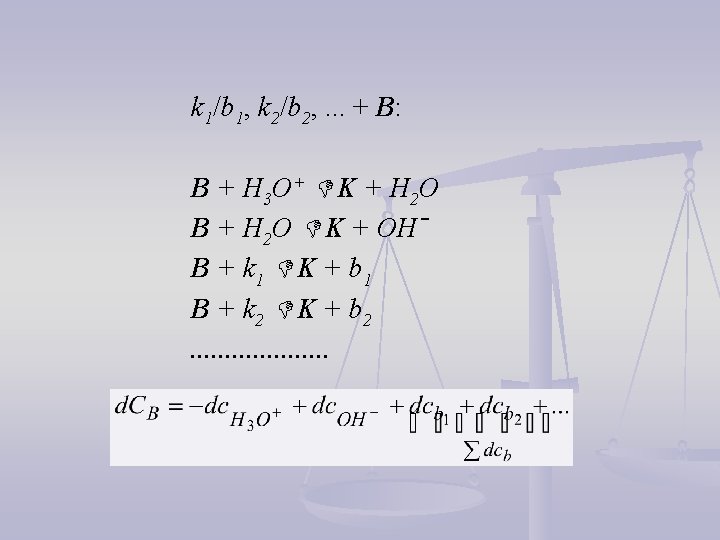
k 1/b 1, k 2/b 2, . . . + B: B + H 3 O+ K + H 2 O B + H 2 O K + OHˉ B + k 1 K + b 1 B + k 2 K + b 2. . . . .

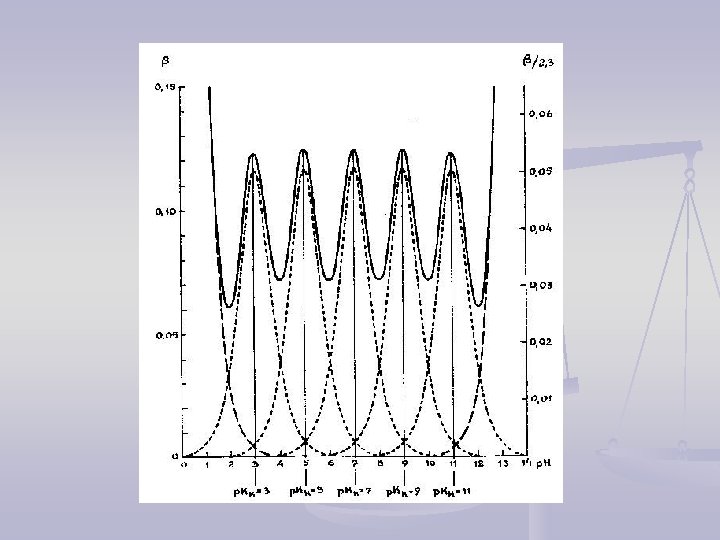
PUFERSKI KAPACITET JE ADITIVNA VELIČINA
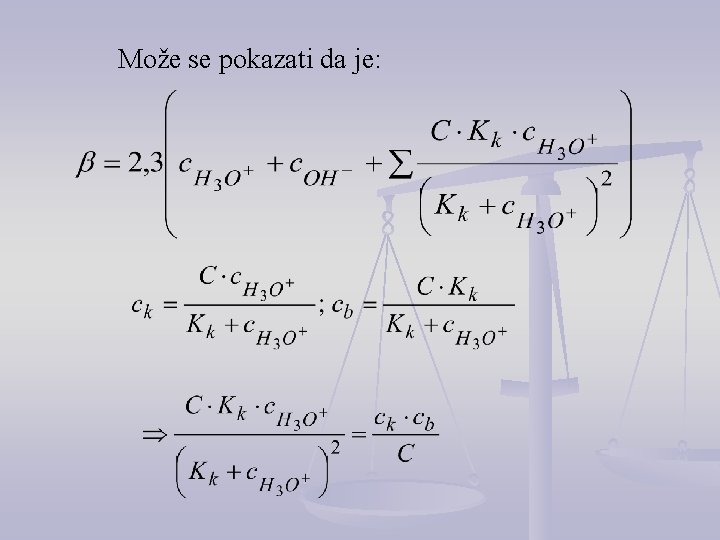
Može se pokazati da je:
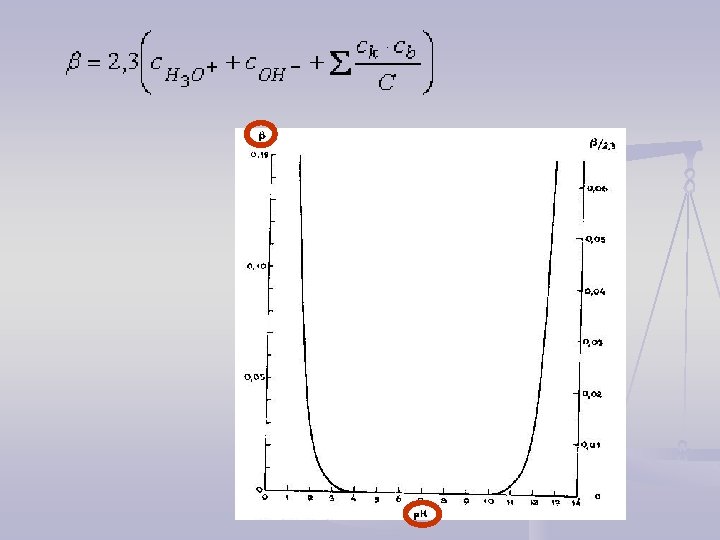


Pripremanje rastvora pufera Ø mešanjem odgovarajućih rastvora (promena koncentracije zbog promene zapremine!!!) Ø parcijalnom neutralizacijom: HA + Na. OH Na. A + H 2 O
- Slides: 15