PUESTA AL DA INMUNOTERAPIA EN MELANOMA Inmunoterapia en











- Slides: 29

PUESTA AL DÍA: INMUNOTERAPIA EN MELANOMA Inmunoterapia en la práctica clínica: melanoma avanzado Eva Muñoz Couselo, MD, Ph. D Hospital Vall d’Hebrón, Barcelona

Disclosures • Advisory board • Amgen, Bristol-Myers Squibb, Merck, Sharp & Dohme, Novartis, Pierre Fabre, Sanofi and Roche • Honoraria • Amgen, Bristol-Myers Squibb, Merck, Sharp & Dohme, Novartis, Pierre Fabre, and Roche • Clinical trial participation (principal investigator) • Amgen, Bristol-Myers Squibb, Glaxo. Smith. Kline, Merck, Sharp & Dohme, Novartis, Pierre Fabre, Regeneron and Roche

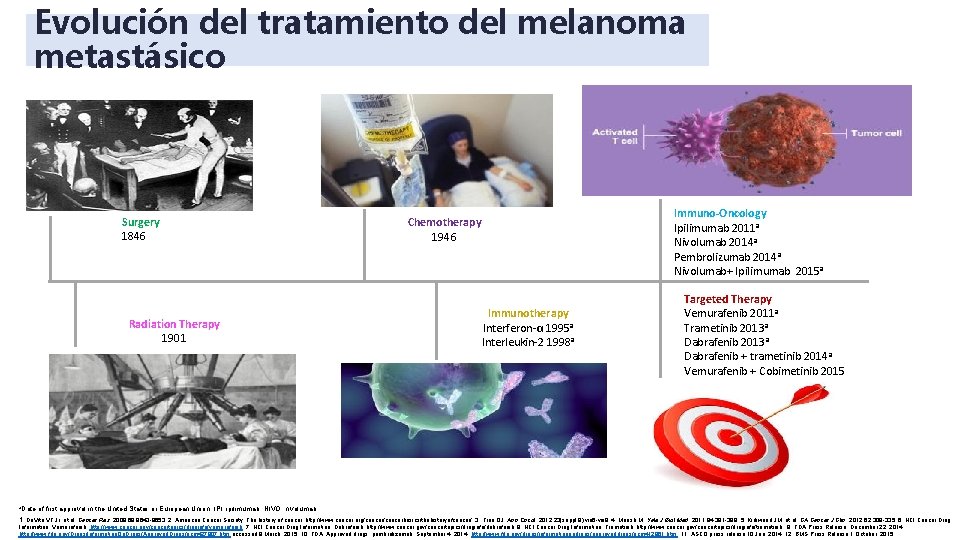
Evolución del tratamiento del melanoma metastásico Surgery 1846 Radiation Therapy 1901 Immuno-Oncology Ipilimumab 2011 a Nivolumab 2014 a Pembrolizumab 2014 a Nivolumab+ Ipilimumab 2015 a Chemotherapy 1946 Immunotherapy Interferon-α 1995 a Interleukin-2 1998 a Targeted Therapy Vemurafenib 2011 a Trametinib 2013 a Dabrafenib + trametinib 2014 a Vemurafenib + Cobimetinib 2015 a. Date of first approval in the United States or European Union. IPI, ipilimumab; NIVO, nivolumab. 1. De. Vita VT Jr, et al. Cancer Res. 2008; 68: 8643 -8653. 2. American Cancer Society. The history of cancer. http: //www. cancer. org/cancerbasics/thehistoryofcancer/. 3. Finn OJ. Ann Oncol. 2012; 23(suppl 8): viii 6 -viii 9. 4. Mansh M. Yale J Biol Med. 2011; 84: 381 -389. 5. Kirkwood JM, et al. CA Cancer J Clin. 2012; 62: 309 -335. 6. NCI Cancer Drug Information. Vemurafenib. http: //www. cancer. gov/cancertopics/druginfo/vemurafenib. 7. NCI Cancer Drug Information. Dabrafenib. http: //www. cancer. gov/cancertopics/druginfo/dabrafenib. 8. NCI Cancer Drug Information. Trametinib. http: //www. cancer. gov/cancertopics/druginfo/trametinib. 9. FDA Press Release. December 22, 2014 http: //www. fda. gov/Drugs/Information. On. Drugs/Approved. Drugs/ucm 427807. htm accessed 9 March, 2015. 10. FDA. Approved drugs: pembrolizumab. September 4, 2014. http: //www. fda. gov/drugs/informationondrugs/approveddrugs/ucm 412861. htm ; 11. ASCO press release 10 Jan, 2014. 12. BMS Press Release 1 October, 2015.

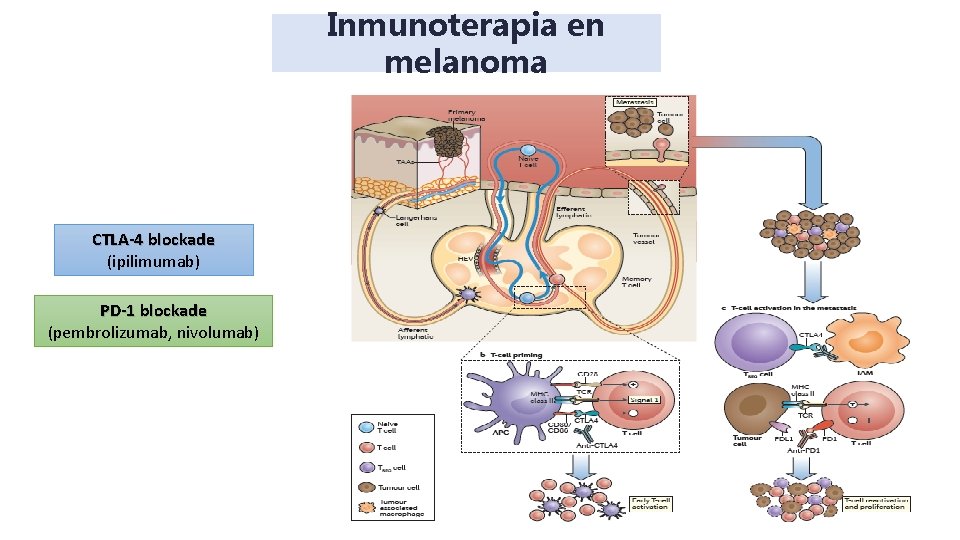
Inmunoterapia en melanoma CTLA-4 blockade (ipilimumab) PD-1 blockade (pembrolizumab, nivolumab) Ribas A. N Engl J Med. 2012; 366: 2517 -2519

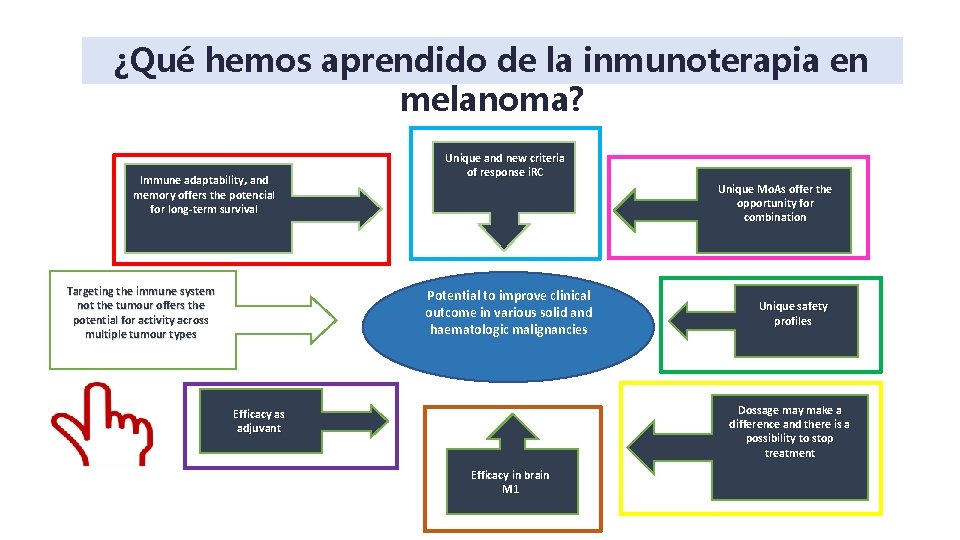
¿Qué hemos aprendido de la inmunoterapia en melanoma? Immune adaptability, and memory offers the potencial for long-term survival Targeting the immune system not the tumour offers the potential for activity across multiple tumour types Unique and new criteria of response i. RC Unique Mo. As offer the opportunity for combination Potential to improve clinical outcome in various solid and haematologic malignancies Unique safety profiles Dossage may make a difference and there is a possibility to stop treatment Efficacy as adjuvant Efficacy in brain M 1

Diferentes criterios de valoración de respuesta al tratamiento Criterios de la respuesta inmunológica (ic. RC) • Los pacientes pueden presentar enfermedad estable muy prolongada seguida de respuesta. • En algunos casos hay una respuesta inicial seguida de una muy lenta inducción de RC. • Otros casos presentan progresión inicial por aparición de nuevas lesiones seguido de una estabilización prolongada de la enfermedad o bien una respuesta -> PSEUDO-PROGRESIÓN: en melanoma se describe en torno a un 8 -10% de los casos (más con ipilimumab) ir. RC identifica hasta un 15% adicional de los pacientes que se benefician del tratamiento con inmunoterapia

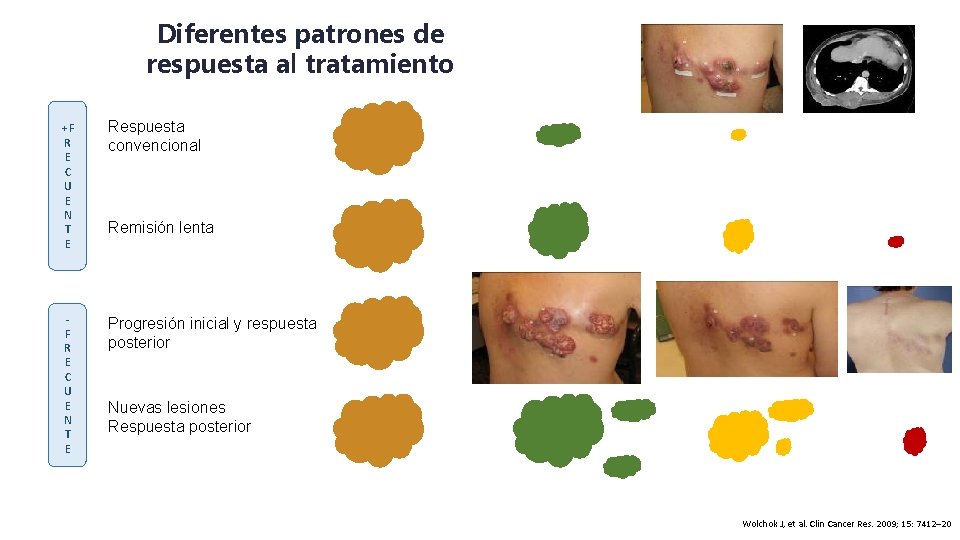
Diferentes patrones de respuesta al tratamiento +F R E C U E N T E Respuesta convencional Remisión lenta Progresión inicial y respuesta posterior Nuevas lesiones Respuesta posterior Wolchok J, et al. Clin Cancer Res. 2009; 15: 7412– 20

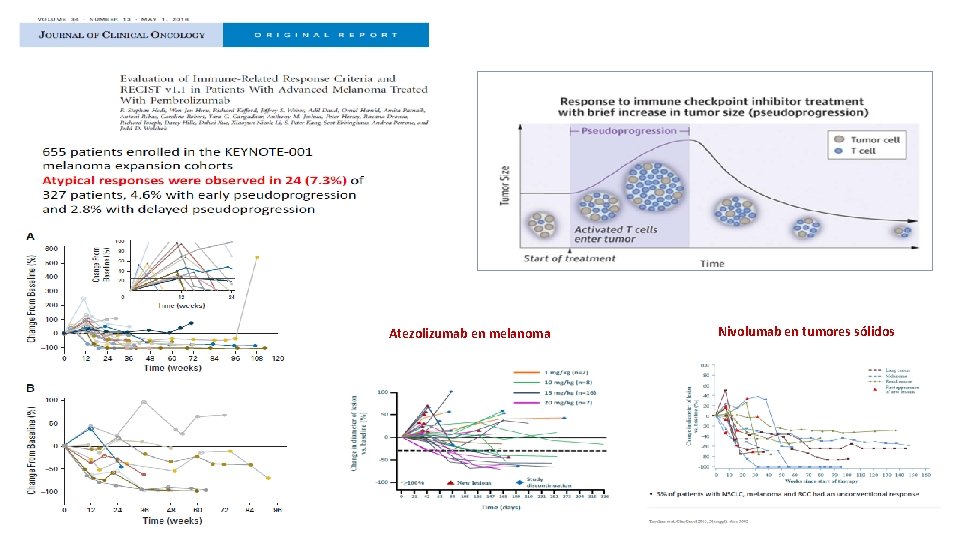
Atezolizumab en melanoma Nivolumab en tumores sólidos

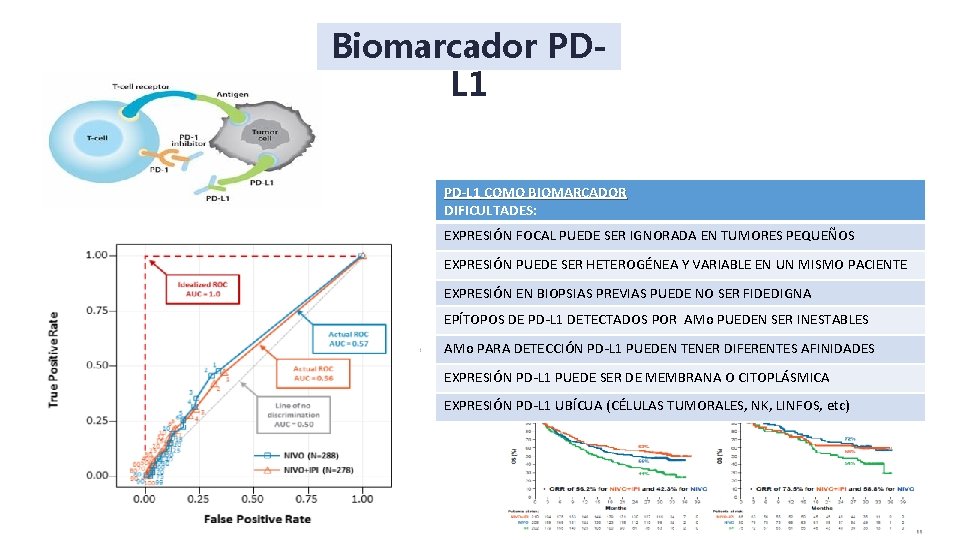
Biomarcador PDL 1 PD-L 1 COMO BIOMARCADOR DIFICULTADES: EXPRESIÓN FOCAL PUEDE SER IGNORADA EN TUMORES PEQUEÑOS EXPRESIÓN PUEDE SER HETEROGÉNEA Y VARIABLE EN UN MISMO PACIENTE EXPRESIÓN EN BIOPSIAS PREVIAS PUEDE NO SER FIDEDIGNA EPÍTOPOS DE PD-L 1 DETECTADOS POR AMo PUEDEN SER INESTABLES AMo PARA DETECCIÓN PD-L 1 PUEDEN TENER DIFERENTES AFINIDADES EXPRESIÓN PD-L 1 PUEDE SER DE MEMBRANA O CITOPLÁSMICA EXPRESIÓN PD-L 1 UBÍCUA (CÉLULAS TUMORALES, NK, LINFOS, etc)

Largos supervivientes al tratamiento 100 IPI (Pooled analysis)1 Overall Survival (%) 90 NIVO Monotherapy (Phase 1 CA 209 -003)2 80 70 60 5 -year OS rate of 34% in heavily pretreated patients with advanced melanoma 50 40 N=107 30 N=1, 861 20 10 0 0 1 2 3 4 5 6 7 Years 1. Schadendorf et al. J Clin Oncol 2015; 33: 1889 -1894; 2. presentation by Dr. Hodi et al at SMR 2016 International Congress 8 9 10

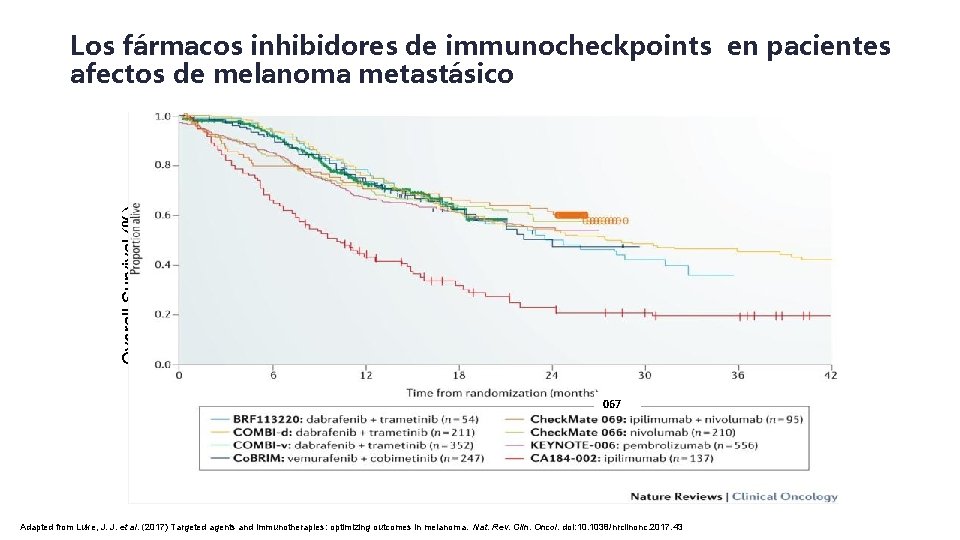
Los fármacos inhibidores de immunocheckpoints en pacientes afectos de melanoma metastásico 100 IPI (Pooled analysis)1 Overall Survival (%) 90 NIVO Monoterapia (Fase 1 CA 209 -003)2 80 PEMBRO Monoterapia (Fase 1 KEYNOTE 001)3 70 NIVO Monoterapia (Fase 3 Checkmate 066)4 60 N=210 PEMBRO Monoterapia (Fase 3 KEYNOTE 006)5 N=241 50 N= 152 40 N=107 30 N=1, 861 20 10 067 0 0 1 2 3 4 5 6 7 8 9 Years Adapted from Luke, J. J. et al. (2017) Targeted agents and immunotherapies: optimizing outcomes in melanoma. Nat. Rev. Clin. Oncol. doi: 10. 1038/nrclinonc. 2017. 43 10

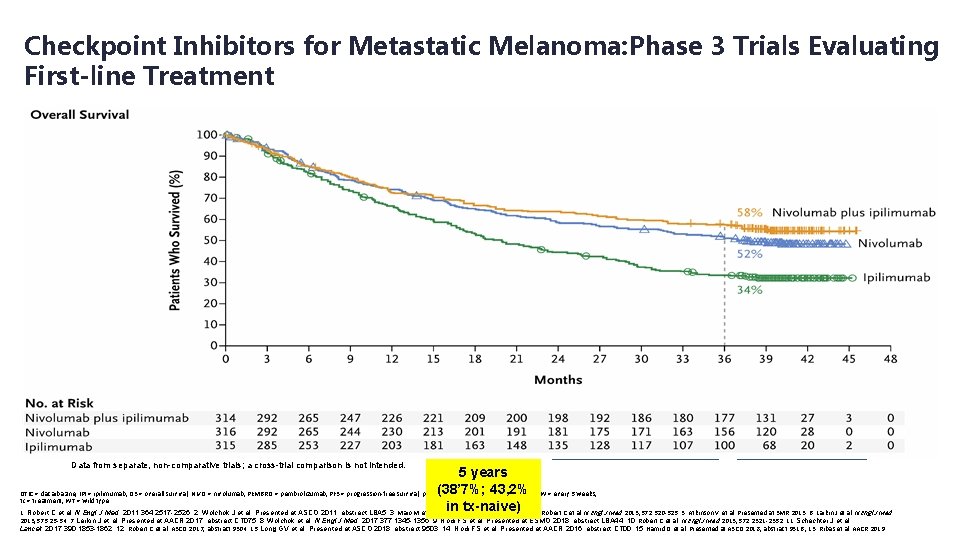
Checkpoint Inhibitors for Metastatic Melanoma: Phase 3 Trials Evaluating First-line Treatment NIVO IPI CA 184 -0241 (IPI 10 mg/kg + DTIC) Check. Mate 0664 (3 mg/kg, BRAF WT) Check. Mate 0676 (3 mg/kg) 2. 82 5. 14 47%1 5 years (18%)3 PEMBRO NIVO+IPI KEYNOTE 00610 (10 mg/kg) Check. Mate 0676 (IPI 3 mg/kg + NIVO 1 mg/kg) Not approved dose Q 2 W Q 3 W 6. 96 5. 611 4. 111 11. 56 73%4 74%7 74%10 68%10 73%7 2 years (58%)5 2 years (59%)7 2 years (55%)11 2 years (64%)7 Phase 1 (NIVO) Check. Mate 003 5 -year OS 35% (3 mg/kg)14 3 years (52%)8 33 months (50%)12 3 years (58%)8 Phase 1 (PEMBRO) KEYNOTE 001 5 -year OS 34% in all pts (41% in tx-naive pts)15 4 years (46%)9 4 years (42%; 44% in tx-naive)13 4 years (53%)9 Median PFS (months) 1 -year OS Long-term survival Data from separate, non-comparative trials; a cross-trial comparison is not intended. 5 years 43, 2% DTIC = dacarbazine; IPI = ipilimumab; OS = overall survival; NIVO = nivolumab; PEMBRO = pembrolizumab; PFS = progression-free survival; pts = (38’ 7%; patients; Q 2 W = every 2 weeks; Q 3 W = every 3 weeks; tx = treatment; WT = wild type. in tx-naive) 1. Robert C et al. N Engl J Med. 2011; 364: 2517 -2526. 2. Wolchok J et al. Presented at ASCO 2011; abstract LBA 5. 3. Maio M et al. J Clin Oncol. 2015; 33: 1191 -1196. 4. Robert C et al. N Engl J Med. 2015; 372: 320 -323. 5. Atkinson V et al. Presented at SMR 2015. 6. Larkin J et al. N Engl J Med. 2015; 373: 23 -34. 7. Larkin J et al. Presented at AACR 2017; abstract CT 075. 8. Wolchok et al. N Engl J Med. 2017; 377: 1345 -1356. 9. Hodi FS et al. Presented at ESMO 2018; abstract LBA 44. 10. Robert C et al. N Engl J Med. 2015; 372: 2521 -2532. 11. Schachter J et al. Lancet. 2017; 390: 1853 -1862. 12. Robert C et al. ASCO 2017; abstract 9504. 13. Long GV et al. Presented at ASCO 2018; abstract 9503. 14. Hodi FS et al. Presented at AACR 2016; abstract CT 00. 15. Hamid O et al. Presented at ASCO 2018; abstract 9516. , 15. Ribas et al. AACR 2019

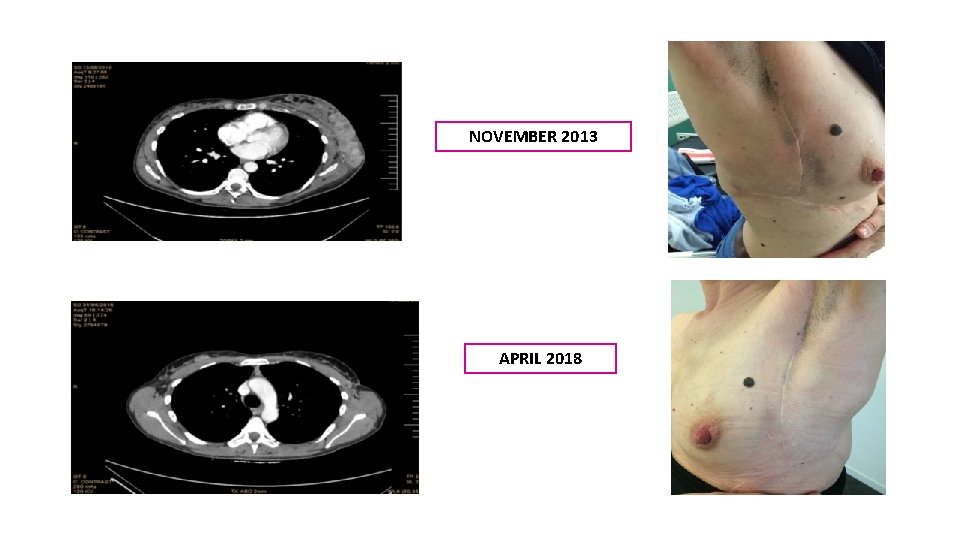
NOVEMBER 2013 APRIL 2018

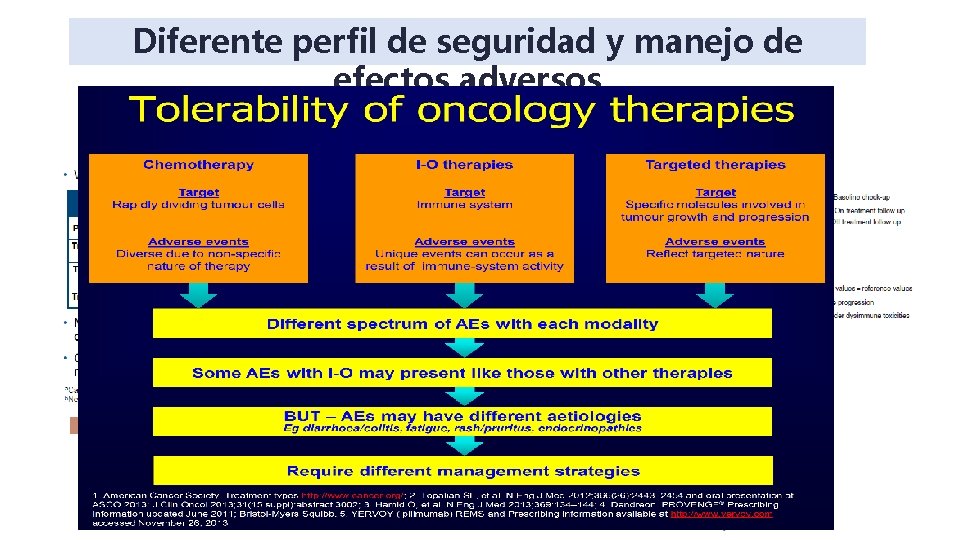
Diferente perfil de seguridad y manejo de efectos adversos Champiat et al. Ann. Oncol. 2016

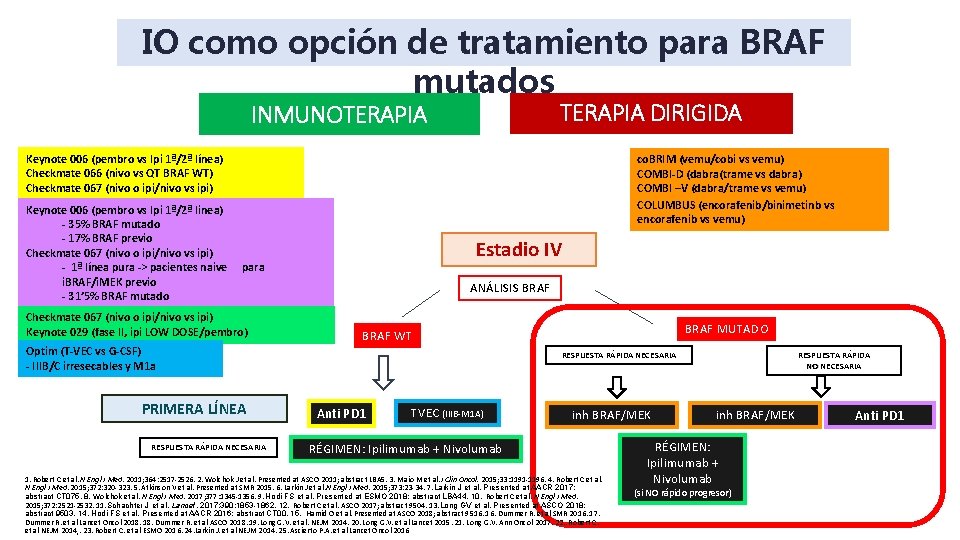
IO como opción de tratamiento para BRAF mutados TERAPIA DIRIGIDA INMUNOTERAPIA Keynote 006 (pembro vs Ipi 1ª/2ª línea) Checkmate 066 (nivo vs QT BRAF WT) Checkmate 067 (nivo o ipi/nivo vs ipi) Keynote 006 (pembro vs Ipi 1ª/2ª linea) - 35% BRAF mutado - 17% BRAF previo Checkmate 067 (nivo o ipi/nivo vs ipi) - 1ª línea pura -> pacientes naive i. BRAF/i. MEK previo - 31’ 5% BRAF mutado co. BRIM (vemu/cobi vs vemu) COMBI-D (dabra(trame vs dabra) COMBI –V (dabra/trame vs vemu) COLUMBUS (encorafenib/binimetinb vs encorafenib vs vemu) Estadio IV para Checkmate 067 (nivo o ipi/nivo vs ipi) Keynote 029 (fase II, ipi LOW DOSE/pembro) ANÁLISIS BRAF Optim (T-VEC vs G-CSF) - IIIB/C irresecables y M 1 a PRIMERA LÍNEA RESPUESTA RÁPIDA NECESARIA BRAF MUTADO BRAF WT RESPUESTA RÁPIDA NECESARIA Anti PD 1 TVEC (IIIB-M 1 A) inh BRAF/MEK RÉGIMEN: Ipilimumab + Nivolumab 1. Robert C et al. N Engl J Med. 2011; 364: 2517 -2526. 2. Wolchok J et al. Presented at ASCO 2011; abstract LBA 5. 3. Maio M et al. J Clin Oncol. 2015; 33: 1191 -1196. 4. Robert C et al. N Engl J Med. 2015; 372: 320 -323. 5. Atkinson V et al. Presented at SMR 2015. 6. Larkin J et al. N Engl J Med. 2015; 373: 23 -34. 7. Larkin J et al. Presented at AACR 2017; abstract CT 075. 8. Wolchok et al. N Engl J Med. 2017; 377: 1345 -1356. 9. Hodi FS et al. Presented at ESMO 2018; abstract LBA 44. 10. Robert C et al. N Engl J Med. 2015; 372: 2521 -2532. 11. Schachter J et al. Lancet. 2017; 390: 1853 -1862. 12. Robert C et al. ASCO 2017; abstract 9504. 13. Long GV et al. Presented at ASCO 2018; abstract 9503. 14. Hodi FS et al. Presented at AACR 2016; abstract CT 00. 15. Hamid O et al. Presented at ASCO 2018; abstract 9516. Dummer R. et al SMR 2016. 17. Dummer R. et al Lancet Oncol 2018. Dummer R. et al ASCO 2018. 19. Long G. V. et al. NEJM 2014. 20. Long G. V. et al Lancet 2015. 21. Long G. V. Ann Oncol 2017. 22. . Robert C. et al NEJM 2014, . 23. Robert C. et al ESMO 2016. 24. Larkin J. et al NEJM 2014. 25. Ascierto P. A. et al Lancet Oncol 2016 RESPUESTA RÁPIDA NO NECESARIA inh BRAF/MEK RÉGIMEN: Ipilimumab + Nivolumab (si NO rápido progresor) Anti PD 1

Oportunidad de múltiples combinaciones Checkpoint inhibition: inhibition Balance between inhibitory and stimulatory receptors dictates T cell priming Checkmate 067, Checkmate 511 IDO 1 Epcadostat + pembrolizumab Relatlimab + nivolumab Mellman I, et al. Nature 2011

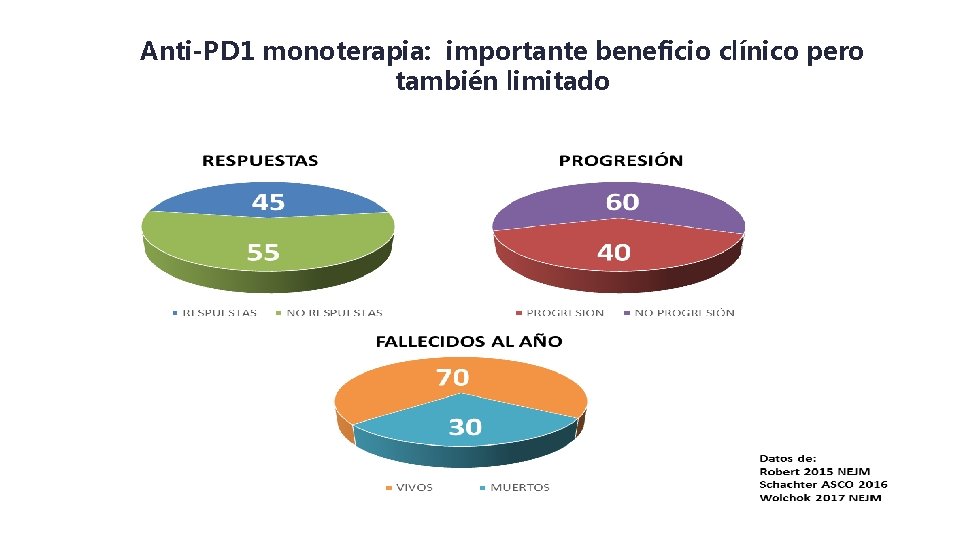
Anti-PD 1 monoterapia: importante beneficio clínico pero también limitado

Anti-PD 1 + Anti-CTLA 4 Anti PD 1 + Anti. CTLA-4

Rapid clinically significant responses usually with limited durability Less frequent objective responses but clinically significant durability Fast and frequent and durable responses with both

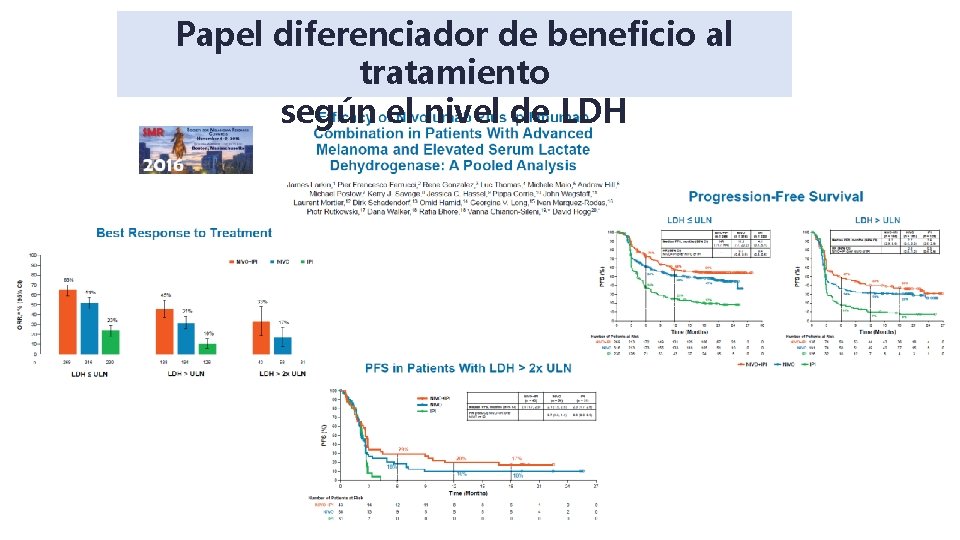
Papel diferenciador de beneficio al tratamiento según el nivel de LDH

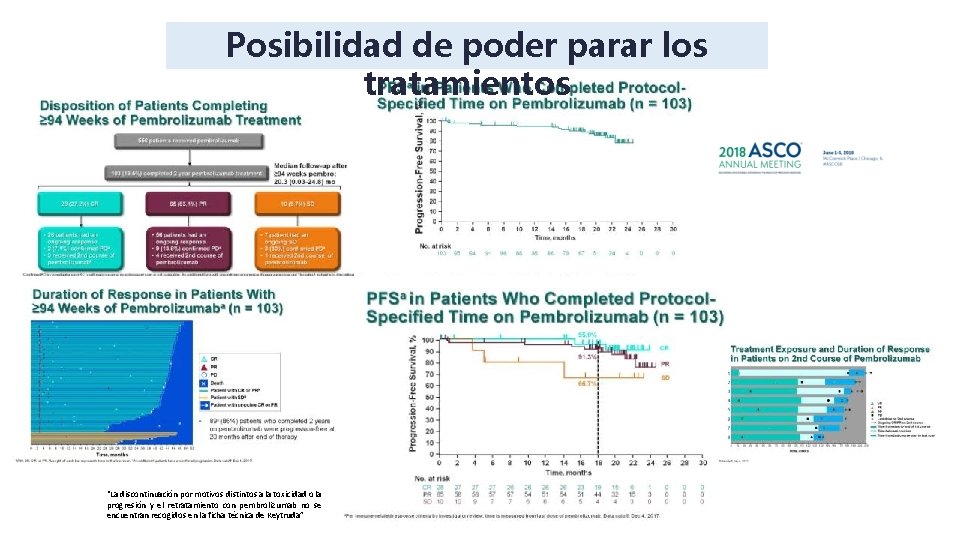
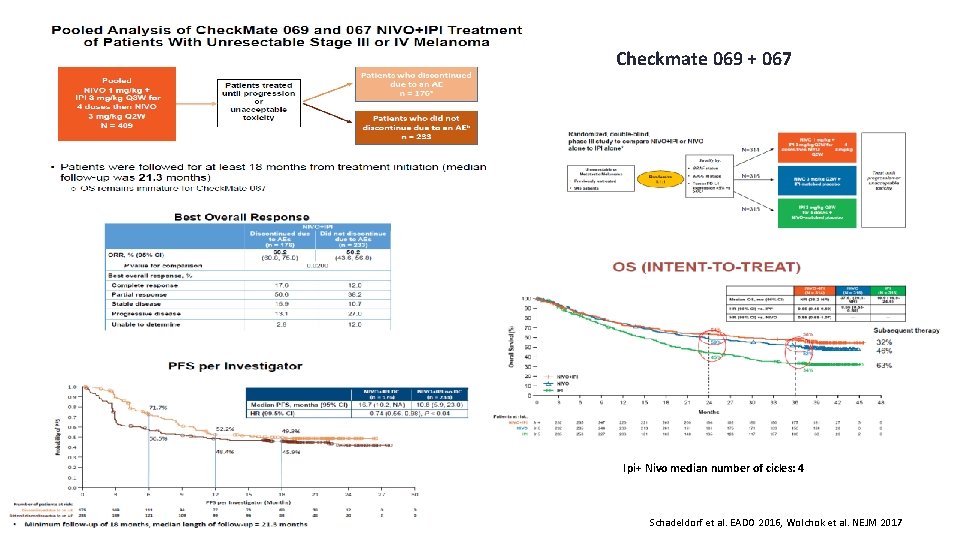
Posibilidad de poder parar los tratamientos EADO 2016 “La discontinuación por motivos distintos a la toxicidad o la progresión y el retratamiento con pembrolizumab no se encuentran recogidos en la ficha técnica de Keytruda”

Checkmate 069 + 067 Ipi+ Nivo median number of cicles: 4 Schadeldorf et al. EADO 2016, Wolchok et al. NEJM 2017

Treatment beyond progression

Posibilidad de secuenciar tratamientos Ipilimumab 2ª línea: 9 meses de mediana de SG adicional en pacientes pre tratados con anti-PD 1 Check. Mate 066: 57 pacientes pretratados con Nivolumab recibieron Ipilimumab en 2ª línea 1. Hodi et al. N Engl J Med. 2010; 363: 711 -23. 2. Atkinson et al. Presentado en el Society Melanoma Research 2015, San Francisco, EE. UU. 3. Schadendorf et al. J Clin Oncol. 2015; 33: 1889 -94. 4. Bowyer et al. Br J Cancer. 2016; 114: 1084 -9.

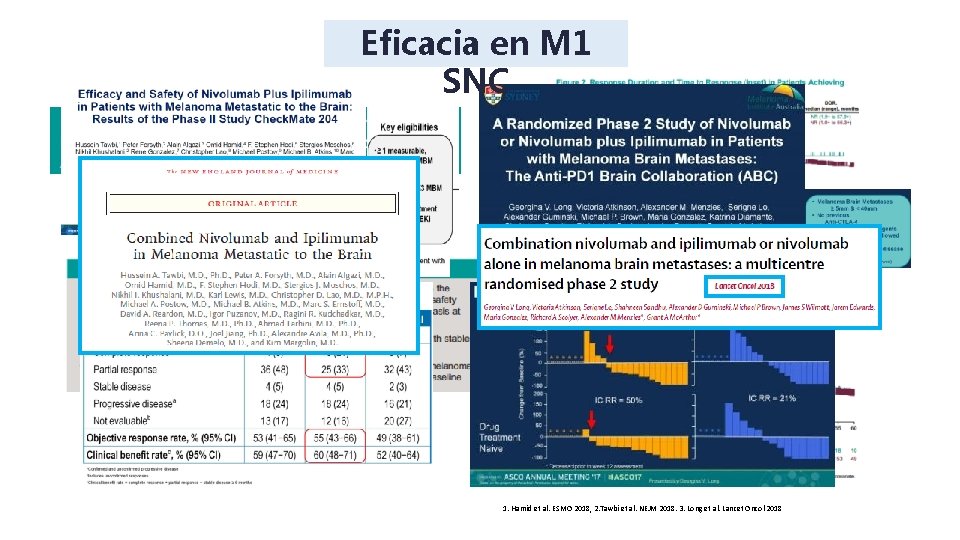
Eficacia en M 1 SNC 1. Hamid et al. ESMO 2018, 2. Tawbi et al. NEJM 2018. 3. Long et al. Lancet Oncol 2018

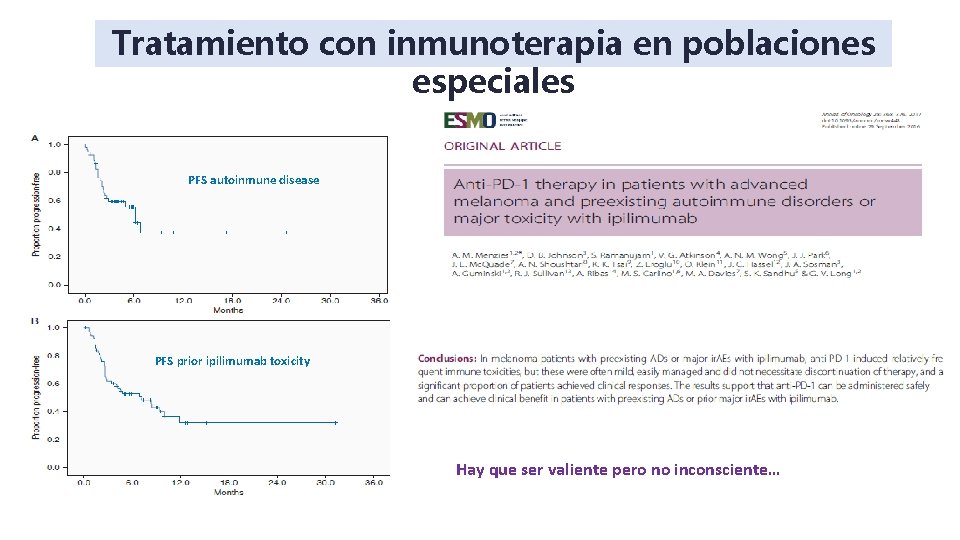
Tratamiento con inmunoterapia en poblaciones especiales PFS autoinmune disease PFS prior ipilimumab toxicity Hay que ser valiente pero no inconsciente…

CONCLUSIONES Previo a 2011: - Mantener la calidad de vida de los pacientes Paliar los síntomas Minimizar los efectos adversos relacionados con el tratamiento Avances en MELANOMA • Ipilimumab 2011 • Nivolumab 2014 • Pembrolizumab 2014 • Nivolumab+ Ipilimumab 2015 • Vemurafenib 2011 • Trametinib 2013 • Dabrafenib + trametinib 2014 • Vemurafenib + Cobimetinib 2015 • Adjuvant Nivolumab, Pembrolizumab and Dabrafenib/Trametinib 2018/2019 En 2019: - Aumentar la SUPERVIVENCIA de los pacientes - Selección de pacientes: M 1 SNC, mucosas/ocular, estatus BRAF, carga tumoral, ECOG, nivel LDH, … - Optimizar las diferentes opciones de tratamiento: combinaciones, secuencias, biomarcadores, … - Incorporación del tratamiento adyuvante como estándar de tratamiento (pacientes alto riesgo) - Neoadyuvancia - Posibilidad de flat dose, de poder parar los tratamientos y de treatment beyond progression - Mantener la calidad de vida de los pacientes - Paliar los síntomas - Minimizar los efectos adversos relacionados con el tratamiento

emunoz@vhio. net