Przed matur Przygotowaa Beata Szuliska II LO Bytom

Przed maturą… Przygotowała: Beata Szulińska – II LO Bytom
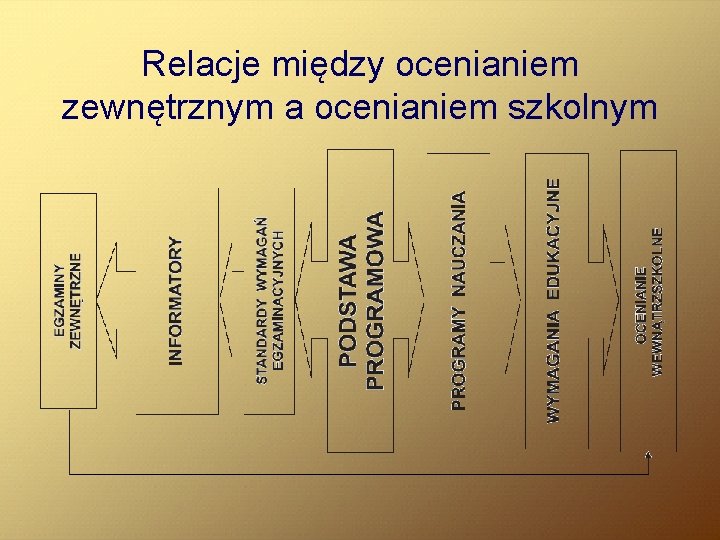
Relacje między ocenianiem zewnętrznym a ocenianiem szkolnym

Główne obszary obejmujące standardy wymagań edukacyjnych: v Wiadomości i rozumienie v Korzystanie z informacji v Tworzenie informacji

Typy zadań maturalnych: u u u u Zadania Zadania krótkiej odpowiedzi z luką wielokrotnego wyboru szacunkowe prawda/fałsz na dobieranie obliczeniowe „doświadczalne”

… wymagają odpowiedzi zwięzłej, w postaci jednego lub dwóch zdań, symboli i wzorów chemicznych, równań reakcji, obliczeń matematycznych. Często poprzedzone informacją, z której uczeń powinien skorzystać rozwiązując problem. Czasowniki operacyjne: • zapisz (równanie reakcji, wzór, nazwę) • uzupełnij tabelę • uzasadnij • podaj • określ PRZYKŁAD

Zadanie 1. (4 pkt) W wyniku dysocjacji elektrolitycznej stwierdzono obecność w roztworze następujących jonów: Al(NO 3)3 a) Al 3+ i NO − ……………… 3 b) Fe 3+ i SO 42 - Fe 2(SO 4)3 ……………… c) NH 4+, H+ i CO 32 - NH 4 HCO 3 ……………… (Ca. OH)3 PO 4 ……………… d) Ca 2+, OH− i PO 43 - Podaj wzory sumaryczne soli, które uległy dysocjacji, zakładając, że jony obecne w roztworze pochodzą tylko procesu dysocjacji. brgbr

… uczeń wpisuje we wskazanym miejscu słowa, liczby, wzory lub symbole. Polegają na uzupełnieniu tekstu, pojedynczych zdań, równań reakcji itp. Czasowniki operacyjne: • wpisz • uzupełnij PRZYKŁAD

Zadanie 1. (7 pkt) Uzupełnij podane zdania wpisując odpowiednio słowa: najmniejsza i największa (w odpowiedniej formie gramatycznej). największą Atom fransu odznacza się ……………… wartością promienia największą atomowego w okresie oraz ……………… wartością promienia największą atomowego i ……………… wartością promienia jonowego w grupie. najmniejszą wartością elektroujemności w okresie Frans cechuje się ……………… najmniejszą wartością elektroujemności w grupie. Frans ma i ……………… najmniejszą wartość energii jonizacji w okresie i ……………… najmniejszą ……………… wartość energii jonizacji w grupie. brgbr

… uczeń wskazuje jedną lub kilka ze zbioru podanych odpowiedzi. Czasowniki operacyjne: • wskaż • podkreśl • wypisz • zaznacz PRZYKŁAD

Zadanie 1. (5 pkt) Dany jest zbiór jonów: Sr 2+, Te 2 -, Cs+, I 7+, Sn 4+, Rb+, Sb 3 -, I‾, Ba 2+. Podkreśl symbole jonów, które mają konfigurację elektronową ksenonu. brgbr

… uczeń zaznacza, czy podana informacja jest prawdziwa, czy fałszywa. Czasowniki operacyjne: • wskaż zdanie prawdziwe • oceń poprawność informacji wpisując TAK/NIE lub PRAWDA/FAŁSZ PRZYKŁAD

Zadanie 1. (5 pkt) Dane są trzy orbitale jednej powłoki: Oceń prawdziwość poniższych twierdzeń wpisując właściwą odpowiedź: TAK – jeśli zdanie jest prawdziwe, NIE – jeśli jest fałszywe. Orbitale A i B różnią się wartością magnetycznej liczby kwantowej. TAK …… Orbitale A i B różnią się wartością głównej liczby kwantowej. NIE …… Orbitale A i B cechuje identyczna energia i różna orientacja przestrzenna. TAK …… Orbitale B i C cechuje identyczna wartość pobocznej liczby kwantowej. NIE …… Orbital C oznacza się symbolem literowym p. brgbr …… NIE

… wymagają połączenia podanych informacji w pary, grupowania, lub porządkowania ich według określonego kryterium. Sprawdzają one umiejętność kojarzenia pojęć, praw faktów, zjawisk, właściwości związków itp. Czasowniki operacyjne: • przyporządkuj • połącz • dobierz • uszereguj PRZYKŁAD 1 PRZYKŁAD 2

Zadanie 1. (6 pkt) Substancjom chemicznym podanym w kolumnie pierwszej przyporządkuj informacje dotyczące przewodnictwa prądu elektrycznego podane w kolumnie drugiej. W niektórych przypadkach należy przyporządkować więcej niż jedną informację. 1. rtęć a) przewodnik w warunkach normalnych 2. wodorotlenek sodu b) izolator w warunkach normalnych 3. siarka c) przewodnik po stopieniu 4. sacharoza d) przewodnik w roztworze wodnym a b, c, d b b 1. ………………. . . 2. ………………… 3. ………………… 4. ………………… brgbr

Zadanie 1. (4 pkt) W tabeli przedstawiono stałe dysocjacji K amoniaku i kilku związków organicznych będących zasadami. Uszereguj podane zasady według rosnącej mocy. zasada K amoniak 1, 8∙ 10 -5 anilina 3, 8∙ 10 -10 etyloamina 5, 6∙ 10 -4 pirydyna 1, 7∙ 10 -9 anilina, pirydyna, amoniak, etyloamina …………………………………… brgbr

… uczeń prezentuje swój tok rozumowania podczas rozwiązywania problemu, dokonuje obliczeń – operacji na danych i jednostkach. Wynik powinien zostać podany w postaci odpowiedzi słownej. Czasowniki operacyjne: • oblicz PRZYKŁAD

Zadanie 1. (3 pkt) Reakcja przebiega według równania: 2 Al 2 O 3 + 3 H 2 2 Al + 3 H 2 O Oblicz, ile gramów glinu powstało w reakcji, jeżeli równocześnie otrzymano 0, 6 mola wody. Obliczenia: Dane: n H O = 0, 6 mola 2 MAl = 27 g/mol Szukane: m. Al = ? m. Al 2 mol· 27 g/mol = n. H O 3 mol 2 m. Al = 18 g 0, 6 mol 1 mol m. Al = 10, 8 g. Odp. : W reakcji powstało 10, 8 grama glinu. brgbr

… uczeń planuje eksperymenty chemiczne lub uzupełnia ich opis. Uczeń powinien wykazać się znajomością różnicy pomiędzy obserwacją i wnioskiem. Czasowniki operacyjne: • uzupełnij opis doświadczenia, podaj obserwacje i/lub wnioski. • zaprojektuj doświadczenie PRZYKŁAD
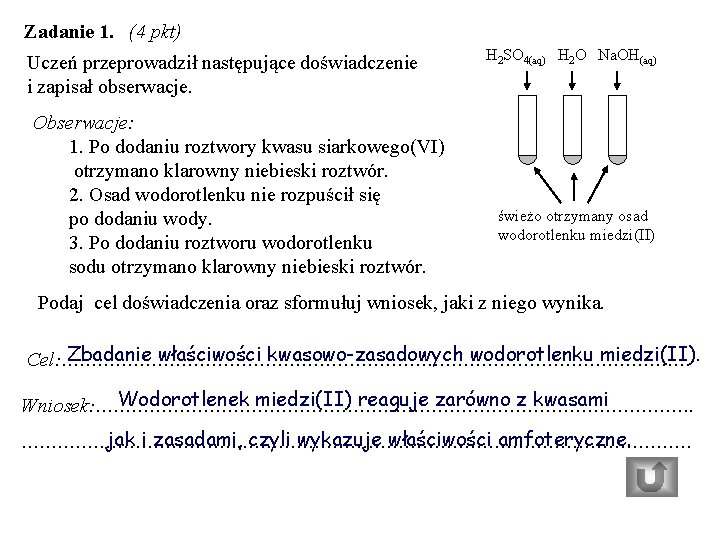
Zadanie 1. (4 pkt) Uczeń przeprowadził następujące doświadczenie i zapisał obserwacje. Obserwacje: 1. Po dodaniu roztwory kwasu siarkowego(VI) otrzymano klarowny niebieski roztwór. 2. Osad wodorotlenku nie rozpuścił się po dodaniu wody. 3. Po dodaniu roztworu wodorotlenku sodu otrzymano klarowny niebieski roztwór. H 2 SO 4(aq) H 2 O Na. OH(aq) świeżo otrzymany osad wodorotlenku miedzi(II) Podaj cel doświadczenia oraz sformułuj wniosek, jaki z niego wynika. Zbadanie właściwości kwasowo-zasadowych wodorotlenku miedzi(II). Cel: ……………………………………………… Wodorotlenek miedzi(II) reaguje zarówno z kwasami Wniosek: ……………………………………………. jak i zasadami, czyli wykazuje właściwości amfoteryczne. ………………………………………………… brgbr

Nabycie umiejętności rozwiązywania różnego typu zadań wymaga wielu ćwiczeń. Uczniowie powinni umiejętności przez edukacji chemicznej. zdobywać cały te okres

Problemy i najczęściej popełniane błędy…

Uczeń nie podejmuje próby rozwiązania zadania, z góry uważając je za trudne. PRZYKŁAD

Atom – budowa i przemiany Informacja do zadania 1, 2 i 3: Procesowi przejścia elektronu ze stanu o wyższej energii E 2 do stanu o niższej energii E 1 towarzyszy emisja fotonu, czyli kwantu energii, któremu odpowiada fala o określonej długości. Wartość energii kwantu jest równa: E 2 - E 1 = hv = h · v - częstotliwość emitowanej fali, λ – długość fali, c – prędkość światła. Stosując poniższe wyrażenie, można obliczyć długość emitowanej fali: R – stała Rydberga, dla atomu wodoru wynosi 1, 1 · 107 m-1 n 1 – numer powłoki, na którą nastąpiło przejście n 2 - numer powłoki, z której nastąpiło przejście Przejściu jedynego elektronu w atomie wodoru z powłok wyższych na powłokę pierwszą odpowiada seria linii widmowych, zwana serią Lymana, na powłokę drugą – seria Balmera, na trzecią – seria Paschena. Kolejne serie to: seria Bracketa, seria Pfunda i seria Humpreysa. W zależności od długości fali serie linii widmowych mogą znajdować się w różnych zakresach promieniowania elektromagnetycznego (1 nm = 1· 10 -9 m). 1 3 2

Zadanie 1. (1 pkt) Napisz wyrażenie pozwalające obliczyć długość fali dowolnej linii serii Humpreysa. R – stała Rydberga, dla atomu wodoru wynosi 1, 1 · 107 m-1 Przejściu jedynego elektronu w atomie wodoru z powłok wyższych na powłokę pierwszą odpowiada seria linii widmowych, zwana serią Lymana, na powłokę drugą – seria Balmera, na trzecią – seria Paschena. Kolejne serie to: seria Bracketa, seria Pfunda i seria Humpreysa → n 1 = 6

Zadanie 2. (1 pkt) Na schematycznym rysunku przedstaw jedno z przejść elektronowych (dowolne) odpowiadające serii Balmera. n=5 n=4 n=3 n=2 n=1 Przejściu jedynego elektronu w atomie wodoru z powłok wyższych na powłokę pierwszą odpowiada seria linii widmowych, zwana serią Lymana, na powłokę drugą – seria Balmera, na trzecią – seria Paschena. Kolejne serie to: seria Bracketa, seria Pfunda i seria Humpreysa → n = 2

Zadanie 3. (1 pkt) Podaj, w jakim zakresie (zakresach) promieniowania elektromagnetycznego znajdują się linie serii Balmera, jeżeli graniczne wartości długości fal wynoszą λ=656 nm i λ= 364 nm: a) tylko w zakresie widzialnym, b) w zakresie widzialnym i podczerwieni, c) w zakresie widzialnym i ultrafiolecie, d) w ultrafiolecie.

Uczeń nie rozwiązuje bardzo łatwego zadania „wietrząc podstęp”. PRZYKŁAD

Zadanie 1. (3 pkt) Oblicz stężenie procentowe jodu w jodynie, jeżeli otrzymano ją w wyniku rozpuszczenia 8 gramów jodu w 72 gramach etanolu. Obliczenia: Dane: mrozp= 72 g ms=8 g Szukane: C%=? mr= ms + mrozp = 8 g + 72 g = 80 g Odp. : Stężenie procentowe jodu w jodynie wynosi 10%.

Uczeń pobieżnie analizuje treść zadania, pomijając istotne dane. PRZYKŁAD

Zadanie 1. (1 pkt) soli Z jednego mola soliw wyniku dysocjacji powstają trzy mole jonów (jeden rodzaj kationów i jeden rodzaj anionów); stosunek ilościowy soli kationów do anionów wynosi 1: 2. Wzór sumaryczny soli to: a) b) c) d) Na 2 Si. O 3 Fe(OH)2 KCl. O 2 Mg. Cl 2

Uczeń poprawnie rozwiązuje zadania obliczeniowe, ale nie udziela odpowiedzi lub udziela odpowiedzi błędnej. PRZYKŁAD

Zadanie 1. (3 pkt) Oblicz i podaj masy roztworów 3% i 10% potrzebne do przygotowania 100 g roztworu 6 -procentowego. Obliczenia: Dane: C 1= 3% C 2= 10% Szukane: m 1= ? m 2=? C 3= 6% → mcz= 100 g/7=14, 3 g m 21 = 3 • 14, 3 g = 42, 8 g m 12= 100 g – 42, 8 g = 57, 2 g m 3= m 1 + m 2 = 100 g Odp. : Potrzeba 57, 2 42, 8 g pierwszego roztworu i 42, 8 57, 2 g drugiego roztworu.

Uczeń poprawnie rozwiązuje problemy, ale udziela odpowiedzi niezgodnej z poleceniem. PRZYKŁAD

Zadanie 1. (3 pkt) W atomie pierwiastka E elektrony są rozmieszczone na dwóch powłokach. Papierek uniwersalny zanurzony w roztworze wodnym tlenku pierwiastka E na jego najwyższym stopniu utlenienia zabarwia się na czerwono, a w wodnym nazwę roztworze wodorku pierwiastka E zabarwia się na niebiesko. Podaj nazwę pierwiastka E oraz wzory sumaryczne tlenku i wodorku, o których mowa w zadaniu. azot N N 2 O 5 NH 3

Uczeń poprawnie rozwiązuje problemy, ale udziela kilku (jego zdaniem równoważnych) odpowiedzi. PRZYKŁAD

Zadanie 1. (1 pkt) Atom pewnego pierwiastka ma konfigurację elektronową: K 2 L 8 M 18 N 7. Br - brom Podaj nazwę tego pierwiastka: ………………. nazwę Zadanie 2. (1 pkt) Atom pewnego pierwiastka ma konfigurację elektronową: 1 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d 1. Sc- skand Podaj symbol tego pierwiastka: ………… symbol Zadanie 3. (1 pkt) Atom pewnego pierwiastka ma konfigurację elektronową: [Kr]5 s 2 4 d 10 5 p 2. Sn - 50 liczbę atomową Podaj liczbę atomową tego pierwiastka: ………………….

Uczeń nie potrafi precyzyjnie wyrazić swoich myśli – nieporadność językowa. PRZYKŁAD

Zadanie 1. (2 pkt) Badano zachowanie cynku, miedzi i magnezu wobec rozcieńczonego kwasu solnego, przeprowadzając doświadczenie przedstawione na poniższym rysunku: Korzystając ze skróconego szeregu aktywności metali: K, Ca, Mg, Zn, Pb, H, Cu, Ag, Au wskaż, w których probówkach przebiegały reakcje chemiczne. Wyjaśnij, dlaczego we wskazanych przez ciebie probówkach metale reagowały z kwasem solnym. I i III Metale reagowały z kwasem solnym w probówkach: …………. są wyżej. z kwasem solnym, Cynk i magnez reagują Wyjaśnienie: …………………………………… ponieważ w szeregu reaktywności znajdują się …………………………………………… przed wodorem. ………………………………

Uczeń nie potrafi prezentować danych w formie graficznej. PRZYKŁAD
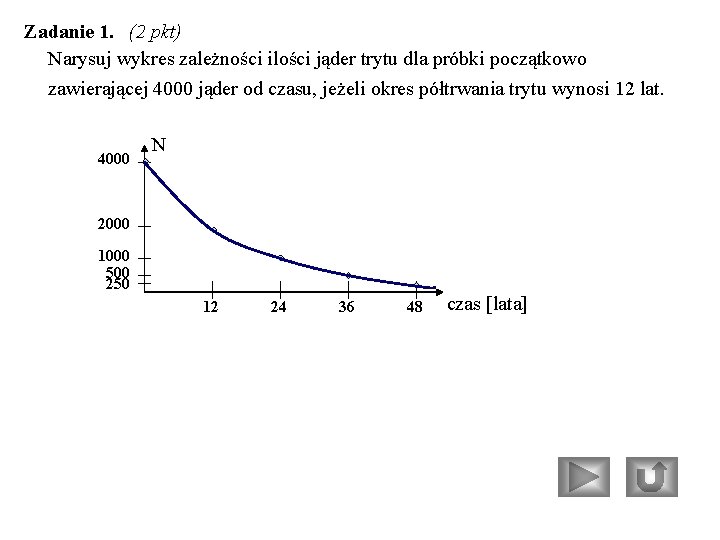
Zadanie 1. (2 pkt) Narysuj wykres zależności ilości jąder trytu dla próbki początkowo zawierającej 4000 jąder od czasu, jeżeli okres półtrwania trytu wynosi 12 lat. 4000 N 2000 1000 500 250 12 24 36 48 czas [lata]

Nabycie umiejętności rozwiązywania różnego typu zadań wymaga wielu ćwiczeń. Uczniowie powinni umiejętności przez edukacji chemicznej. zdobywać cały te okres
- Slides: 41