Prvodn list ablona III2 Inovace a zkvalitnn vuky

Průvodní list Šablona: III/2 Inovace a zkvalitnění výuky prostřednictvím ICT Vzdělávací materiál: Prezentace Určen pro: 1. ročník oboru Strojírenství a 2. ročník oboru Ekonomika a podnikání Vzdělávací oblast: Strojírenská technologie – Nauka o materiálu Název učebního materiálu: Vnitřní stavba kovů Jméno autora: Ing. Miroslava Jeřichová Datum vytvoření: 15. 7. 2013 Reg. č. projektu: CZ. 1. 07/1. 5. 00/34. 0627

Klíčová slova: atom, Bohrův model atomu, elektron, proton, neutron, iontová, kovalentní, kovová vazba, Van der Waalsovy síly. Anotace: Prezentace je určena žákům 1. ročníku oboru Strojírenství pro výuku v předmětu Strojírenská technologie a žákům 2. ročníku oboru Ekonomika a podnikání v předmětu Strojírenská výroba. Inovuje výuku použitím multimediálních pomůcek – prezentace. Metodické pokyny: Tento materiál uplatní učitel při výkladu dané látky, použité obrázky a fotografie zvýší názornost výkladu. Prezentaci mohou žáci použít i v rámci samostatné domácí přípravy na výuku.

Vnitřní stavba kovů Metalografie Atomová stavba prvků – historický vývoj Stavba atomu Chemické vazby

Metalografie Zabývá se zkoumáním a pozorováním vnitřní stavby (struktury) kovů a jejich slitin Pomocí vnitřní stavby kovů a meziatomových vazeb lze předpokládat vlastnosti jednotlivých materiálů, jejichž znalost umožní jejich hospodárné a efektivní využití Vlastnosti materiálů souvisí s chemickým složením a právě s jejich strukturou V technické praxi se vlastnosti dělí na : 1. Fyzikální – takové vlastnosti, které souvisí s krystalickou strukturou např. elektrická a tepelná vodivost, měrný elektrický odpor, supravodivost….

Metalografie 2. Chemické – dochází k rozrušení povrchu kovů vlivem chemických účinků různých látek 3. Mechanické – materiály jsou vystaveny určitému způsobu namáhání (tah, tlak, smyk, krut, ohyb), aby jim materiál odolal musí mít určitou pevnost, tvrdost, houževnatost…. . 4. Technologické – pomocí těchto vlastností se dá materiál zpracovávat určitou technologií např. svařitelnost, obrobitelnost, tvárnost, slévatelnost…. .

Atomová stavba prvků – historický vývoj Demokritos (5. stol. př. n. l. ) - látky jsou složeny z částic, které se již nedají dělit atomy, (atomos = nedělitelný) 18. stol. – rozvoj chemie Dalton - začátek 18. stol - atom nelze zničit, autor atomové hypotézy - je tolik různých atomů, kolik je prvků, atomy téhož prvku jsou stejné, atomy různých prvků se liší hmotnostmi a dalšími chemickými vlastnostmi

Atomová stavba prvků – historický vývoj Thomson (1898) – objev atomy obsahují elektrony „ pudinkový model atomu „ podle něhož jsou atomy miniaturní homogenní koule kladně nabité hmoty, do níž jsou vnořeny elektrony (anglický pudink se zapečenými hrozinkami)
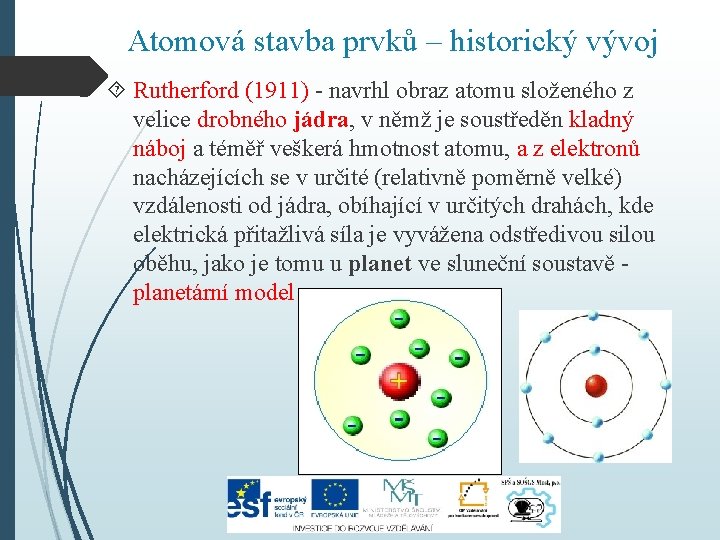
Atomová stavba prvků – historický vývoj Rutherford (1911) - navrhl obraz atomu složeného z velice drobného jádra, v němž je soustředěn kladný náboj a téměř veškerá hmotnost atomu, a z elektronů nacházejících se v určité (relativně poměrně velké) vzdálenosti od jádra, obíhající v určitých drahách, kde elektrická přitažlivá síla je vyvážena odstředivou silou oběhu, jako je tomu u planet ve sluneční soustavě planetární model
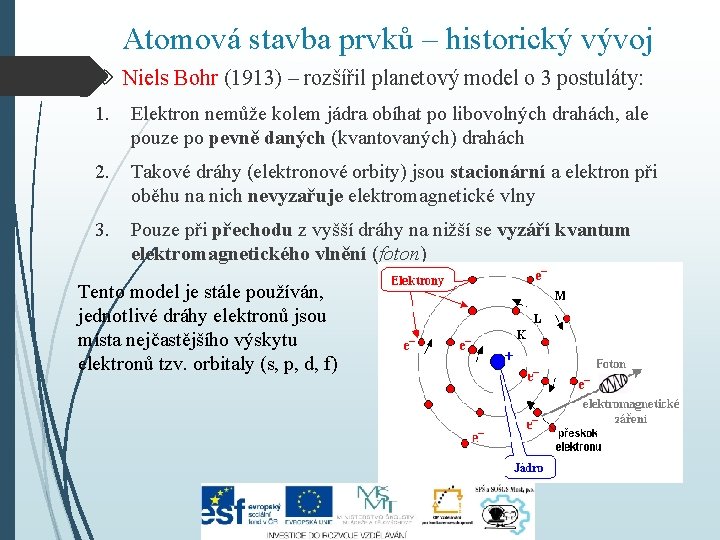
Atomová stavba prvků – historický vývoj Niels Bohr (1913) – rozšířil planetový model o 3 postuláty: 1. Elektron nemůže kolem jádra obíhat po libovolných drahách, ale pouze po pevně daných (kvantovaných) drahách 2. Takové dráhy (elektronové orbity) jsou stacionární a elektron při oběhu na nich nevyzařuje elektromagnetické vlny 3. Pouze při přechodu z vyšší dráhy na nižší se vyzáří kvantum elektromagnetického vlnění (foton) Tento model je stále používán, jednotlivé dráhy elektronů jsou místa nejčastějšího výskytu elektronů tzv. orbitaly (s, p, d, f)

Atomová stavba prvků – historický vývoj Chadwick (1932) - objevil neutron v jádře de Broglie (teorie částicových vln) + Shrodinger (Shrodingerova rovnice) + Heisenbergova relace neurčitosti určení tzv. orbitalů (místo pravděpodobného výskytu elektronů)

Stavba atomu Průměr atomu je řádově 10 -8 cm ( atom je mnohem menší než vlnová délka světla, ani elektronovým mikroskopem nejsou atomy přímo pozorovatelné), jádro je ještě 100 000 krát menší! - jeho průměr činí jen 10 -13 cm Atom se skládá z jádra a obalu, navenek je elektronegativní Jádro – obsahuje kladně nabité částice = protony a částice bez náboje = neutrony Protony a neutrony (nukleony) jsou v jádře drženy jadernými silami Protonové číslo Z udává počet protonů v jádře, a tím tedy chemickou povahu atomu Protonové č. Z je pořadovým číslem v Mendělejevově periodické tabulce chemických prvků atomové číslo

Stavba atomu Nukleonové číslo N – udává počet nukleonů, určuje hmotnost atomového jádra, nazývá se též hmotnostní číslo a značí se A NX Z - např. hélium 4 He 2, uhlík 12 C 6, uran 238 U 92 Obal atomu obsahuje elektrony, částice záporně nabité, jejich hmotnost v porovnání s hmotností nukleonů je nepatrná Počet elektronů v obalu = počtu protonů (Z) Elektron se pohybuje tak rychle, že nelze přesně určit, kde se nachází – k popisu polohy slouží orbitaly = sféry (oblast nejpravděpodobnější polohy elektronu v obalu jádra) Existuje 7 sfér, nejblíže jádru je sféra 1, nejdále 7 Nejmenší energii mají elektrony ve sféře 1, nejvyšší ve sféře 7 Nejsnáze se uvolňují elektrony z nejvzdálenější sféry = valenční elektrony, poslední sféra má maximálně 8 elektronů
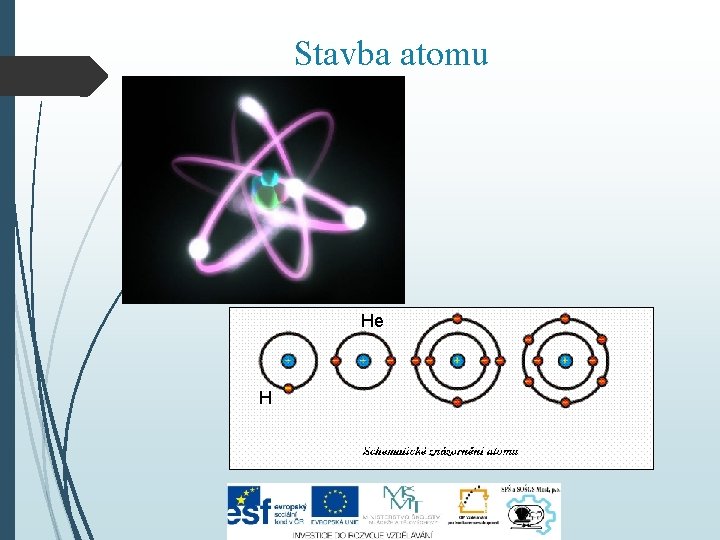
Stavba atomu He H

Stavba atomu Sféra s plným počtem elektronů je stabilní, takové prvky jsou velmi stálé, jsou chemicky netečné, s jinými prvky se neslučují Donor = atom, který má ve vnější sféře méně než polovinu elektronů, je uvolňuje kation Akceptor = atom, který má ve vnější sféře více než polovinu elektronů, je přijímá anion Záporné a kladné ionty se snadno slučují Jednotlivé atomy nebo skupiny atomů se slučují ve větší celky molekuly, makromolekuly Síly, které způsobují vzájemné vázání atomů v molekuly, označujeme chemickou vazbou

Druhy vazeb: Chemické vazby 1. Iontová – nejjednodušší, vzniká u prvků, které jsou v periodické tabulce daleko od sebe tzn. s rozdílnou elektronegativitou (vyšší než 1, 67), prvek s malou elektronegativitou elektrony uvolní kation, prvek se silnou elektronegativitou elektrony přijímá anion, vznikají iontové sloučeniny, například chlorid sodný, nebo oxid hořečnatý, vazba je polární
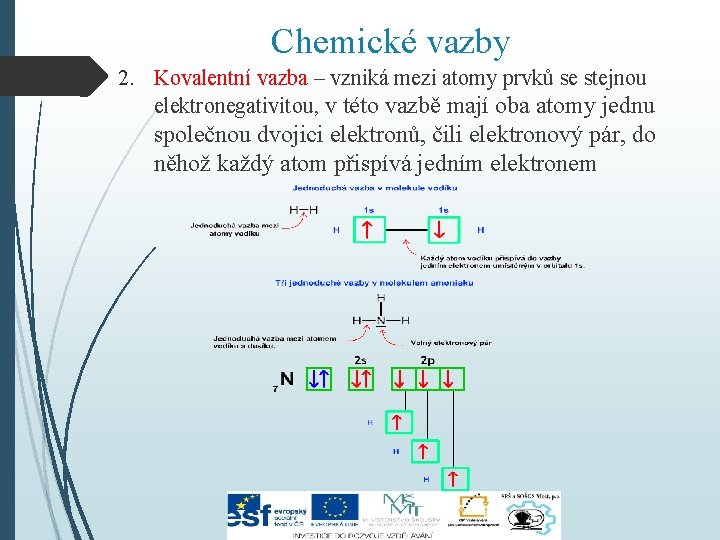
Chemické vazby 2. Kovalentní vazba – vzniká mezi atomy prvků se stejnou elektronegativitou, v této vazbě mají oba atomy jednu společnou dvojici elektronů, čili elektronový pár, do něhož každý atom přispívá jedním elektronem

Chemické vazby 3. Kovová vazba – u kovů, které mají prostorovou mřížku, v této mřížce jsou umístěny kladné ionty, mezi kterými se volně pohybují volné valenční elektrony elektronový mrak velká tepelná a elektrická vodivost, kujnost, vysoká teplota tání…. . 4. Van der Waalsovy síly - jsou přitažlivé nebo odpudivé interakce mezi atomy nebo molekulami, jsou to síly fyzikální povahy, jsou velmi slabé 5. Vodíková vazba - je založena na přitahování opačných nábojů, vyskytuje se např. ve vodě, atom vodíku navázaný na kyslík má náboj kladný, kyslík jiné molekuly má volný elektronový pár, který má náboj záporný, vodík je přitahován, vzniká vazba podobná iontové, ale slabší
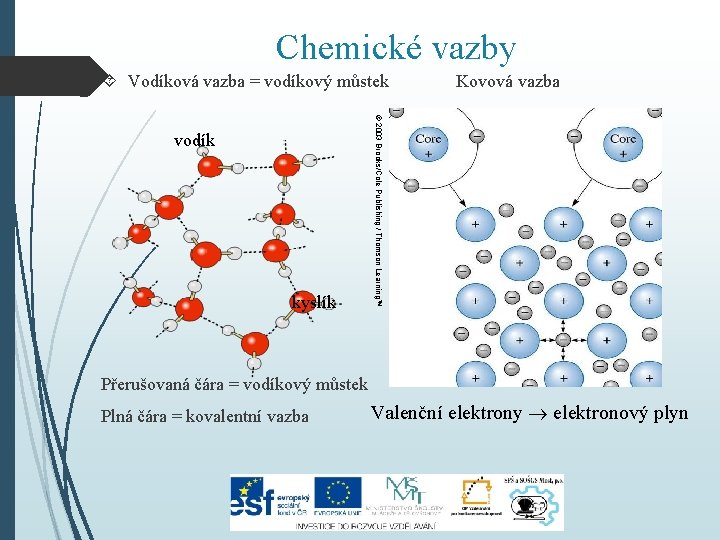
Chemické vazby Vodíková vazba = vodíkový můstek Kovová vazba kyslík © 2003 Brooks/Cole Publishing / Thomson Learning™ vodík Přerušovaná čára = vodíkový můstek Plná čára = kovalentní vazba Valenční elektrony elektronový plyn
![Použité zdroje: Zdroje obrázků: FASTFISSION. wikipedia. cz [online]. [cit. 11. 9. 2013]. Dostupný na Použité zdroje: Zdroje obrázků: FASTFISSION. wikipedia. cz [online]. [cit. 11. 9. 2013]. Dostupný na](http://slidetodoc.com/presentation_image/1fee1a11d6a549acf89ccf274992de82/image-19.jpg)
Použité zdroje: Zdroje obrázků: FASTFISSION. wikipedia. cz [online]. [cit. 11. 9. 2013]. Dostupný na WWW: http: //upload. wikimedia. org/wikipedia/commons/thumb/f/ff/Plum_pudding_atom. svg/348 px. Plum_pudding_atom. svg. png, AUTOR NEUVEDEN. seznam. cz [online]. [cit. 11. 9. 2013]. Dostupný na WWW: http: //www. eprojekt. gjs. cz/Services/Downloader. ashx? id=333&disposition=inlin AUTOR NEUVEDEN. seznam. cz [online]. [cit. 11. 9. 2013]. Dostupný na WWW: http: //astronuklfyzika. cz/Struktura. Atomu. gif AUTOR NEUVEDEN. seznam. cz [online]. [cit. 11. 9. 2013]. Dostupný na WWW: http: //www. eprojekt. gjs. cz/Image. View. aspx? id=339&guid=59690 c 9 e 72334 ff 6932 dbbda 5 f 2 a 4728 AUTOR NEUVEDEN. seznam. cz [online]. [cit. 11. 9. 2013]. Dostupný na WWW: http: //artemis. osu. cz/mmfyz/am/am_1_5_soubory/image 041. gif AUTOR NEUVEDEN. seznam. cz [online]. [cit. 15. 9. 2013]. Dostupný na WWW: http: //chemvazba. moxo. cz/Vyvoj/jednoducha_vazba. gif AUTOR NEUVEDEN. seznam. cz [online]. [cit. 15. 9. 2013]. Dostupný na WWW: http: //upload. wikimedia. org/wikipedia/commons/thumb/e/ed/Wasserstoffbr%C 3%BCckenbindungen. Wasser. svg/220 px-Wasserstoffbr%C 3%BCckenbindungen-Wasser. svg. png Použitá literatura:

Použité zdroje: Použitá literatura: Řasa J. a kolektiv: Strojírenská technologie I (1. díl), Scientia s. r. o. pedagogické nakladatelství Praha 2002 Neuwirthová L. : Manuál pro výuku Materiály a nanomateriály, Centrum nanotechnologií Ostrava-Poruba
- Slides: 20