Prvky VIII B skupiny trida elezo 26 Fe

Prvky VIII. B skupiny – triáda železo (26 Fe) • výskyt: • • hematit (krevel) - Fe 2 O 3 limonit (hnědel) - 2 Fe. O 3· 3 H 2 O magnetit (magnetovec) - Fe 3 O 4 siderit (ocelek) - Fe. CO 3 pyrit - Fe. S 2 minerální vody [Fe(HCO 3)2] železo je esenciální prvek, 70% v lidském těle je součástí hemoglobinu a 20 -25% se nachází v podobě zásobních bílkovin

• průmyslová výroba: • pec se zaváží směsí rudy (obvykle hematitem), koksu a vápence • poté se zdola vhání horký vzduch - tím se spaluje koks a v nejnižší části pece se dosáhne teploty 2000°C, zatímco na jejím vrcholu je teplota asi 200°C • ruda se redukuje na železo a křemičitá hlušina účinkem vápence přichází na strusku (v podstatě Ca. Si. O 3)

• redukce nepřímá (redukce CO) - probíhá v rozmezích asi 400 - 1000°C ve vyšší části pece: 3 Fe 2 O 3+ CO 2 Fe 3 O 4 + CO 2 Fe 3 O 4 + CO 3 Fe. O + CO 2 Fe. O + CO Fe + CO 2

• redukce přímá (redukce uhlíkem) - probíhá v nižší části pece v asi 1000 -1800 °C: • Fe 2 O 3+ 3 C 2 Fe + 3 CO Fe 3 O 4 + 4 C 3 Fe + 4 CO Fe. O + C Fe + CO • roztavené železo a struska se hromadí na dně pece, odkud se odděleně vypouštějí • takto vyredukované železo obsahuje značné množství uhlíku • struska se využívá jako stavební materiál (výroba tvárnic) a také při výrobě určitých druhů cementů
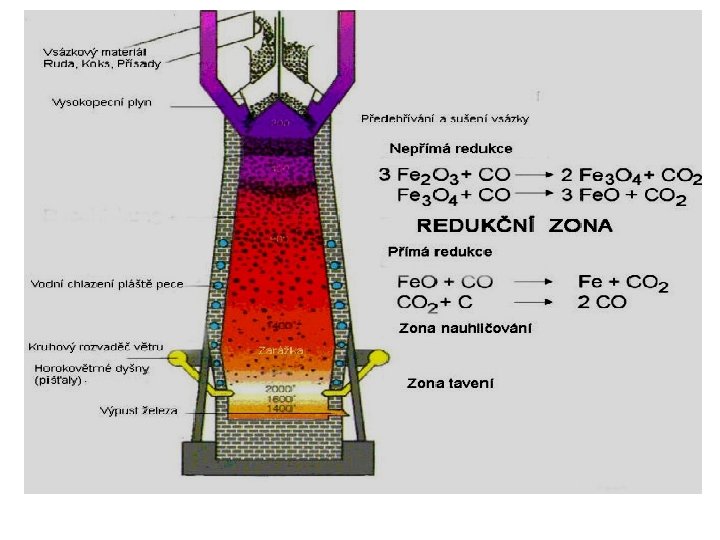

vysoká pec

• Surové železo je buď šedé nebo bílé, v prvním případě obsahuje železo mnohem více křemíku než manganu a má barvu na lomu šedou nebo je poměr obrácený a barva lomu je bílá. • Šedé železo se obvykle přetavuje, aby se zbavilo mechanických nečistot, a pak se používá jako tzv. litina k odlévání železných předmětů. • Dá se dobře obrábět, ale není kujné.

• Bílé železo se zkujňuje, tedy zušlechťuje, různými způsoby, které je mají zbavit přebytečného uhlíku, fosforu, síry, křemíku a jiných prvků, které železu dodávají křehkosti. • Stane se tak jejich oxidací a podle množství uhlíku, které v materiálu zbude, se získá kujné železo nebo ocel.

výroba oceli – kyslíkový konvertor

výroba oceli – elektrická oblouková pec

• tvrdost se zvyšuje kalením - zahřátí oceli a ochlazení ve vodě nebo oleji • fyzikální vlastnosti: • bílý lesklý kov, měkký, kujný, tažný • do teploty 768°C (Curieho teplota) je ferromagnetické

• chemické vlastnosti: • na suchém vzduchu stálé • na vlhkém vzduchu se pokrývá vrstvou Fe(OH)3 (rezavění) • s kyslíkem reaguje za vzniku Fe 2 O 3 nebo Fe 3 O 4 • snadno se rozpouští ve zředěných kyselinách, vznikají železnaté soli • v oxidujících kyselinách se pasivuje

• sloučeniny: • hydroxid železnatý – reakcí vodného roztoku obsahujícího Fe 2+ s hydroxidy - vzniká vločkovitá sraženina, která, je-li připravena za naprostého vyloučení vzduchu je bílá – v přítomnosti kyslíku Fe(OH)2 tmavne a přechází na červenohnědý Fe(OH)3

• disulfid železnatý – může se připravit zahříváním Fe 2 O 3 v atmosféře H 2 S – zahříváním za přístupu vzduchu vzniká Fe 2 O 3 a SO 2

• síran železnatý • bezvodý - bílá látka • s vodou krystaluje jako heptahydrát - zelená skalice Fe. SO 4· 7 H 2 O • (NH 4)2 Fe(SO 4)2· 6 H 2 O - Mohrova sůl - látka na vzduchu stálá - význam v analytické chemii

• uhličitan železnatý • bílá sraženina • na vzduchu hnědne, neboť se oxiduje • nerozpustný ve vodě, obsahuje-li však vodu a rozpuštěný CO 2 tvoří se rozpustný Fe(HCO 3)2, který je součástí minerálních vod
![komplexní sloučeniny: - K 4[Fe(CN)6] - hexakyanoželeznatan draselný (žlutá krevní sůl) • připravuje se komplexní sloučeniny: - K 4[Fe(CN)6] - hexakyanoželeznatan draselný (žlutá krevní sůl) • připravuje se](http://slidetodoc.com/presentation_image/45add07278188c8dadc60a6d3b6db3cd/image-17.jpg)
komplexní sloučeniny: - K 4[Fe(CN)6] - hexakyanoželeznatan draselný (žlutá krevní sůl) • připravuje se reakcí: • Fe. SO 4 + 6 KCN K 4[Fe(CN)6] + K 2 SO 4 • ve vodě dobře rozpustný, není toxický • reakcí se železitou solí vzniká - tmavě modrá sraženina, berlínská modř: 3 K 4[Fe(CN)6] + 4 Fe. Cl 3 Fe 4[Fe(CN)6]3 + 12 KCl

• Fe. Cl 3· 6 H 2 O – prostředek k leptání, zvláště důležitá je jeho schopnost leptat měď, čehož se využívá při výrobě tištěných elektrických obvodů – úprava vody slouží jako koagulační činidlo, (vytváří vločky, které sorpcí odstraní z vody rozpuštěné organické i suspendované látky)

• hydroxid železitý – složení lépe vystihuje vzorec Fe 2 O 3·n. H 2 O – látka má amfoterní charakter – adsorpční vlastnost - čištění vod, v lékařství při otravách As 2 O 3

• síran železitý • krystaluje v podobě šesti různých hydrátů (12, 10, 9, 7, 6 a 3 H 2 O) • nejčastěji jako nonahydrát, používá se jako koagulační činidlo, při úpravě pitné vody, ale též při čištění odpadních vod
![- K 3[Fe(CN)6] - hexakyanoželezitan draselný (červená krevní sůl) • příprava oxidací hexakyanoželeznatanu draselného - K 3[Fe(CN)6] - hexakyanoželezitan draselný (červená krevní sůl) • příprava oxidací hexakyanoželeznatanu draselného](http://slidetodoc.com/presentation_image/45add07278188c8dadc60a6d3b6db3cd/image-21.jpg)
- K 3[Fe(CN)6] - hexakyanoželezitan draselný (červená krevní sůl) • příprava oxidací hexakyanoželeznatanu draselného např. chlórem v roztoku okyseleném kyselinou chlorovodíkovou: 2 K 4[Fe(CN)6] + Cl 2 2 K 3[Fe(CN)6] + 2 KCl • krystalizuje v červených krystalech, které se dobře rozpouští ve vodě na žlutý roztok

• je jedovatý, má oxidační účinky • reakcí s ionty železnatými dává modrou sraženinu, Turnbullova modř: • 3 Fe. SO 4 + 2 K 3[Fe(CN)6] Fe 3[Fe(CN)6]2 + 3 K 2 SO 4

kobalt (27 Co) • výskyt: • smaltin - Co. As 2 • kobaltin - Co. As. S • součást vitamínu B 12 • průmyslová výroba: • rudy se nejprve praží, kov se tak převede na oxid se redukuje uhlíkem, vodíkem nebo hliníkem

• fyzikální vlastnosti: • • lesklý, stříbřitý kov s modrým nádechem tvrdší než železo, kujný, tažný feromagnetický - Curieho teplota > 1100 °C jeden izotop - 60 Co

• chemické vlastnosti: • na vzduchu je za normální teploty stálý • ve zředěných kyselinách se rozpouští obtížně • tvoří komplexní sloučeniny

• využití: • výroba barev - výroba porcelánu a skla • sloučeniny kobaltu se používají jako katalyzátory v organických reakcích • výroba slitin (Alnico - Al, Ni, Co) - výroba permanentních magnetů • pokobaltování - ochrana před korozí ovocnými šťávami (příbory), 60 Co (poločas rozpadu - 5271 let) • koncentrovaný zdroj záření gama v lékařství při léčbě zhoubných nádorů

• sloučeniny: • chlorid kobaltnatý • indikátor kvality silikagelu používaného jako sušící prostředek (změna barvy modré na růžovou, ke které dochází při přechodu z bezvodé formy na hydratovanou)

nikl (28 Ni) • výskyt: • nikelin - Ni. As • průmyslová výroba: • karbonylový způsob - pražením vzniklý oxid nikelnatý redukujeme vodním plynem (CO + H 2) • houbovitý nikl pak reaguje při teplotě 50 - 60°C s oxidem uhelnatým

• vzniká těkavý tetrakarbonyl niklu, který se potom rozloží vedením přes tablety z čistého niklu při teplotě 230°C a uvolněný CO se vrací zpět • nikl vyrobený tímto způsobem dosahuje čistoty asi 99, 95%

• fyzikální vlastnosti: • stříbrobílý, lesklý, kujný, tažný kov • chemické vlastnosti: • ve zředěných kyselinách se rozpouští jen zvolna • odolný vůči působení alkalických hydroxidů • koncentrovaná HNO 3 nikl pasivuje

• využití: • • přísada do ocelí (korozivzdorné) výroba slitin katalyzátor (hydrogenace) akumulátorové baterie (Ni/Fe)
- Slides: 31