Prvky VII B skupiny mangan 25 Mn vskyt

Prvky VII. B skupiny • mangan (25 Mn) • výskyt: • burel - Mn. O 2 • hausmannit - Mn 3 O 4

hausmannit

• průmyslová výroba: A. rudy se zpracovávají na ferromangan - redukcí Mn. O 2 a Fe 2 O 3 koksem • slitina obsahuje 80% Mn

B. aluminotermie - Mn. O 2 se vyžíhá na tzv. červený oxid Mn 3 O 4, protože Mn. O 2 by reagoval s Al příliš prudce: 3 Mn. O 2 Mn 3 O 4 + O 2 3 Mn 3 O 4 + 8 Al 9 Mn + 4 Al 2 O 3

• fyzikální vlastnosti: • šedobílý kov, tvrdý, ale křehký • pouze jeden izotop vyskytující se v přírodě • chemické vlastnosti: • reaktivní kov, zvláště není-li čistý • je schopen rozkládat vodu a uvolňovat z ní vodík • snadno se rozpouští ve zředěných kyselinách za vzniku manganatých solí

• využití: • manganová ocel (vysoká tvrdost)

• sloučeniny: • oxid manganatý – má bazický charakter, proto se rozpouští v kyselinách na roztoky příslušných manganatých solí – nerozpustný ve vodě

• hydroxid manganatý – bílá látka – rozpouští se v kyselinách na manganaté soli (růžová barva)

• oxid manganičitý – slouží jako oxidační činidlo – nerozpustný oxid, málo reaktivní, amfoterní

• výroba článků • výroba cihel (dodává řadu odstínů od červeného až po hnědý) • odbarvovací prostředek při výrobě skla • katalyzátor

burelové sklo

• oxid manganistý – zelená olejovitá kapalina – stáním pozvolna uvolňuje kyslík a přechází na Mn. O 2 – většinu organických látek oxiduje za současné exploze

• kyselina manganistá – nedá se získat čistá, velmi silná – oxidační činidlo

• manganistan draselný • tmavě fialové krystaly • silné oxidační činidlo (výroba sacharinu, kys. benzoové) • dezinfekční prostředek • KMn. O 4 se redukuje do různého stupně podle prostředí: • kyselé prostředí: Mn. O 4 - + 8 H+ + 5 e- Mn 2+ + 4 H 2 O
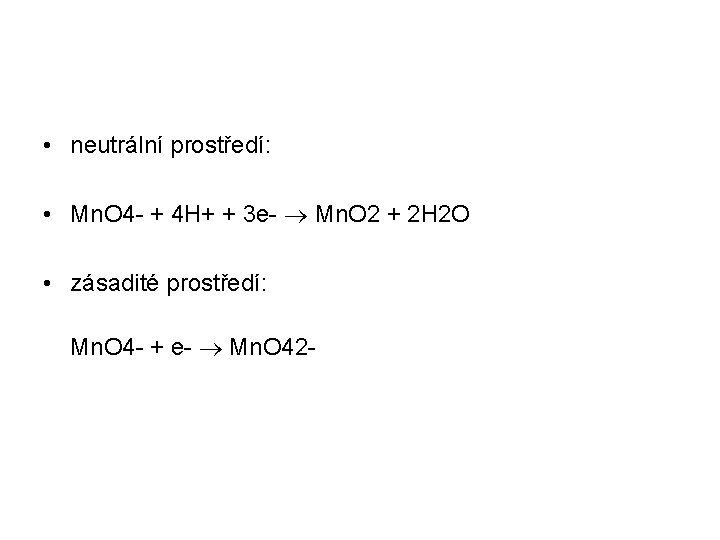
• neutrální prostředí: • Mn. O 4 - + 4 H+ + 3 e- Mn. O 2 + 2 H 2 O • zásadité prostředí: Mn. O 4 - + e- Mn. O 42 -

difúze manganistanu draselného
- Slides: 16