Prvky II B skupiny zinek 30 Zn vskyt

Prvky II. B skupiny • zinek (30 Zn) • výskyt: • sfalerit Zn. S • dospělý člověk má obsaženy 2 g Zn v enzymech

sfalerit

• průmyslová výroba: • rudy uhličitanové se žíháním zbaví CO 2, rudy sfaleritové se praží, tak se převedou na oxid: Zn. CO 3 Zn. O + CO 2 2 Zn. S + 3 O 2 2 Zn. O + 2 SO 2 • takto upravené rudy se redukují koksem

• Zn. O + C Zn + CO • vyredukovaný zinek se oddestiluje a přetavením se čistí

• fyzikální vlastnosti: • lesklý šedobílý kov, křehký • chemické vlastnosti: • na vlhkém vzduchu se pokrývá vrstvou oxidu, hydroxidu nebo uhličitanu • slučuje se s kyslíkem na Zn. O, sírou • v neoxidujících kyselinách se rozpouští za vývoje H 2 • rozpouští se ve vodných roztocích alkalických hydroxidů za vzniku iontu [Zn(OH)4]2 • Zn + 2 Na. OH + 2 H 2 O Na 2[Zn(OH)4] + H 2

zinek

• využití: • • • slitiny zinkový plech - střechy výroba článků v laboratoři k přípravě vodíku redukční činidlo (granulovaný nebo práškový)

využití zinku

• sloučeniny: • halogenidy • Zn. Cl 2 – nejdůležitější – impregnace dřeva – úprava textilií – čištění povrchu kovů před pájením – Zn. Br 2, Zn. I 2 - bílé rozpustné látky

• sulfid zinečnatý • směs Zn. S + Ba. SO 4 - bílá barva

• oxid zinečnatý – spalováním Zn na vzduchu: 2 Zn + O 2 2 Zn. O – bílý, nerozpustný v H 2 O – rozpustný v kyselinách i zásadách - typicky amfoterní oxid: Zn. O + 2 HCl Zn. Cl 2 + H 2 O Zn. O + Na. OH + H 2 O Na[Zn(OH)3] Zn. O + 2 Na. OH + H 2 O Na 2[Zn(OH)4]

• využití: – výroba pryže - zkracuje dobu vulkanizace – pigment ve výrobě barev, má výhodu nad tradiční olovnatou bělobou v tom, že je netoxický, nevýhodou je, že má menší krycí schopnost (zinková běloba) – lékařství - zinkové masti a zásypy

• hydroxid zinečnatý – bílá sraženina – nepatrně rozpustný v H 2 O – amfoterní charakter: Zn(OH)2 + H 2 SO 4 Zn. SO 4 + 2 H 2 O Zn(OH)2 + Na. OH Na[Zn(OH)3]

• síran zinečnatý – krystaluje z roztoku jako heptahydrát Zn. SO 4· 7 H 2 O = bílá skalice – konzervační činidlo na dřevo – mořidlo v textilním průmyslu – velmi čistý v očním lékařství

kadmium (48 Cd) • výskyt: • greenockit Cd. S • zinkové rudy s obsahem 0, 2 - 0, 4% Cd • průmyslová výroba: • při výrobě zinku, oddestiluje se dříve než Zn (Cd je těkavější)

• fyzikální vlastnosti: • stříbrný, tažný kov s namodralým leskem • chemické vlastnosti: • méně reaktivní než zinek

• využití: • výroba článků • slitiny • atomové reaktory - bezpečnostní a regulační tyče

• sloučeniny: • oxid kademnatý • využití: • Ni-Cd akumulátory • katalyzátor hydrogenačních a dehydrogenačních reakcí

sulfid kademnatý • žlutá barva (kadmiová žluť) • přidáním Cd. Se, Zn. S, Hg. S k Cd. S - tepelně stálé pigmenty zářivých barev od světle žluté do tmavě červené, koloidní disperze těchto látek se používají k barvení transparentních skel

• síran kademnatý • krystalický - Cd. SO 4· 8 H 2 O • Westonovy články

• Kadmium je mimořádně toxické a v lidském těle se hromadí v ledvinách a v játrech. Dlouhodobý příjem i velmi malých množství Cd vede k selhání funkce ledvin. Může inhibovat působení enzymů obsahujících Zn tím, že nahrazuje atomy zinku.

• rtuť(80 Hg) • výskyt: • cinabarit (rumělka) - Hg. S • průmyslová výroba: A. ruda se praží, uvolňuje se rtuť a oxid siřičitý, páry rtuti se ochlazením zkondenzují Hg. S + O 2 (600 °C) Hg + SO 2

B. pražení rudy se železným odpadem nebo páleným vápnem Hg. S + Fe Hg + Fe. S 4 Hg. S + 4 Ca. O 4 Hg + 3 Ca. S + Ca. SO 4

cinabarit - rumělka

• fyzikální vlastnosti: • kapalný, stříbrobílý, lesklý kov • páry jsou monoatomické, toxické • vysoký měrný elektrický odpor, vysoká hustota

• chemické vlastnosti: • na vzduchu stálý (neoxiduje se) • při zahřátí k teplotě varu se pokrývá vrstvičkou Hg. O • rozpouští se v konc. HNO 3 a horké konc. H 2 SO 4 za vzniku rtuťnatých solí a oxidů dusíku nebo síry: Hg + 4 HNO 3 Hg(NO 3)2 + 2 NO 2 + 2 H 2 O Hg + 2 H 2 SO 4 Hg. SO 4 + SO 2 + 2 H 2 O • slitiny s kovy - amalgámy - roztoky kovů (Zn, Cd) • nejsnadněji tvoří amalgámy těžké kovy, zatímco lehčí kovy první přechodné řady (s výjimkou Mn, Cu) jsou ve rtuti nerozpustné
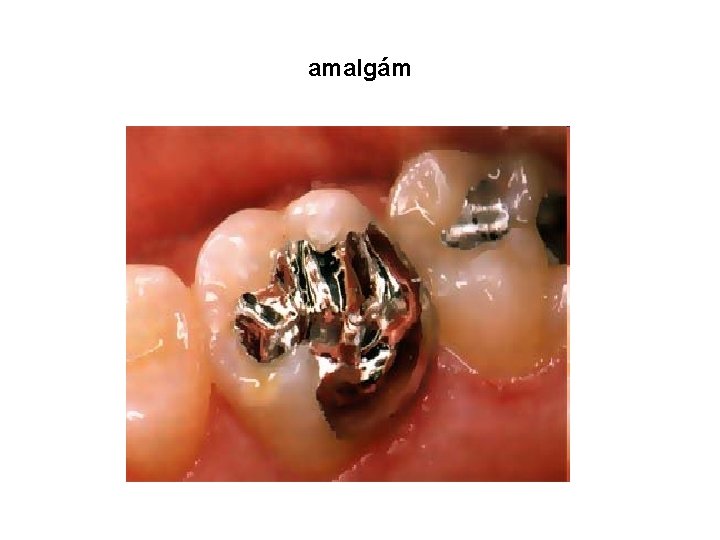
amalgám

• využití: • výroba Na. OH • fyzikální přístroje (teploměry, tlakoměry) • amalgámy - zubní lékařství (plombování)

• sloučeniny: • Hg. I - rtuťné s dimérním iontem Hg 22+ • halogenidy • Hg 2 Cl 2 - kalomel - dříve hodně používán v lékařství • síran rtuťnatý – málo rozpustný – katalyzátor v organické chemii:

• Hg. II - rtuťnaté s iontem Hg 2+ • halogenidy • nejběžnější Hg. Cl 2 – tzv. sublimát - rozpustný v H 2 O – prudký jed – dezinfekční prostředek – ochrana dřeva před hnitím

• jodid rtuťnatý • rozpustný v alkalickém jodidu: 2 KI + Hg. I 2 K 2[Hg. I 4] - tetrajodortuťnatan draselný • součást Nesslerova činidla, k důkazu NH 3

• oxid rtuťnatý – v červené a žluté modifikaci - rozdíl v barvě je způsoben velikostí částic – červená - tepelným rozkladem Hg(NO 3)2 nebo zahříváním Hg v kyslíku (350 °C) – žlutá - za studena - srážením roztoků rtuťnatých solí alkalickými hydroxidy

• sulfid rtuťnatý – 2 modifikace - přímou syntézou prvků za chladu nebo srážením sirovodíkem dostaneme modifikaci černou, která sublimací přejde v modifikaci červenou – nerozpustný v H 2 O, rozpouští se pouze v lučavce královské – barva a líčidlo

• síran rtuťnatý – bílá krystalická látka – katalyzátor v organické chemii
- Slides: 34