Prvky 2 skupiny Be a Mg kovy alkalickch

Prvky 2. skupiny (Be a Mg, kovy alkalických zemín – Ca, Sr, Ba a Ra) Aj keď oxidy a hydroxidy MO a M(OH)2 (Ca, Sr, Ba a Ra) sú pomerne málo rozpustné vo vode, sú silno zásadité, podobne ako analogických zlúčeniny alk. kovov. Navyše sa tieto zlúčeniny nazývali ako zeminy. Preto sa pre prvky Ca, Sr, Ba a Ra začal používať aj názov kovy alkalických zemín. Často sa pojem kovy alk. zemín používa pre všetky prvky 2. skupiny (? ). Sú si podobné ako alk. kovy, avšak Be sa od ostatných kovov 2. skupiny líši výraznejšie ako Li od kovov 1. skupiny. Ra je rádioaktívne (izotop 226 Ra má polčas rozpadu 1 622 rokov). sa používalo na liečbu rakoviny – nahradené inými izotopmi. 226 Ra Elektrónová konfigurácia ns 2 – valenčné elektróny sú len slabo viazané k atómovým jadrám. Malé hodnoty ionizačných energií ochota k tvorbe katiónov M 2+ v tuhom stave aj v roztoku. Najdôležitejšími faktormi, ktoré ovplyvňujú chemické vlastností prvkov 2. skupiny sú ich ionizačné energie a iónové polomery.
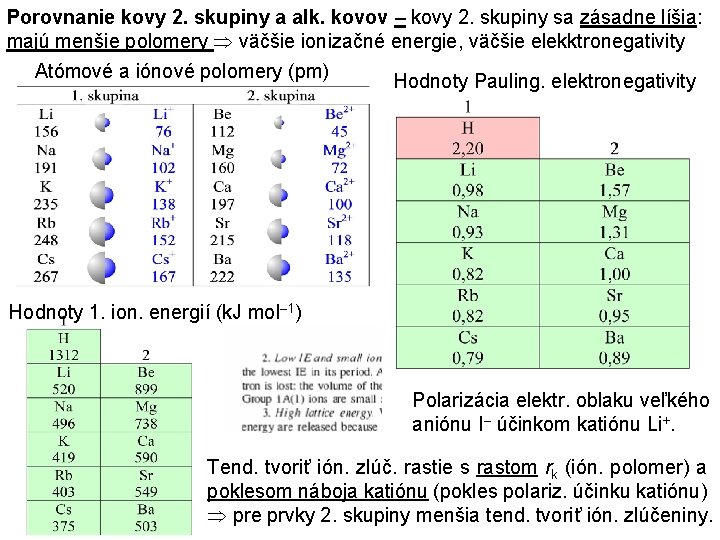
Porovnanie kovy 2. skupiny a alk. kovov – kovy 2. skupiny sa zásadne líšia: majú menšie polomery väčšie ionizačné energie, väčšie elekktronegativity Atómové a iónové polomery (pm) Hodnoty Pauling. elektronegativity Hodnoty 1. ion. energií (k. J mol– 1) Polarizácia elektr. oblaku veľkého aniónu I– účinkom katiónu Li+. Tend. tvoriť ión. zlúč. rastie s rastom rk (ión. polomer) a poklesom náboja katiónu (pokles polariz. účinku katiónu) pre prvky 2. skupiny menšia tend. tvoriť ión. zlúčeniny.
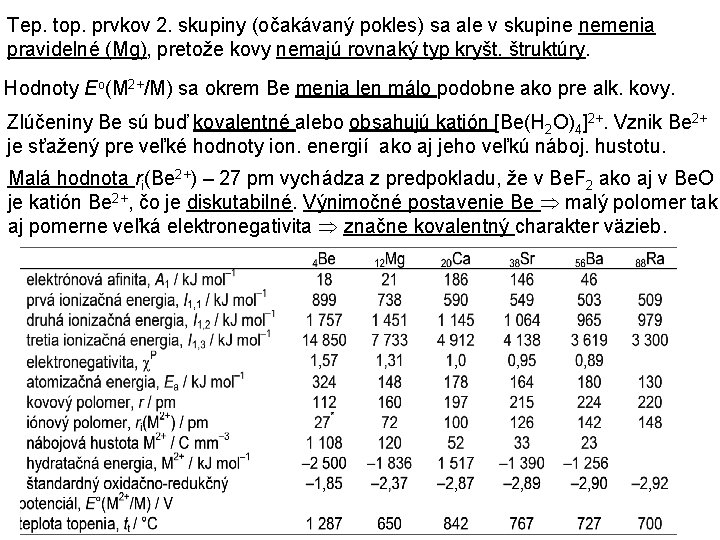
Tep. top. prvkov 2. skupiny (očakávaný pokles) sa ale v skupine nemenia pravidelné (Mg), pretože kovy nemajú rovnaký typ kryšt. štruktúry. Hodnoty Eo(M 2+/M) sa okrem Be menia len málo podobne ako pre alk. kovy. Zlúčeniny Be sú buď kovalentné alebo obsahujú katión [Be(H 2 O)4]2+. Vznik Be 2+ je sťažený pre veľké hodnoty ion. energií ako aj jeho veľkú náboj. hustotu. Malá hodnota ri(Be 2+) – 27 pm vychádza z predpokladu, že v Be. F 2 ako aj v Be. O je katión Be 2+, čo je diskutabilné. Výnimočné postavenie Be malý polomer tak aj pomerne veľká elektronegativita značne kovalentný charakter väzieb.
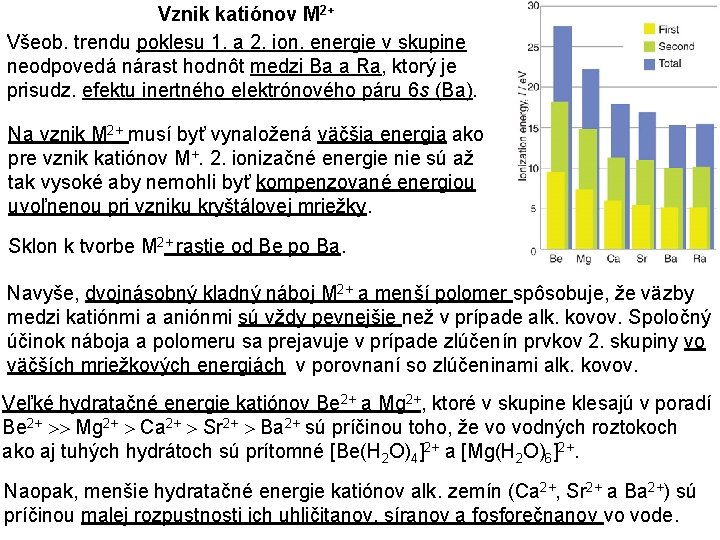
Vznik katiónov M 2+ Všeob. trendu poklesu 1. a 2. ion. energie v skupine neodpovedá nárast hodnôt medzi Ba a Ra, ktorý je prisudz. efektu inertného elektrónového páru 6 s (Ba). Na vznik M 2+ musí byť vynaložená väčšia energia ako pre vznik katiónov M+. 2. ionizačné energie nie sú až tak vysoké aby nemohli byť kompenzované energiou uvoľnenou pri vzniku kryštálovej mriežky. Sklon k tvorbe M 2+ rastie od Be po Ba. Navyše, dvojnásobný kladný náboj M 2+ a menší polomer spôsobuje, že väzby medzi katiónmi a aniónmi sú vždy pevnejšie než v prípade alk. kovov. Spoločný účinok náboja a polomeru sa prejavuje v prípade zlúčenín prvkov 2. skupiny vo väčších mriežkových energiách v porovnaní so zlúčeninami alk. kovov. Veľké hydratačné energie katiónov Be 2+ a Mg 2+, ktoré v skupine klesajú v poradí Be 2+ Mg 2+ Ca 2+ Sr 2+ Ba 2+ sú príčinou toho, že vo vodných roztokoch ako aj tuhých hydrátoch sú prítomné [Be(H 2 O)4]2+ a [Mg(H 2 O)6]2+. Naopak, menšie hydratačné energie katiónov alk. zemín (Ca 2+, Sr 2+ a Ba 2+) sú príčinou malej rozpustnosti ich uhličitanov, síranov a fosforečnanov vo vode.

Z menšieho polomeru M 2+ väčší polarizačný účinok M 2+ na anióny a preto solí oxokyselín (uhličitany, sírany, dusičnany) ako aj hydroxidy sú kovalentnejšie a tiež aj menej tepelne stále v porovnaní s analog. zlúčeninami alk. kovov. Najväčší polarizačný účinok má najmenší Be 2+ s najväčšou hodnotou nábojovej hustoty a a potom so značným odstupom nasleduje Mg 2+ tuhé Be(II) zlúčeniny sú nielen najviac náchylné k tepelnému rozkladu, ale ak sú rozpustené vo vode podliehajú kyslej hydrolýze: Podobne ako pre ťažšie alk. kovy – K, Rb a Cs aj medzi ťažšími prvkami Ca, Sr a Ba existuje značná podobnosť. Najmä pre chovanie oxidov a hydroxidov Ca, Sr a Ba, ktoré sa blíži alk. kovom uvedenú trojicu prvkov označujeme ako kovy alk. zemín. Pre Be a Mg sa začína prejavovať blízkosť nekovových prvkov. Malý polomer a neobyčajne veľká náb. hustota Be 2+ vyčleňuje Be, podobne ako Li do výnimočného postavenia. Správaním sa Be diagonálne podobá na Al.

Diagonálna podobnosť Be na Al: - obidva kovy sa pôsobení konc. HNO 3 pokrývajú vrstvičkou oxidu (pasivácia), - Be aj Al sa rozpúšťajú v roztokoch hydroxidov za vývoja vodíka, - majú takmer rovnakú elektronegativitu, - berylnaté a hlinité solí podliehajú hydrolýze, - halogenidy Be a Al sa správajú ako Lewisove kyseliny, - halogenidy Be sú polymérne, halogenidy Al sú polymérne alebo dimérne. - Be a Al prejavuje silnú tendenciu k tvorbe kovalentných väzieb. Be má predpoklady k tvorbe donor-akceptorových väzieb (sp 3 orbitály) veľký počet koordinačných zlúčenín ako sú napr. hydráty s katiónom [ Be(H 2 O)4]2+ alebo abiónom [Be. F 4]2–. Atómy Be a Mg v hydridoch a v niektorých organokovových zlúčeninách sa viažu elektrónovodeficitnými viaccentrovými väzbami. Takéto väzby sa nachádzajú v reťazcových hydridoch napr. Be. H 2 a v dimetylberýliu a dimetylmagnéziu.

Fyzikálne, chem. vlastnosti Be a Mg a kovov alkalických zemín Be a Mg – sú šedivé kovy. Kovy alk. zemín Ca, Sr a Ba sú mäkké a striebristé. Všetky sú kujné, ťažné a pomerne krehké. Väčšie hod. tt, tv a hustoty v porovnaní s alk. kovmi Látkové vlastnosti kovov 2. skupiny Porovanie teplôt topenia alkalických kovov a kovov 2. skupiny Be Mg Ca
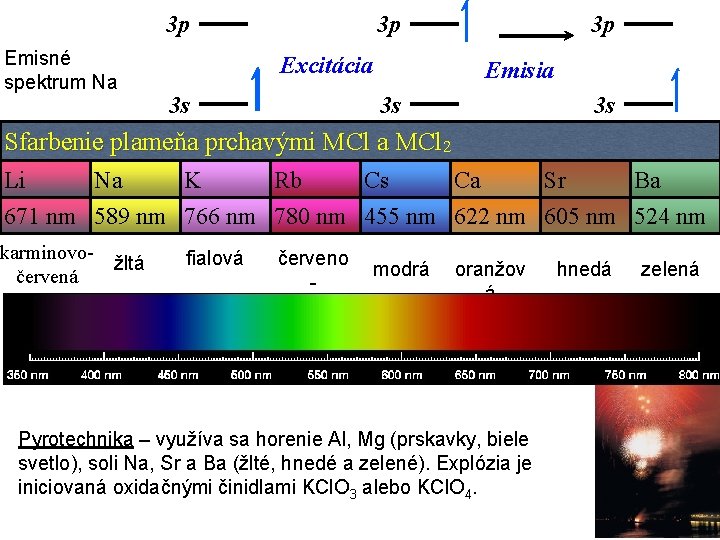
3 p Emisné spektrum Na 3 p 3 p Excitácia 3 s Emisia 3 s 3 s Sfarbenie plameňa prchavými MCl a MCl 2 Li Na K Rb Cs Ca Sr Ba 671 nm 589 nm 766 nm 780 nm 455 nm 622 nm 605 nm 524 nm karminovočervená žltá fialová červeno falová modrá oranžov á Pyrotechnika – využíva sa horenie Al, Mg (prskavky, biele svetlo), soli Na, Sr a Ba (žlté, hnedé a zelené). Explózia je iniciovaná oxidačnými činidlami KCl. O 3 alebo KCl. O 4. hnedá zelená

Reakcie kovov 2. skupiny: kovy 2. skupiny sú výborné redukovadla, reagujú priamo s väčšinou nekovov. Pri zahrievaní všetky kovy 2. skupiny reagujú s O 2 za vzniku oxidy MO (s Ba vzniká aj malé množstvo Ba. O 2): s N 2 za vzniku nitridov M 3 N 2: s halogénmi vznikajú halogenidy MX 2: Rozdielne chovanie kovov 2. skupiny môžeme ukázať v nasledujúcej kapitole na reakciách vzniku hydridov a karbidov. Reakciou s H 2 vznikajú iónové hydridy (okrem Be), reakcia s Mg prebieha až pri zvyšenom tlaku: M(s) + H 2(g) MH 2(s) M = Mg, Ca, Sr a Ba S uhlíkom reaguje Be za vzniku karbidu Be 2 C, ktorý reaguje s vodou: Be 2 C(s) + 4 H 2 O(l) Be(OH)2(s) + CH 4(g) ostatné kovy druhej skupiny reakciou s uhlíkom tvoria acetylidy MC 2, ktoré reagujú s vodou: MC 2(s) + 2 H 2 O(l) M(OH)2(s) + C 2 H 2(g)
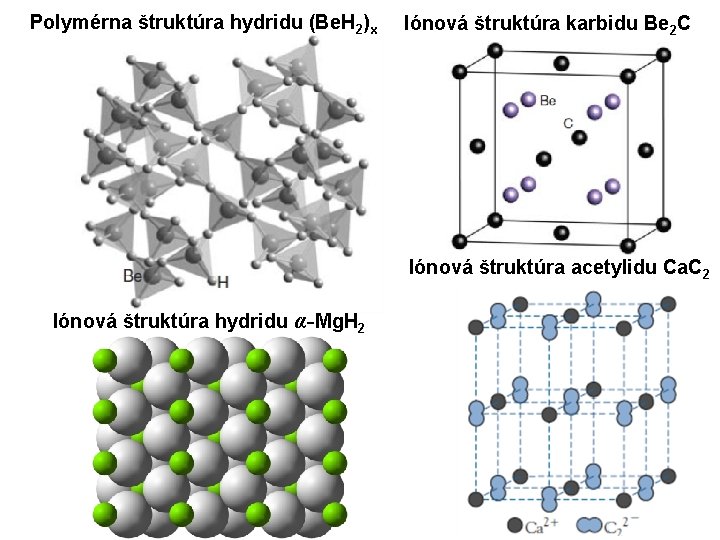
Polymérna štruktúra hydridu (Be. H 2)x Iónová štruktúra karbidu Be 2 C Iónová štruktúra acetylidu Ca. C 2 Iónová štruktúra hydridu α-Mg. H 2

Reakcia Ca. C 2 (tradičný názov karbid) s vodou sa v oblastiach kde je uhlie dôležitejšou surovinou ako ropa priemyslovo využíva na výrobu etínu: Ca. C 2(s) + 2 H 2 O(l) Ca(OH)2(s) + C 2 H 2(g) Ca. C 2 sa vyrába z Ca. O reakciou s C pri 2 300 K. Ca. O vzniká kalcináciou Ca. CO 3: Ca. C 2 sa predovšetkým využíva na výrobu dusíkatého hnojiva Ca. CN 2 pri 1 300 K: Be a Mg sa na vzduchu pasivujú (vzniká Be. O alebo Mg. O) pri bežnej teplote kineticky inertné voči O 2 a H 2 O. 2 Be(s) + O 2(g) 2 Be. O(s) (ochranná povrchová vrstva) Mg reaguje s vod. parou alebo horúcou vodou: Mg(s) + 2 H 2 O(l) Mg(OH)2(s) + H 2(g) Kovy alk. zemín (Ca, Sr a Ba) reagujú už so studenou vodou: M(s) + 2 H 2 O(l) M(OH)2(aq) + H 2(g) Be a Mg sa ochotne rozpúšťajú v neoxid. kyselinách. Be aj Be. O a Be(OH)2 sa rozpúšťajú v roztokoch hydroxidov alklických kovov. Reakcie Ca s H 2 O

10. 3 Vysvetlite, prečo v prípade tvorby roztoku chloridu sodného dochádza k väčšiemu rastu entropie ako v prípade roztoku chloridu horečnatého. Riešenie: Mg 2+ má vysokú náb. hustotu, ktorá spôsobuje, že molekuly vody sú v hydráte viac usporiadané ako je to v prípade Na+, ktorý ma nižšiu náb. hustotu. 10. 5 Vysvetlite, prečo soli Mg(II) majú sklon tvoriť hydráty s veľkým počtom molekúl vody. Riešenie: Vyššia náb. hustota Mg 2+ spôsobuje silnejšie viazanie polár. molekúl vody. Mg 2+ má najväčšiu náb. hustotu z katiónov 2. skupiny (s výnimkou Be 2+) a teda bude mať tendenciu byť značne hydratovaný. 10. 6 Vysvetlite, prečo Be 2+ tvorí [Be(H 2 O)4]2+ a Mg 2+ tvorí [Mg(H 2 O)6]2+. Riešenie: Be je prvok 2. a Mg 3. periódy. Aj sterické dôvody. 10. 7 Ako sa chémia Mg líši od chémie kovov alk. zemín (Ca, Sr a Ba). Vysvetlite. Riešenie: Mg tvorí veľký počet zlúčenín s koval. väzbami, napr. Grignardové činidlo z väčšej náb. hustoty Mg 2+ v porovnaní s ostatnými katiónmi alk. zemín, čo vedie k väčšej tendencii viazať sa kovalentnými väzbami.

10. 8 Napíšte rovnice chemických reakcií kovov druhej skupiny s vodou. 10. 15 Pri štúdiu chémie prvkov 2. skupiny sa zvyčajne ignoruje rádioaktívny prvok tejto skupiny, Ra. Na základe skupinových trendov navrhnite charakteristické vlastnosti Ra a jeho zlúčenín. Riešenie: Zlúčeniny Ra by mohli byť iónové a bezfarebné (okrem prípadov ak je farebný anión) a pretože Ra 2+ má najmenšiu náb. hustotu z katiónov skupiny, je nepravd. tvorba hydrátov soli. Ra bude intenzívne reagovať s vodou za tvorby veľmi rozp. hydroxidu: Ra(s) + 2 H 2 O(l) → Ra(OH)2(aq) + H 2(g) Síran rádnatý by mal byť veľmi málo rozpustný: Ra 2+(aq) + SO 42−(aq) → Ra. SO 4(s) Zohrievaním rádia by mohlo dôjsť k rýchlej reakcií s dikyslíkom : Ra(s) + O 2(g) → Ra. O 2(s)

Výskyt kovov 2. skupiny Be sa vyskytuje vo forme minerálu berylu Be 3 Al 2 Si 6 O 18. Mg je 8. a Ca 5. najrozširenejším prvkom v zem. kôre. Súčasne je Mg 3. najrozšírenejším prvkom v morskej vode. Mg, Ca, Sr a Ba sa v zn. množstve vyskytujú ako v mineráloch tak aj v podobe soli rozp. v morskej vode. Výskyt kovov 2. skupiny v Zemskej kôre (v jedn. ppm) Dôležitými minerálmi Mg, Ca, Sr a Ba sú dolomit (Ca. CO 3 Mg. CO 3), magnezit (Mg. CO 3), karnalit (KCl Mg. Cl 2 6 H 2 O), Ca. CO 3 v mineráloch krieda, vápenec a mramor, sádrovec (Ca. SO 4 2 H 2 O), celestín (Sr. SO 4), stroncanit (Sr. SO 4) a baryt (Ba. SO 4). Be, Sr a Ba sa v prírode nachádza omnoho menej ako Mg a Ca. Vápenec Ca. CO 3 Sádrovec Ca. SO 4. 2 H 2 O Najbežnejšie vápenaté minerály Kazivec Ca. F 2

Výroba kovov 2. skupiny Be sa vyrába extrakciou (luhovaním) z berylu Be 3 Al 2 Si 6 O 18. Ruda sa najprv luží H 2 SO 4 a párou a vzniknutý Be. SO 4 sa prevádza na Be(OH)2, ktorý sa používa pri výrobe Be, zliatin Be a Be. O. Výroba Be je založená buď na redukcii Be. F 2 Mg alebo elektrolýzov taveniny zmesi Be. Cl 2 a Na. Cl. Ca sa vyrába elektrolýzou taveniny Ca. Cl 2 a Ca. F 2. Sr a Ba sa získavajú red. ich oxidov Al alebo elektrolýzou MCl 2 (M = Sr, Ba). Z kovov 2. skupiny sa vo veľkom vyrába len Mg, ktorý sa pripravuje buď z dolomitu alebo z morskej vody. Pri 1. spôsobe sa tep. rozkladom Ca. CO 3 Mg. CO 3 získa zmes Mg. O a Ca. O, ktorá sa redukuje ferosiliciom Fe. Si: a následne sa horčík oddelí vákuovou destiláciou.
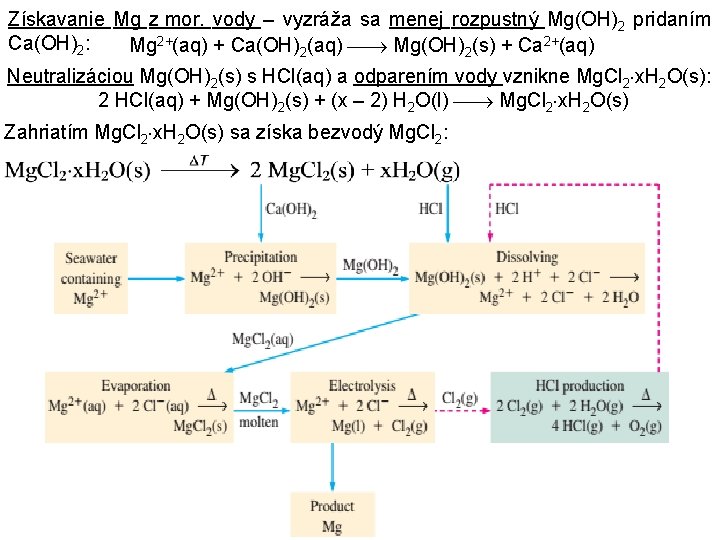
Získavanie Mg z mor. vody – vyzráža sa menej rozpustný Mg(OH)2 pridaním Ca(OH)2: Mg 2+(aq) + Ca(OH)2(aq) Mg(OH)2(s) + Ca 2+(aq) Neutralizáciou Mg(OH)2(s) s HCl(aq) a odparením vody vznikne Mg. Cl 2 x. H 2 O(s): 2 HCl(aq) + Mg(OH)2(s) + (x – 2) H 2 O(l) Mg. Cl 2 x. H 2 O(s) Zahriatím Mg. Cl 2 x. H 2 O(s) sa získa bezvodý Mg. Cl 2:
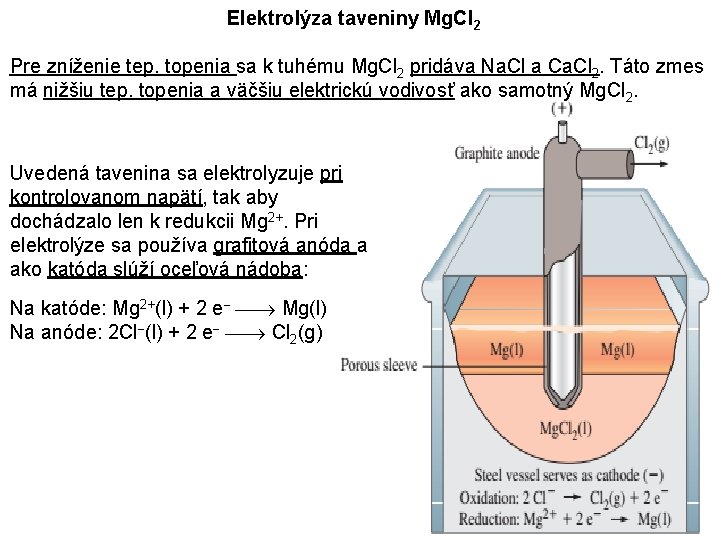
Elektrolýza taveniny Mg. Cl 2 Pre zníženie tep. topenia sa k tuhému Mg. Cl 2 pridáva Na. Cl a Ca. Cl 2. Táto zmes má nižšiu tep. topenia a väčšiu elektrickú vodivosť ako samotný Mg. Cl 2. Uvedená tavenina sa elektrolyzuje pri kontrolovanom napätí, tak aby dochádzalo len k redukcii Mg 2+. Pri elektrolýze sa používa grafitová anóda a ako katóda slúží oceľová nádoba: Na katóde: Mg 2+(l) + 2 e Mg(l) Na anóde: 2 Cl (l) + 2 e Cl 2(g)

Využitie kovov 2. skupiny Be je jedným z najľahších kovov s veľmi vysokou tep. topenia a inertnosťou voči vzd. oxidáxcii, čo určuje jeho priem. využitie. V dôsledku malej elektrónovej hustoty (slabo pohlcuje elektromag. žiarenie) a preto sa z Be vyrábajú okienka rentgenových lámp. Vďaka vysokej tep. topenia a malej účinnosti pri pohlcovaní neutrónov je Be využívané v jadrovej energetike. Prítomnosť Mg v zliatinách s Al dáva materiálu väčšiu mech. pevnosť a odolnosť proti korózii. Zo zliatiny Mg/Al sa vyrábajú časti lietadiel a automobilov. Ďalšie využitie Mg zahrňuje farmac. prípravky ako antiacidita (prostriedok proti páleniu žahy), horečnaté mlieko Mg(OH)2 a preháňadla (napr. horká soľ, Mg. SO 4 7 H 2 O). Ióny Mg 2+ a Ca 2+ sú v biologických systémoch katalyzátormi premeny difosforečnanov na trifosforečnany. Pre Ca sa omnoho viac využívajú jeho zlúčeniny (Ca. O, Ca(OH)2, Ca. O Mg. O, Ca(OH)2 Mg. O a Ca(OH)2 Mg(OH)2) ako samotný kov. Ca. O sa vyrába kalcináciou (tep. rozkladom) Ca. CO 3 a používa sa predovšetkým ako súčasť stavebnej malty. Suchú zmes piesku (pôsobí ako spojivo) a Ca. O môžeme skladovať a prepravovať, Po pridaní vody a absorpcii CO 2 v malte vznikne Ca. CO 3: Ca. O(s) + H 2 O(l) Ca(OH)2(aq, s) pálené vápno hasené vápno Ca(OH)2(aq, s) + CO 2(g) Ca. CO 3(s) + H 2 O(l)

Iné dôležité využitie Ca. O je v oceliarskom, drevárskom a papierenskom priemysle a pri výrobe Mg. Veľké množstvo Ca. CO 3 sa spotrebuje pri výrobe ocele, skla, cementu, betónu a už uvedenom Solvayovom procese. Pre životné prostredie má význam použitie Ca. CO 3 a Ca(OH)2 pri odstranovaní SO 2. Ca. F 2 sa vyskytuje v prírode ako minerál fluorit – surovina na výrobu HF: Ca. F 2(s) + 2 H 2 SO 4(konc. ) 2 HF(g) + Ca(HSO 4)2(aq) Zlúčeniny Sr sa v súčasnosti najviac využívajú v pyrotechnike, v zliatinách a ako pigmenty. Menšie množstvo Ba. SO 4 („barytová kaša“) pre jeho schpnosť pohlcovať rentgenové žiarenie sa využíva pri obrazovaniu zaživacieho traktu. Pre vysokú reaktivitu s plynnými O 2 a N 2 sa Ba užíva vo vákuových trubiciach a lampách ako pohlčovač týchto plynov.
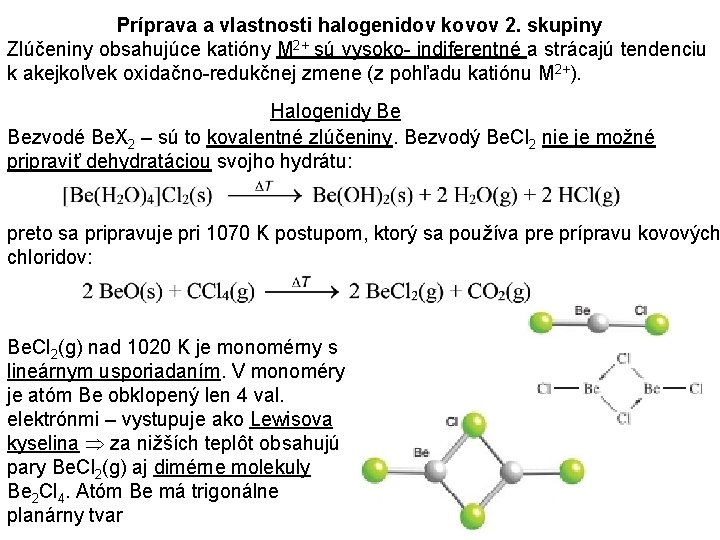
Príprava a vlastnosti halogenidov kovov 2. skupiny Zlúčeniny obsahujúce katióny M 2+ sú vysoko- indiferentné a strácajú tendenciu k akejkoľvek oxidačno-redukčnej zmene (z pohľadu katiónu M 2+). Halogenidy Be Bezvodé Be. X 2 – sú to kovalentné zlúčeniny. Bezvodý Be. Cl 2 nie je možné pripraviť dehydratáciou svojho hydrátu: preto sa pripravuje pri 1070 K postupom, ktorý sa používa pre prípravu kovových chloridov: Be. Cl 2(g) nad 1020 K je monomérny s lineárnym usporiadaním. V monoméry je atóm Be obklopený len 4 val. elektrónmi – vystupuje ako Lewisova kyselina za nižších teplôt obsahujú pary Be. Cl 2(g) aj dimérne molekuly Be 2 Cl 4. Atóm Be má trigonálne planárny tvar
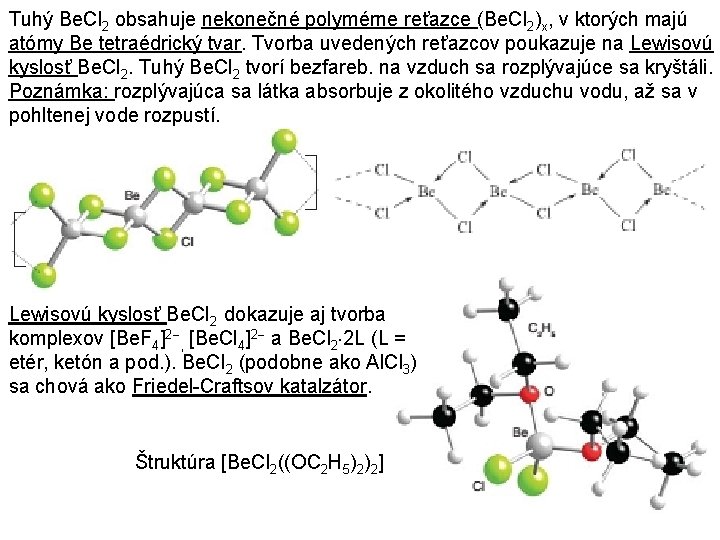
Tuhý Be. Cl 2 obsahuje nekonečné polymérne reťazce (Be. Cl 2)x, v ktorých majú atómy Be tetraédrický tvar. Tvorba uvedených reťazcov poukazuje na Lewisovú kyslosť Be. Cl 2. Tuhý Be. Cl 2 tvorí bezfareb. na vzduch sa rozplývajúce sa kryštáli. Poznámka: rozplývajúca sa látka absorbuje z okolitého vzduchu vodu, až sa v pohltenej vode rozpustí. Lewisovú kyslosť Be. Cl 2 dokazuje aj tvorba komplexov [Be. F 4]2 , [Be. Cl 4]2 a Be. Cl 2 2 L (L = etér, ketón a pod. ). Be. Cl 2 (podobne ako Al. Cl 3) sa chová ako Friedel-Craftsov katalzátor. Štruktúra [Be. Cl 2((OC 2 H 5)2)2]

Halogenidy Mg, Ca, Sr a Ba Fluoridy Mg, Ca, Sr a Ba sú iónové zlúčeniny s vysokými tep. topenia. Sú málo rozpustné vo vode. Halogenidy Mg. X 2 (X = Cl, Br a I) kryštalizujú z vodných roztokov vo forme hydrátov – napr. Mg. Cl 2 6 H 2 O, ktoré pri zahrievaní čiastočne hydrolyzujú Preto sa bezvodé halogenidy Mg. X 2 pripravujú napr. reakciou: Mg(s) + Cl 2(g) Mg. Cl 2(s) Príprava MX 2(aq) – z uhličitanov alebo hydroxidov reakciou s vodnými roztokmi HX(aq) M(OH)2(s) + 2 HX(aq) MX 2(aq) + 2 H 2 O(l) MCO 3(s) + 2 HX(aq) MX 2(aq) + CO 2(g) + H 2 O(l) Z vodných roztokov kryštalizujú ako hydráty napr. Sr. X 2. 6 H 2 O, Ba. X 2. 2 H 2 O, Ca. X 2. 6 H 2 O a pod.

Bezvodé halogenidy MCl 2, MBr 2 a MI 2 (M = Ca, Sr a Ba) môžu byť pripravené dehyratáciou svojich hydrátov. Tieto halogenidy sú hygroskopické a Ca. Cl 2 (získaný pri Solvayovom procese) sa používa ako laboratórne sušiace činidlo. V tuhom stave majú halogenidy MX 2 vrstevnatú štruktúru typu Cd. I 2. Väčšina týchto halogenidov je rozpustná v polárnych aprotických rozpúšťadlách (éter, pyridín a pod. ). Vrstevnatá štruktúra Mg. Cl 2 Atóm Mg(II) má koord. číslo 6 Poznámka: hygroskopická tuhá látka absorbuje vodu z okolitej atmosféry, bez toho aby sa stala kvapalinou.
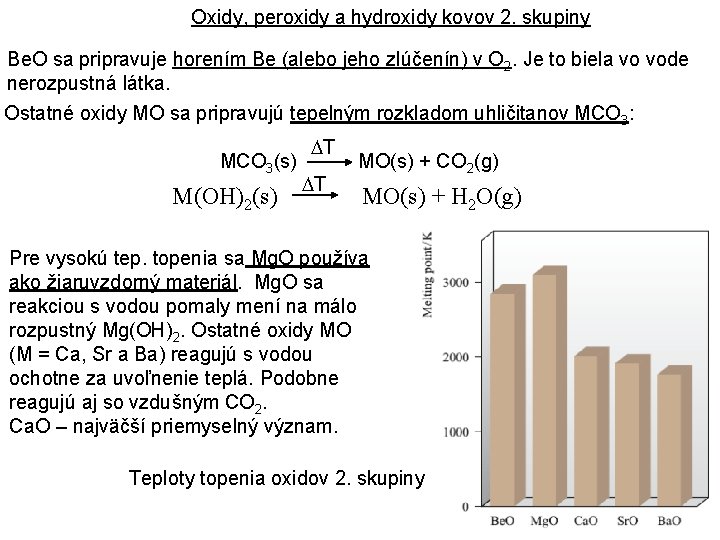
Oxidy, peroxidy a hydroxidy kovov 2. skupiny Be. O sa pripravuje horením Be (alebo jeho zlúčenín) v O 2. Je to biela vo vode nerozpustná látka. Ostatné oxidy MO sa pripravujú tepelným rozkladom uhličitanov MCO 3: MCO 3(s) M(OH)2(s) T T MO(s) + CO 2(g) MO(s) + H 2 O(g) Pre vysokú tep. topenia sa Mg. O používa ako žiaruvzdorný materiál. Mg. O sa reakciou s vodou pomaly mení na málo rozpustný Mg(OH)2. Ostatné oxidy MO (M = Ca, Sr a Ba) reagujú s vodou ochotne za uvoľnenie teplá. Podobne reagujú aj so vzdušným CO 2. Ca. O – najväčší priemyselný význam. Teploty topenia oxidov 2. skupiny
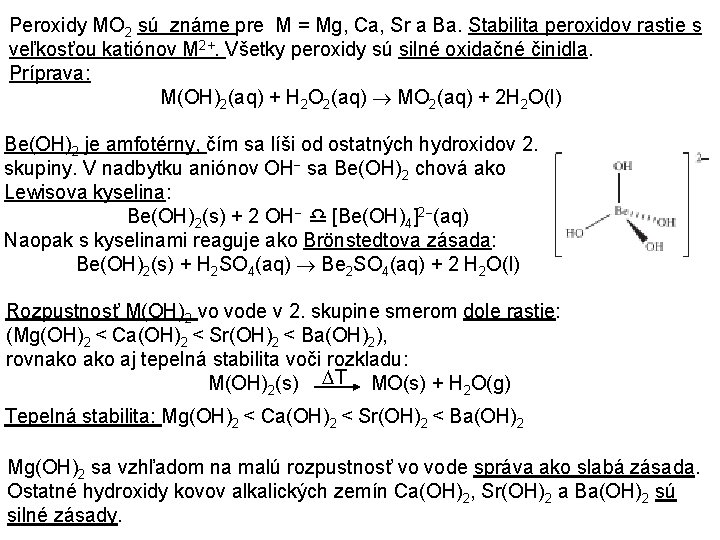
Peroxidy MO 2 sú známe pre M = Mg, Ca, Sr a Ba. Stabilita peroxidov rastie s veľkosťou katiónov M 2+. Všetky peroxidy sú silné oxidačné činidla. Príprava: M(OH)2(aq) + H 2 O 2(aq) MO 2(aq) + 2 H 2 O(l) Be(OH)2 je amfotérny, čím sa líši od ostatných hydroxidov 2. skupiny. V nadbytku aniónov OH sa Be(OH)2 chová ako Lewisova kyselina: Be(OH)2(s) + 2 OH [Be(OH)4]2 (aq) Naopak s kyselinami reaguje ako Brönstedtova zásada: Be(OH)2(s) + H 2 SO 4(aq) Be 2 SO 4(aq) + 2 H 2 O(l) Rozpustnosť M(OH)2 vo vode v 2. skupine smerom dole rastie: (Mg(OH)2 < Ca(OH)2 < Sr(OH)2 < Ba(OH)2), rovnako aj tepelná stabilita voči rozkladu: M(OH)2(s) T MO(s) + H 2 O(g) Tepelná stabilita: Mg(OH)2 < Ca(OH)2 < Sr(OH)2 < Ba(OH)2 Mg(OH)2 sa vzhľadom na malú rozpustnosť vo vode správa ako slabá zásada. Ostatné hydroxidy kovov alkalických zemín Ca(OH)2, Sr(OH)2 a Ba(OH)2 sú silné zásady.
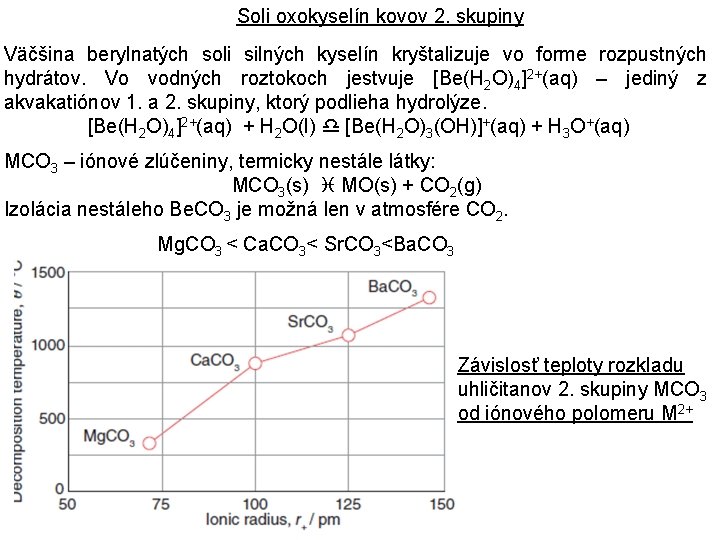
Soli oxokyselín kovov 2. skupiny Väčšina berylnatých soli silných kyselín kryštalizuje vo forme rozpustných hydrátov. Vo vodných roztokoch jestvuje [Be(H 2 O)4]2+(aq) – jediný z akvakatiónov 1. a 2. skupiny, ktorý podlieha hydrolýze. [Be(H 2 O)4]2+(aq) + H 2 O(l) [Be(H 2 O)3(OH)]+(aq) + H 3 O+(aq) MCO 3 – iónové zlúčeniny, termicky nestále látky: MCO 3(s) MO(s) + CO 2(g) Izolácia nestáleho Be. CO 3 je možná len v atmosfére CO 2. Mg. CO 3 < Ca. CO 3< Sr. CO 3<Ba. CO 3 Závislosť teploty rozkladu uhličitanov 2. skupiny MCO 3 od iónového polomeru M 2+

MCO 3 sú vo vode málo rozpustné. Uhličitany MCO 3 sa rozpúšťajú vo vodných roztokoch CO 2: MCO 3(s) + CO 2(g) + H 2 O(l) M(HCO 3)2(aq) – stále len vo vod. roztoku sýtenom CO 2. V tuhom stave neboli izolované. Tvrdá voda obsahuje ióny Mg 2+ a Ca 2+ - tieto Ióny tvoria zrazeniny so stearátovými aniónmi z mydiel – povlak na vaniach a umývadlách. Prechodná tvrdosť vody – spôsobená Mg(HCO 3)2(aq) a Ca(HCO 3)2(aq) – môžeme odstraniť varom: Ca(HCO 3)2(aq) Ca. CO 3(s) + CO 2(g) + H 2 O(l) alebo reakciou s Ca(OH)2: Ca(HCO 3)2(aq) + Ca(OH)2(aq) 2 Ca. CO 3(s) + H 2 O(l) Trvalá tvrdosť vody – je spôsobená inými soľami Mg 2+ a Ca 2+ (napr. síranmi). Odstraňujú sa zmäkčovaním vody pomocou meniča katiónov, ktorými sa nechá tvrdá voda pretekať. Pracie prášky obsahujú prídavné látky, ktoré ióny Mg 2+ a Ca 2+ z vody odstraňujú. K tomu sa používajú polyfosforečnany, v poslednej dobe sa dáva prednosť zeolitom. Reakciou uhličitanov alkalických kovov s berylnatými a horečnatými zlúčeninami sa tvoria hydroxid-uhličitany (Mg. CO 3. Mg(OH)2. 4 H 2 O)
![Koordinačné zlúčeniny prvkov 2. skupiny Hexakarboxyláto-oxoberylnáte komplexy [Be 4 O(RCOO)6] (R = H, R Koordinačné zlúčeniny prvkov 2. skupiny Hexakarboxyláto-oxoberylnáte komplexy [Be 4 O(RCOO)6] (R = H, R](http://slidetodoc.com/presentation_image_h2/6c66ba64dea2986ab039ddf6277a5033/image-28.jpg)
Koordinačné zlúčeniny prvkov 2. skupiny Hexakarboxyláto-oxoberylnáte komplexy [Be 4 O(RCOO)6] (R = H, R a Ar). Štvorväzbový atóm kyslíka v strede tetraédra – vo vrcholoch atómy Be (Be 4 O) – tieto sú tetraédrické. Štruktúrny typ obsahujúci jednotky M 4 O sa vyskytuje s rôznymi mostíkovými ligandmi aj pre atómy Mg(II), Zn(II), Cu(II), Ni(II), Co(II) a Fe(II). [Be 4 O(Me. COO)6] Kovy alkalických zemín – tvoria veľkú skupinu KZ s N-, O- a S-donorovými acyklickými chelát. ligandmi (napr. s etyléndiamino-tetracetátovým(4 -) a. - edta 4 -) M 2+(aq)+edta 4 -(aq) [M(edta)]2 -(aq) (M = Mg, Ca, Sr, . . ) Štruktrúra [M(edta)]2 -
![[M(edta)]2 - - päťčlánkových chelátových kruhov (metalocykly), veľká stabilita týchto KZ. Komplexometrické stanovenie iónov [M(edta)]2 - - päťčlánkových chelátových kruhov (metalocykly), veľká stabilita týchto KZ. Komplexometrické stanovenie iónov](http://slidetodoc.com/presentation_image_h2/6c66ba64dea2986ab039ddf6277a5033/image-29.jpg)
[M(edta)]2 - - päťčlánkových chelátových kruhov (metalocykly), veľká stabilita týchto KZ. Komplexometrické stanovenie iónov kovových prvkov (Ni 2+, Co 2+ a pod. ). Organokovové zlúčeniny Be a Mg Grignardove reagenty – roztoky vznikajúce pomalým pridávaním RX alebo Ar. X (X = Cl, Br a I) do suspenzie Mg stružlín vo vhodnom org. rozpúšťadle (Et 2 O, THF, C 6 H 6) za stáleho miešania a vylúčenia vzduchu a vlhkosti. Reakcia: Mg(s) + RX(solv) RMg. X(solv) Štruktúra [Mg. Br. Et(Et 2 O)2] Štruktúra [Mg(edta)(H 2 O)]2 -

10. 9 Vysvetlite spôsob vzniku jaskýň v ložiskách vápenca. Riešenie: Dažďová voda obsahujúca CO 2 presakuje do vápencových ložísk a reaguje s Ca. CO 3 : Ca. CO 3(s) + CO 2(g) + H 2 O(l) Ca(HCO 3)2(aq) 10. 13 Stručne diskutujte diagonálnu podobnosť chémie berýlia a hliníka. Riešenie: Na povrchu oboch kovov sa tvoria povlaky oxidov, ktoré ich pasivujú; Be aj Mg sú amfotérne kovy, ktoré tvoria anióny [Be(OH)4]2 a [Al(OH)4] ; obidva kovy tvoria karbidy obsahujúce anión C 4. 10. 17 Z akého minerálu (napíšte vzorec) obsahujúceho vápnik sa skladajú kosti stavovcov? Riešenie: tris(fosforečnan)-hydroxid pentavápenatý Ca 5(OH)(PO 4)3.
- Slides: 30