Prvention de la maladie thromboembolique veineuse chez les

Prévention de la maladie thrombo-embolique veineuse chez les patients médicaux Bruno TRIBOUT Médecine Vasculaire CHU AMIENS

Prévention MTEV lors Accident Vasculaire Cérébral

Prévention MTEV lors AVC ischémique : méta-analyses (1) Essais TVP / N patients RRRelatif incidence TVP [IC 95%] 4 161 / 257 63% [ 57 - 69 %] faible dose 2 47 / 202 23% [ 17 - 29 %] - 63% HBPM 4 27 / 167 16% [ 10 - 22 %] - 75% Contrôles HNF Danaparoïde Clagett ACCP 1998

Prévention MTEV par anticoagulants lors AVC ischémique : méta-analyses (2) 15 essais (n=1599) réduction [IC 95%] risque absolu* Nb patients à traiter# TVP (n=916) - 28 % [ 23 à 33% ] 3, 6 EP - 0, 4 % [ 0, 1 à 0, 6% ] 250 *nombre d ’évènements évités pour 100 patients traités # nombre de patients à traiter pour éviter 1 évènement Gubitz GJ, Sandercock PAG Drugs & Aging 1999; 15: 29 -36
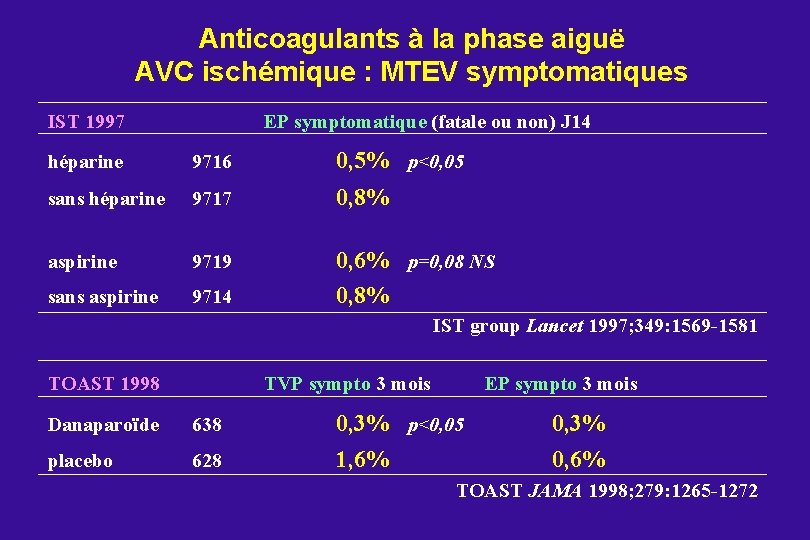
Anticoagulants à la phase aiguë AVC ischémique : MTEV symptomatiques IST 1997 EP symptomatique (fatale ou non) J 14 héparine 9716 0, 5% p<0, 05 sans héparine 9717 0, 8% aspirine 9719 sans aspirine 9714 0, 6% p=0, 08 NS 0, 8% IST group Lancet 1997; 349: 1569 -1581 TOAST 1998 TVP sympto 3 mois EP sympto 3 mois Danaparoïde 638 0, 3% p<0, 05 0, 3% placebo 628 1, 6% 0, 6% TOAST JAMA 1998; 279: 1265 -1272

International Stroke Trial : HNF et/ou Aspirine, rien (1) AVC aigü 48 h hémorragie intra-crânienne au scanner systématique indications ou contre-indications à héparine ou aspirine faible bénéfice potentiel : résolution en qq heures Inclusion : Exclusions : handicap sévère préalable risque accru effets indésirables : - allergie aspirine, - ulcère gastroduodénal actif ou hémorragie digestive récente, - déjà sous anticoagulants au long cours

International Stroke Trial : HNF et/ou Aspirine, rien (2) Traitement : administration en ouvert Héparine HNF sous-cutanée 5000 UI 2 x/j (25%) HNF sous-cutanée 12500 UI 2 x/j (25%) : adaptation TCA optionnelle sans héparine (50%) Aspirine : poursuite autorisée AINS aspirine 300 mg/j (50%) : sonde gastrique, suppositoire ou IV si nécessaire sans aspirine (50%) phase aiguë : durée 14 j puis

International Stroke Trial : HNF et/ou Aspirine, rien (3) Critères : Primaires mortalité globale à J 14 décès ou dépendance nécessitant une tierce personne à 6 mois Secondaires AVC hémorragique symptomatique confirmé objectivement à J 14 AVC ischémique ou type non précisé à J 14 hémorragie majeure extra-crânienne : décès ou tranfusion à J 14 embolie pulmonaire symptomatique ou fatale J 14 mortalité globale à 6 mois dépendance ou récupération incomplète à 6 mois

International Stroke Trial : HNF et/ou Aspirine, rien (4) Caractéristiques des patients étude mondiale : 19435 patients âge > 70 ans : 61 % ; âge > 80 ans : 26 % trouble de la conscience : 23 % fibrillation auriculaire : 16 % PA systolique > 180 mm. Hg : 28 % AVC lacunaire : 24 % médiane randomisation : 19 h Scanner non réalisé : 4 % antithrombotiques avant inclusion : aspirine 20 % ; héparine 2 % perdus de vue : 0, 8 % à 6 mois IST Lancet 1997; 349: 1569 -1581

International Stroke Trial : HNF et/ou Aspirine, rien (5) Analyse par sous-groupes Fibrillation auriculaire : 3169 (16%) et héparine sans héparine avec héparine FA sans FA récidive AVC ischémique J 14 4, 9 % 3, 6 % 2, 8 % 2, 9 % AVC hémorragique 0, 4 %

International Stroke Trial : HNF et/ou Aspirine, rien (5) Analyse par sous-groupes Fibrillation auriculaire : 3169 (16%) et aspirine sans aspirine avec aspirine FA sans FA récidive AVC ischémique J 14 4, 5 % 3, 8 % 3, 3 % 2, 7 % AVC hémorragique 1, 1 % 0, 7 %
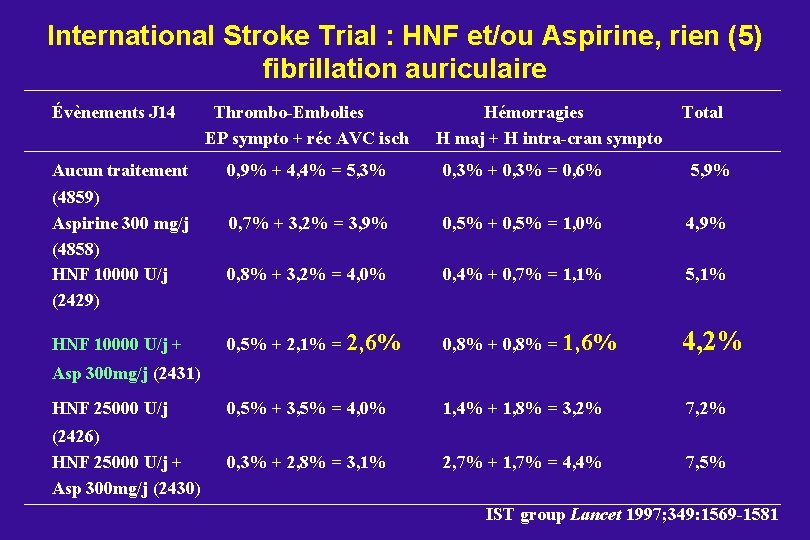
International Stroke Trial : HNF et/ou Aspirine, rien (5) fibrillation auriculaire Évènements J 14 Aucun traitement Thrombo-Embolies EP sympto + réc AVC isch Hémorragies H maj + H intra-cran sympto Total 0, 9% + 4, 4% = 5, 3% 0, 3% + 0, 3% = 0, 6% 5, 9% 0, 7% + 3, 2% = 3, 9% 0, 5% + 0, 5% = 1, 0% 4, 9% 0, 8% + 3, 2% = 4, 0% 0, 4% + 0, 7% = 1, 1% 5, 1% 0, 5% + 2, 1% = 2, 6% 0, 8% + 0, 8% = 1, 6% 4, 2% HNF 25000 U/j 0, 5% + 3, 5% = 4, 0% 1, 4% + 1, 8% = 3, 2% 7, 2% (2426) HNF 25000 U/j + Asp 300 mg/j (2430) 0, 3% + 2, 8% = 3, 1% 2, 7% + 1, 7% = 4, 4% 7, 5% (4859) Aspirine 300 mg/j (4858) HNF 10000 U/j (2429) HNF 10000 U/j + Asp 300 mg/j (2431) IST group Lancet 1997; 349: 1569 -1581
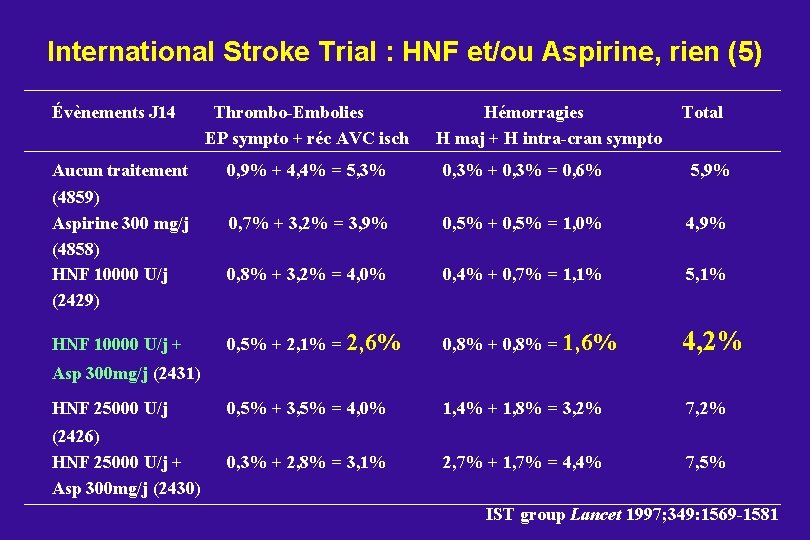
International Stroke Trial : HNF et/ou Aspirine, rien (5) Évènements J 14 Aucun traitement Thrombo-Embolies EP sympto + réc AVC isch Hémorragies H maj + H intra-cran sympto Total 0, 9% + 4, 4% = 5, 3% 0, 3% + 0, 3% = 0, 6% 5, 9% 0, 7% + 3, 2% = 3, 9% 0, 5% + 0, 5% = 1, 0% 4, 9% 0, 8% + 3, 2% = 4, 0% 0, 4% + 0, 7% = 1, 1% 5, 1% 0, 5% + 2, 1% = 2, 6% 0, 8% + 0, 8% = 1, 6% 4, 2% HNF 25000 U/j 0, 5% + 3, 5% = 4, 0% 1, 4% + 1, 8% = 3, 2% 7, 2% (2426) HNF 25000 U/j + Asp 300 mg/j (2430) 0, 3% + 2, 8% = 3, 1% 2, 7% + 1, 7% = 4, 4% 7, 5% (4859) Aspirine 300 mg/j (4858) HNF 10000 U/j (2429) HNF 10000 U/j + Asp 300 mg/j (2431) IST group Lancet 1997; 349: 1569 -1581
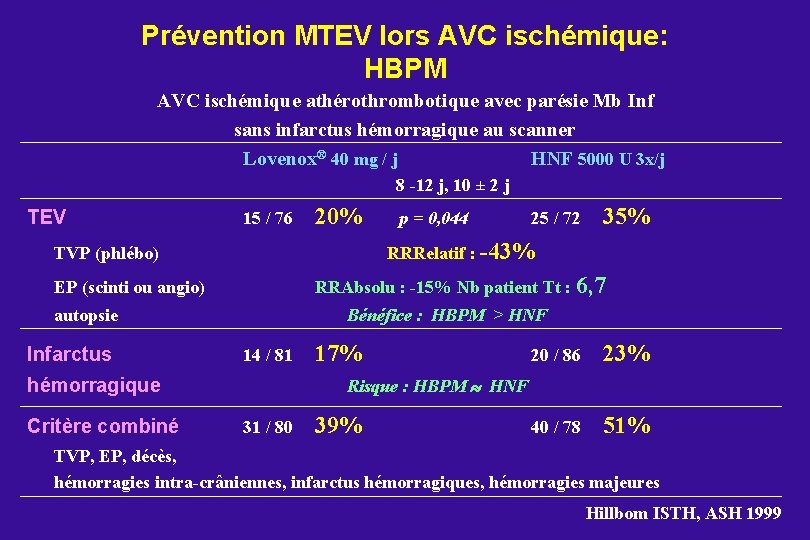
Prévention MTEV lors AVC ischémique: HBPM AVC ischémique athérothrombotique avec parésie Mb Inf sans infarctus hémorragique au scanner Lovenox® 40 mg / j HNF 5000 U 3 x/j 8 -12 j, 10 ± 2 j TEV 15 / 76 20% 35% RRAbsolu : -15% Nb patient Tt : 6, 7 EP (scinti ou angio) autopsie Bénéfice : HBPM > HNF 14 / 81 17% 20 / 86 23% 40 / 78 51% Risque : HBPM HNF hémorragique Critère combiné 25 / 72 RRRelatif : -43% TVP (phlébo) Infarctus p = 0, 044 31 / 80 39% TVP, EP, décès, hémorragies intra-crâniennes, infarctus hémorragiques, hémorragies majeures Hillbom ISTH, ASH 1999

Prévention MTEV lors Infarctus du Myocarde
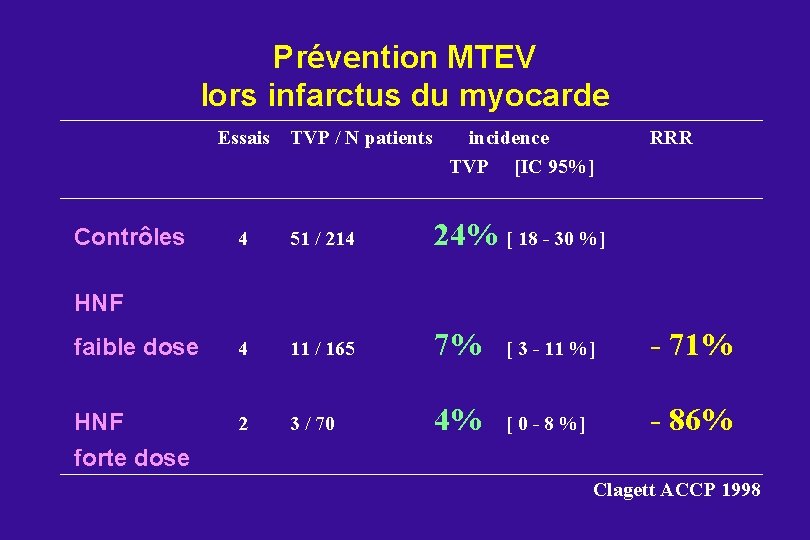
Prévention MTEV lors infarctus du myocarde Essais TVP / N patients incidence TVP [IC 95%] RRR 4 51 / 214 24% [ 18 - 30 %] faible dose 4 11 / 165 7% [ 3 - 11 %] - 71% HNF 2 3 / 70 4% [ 0 - 8 %] - 86% Contrôles HNF forte dose Clagett ACCP 1998
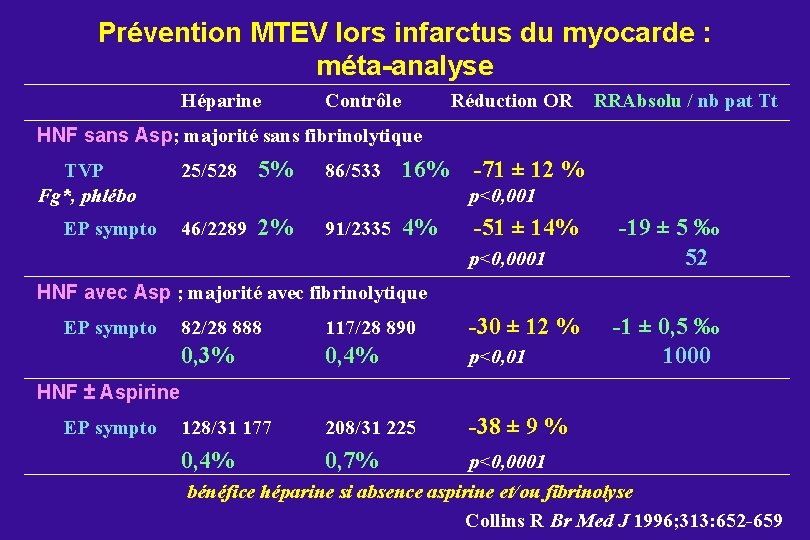
Prévention MTEV lors infarctus du myocarde : méta-analyse Héparine Contrôle Réduction OR RRAbsolu / nb pat Tt HNF sans Asp; majorité sans fibrinolytique TVP Fg*, phlébo EP sympto 25/528 5% 86/533 16% -71 ± 12 % p<0, 001 46/2289 2% 91/2335 4% -51 ± 14% p<0, 0001 -19 ± 5 ‰ 52 HNF avec Asp ; majorité avec fibrinolytique EP sympto 82/28 888 117/28 890 -30 ± 12 % 0, 3% 0, 4% p<0, 01 128/31 177 208/31 225 -38 ± 9 % 0, 4% 0, 7% -1 ± 0, 5 ‰ 1000 HNF ± Aspirine EP sympto p<0, 0001 bénéfice héparine si absence aspirine et/ou fibrinolyse Collins R Br Med J 1996; 313: 652 -659

Prévention de MTEV chez les patients Cancéreux Médicaux

Facteurs de risque de MTEV lors Cancer Chimiothérapie Tamoxifène Cathéters veineux centraux Stade du K : Stade IV (M+) > Stade II masse tumorale, comorbidité Comorbidités associées : chirurgie, alitement, infection Levine MN Thromb Haemost 1997; 78: 133 -136
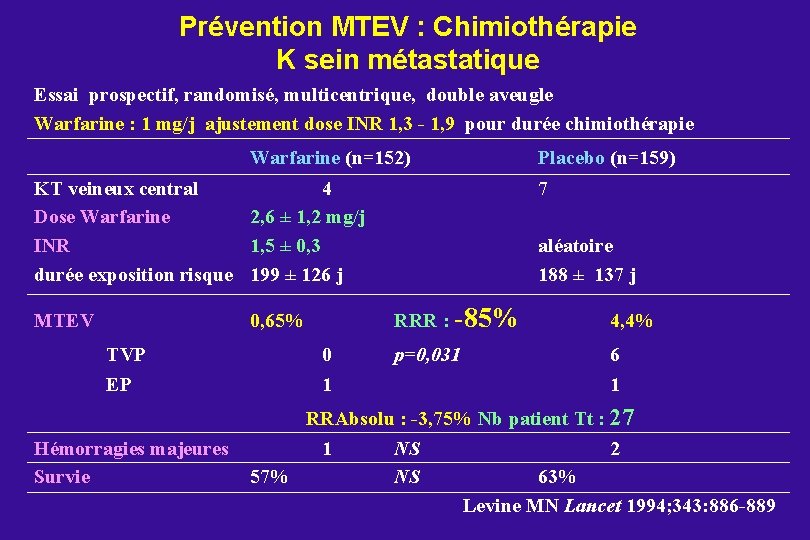
Prévention MTEV : Chimiothérapie K sein métastatique Essai prospectif, randomisé, multicentrique, double aveugle Warfarine : 1 mg/j ajustement dose INR 1, 3 - 1, 9 pour durée chimiothérapie Warfarine (n=152) KT veineux central 4 Dose Warfarine 2, 6 ± 1, 2 mg/j INR 1, 5 ± 0, 3 durée exposition risque 199 ± 126 j MTEV 0, 65% TVP 0 EP 1 Hémorragies majeures Survie Placebo (n=159) 7 aléatoire 188 ± 137 j RRR : -85% 4, 4% p=0, 031 6 1 RRAbsolu : -3, 75% Nb patient Tt : 27 1 NS 2 57% NS 63% Levine MN Lancet 1994; 343: 886 -889

Prévention thromboses cathéters veineux centraux chez cancéreux : warfarine faible dose Essai prospectif, randomisé, ouvert KT veineux central sous-clavier + chambre implantable : flush héparine, prélèvements sanguins Warfarine 1 mg/j débuté 3 j avant insertion 90 j : TP-INR non modifié Warfarine (n=42) TVP phlébo J 90 4/42 Contrôle (n=40) 9, 5% RRR : -74% 15/40 37, 5% p<0, 001 RRAbsolu : -28% Nb patient Tt : 3, 6 TVP sympto/TVP phlébo 4/4 10/15 Bern MM Ann Intern Med 1990; 112: 423 -428

Prévention thromboses cathéters veineux centraux chez cancéreux : HBPM Essai prospectif, randomisé, ouvert KT veineux central sous-clavier + chambre implantable : flush héparine Fragmine® 2500 UI sc/j débutée 2 h avant insertion 90 j TVP phlébo J 90 Fragmine® (n=16) Contrôle (n=13) 1/16 8/13 6% 62% p=0, 002 RR : 6, 75 [1, 05 - 43, 58] RRRelatif : -90% Hémorragies RRAbsolu : -56% Nb patient Tt : 1, 8 0 0 arrêt prématuré essai bénéfice observé Monreal M Thromb Haemost 1996; 75: 251 -253

Recommandations pour prévention MTEV chez les patients cancéreux médicaux Indication Cathéter veineux central Prophylaxie 1) Warfarine 1 mg/j si échec 2) Fragmine® 2500 UI/j Patient ambulatoire Warfarine faible dose ATCD MTEV INR cible : 1, 5 [1, 3 - 1, 9] compression par masse pelvienne chimiothérapie Patient alité HNF ou HBPM Levine MN Thromb Haemost 1997; 78: 133 -136

Prévention de MTEV en Réanimation Médicale

MTEV en Réanimation Médicale u Neuhaus 1978 EP autopsie 27 % Décompensation respiratoire u Hirsh 1995 Dec Resp, H digestive, Dec Cardiaque, Sepsis écho-doppler veineux 2 x/sem + 1 sem après sortie réa TVP 33% TVP distale 12 % TVP proximale 16 % TVP mb sup 5 % (KT veineux central) Malgré prophylaxie effectuée chez 61 % Aucun F Risque individualisable prédictif survenue TVP en dehors séjour Réa u Holzapfel 1996 Ventilation mécanique pour Dec BPCO avec écho-doppler initial normal TVP phlébo (J 10 5) groupe placebo 28 % TVP distales TVP proximales 20 % 8%

Prévention MTEV en réanimation médicale HBPM Essai randomisé, multicentrique, double aveugle Ventilation mécanique pour décompensation respiratoire aiguë BPCO avec écho-doppler initial normal (n = 223) Fraxiparine® 0, 4 ml / j si < 70 kg Placebo (n = 109) 0, 6 ml / j si > 70 kg (n = 114) délai 24 h - durée 10 ± 5 j âge 69, 4 ± 7, 7 ans p=0, 02 66, 8 ± 8, 2 ans TVP phlébo 12/84 TVP distales TVP proximales 14 % 11% 3% p=0, 03 RRRelatif : -50% RRAbsolu : -14% 24/86 28 % 20 % 8% Nb patient Tt : 7, 1 Hémorragies 5% 8% Holzapfel L, Fraisse F Am J Respiratory Critical Care Med 1996; 153: Abstract A 96

Prévention MTEV chez patients médicaux : données avant MEDENOX
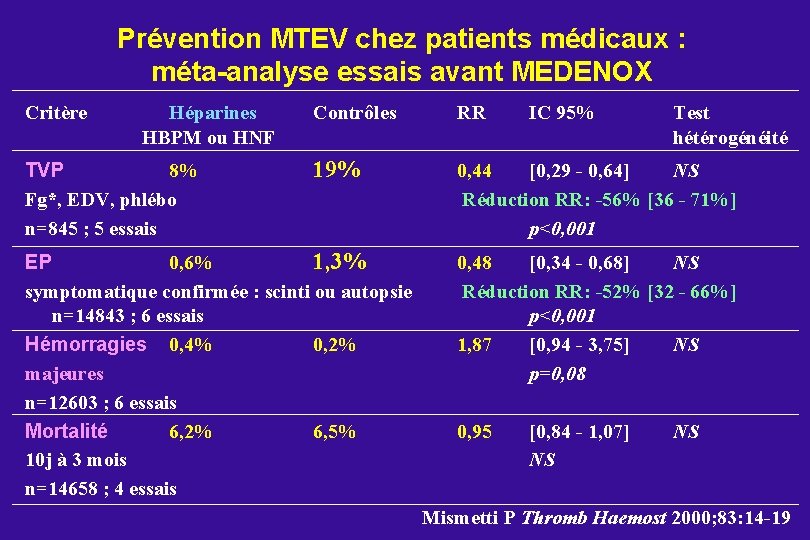
Prévention MTEV chez patients médicaux : méta-analyse essais avant MEDENOX Critère Héparines HBPM ou HNF TVP 8% Fg*, EDV, phlébo n=845 ; 5 essais Contrôles RR 19% 0, 44 [0, 29 - 0, 64] NS Réduction RR: -56% [36 - 71%] p<0, 001 EP 0, 6% 1, 3% symptomatique confirmée : scinti ou autopsie n=14843 ; 6 essais Hémorragies 0, 4% 0, 2% majeures n=12603 ; 6 essais Mortalité 6, 2% 6, 5% 10 j à 3 mois n=14658 ; 4 essais IC 95% Test hétérogénéité 0, 48 [0, 34 - 0, 68] NS Réduction RR: -52% [32 - 66%] p<0, 001 1, 87 [0, 94 - 3, 75] NS p=0, 08 0, 95 [0, 84 - 1, 07] NS NS Mismetti P Thromb Haemost 2000; 83: 14 -19
- Slides: 28