Prvek chemick ltka sloen z atom vtinou neslouench









- Slides: 12

Prvek = chemická látka složená z atomů (většinou nesloučených) se stejným Z charakterizován : – značkou – názvem – protonovým číslem Z

Prvek vznik názvů podle: – – vlastnosti – Cl – žlutozelený zdroje výskytu – Ca – vápenec, H – voda země objevu – Ge – Německo významného vědce – Nobelium

Prvek prvky dělím na: Kovy • tepelně a elektricky vodivé • za běžných podmínek pevné (výjimka rtuť) • kovově lesklé, dobře opracovatelné (kujné, tažné) • tvoří přibližně 80% všech prvků • často podléhají korozi – chemická a fyzikální změna na povrchu kovů působením vlhkosti, kyslíku apod. • slitiny = směsí roztavených kovů → zlepšení vlastností

Prvek Nekovy • nemají vlastnosti kovů nebo jen některé z nich • pevné, kapalné i plynné • asi 15

Prvek Polokovy • přechod mezi kovy a nekovy • vzhledem připomínají kovy, vlastnostmi nekovy • většinou křehké, nejsou kujné, malá elektrická vodivost – zvyšuje se po zahřátí

Prvek • všechny prvky jsou dle protonového čísla uspořádány do PSP Struktura atomů: H Si Ca

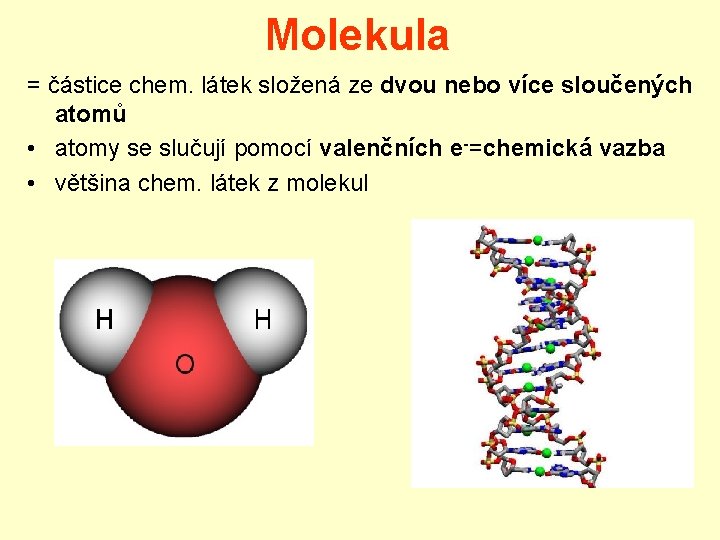
Molekula = částice chem. látek složená ze dvou nebo více sloučených atomů • atomy se slučují pomocí valenčních e-=chemická vazba • většina chem. látek z molekul

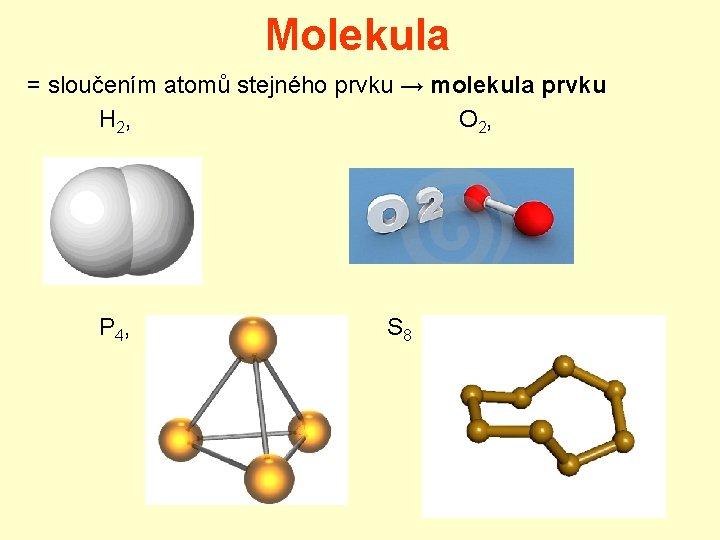
Molekula = sloučením atomů stejného prvku → molekula prvku H 2, O 2, P 4, S 8

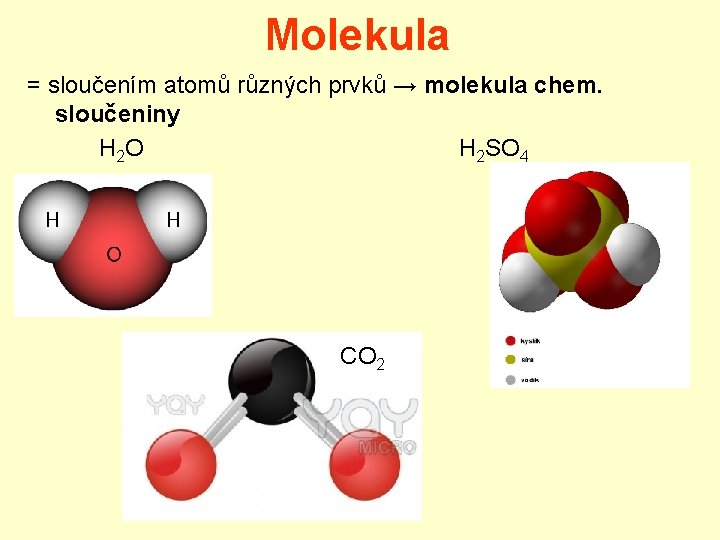
Molekula = sloučením atomů různých prvků → molekula chem. sloučeniny H 2 O H 2 SO 4 CO 2

Molekula Chem. sloučenina = chem. látka složená ze sloučených atomů 2 nebo více prvků • vznik sloučeniny H + H→ H 2

Molekula Atom, který má ve valenční vrstvě více nepárových e-, může vytvářet více chem. vazeb s atomy stejného nebo i jiných prvků • Podle toho, kolik chem vazeb je atom schopen vytvořit se hodnotí jeho vaznost • prvky mohou být ve sloučeninách maximálně osmivazné

Molekula Př: • O – 2 nepárové e- →vazby s atomy vodíku → v molekule H 2 O je atom O dvouvazný