Prrentre en Chimie Sance n 1 Fiche n







- Slides: 14

Prérentrée en Chimie Séance n 1. Fiche n 12 b Conversion et unités Septembre 2020 Carole Marbeuf-Gueye CONSEIL: Regarder ce document sous powerpoint en format diaporama grand écran pour profiter des animations…et réfléchir aux questions avant les réponses

Programme Mise à niveau chimie 2020: *ATOME (fiches n 1 à 5) 1. 1 Description atome 1. 2 Quantité de matière et NAvogadro 1. 3 intro nombres quantiques , orbitales atomiques et Configurations électroniques 1. 4 Tableau périodique 1. 5 Intro sur rayon atomique, énergie d’ionisation , affinité électronique; électronégativité entre 2 atomes *MOLECULE (fiches n 6 à 8) 2. 1 Initiation aux Formules de Lewis 2. 2 Dessins d’une tétraèdre 2. 3 Dessin dans l’espace de molécules: erreurs à éviter *REACTIONS (fiches n 9 à 10) 3. 1 Équilibrer une équation chimique, stoechiométrie 3. 2. échanges d’énergie 3. 3 vitesses de réaction légendes • « Oui Si » : partie non prioritaire sera vu en L 1 et L 1 sem 2 L 2 * étudiants de médecine LAS et PAS: fiches conseillées avant cours chimie orga du Socle *Pour les TP (fiche n 11) * Notations/Calculs en chimie (fiche 12 a)/conversion et unités (fiche n 12 b)

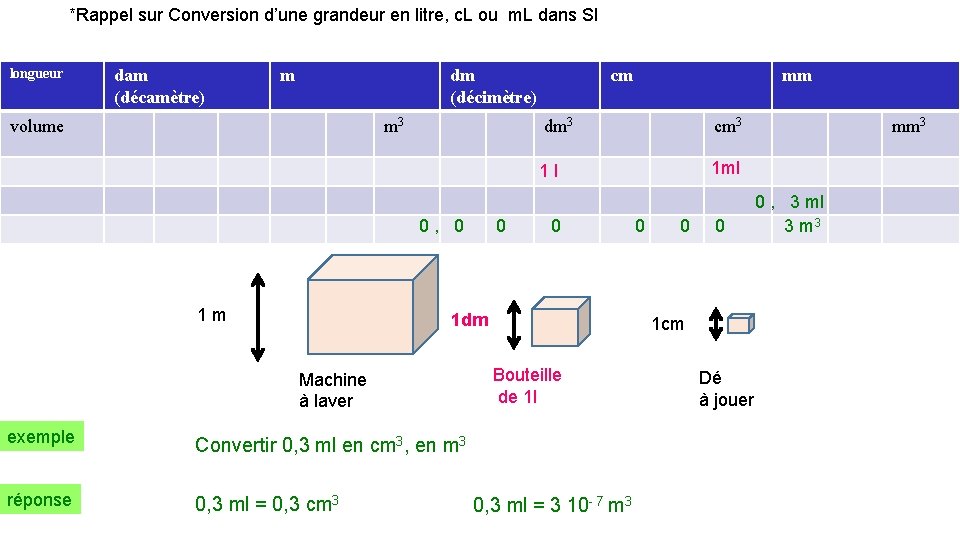
*Rappel sur Conversion d’une grandeur en litre, c. L ou m. L dans SI longueur dam (décamètre) m dm (décimètre) volume m 3 cm dm 3 cm 3 1 l 1 ml 0 , 0 0 1 m 1 dm Machine à laver exemple Convertir 0, 3 ml en cm 3, en m 3 réponse 0, 3 ml = 0, 3 cm 3 mm 0 , 3 ml 0 0 0 3 m 3 1 cm Bouteille de 1 l 0, 3 ml = 3 10 - 7 m 3 Dé à jouer mm 3

Toutes les promo *Testez vos connaissances sur les unités du Système international (SI )! Compléter le tableau des pages suivantes (Lorsqu’il y a plusieurs choix d’unité pour une grandeur donnée, souligner l'unité du S. I. et convertir les autres unités. )

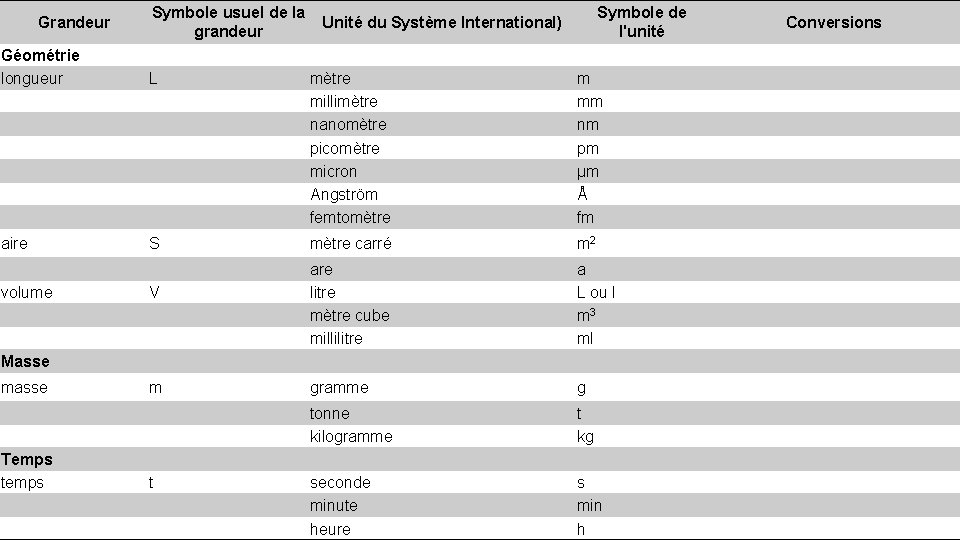
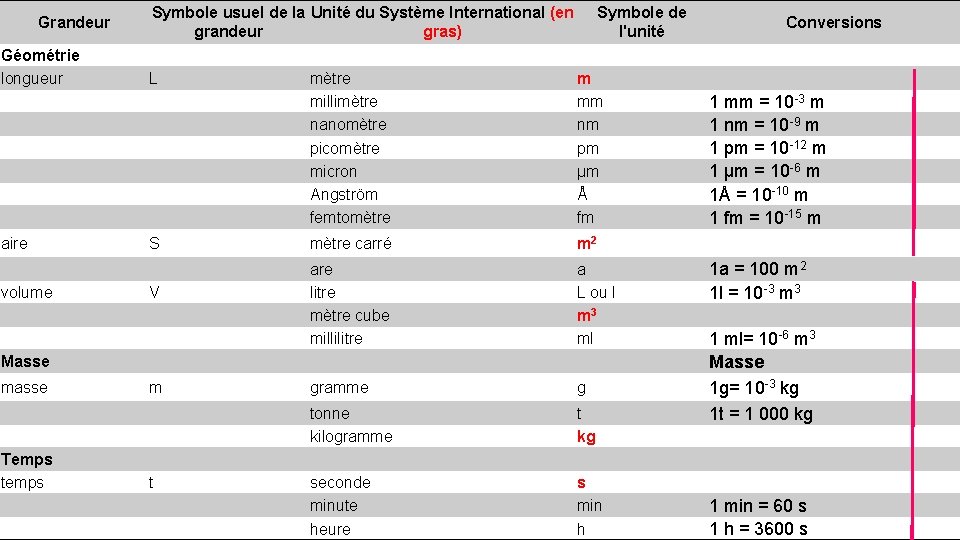
Grandeur Symbole usuel de la Unité du Système International) grandeur Symbole de l'unité Géométrie longueur L mètre millimètre nanomètre picomètre micron Angström femtomètre m mm nm pm µm Å fm aire S mètre carré m 2 are litre mètre cube millilitre a L ou l m 3 ml gramme g tonne kilogramme t kg seconde minute heure s min h volume V Masse masse Temps temps m t Conversions

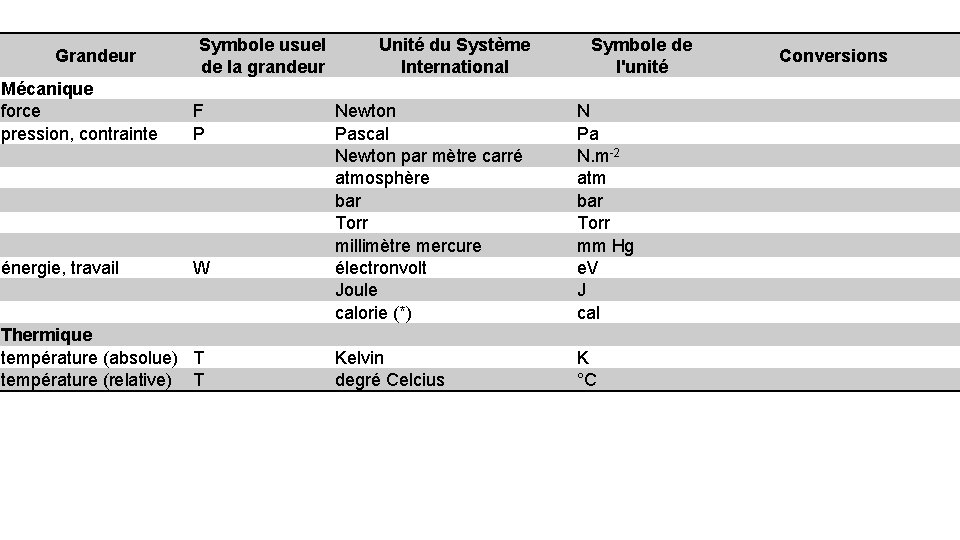
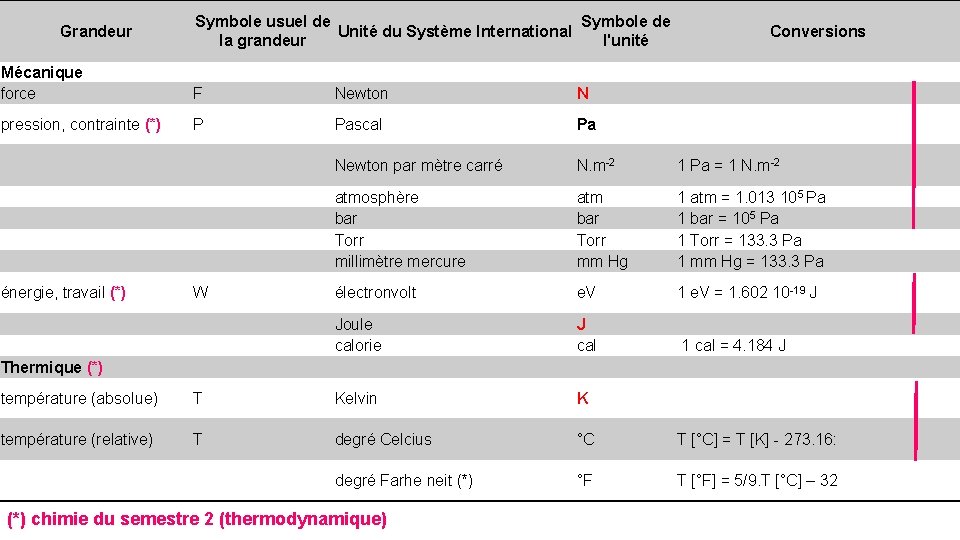
Grandeur Symbole usuel de la grandeur Mécanique force pression, contrainte F P énergie, travail W Thermique température (absolue) T température (relative) T Unité du Système International Symbole de l'unité Newton Pascal Newton par mètre carré atmosphère bar Torr millimètre mercure électronvolt Joule calorie (*) N Pa N. m-2 atm bar Torr mm Hg e. V J cal Kelvin degré Celcius K °C Conversions

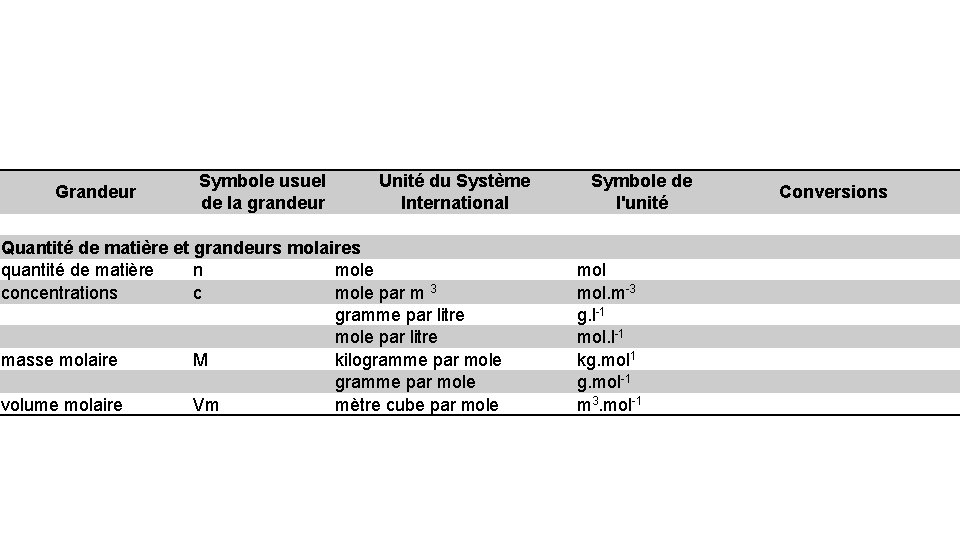
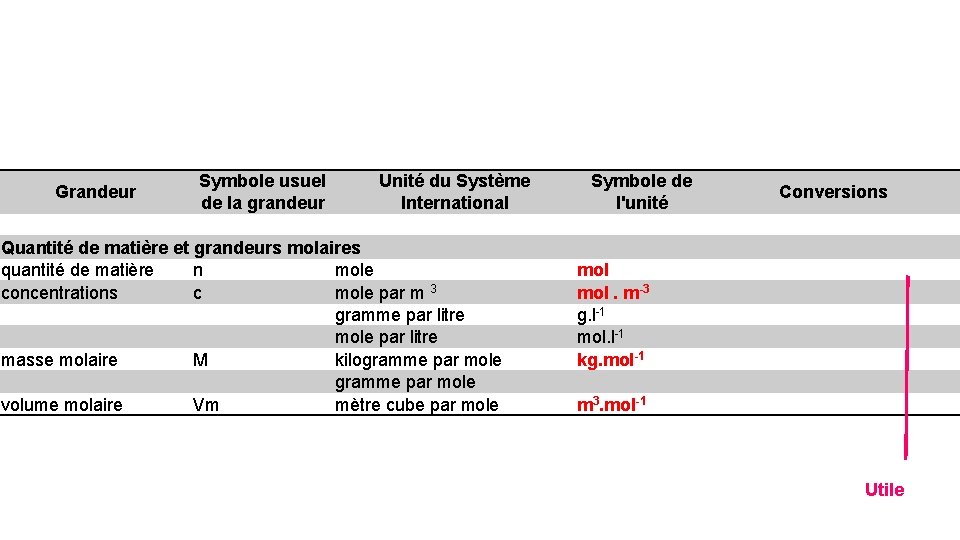
Grandeur Symbole usuel de la grandeur Unité du Système International Quantité de matière et grandeurs molaires quantité de matière n mole concentrations c mole par m 3 gramme par litre mole par litre masse molaire M kilogramme par mole volume molaire Vm mètre cube par mole Symbole de l'unité mol. m-3 g. l-1 mol. l-1 kg. mol 1 g. mol-1 m 3. mol-1 Conversions

Grandeur Géométrie longueur aire volume Symbole usuel de la Unité du Système International (en grandeur gras) L S V Symbole de l'unité mètre millimètre nanomètre picomètre micron Angström femtomètre m mm nm pm µm Å fm mètre carré m 2 are litre mètre cube millilitre a L ou l m 3 ml gramme g tonne kilogramme t kg seconde minute heure s min h Masse masse Temps temps m t Conversions 1 mm = 10 -3 m 1 nm = 10 -9 m 1 pm = 10 -12 m 1 µm = 10 -6 m 1Å = 10 -10 m 1 fm = 10 -15 m 1 a = 100 m 2 1 l = 10 -3 m 3 1 ml= 10 -6 m 3 Masse 1 g= 10 -3 kg 1 t = 1 000 kg 1 min = 60 s 1 h = 3600 s

Grandeur Symbole usuel de Symbole de Unité du Système International la grandeur l'unité Conversions Mécanique force F Newton N pression, contrainte (*) P Pascal Pa Newton par mètre carré N. m-2 1 Pa = 1 N. m-2 atmosphère bar Torr millimètre mercure atm bar Torr mm Hg 1 atm = 1. 013 105 Pa 1 bar = 105 Pa 1 Torr = 133. 3 Pa 1 mm Hg = 133. 3 Pa électronvolt e. V 1 e. V = 1. 602 10 -19 J Joule calorie J cal 1 cal = 4. 184 J énergie, travail (*) W Thermique (*) température (absolue) T Kelvin K température (relative) T degré Celcius °C T [°C] = T [K] - 273. 16: degré Farhe neit (*) °F T [°F] = 5/9. T [°C] – 32 (*) chimie du semestre 2 (thermodynamique)

Grandeur Symbole usuel de la grandeur Unité du Système International Quantité de matière et grandeurs molaires quantité de matière n mole concentrations c mole par m 3 gramme par litre mole par litre masse molaire M kilogramme par mole volume molaire Vm mètre cube par mole Symbole de l'unité Conversions mol. m-3 g. l-1 mol. l-1 kg. mol-1 m 3. mol-1 Utile

Explication pour la conversion entre l’unité de masse atomique (u. m. a) et le g ou kg (ED 1 atomistique du parcours LSV 1) Définition de l’u. m. a : 1 u. m. a est égale à 1/12ème de la masse d’un atome de carbone 12 C Définition du nombre d’Avogadro NA : réponse 12 g de carbone 12 C contient exactement NA atomes de 12 C 1 u. m. a= (1/12 ) m (12 C ) = 12/ NA avec NA = 6. 02252 10 23 d’où le facteur de conversion entre u. m. a et kg : 1 u. ma = 1/12 (12/ NA) 1 u. ma pour un atome “correspondra” à 1 g. mol-1 pour sa masse molaire = 1/ NA g 1 u. ma = 1. 6604 10 -24 g 1 u. m. a = 1. 6604 10 -27 kg

Conversions d’énergie: e. V en J , rydberg en J ou e. V * Comment retrouver la conversion des e. V en J ? travail électrique (Wél) que subit un e- soumis à une différence de potentiel de 1 V : |Wél | = | q V | Charge élémentaire q = 1, 602 10 -19 C réponse Il suffit de savoir qu’un travail est en J puisque [W] a la grandeur d’une énergie: ML 2 T-2 (voir prérentrée physique pour équation aux dimensions ) un e- soumis à une différence de potentiel de 1 V subit le travail : Wél = | q V | W électrique = 1 e. V = 1, 602 10 -19 1 V = 1, 602 10 -19 J (unité en atomistique) d’où 1 e. V = 1. 602 10 -19 J

* Comment retrouver la Conversion entre des Joules (J) et des Rydberg (Ry) Constante de Rydberg : RH = 1, 097 107 m-1 Constante de Planck : h = 6, 626 10 -34 J. s 1 Rydberg : 1 Ry = h. c. RH réponses - Équation aux dimensions du Rydberg (Ry) et de la constante de Rydberg RH: [Ry]= [h c RH] = (ML 2 T-2. T) ( L. T-1) (L-1) = ML 2 T-2 c’est une énergie (Autre manière, en utilisant En = - Ry / n 2) donc la relation entre l’unité d’énergie Ry et le J est : 1 Ry = 6. 626 10 -34 2. 99 10 8 1. 097 10 7 = 2, 173 10 -18 J (1 Ry Unité en atomistique et spectroscopie = 2, 173 10 -18 /1. 602 10 -19 )e. V = 13. 6 e. V ) Pas au prog du parcours médecine

Bilan de vos réponses… 3 points importants: 1) Avez-vous fait une erreur sur les exemples de sous-multiples d’unité? 2) Avez-vous commis l’erreur de considérer que les grandeurs telles que des concentrations en mol. l-1, des volumes en litre , des masse en g sont dans le SI ? 3) Savez-vous retrouver facilement la conversion des e. V en J ?