Protenas y transporte de O 2 Hemoglobina y

Proteínas y transporte de O 2 Hemoglobina y mioglobina (Relación estructura: función) Dr. Luis A. Mora B. Cátedra de Bioquímica UCIMED

Introducción La función de las proteínas depende de su estructura y de los cambios conformacionales que puedan llevar a cabo. Proteínas de transporte de oxígeno: mioglobina y hemoglobina


Pigmentos respiratorios • Hemoglobina y citocromos ( rojos )-conjugadas. • Grupo prostético: HEME : tetrapirrol cíclico de naturaleza porfirínica • Hemoproteínas: mioglobina, catalasa, peroxidasas, triptofano pirrolasa y xantina oxidasa. • Cuatro cadenas polipeptídicas: estructura primaria origina propiedades fisicoquímicas y biológicas distintas. • Estructura cuaternaria-forma tetraédrica.

Mioglobina 1 - Función: v Células musculares Almacena O 2 y lo transporta a mitocondrias v Tensión baja de O 2 v Curva de disociación de O 2 v

Mioglobina 2 - Estructura: -globina una cadena de 153 residuos de AA • aproximadamente el 75% de su estructura -posee 8 segmentos alfa helicoidales (A-H) -Residuos polares en el exterior y no polares en el interior. • -heme: Se acomoda en bolsa hidrofóbica Función: unión del O 2 a la Mb ( Hb). Sin heme no hay unión. Estructura: hierro ferroso (unión) y proto IX (4 grupos pirrólicos) Unión al oxígeno § Valencias de coordinación o ligandos. § Protección de la bolsa hidrofóbica contra la oxidación del Fe. Metamioglobina no funcional (H 2 O) Electrón extra impide formación de ligando para unión de O 2

Hemoglobina 1 - Características: t Su empacamiento le permite estar a altas conc. dentro del glób. rojo sin problemas de presión osmótica o viscosidad t Hay 5 millones de glób. rojos/m. L de sangre t Cada glób. rojo tiene 280 millones de moléculas de Hb 2 - Funciones: ¬ Capta O 2 a altas p. O 2 en los pulmones ¬ Capaz de liberarlo a bajas p. O 2 ¬ Transporta CO 2 de los tejidos a pulmones
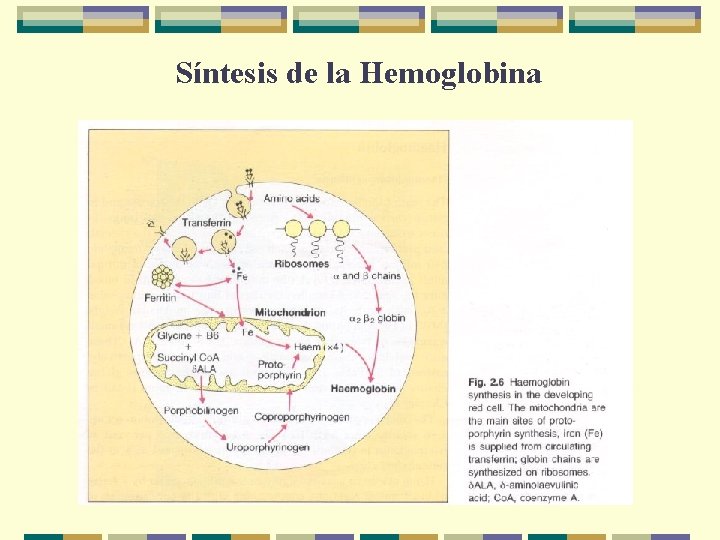
Síntesis de la Hemoglobina

3 - Estructura: ¬ ¬ Tetramérica El Heme está contenido en bolsa hidrofóbica y es idéntico al de la Mb ¬ Presenta gran diversidad estructural y genética (según: edad y necesidades de O 2)
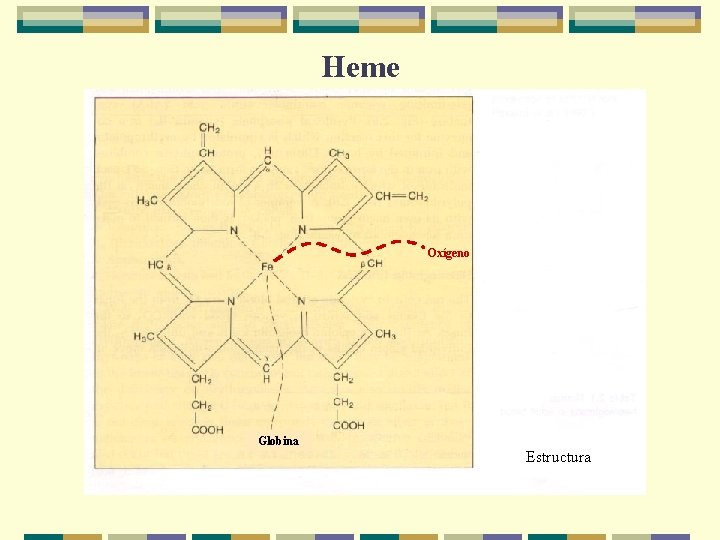
Heme Oxígeno Globina Estructura
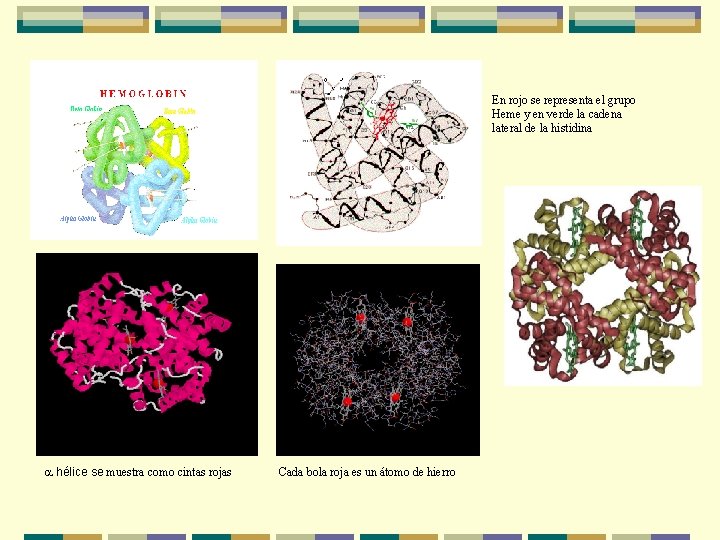
En rojo se representa el grupo Heme y en verde la cadena lateral de la histidina a hélice se muestra como cintas rojas Cada bola roja es un átomo de hierro
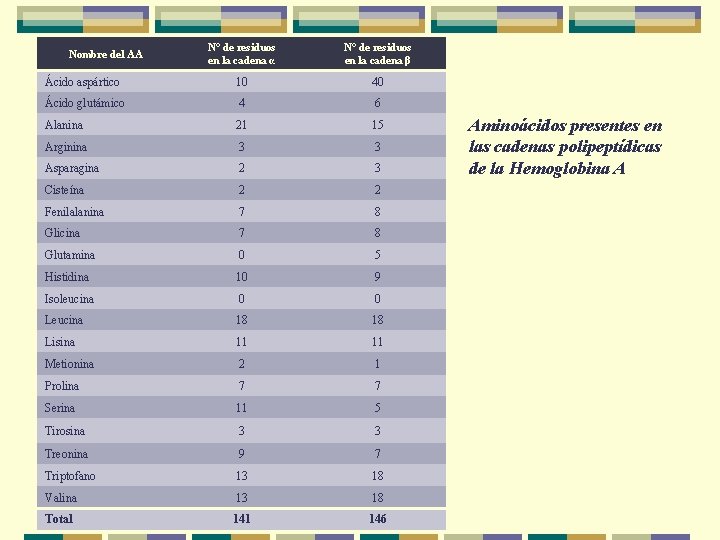
N° de residuos en la cadena α N° de residuos en la cadena β Ácido aspártico 10 40 Ácido glutámico 4 6 Alanina 21 15 Arginina 3 3 Asparagina 2 3 Cisteína 2 2 Fenilalanina 7 8 Glicina 7 8 Glutamina 0 5 Histidina 10 9 Isoleucina 0 0 Leucina 18 18 Lisina 11 11 Metionina 2 1 Prolina 7 7 Serina 11 5 Tirosina 3 3 Treonina 9 7 Triptofano 13 18 Valina 13 18 Total 141 146 Nombre del AA Aminoácidos presentes en las cadenas polipeptídicas de la Hemoglobina A


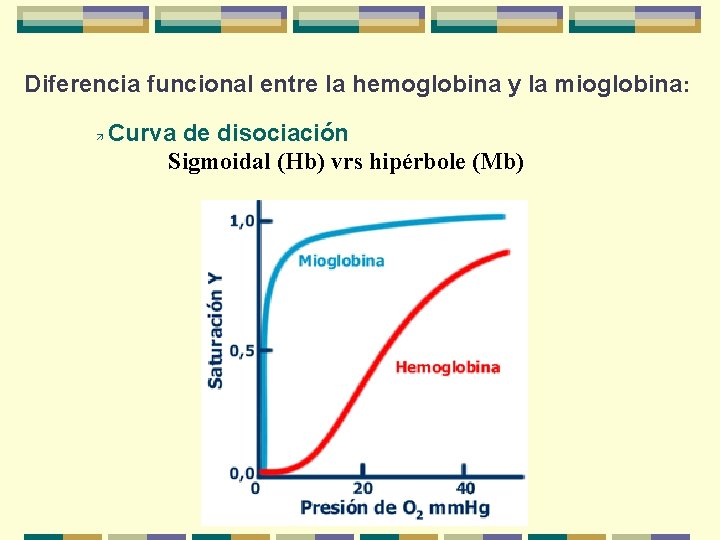
Diferencia funcional entre la hemoglobina y la mioglobina: ä Curva de disociación Sigmoidal (Hb) vrs hipérbole (Mb)

4 - Relaciones función-estructura: • Efectores alostéricos: H+, 2 -3 DPG y CO 2 refuerza el concepto de la relación función-estructura • Hb Fetal • Unión cooperativa del O 2 - Desoxi. Hb: cada unidad unida por enlaces electrostáticos ( el Fe está 0. 4 A fuera del plano del heme por repulsión estérica entre histidina proximal y los átomos de nitrógeno del anillo porfirínico). Forma T: baja afinidad por O 2 - Oxi Hb: rompe los enlaces y origina cambios estructurales en donde los sitios quedan expuestos. Forma R: Mov. del Heme constante de afinidad X 500
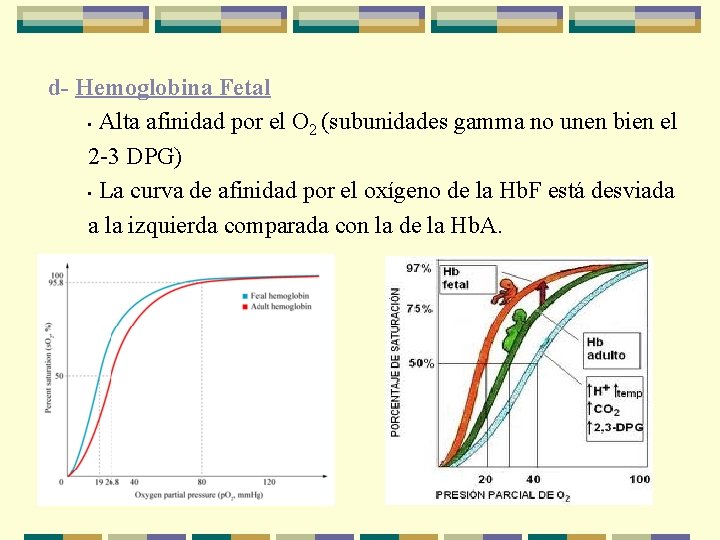
d- Hemoglobina Fetal • Alta afinidad por el O 2 (subunidades gamma no unen bien el 2 -3 DPG) • La curva de afinidad por el oxígeno de la Hb. F está desviada a la izquierda comparada con la de la Hb. A.

Protones H+ y CO 2: El efecto Bohr describe la relación entre la afinidad de la Hb por el O 2 a dif. niveles de p. CO 2 y p. H conc. de H+ Afinidad p. CO 2 (desvío de la curva hacia la derecha) La unión de protones provoca que la Hb pase de la forma R a la T. En los pulmones a alta p. O 2 y p. H 7. 4 pasa a la forma R con menor afinidad por los protones y estos son expulsados. La unión de CO 2 igualmente favorece el paso a la forma T. CO 2 + NH 3 N - COOH +2 H Carbamato

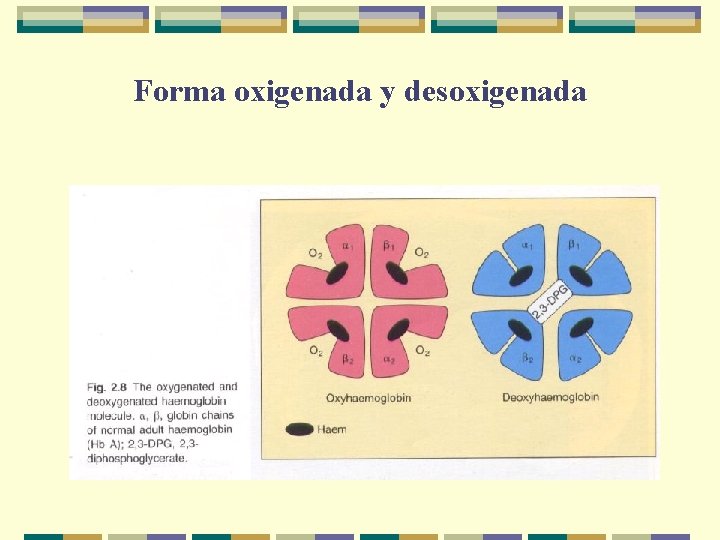
Forma oxigenada y desoxigenada

c- Papel del 2, 3 DPG: v Se encuentra en los GRs en una concentración parecida a la de la Hb v Responsable de bajar significativamente la afinidad de la Hb por el O 2 y promueve el paso a la forma T v Solo una molécula de 2, 3 DPG interactúa con cada tetrámero de Hb v Aumenta en el GR conforme se adaptan a la hipoxia tisular (anemia, grandes altitudes y disfunción pulmonar) v Disminuye en la sangre almacenada por lo que disminuye la capacidad de liberar O 2 a los tejidos
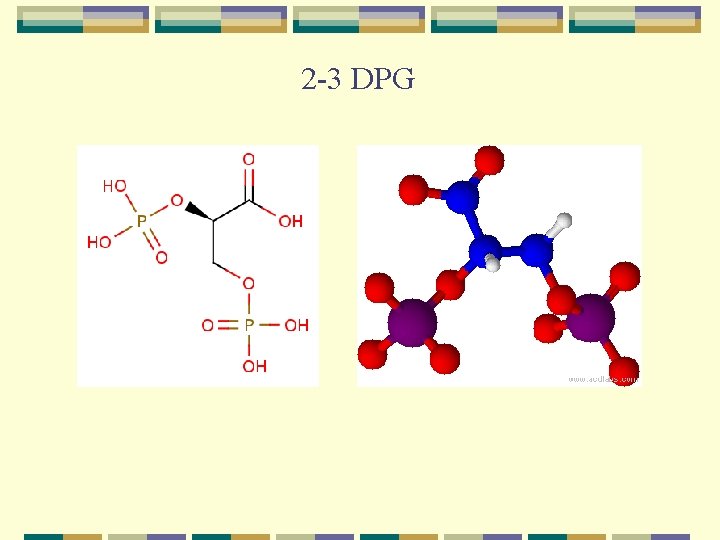
2 -3 DPG
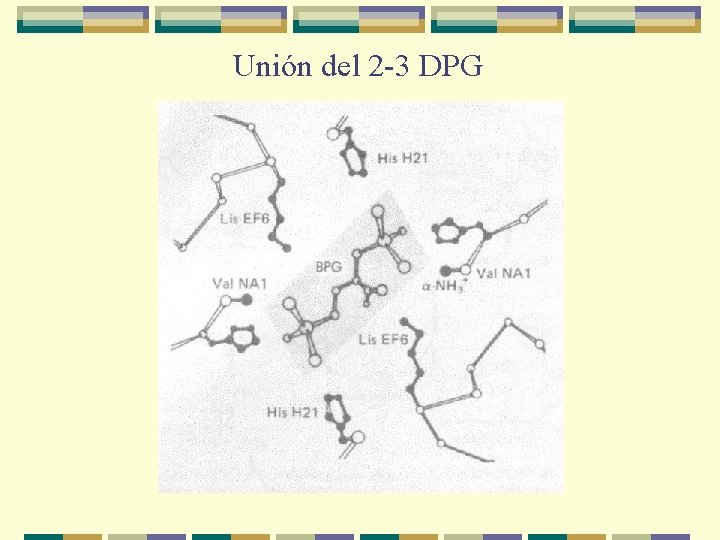
Unión del 2 -3 DPG

Ciclo del 2 -3 DPG

Vía Glicolítica del GR

Hemoglobinopatías

Alteraciones de la hemoglobina Tipo de alteración: v Hereditarias/Adquiridas Cualitativos: Por cambios estructurales Cuantitativos: Por disminución o ausencia en la síntesis de cadenas de globina (Talasemias) Glicosilación Hb. A en diabetes mellitus Hemoglobinopatías: Enfermedades genéticas en las que las subunidades de la Hb han sufrido una mutación. Se han descrito cientos de ellas. Algunas pasan inadvertidas pero otras producen enfermedad desde leve a grave.
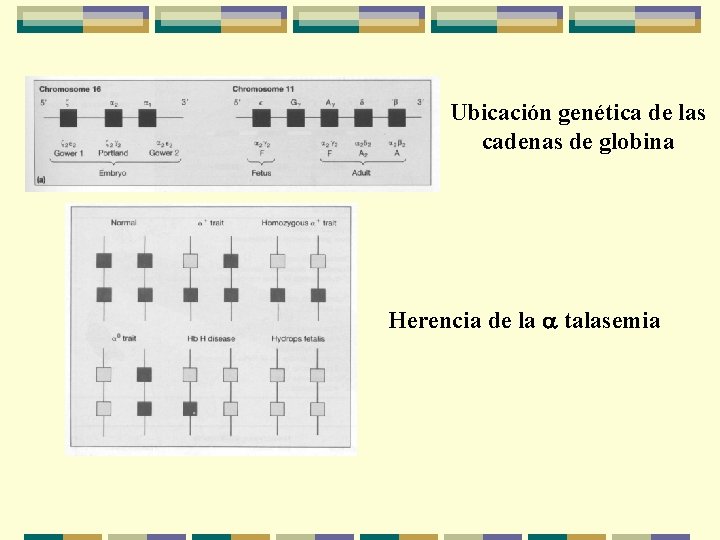
Ubicación genética de las cadenas de globina Herencia de la a talasemia
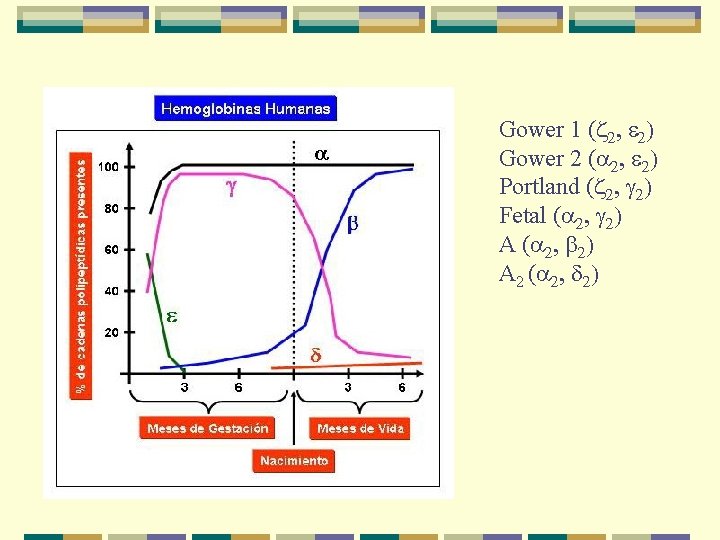
Gower 1 (z 2, e 2) Gower 2 (a 2, e 2) Portland (z 2, g 2) Fetal (a 2, g 2) A (a 2, b 2) A 2 (a 2, d 2)


Clases de hemoglobinopatías • Polimerización anómala de Hb (Hb S) Estructurales (alteración en secuencia aminoácidos lo que produce una alteración en la funcionalidad Hb) Talasemias Variantes de la Hb talasémicas Persistencia hereditaria de la Hb fetal Hemoglobinopatías adquiridas • Afinidad por el O 2 alterada • Alta afinidad (Policitemia) • Baja afinidad (Cianosis) • Hb que se oxidan fácilmente • Inestables (Anemia hemolítica) • Hb M (Metahemoglobinemia) • Talasemia alfa • Talasemia beta • Talasemias delta-beta, gammadeltabeta, alfa-beta • Hb Constant Spring • Hb Lepore Persistencia en adultos de concentraciones altas de Hb. F • Metahemoglobinemia debida a exposición a tóxicos • Sulfohemoglobina debida a exposición a tóxicos • Carboxihemoglobina • Hb F altas en estado de estrés eritroide y displasia de médula ósea

Patrones electroforéticos de algunas hemoglobinopatías

Hemoglobinopatías más frecuentes (por alteración estructural)
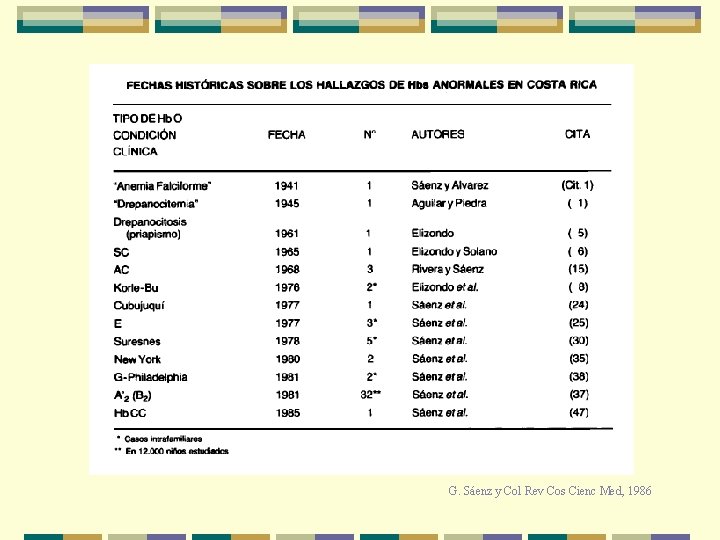
G. Sáenz y Col Rev Cos Cienc Med, 1986
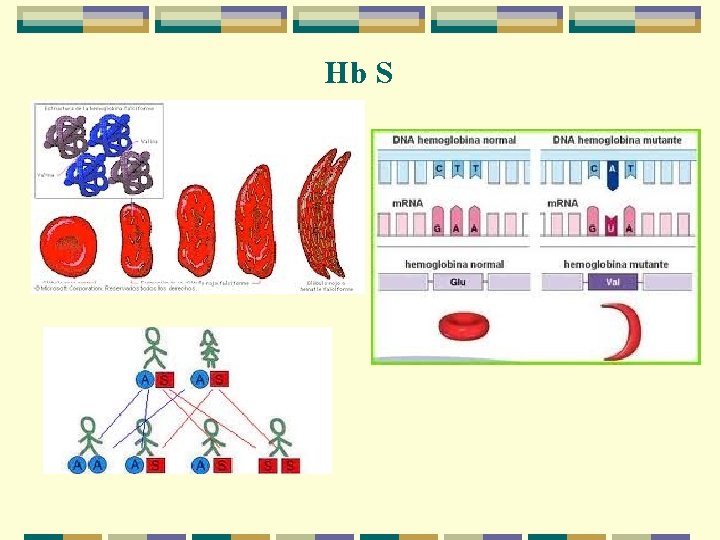
Hb S
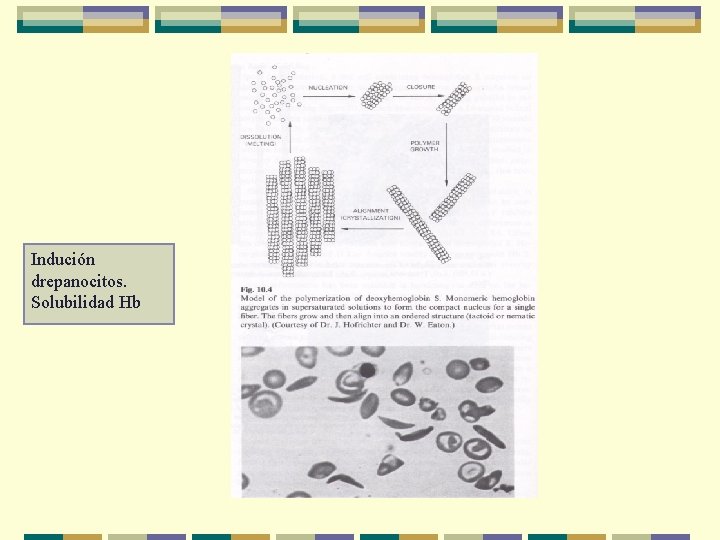
Indución drepanocitos. Solubilidad Hb

Síndromes drepanocíticos
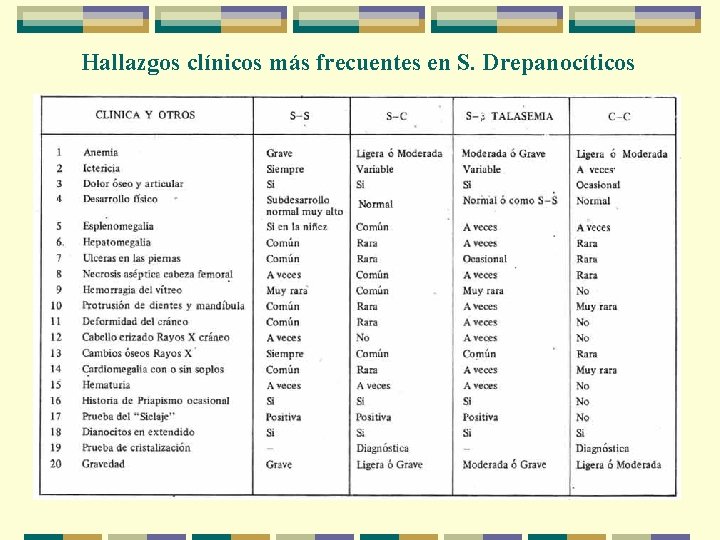
Hallazgos clínicos más frecuentes en S. Drepanocíticos


Talasemia Definición • Grupo de anemias hemolíticas hereditarias. • Disminución de la síntesis de 1 ó + cadenas polipeptídicas de Hb. • Cuadro clínico desde indetectables hasta anemia severa y fatal. (Síndromes talasémicos) Tipos de talasemias: Alfa talasemia: Disminución en la síntesis cadenas α (Exceso cadenas β) Beta talasemia: Disminución en la síntesis cadenas β (Exceso cadenas α)
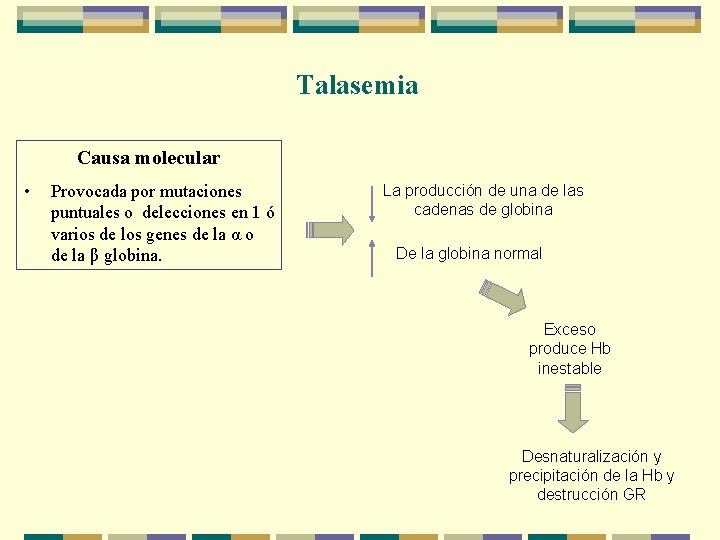
Talasemia Causa molecular • Provocada por mutaciones puntuales o delecciones en 1 ó varios de los genes de la α o de la β globina. La producción de una de las cadenas de globina De la globina normal Exceso produce Hb inestable Desnaturalización y precipitación de la Hb y destrucción GR
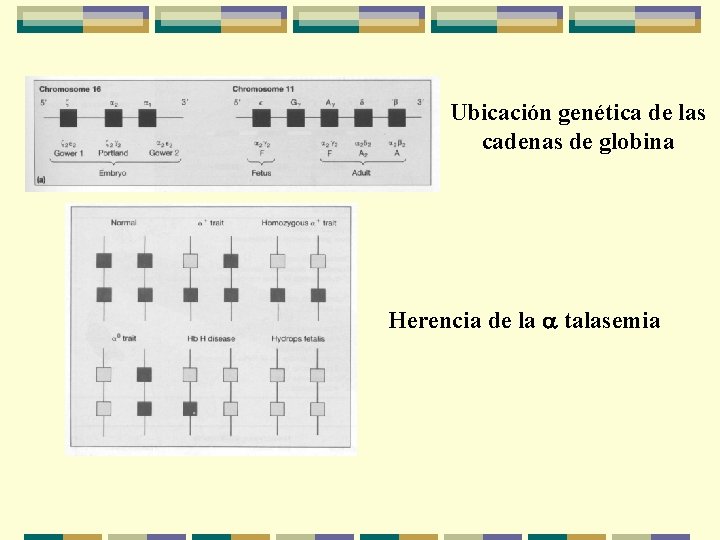
Ubicación genética de las cadenas de globina Herencia de la a talasemia
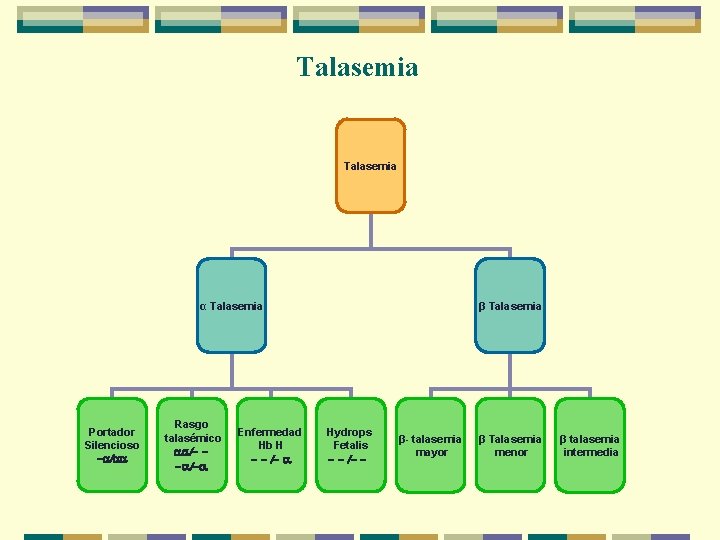
Talasemia α Talasemia Portador Silencioso -a/aa Rasgo talasémico aa/- -a/-a Enfermedad Hb H - - /- a β Talasemia Hydrops Fetalis - - /- - β- talasemia mayor β Talasemia menor β talasemia intermedia

β Talasemia mayor: Anemia del Mediterráneo-Anemia de Cooley 1920: ü Dr. Denton Cooley describió por primera vez la enfermedad Reconoció signos clínicos (niños italianos y griegos) ü Antonio Maccanti describía al mismo tiempo esta hemoglobinopatía Características más importantes: Anemia severa Hb de 4 – 5 g/d. L Dx entre los 6 – 12 meses de edad Hepato esplenomegalia Eritropoyesis ineficaz Dependientes vitalicios de transfusiones (daño de órganos) Alteraciones óseas
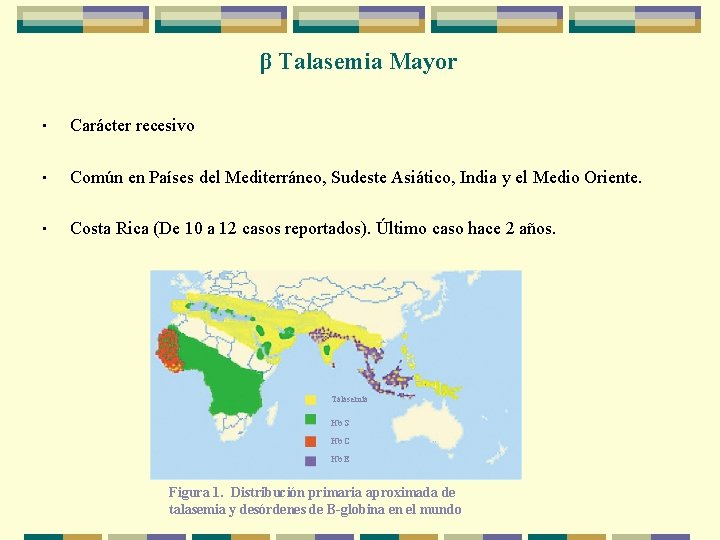
β Talasemia Mayor • Carácter recesivo • Común en Países del Mediterráneo, Sudeste Asiático, India y el Medio Oriente. • Costa Rica (De 10 a 12 casos reportados). Último caso hace 2 años. Talasemia Hb S Hb C Hb E Figura 1. Distribución primaria aproximada de talasemia y desórdenes de B-globina en el mundo



Muchas Gracias
- Slides: 48