Proteinler1 Proteinler Organizmada en fazla bulunan makro molekl

Proteinler-1

Proteinler �Organizmada en fazla bulunan makro molekül �Proteinler, yaşayan varlıklar için elzem azotlu öğelerdir. ,

Aminoasit �Proteinlerin yapı taşıdırlar �Doğada 300 AA vardır. �Fonksiyon ve biyolojik aktivitelerine bakılmaksızın protein yapısında 20 değişik (aa) bulunur. �Bakteri ve bitkilerden en gelişmiş canlılara kadar proteinlerde aynı aa yer alır.

Aminoasitlerin Genel Yapısı Tüm 20 aminoasitte ortak olan yapı: � Bir C atomuna bağlı olarak � Bir hidrojen atomu (–H) � Karboksil grup (-COOH) � Amino grup (-NH 2) � Değişken yan zincirler (R 1… 20) bulunmaktadır. � Proteinlerin içerisinde farklı sayıda ve dizide bulunan amino asitler farklı yapıda ve fonksiyonda binlerce çeşit protein oluşumuna neden olur. � R= H ise. . . . GLİSİN R= CH 3 (Metil) ise. . . . ALANİN R= CH 3 OH ise. . . . SERİN oluşur

Aminoasit Karboksil grubuna en yakın; � 1. C atomuna α-C � 2. C atomuna β-C � 3. C atomuna γ-C � 4. C atomuna δ-C � 5. C atomuna ε-C denilmektedir.

Aminoasit �Biyolojik sistemde en yaygın olan aminoasitler α-aminoasitlerdir. �R grubunun YAPISI, BÜYÜKLÜĞÜ, ELEKTRİK YÜKÜ �AA’lerin ◦ Hidrofilik (polar) ◦ Hidrofobik (nonpolar)

Aminoasit �Standart aminoasitler �Nonstandart aminoasitler �Proteinlerin yapısında bulunmayan aminoasitler
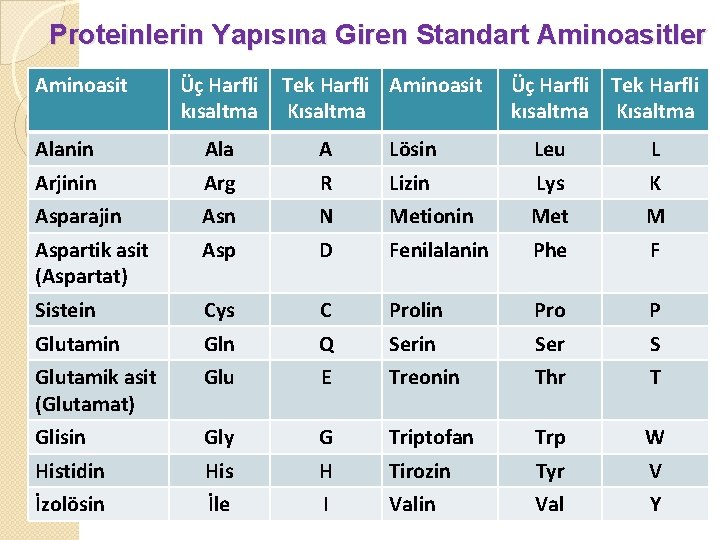
Proteinlerin Yapısına Giren Standart Aminoasitler Aminoasit Üç Harfli kısaltma Tek Harfli Aminoasit Kısaltma Üç Harfli Tek Harfli kısaltma Kısaltma Alanin Ala A Lösin Leu L Arjinin Arg R Lizin Lys K Asparajin Asn N Metionin Met M Aspartik asit (Aspartat) Asp D Fenilalanin Phe F Sistein Cys C Prolin Pro P Glutamin Gln Q Serin Ser S Glutamik asit (Glutamat) Glu E Treonin Thr T Glisin Gly G Triptofan Trp W Histidin His H Tirozin Tyr V İzolösin İle I Valin Val Y
Standart Amino Asitlerin Sınıflandırılması 1 • Yan gruplarına 2 • p. H’larına 3 • Biyolojik durumlarına Göre sınıflandırılırlar !

1 - Yan Gruplarına Göre Sınıflama ü Alifatik yan zincir taşıyan aa’ler Düz zincirli aa’ler • Glisin ◦ Alanin Dallı zincirli aa’ler • Valin ◦ Lösin ◦ İzolösin

1 - Yan Gruplarına Göre Sınıflama ü Aromatik yan zincir taşıyan aa’ler ◦ Fenilalanin ◦ Tirozin ◦ Triptofan

1 - Yan Gruplarına Göre Sınıflama ü Sülfür içeren yan zincirli aa’ler ◦ Metionin ◦ Sistein

1 - Yan Gruplarına Göre Sınıflama ü Hidroksil grubu içeren yan zincirli aa’ler ◦ Serin ◦ Teronin

II- p. H’larına Göre Sınıflama v Nötral aa’ler: Alifatik yan zincir taşıyan aa’ler ◦ Düz zincirli aa’ler: Glisin, Alanin ◦ Dallı zincirli aa’ler: Valin, Lösin, İzolösin Aromatik yan zincir taşıyan aa’ler ◦ Fenilalanin, Tirozin, Triptofan Sülfür içeren yan zincirli aa’ler ◦ Metionin ◦ Sistein Hidroksilli aa’ler ◦ Serin ◦ Teronin

II- p. H’larına Göre Sınıflama v Bazik aa’ler: Yan zincirleri p. H 7’de pozitif yüklüdür ve hepsi 6 C’lu ◦ Lizin ◦ Arginin ◦ Histidin
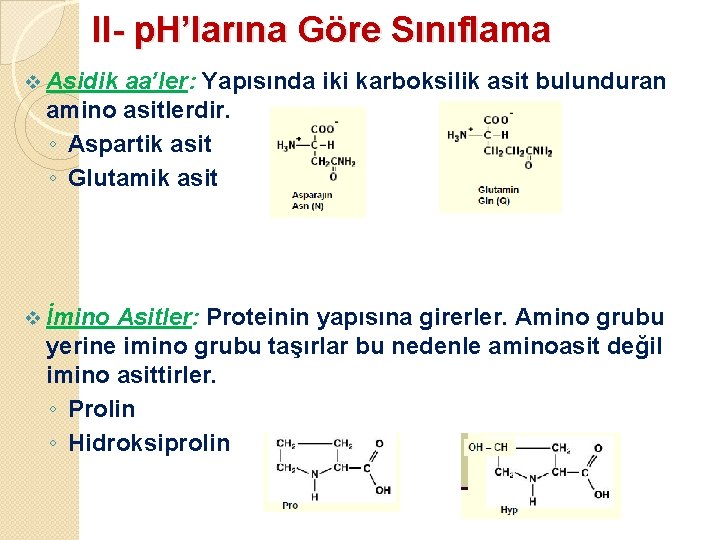
II- p. H’larına Göre Sınıflama v Asidik aa’ler: Yapısında iki karboksilik asit bulunduran amino asitlerdir. ◦ Aspartik asit ◦ Glutamik asit v İmino Asitler: Proteinin yapısına girerler. Amino grubu yerine imino grubu taşırlar bu nedenle aminoasit değil imino asittirler. ◦ Prolin ◦ Hidroksiprolin
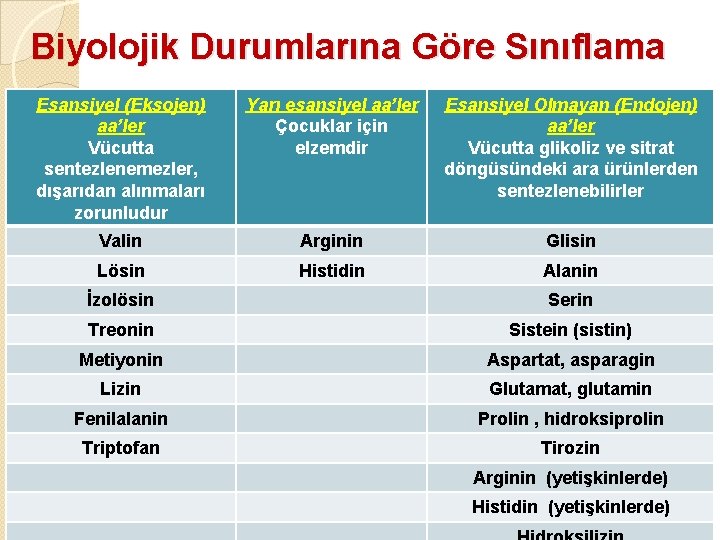
Biyolojik Durumlarına Göre Sınıflama Esansiyel (Eksojen) aa’ler Vücutta sentezlenemezler, dışarıdan alınmaları zorunludur Yarı esansiyel aa’ler Çocuklar için elzemdir Esansiyel Olmayan (Endojen) aa’ler Vücutta glikoliz ve sitrat döngüsündeki ara ürünlerden sentezlenebilirler Valin Arginin Glisin Lösin Histidin Alanin İzolösin Serin Treonin Sistein (sistin) Metiyonin Aspartat, asparagin Lizin Glutamat, glutamin Fenilalanin Prolin , hidroksiprolin Triptofan Tirozin Arginin (yetişkinlerde) Histidin (yetişkinlerde)

Nonstandart amino asitlerin sınıflandırılması Modifiye AA � Bir standart AA polipeptid zinciri yapısına girdikten sonra bir modifikasyona uğrarsa nonstandart AA diye bilinen bazı AA oluşabilir. � Ortak 20 aa’in dışında bazı protein hidrolizatlarından bazı aa’ler elde edilmiştir.
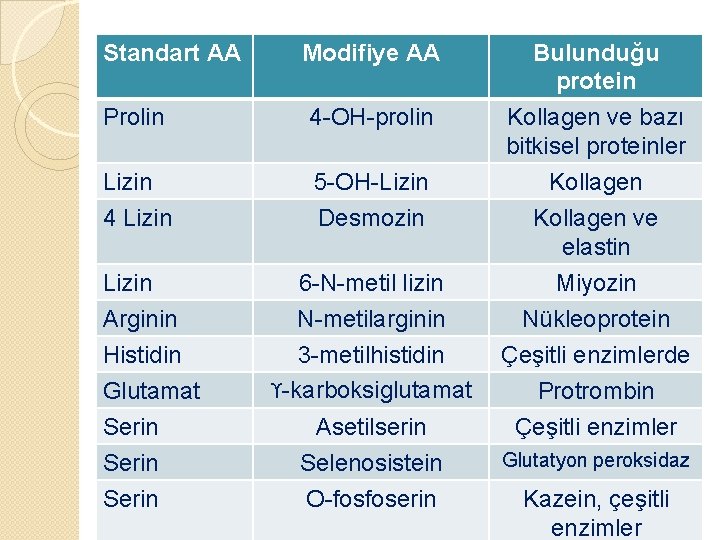
Standart AA Modifiye AA Prolin 4 -OH-prolin Lizin 4 Lizin 5 -OH-Lizin Desmozin Lizin Arginin Histidin Glutamat Serin 6 -N-metil lizin N-metilarginin 3 -metilhistidin ϒ-karboksiglutamat Asetilserin Selenosistein O-fosfoserin Bulunduğu protein Kollagen ve bazı bitkisel proteinler Kollagen ve elastin Miyozin Nükleoprotein Çeşitli enzimlerde Protrombin Çeşitli enzimler Glutatyon peroksidaz Kazein, çeşitli enzimler
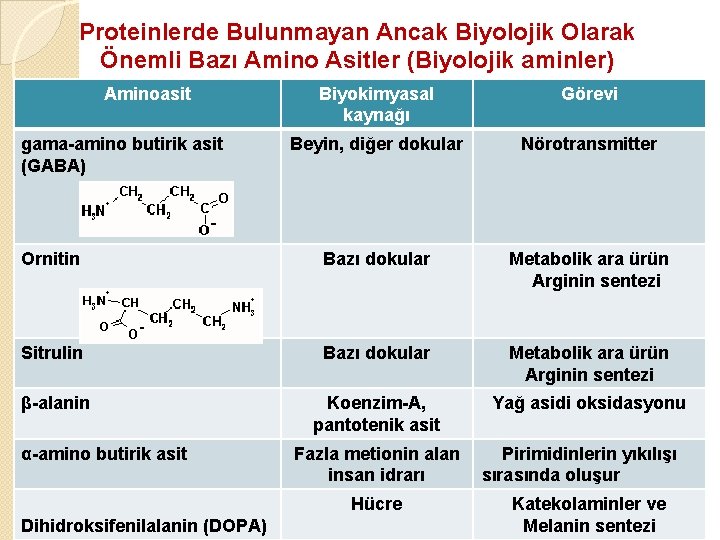
Proteinlerde Bulunmayan Ancak Biyolojik Olarak Önemli Bazı Amino Asitler (Biyolojik aminler) Aminoasit Biyokimyasal kaynağı Görevi Beyin, diğer dokular Nörotransmitter Ornitin Bazı dokular Metabolik ara ürün Arginin sentezi Sitrulin Bazı dokular Metabolik ara ürün Arginin sentezi β-alanin Koenzim-A, pantotenik asit Yağ asidi oksidasyonu gama-amino butirik asit (GABA) α-amino butirik asit Fazla metionin alan insan idrarı Hücre Dihidroksifenilalanin (DOPA) Pirimidinlerin yıkılışı sırasında oluşur Katekolaminler ve Melanin sentezi

Doğa da proteinler içinde bulunmayan ancak doğal olarak meydana gelen aa de bulunmaktadır. � Tiroksin…. . trioglobulinde (tiroid proteini) di iyot tirozinle bulunur. � AIIi. I. . soğan da bulunur. � L (+) ornitin…lizin ve histidin ile birlikte balık proteinlerinde bulunur; Üre döngüsü ara maddesi � L (-) sitrülin. . karpuzda bulunmuş; üre döngüsü ara maddesi � β-alanin…vit olarak pantotenik asit yapısında bulunur � Ornitin-sitrulin…olgunlaşmış peynirlerde arjinin yıkılmasıyla oluşur.

Aminoasitlerin Genel Özellikleri Beyaz renkte, kristal halde edilir. 2. Kristal formda bulundukları zaman erime noktaları yüksektir. 3. Farklı tatlara sahiptirler; Tatlı: Glisin, Alanin, Serin, Prolin Acı: Arginin Tatsız: Triptofan, Lösin 1.

Aminoasitlerin Genel Özellikleri 4. Suda çözünürlükleri fazladır. Sistein ve tirozin dışındaki bütün amino asitler suda kolaylıkla çözünür. Sistin ve tirozin sıcak suda yüksek çözünürlüğe sahiptir. 5. Prolin hariç eter ve alkolde çözünmezler. 6. Kuvvetli asit ve alkalilerde hepsi çözünür.

Aminoasitlerin Genel Özellikleri 7. Glisin hariç tüm a. aler en az bir asimetrik karbon atomuna sahiptir. Optik olarak aktif L ve D serileri var

Aminoasitlerin Genel Özellikleri 8. Elektriksel bakımdan yüklü ve polar yapı AA’lerin –NH 2 ve –COOH grupları ile bazı İyonlaşma: aa’lerin –R grupları sulu iyonlaşabilirler. İyonik denge reaksiyonu; R-COOH <----> R-COO- + H+ R-NH 3+ <-----> R-NH 2 + H+ solüsyonlarda
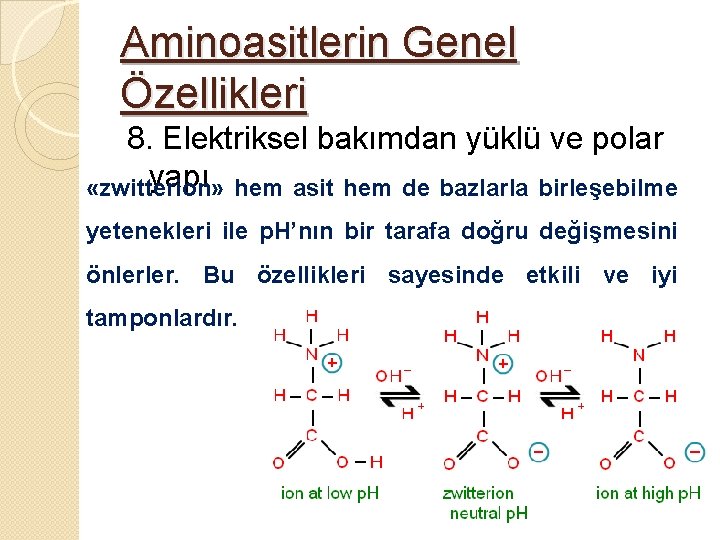
Aminoasitlerin Genel Özellikleri 8. Elektriksel bakımdan yüklü ve polar yapı hem asit hem de bazlarla birleşebilme «zwitterion» yetenekleri ile p. H’nın bir tarafa doğru değişmesini önlerler. Bu özellikleri sayesinde etkili ve iyi tamponlardır.

Aminoasitlerin Genel Özellikleri � İzoelektrik Nokta: Bir amino asidin net yükünün sıfır olduğu p. H’ya izoelektrik nokta p. H denir ve p. I ile gösterilir.

AA İzoelektrik Noktası İyonize olabilen bir yan zincir içermeyen bir amino asit titre edilirse iki adet p. Ka değeri gözlenir. Birinci değer (p. Ka 1) αkarboksil grubuna, ikinci değer (p. Ka 2) α-amino grubuna aittir.

Aminoasitlerin Genel Özellikleri 9. Elektriksel alanda göçerler. Bir amino asit, izoelektrik nokta değerinden yüksek p. H ortamında bazik anyon şeklinde; izoelektrik nokta değerinden düşük p. H ortamında asit katyon şeklinde bulunur

Aminoasitlerin Genel Özellikleri 10. Amfolit yapıya (tampon etki) sahiptirler. � Amfoter özellik: Amino asitler amfoter özellik gösteren maddelerdir. ◦ Yani asidik ortamda baz, bazik ortamda asit gibi davranırlar.

Aminoasitlerin Genel Özellikleri 12. Peptidleri oluştururlar. Asitamid oluşumu

Aminoasitlerin Genel Özellikleri 13. Metillenme ile betainlerin oluşumu Amino asitler zwitterion durumunda iken, - NH 3+ grubundaki 3 hidrojen yerine – CH 3 grupları geçerek betainler oluşur.

Aminoasitlerin Kimyasal Reaksiyonları �Karboksil grubuna ait �Amino grubuna ait �R grubuna ait

Kimyasal Reaksiyonlar Karboksil Grubu 1. Alkollerle esterleşirler: AA’lerin karboksil grupları, asit varlığında alkollerle ester oluşturabilirler.

Kimyasal Reaksiyonlar Karboksil Grubu 2. Amonyak varlığında amidleri oluşturur: AA’in -COOH grubu –NH 2 grubuna sahip komşu bir – NH 2 vericisi ile reaksiyona girerek amid bağı oluşturabilir. �
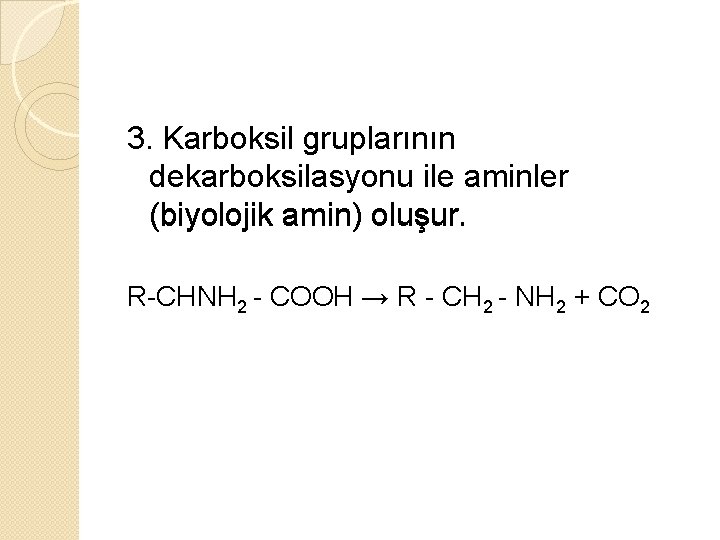
3. Karboksil gruplarının dekarboksilasyonu ile aminler (biyolojik amin) oluşur. R-CHNH 2 - COOH → R - CH 2 - NH 2 + CO 2

Kimyasal Reaksiyonlar Amino Grubu 1. Van Slyke tepkimesi: Amino asitlerin amino grupları, nitröz asitle reaksiyona girerek azot gazı açığa çıkmasına neden olurlar.

Kimyasal Reaksiyonlar Amino Grubu 2. Sanger Tepkimesi Amino asitlerin amino grupları, 1 -fluoro-2, 4 dinitrobenzen ile açık sarı bir bileşik olan 2, 4 dinitrofenilamino asit oluşturur. Terminal AA tayininde kullanılır.

Kimyasal Reaksiyonlar Amino Grubu 3. Oksidatif Deaminasyon: Amino asitlerin deaminasyonu ile α-keto asitler oluşur A. A. + (O) → İmino Asit + H 2 O → α-Keto Asit + NH 3 NH 2 NH I II R-C-COOH + (O) → R-C-COOH + H 2 O I H İmino Asit + H 20 O II R- C -COOH + NH 3 α-Keto Asit

Kimyasal Reaksiyonlar Amino Grubu 4. Ninhidrin Rxn: A. A. + 2 Mol Ninhydrin → İndirgenmiş Ninhydrin ↓NH 3 Mavi-Menekşe Renk (hydrindantine)

Kimyasal Reaksiyonlar Amino Grubu 5. Sörensen titrasyonu; � Aminoasitler, nötral veya hafif alkali çözeltilerde formaldehit ile reaksiyona girerek mono- veya dimetilol türevleri veya Schiff bazı ( N=CH ) meydana getirirler.

Kimyasal Reaksiyonlar R Grubu Aspartik/glutamik asit Histidin (imidazol halkası) Sistein (Tio grubu) Tirozin (Fenol grubu) Lizin (Epsilon amino grubu) Arjinin (Guanido grubu)

Kimyasal Reaksiyonlar R Grubu 1. MİLLON TESTİ: Yapısında fenil grubu bulunan fenilalanin ve tirozin gibi amino asitler, eser miktarda nitröz asit içeren nitrik asitte çözülmüş civa nitrat ile ısıtmakla kırmızı renk verirler. (Tirozin) Fenol grubu + Eser HNO 2 İçeren HNO 3 Çözünmüş Hg(NO 3)2 ↓Isıt Kırmızı Renk

Kimyasal Reaksiyonlar R Grubu 2. KSANTOPROTEİN OLUŞUMU: Yapısında aromatik halka bulunan fenilalanin ve triptofan gibi amino asitler için karakteristiktir. � konsantre nitrik asit ilave edildiğinde önce beyaz bir tortu, ısıtılırsa sarı bir renk meydana gelir. Aromarik Halka (Tirozin, Fenilalanin, Triptofan) + Kon. HNO 3 ↓Isıt Sarı renkli nitro türevleri

Kimyasal Reaksiyonlar R Grubu 3. SAKAGUCHİ TESTİ: Arginin, metal guanidine gibi guanidine türevleri α-Naftol ve sodyum hipobromit varlığında renkli bir maddeye oksitlenirler. Guanidin (Arginin) + Alkali ortam α-Naftol + Na. OBr ↓ KIRMIZI RENK

Kimyasal Reaksiyonlar R Grubu 4. EHRLİCH TESTİ: Yapısında indol grubu bulunan triptofan gibi amino asitler, sülfürik asitte çözülmüş p-dimetilaminobenzaldehit ile reaksiyona sokulursa kırmızımsı pembe bir renk oluşur. İndol türevleri (Triptofan) + p-Dimetilaminobenzaldehit ↓ Asit Ortam KIRMIZI MENEKŞE

Kimyasal Reaksiyonlar R Grubu 5. KURŞUN SÜLFÜR OLUŞUMU: Yapısında tiyol (−SH) veya disülfit (−S−S−) grubu bulunan amino asitler Na. OH ile kaynatıldığında H 2 S veya Na 2 S oluşur; ortama kurşun asetat çözeltisi ilave edildiğinde siyah renkli Pb. S çöker. Sistin, Sistein Kuvvetli alkali Kurşun asetat çözeltisi Isıt Pb. S (siyah renk)

Kimyasal Reaksiyonlar R Grubu 6. PAULY TEPKİMESİ Yapısında fenil ya da imidazol grubu bulunan fenilalanin, tirozin, histidin gibi aminoasitler, alkali ortamlarda sulfanilik asit ve sodyum nitrit karışımı ile tepkimeye girerlerse kırmızı renk verirler.

Kimyasal Reaksiyonlar R Grubu 7. NİTROPRUSSİYAT TEPKİMESİ Yapısında serbest sülfhidril grubu bulunan sistein gibi amino asitler, seyreltik amonyum hidroksitte çözülmüş sodyum nitroprussiyat ile kırmızı renk verirler.
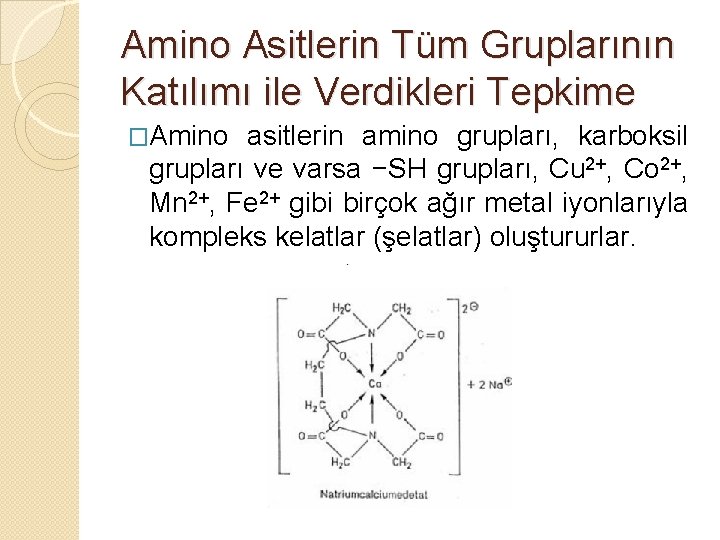
Amino Asitlerin Tüm Gruplarının Katılımı ile Verdikleri Tepkime �Amino asitlerin amino grupları, karboksil grupları ve varsa −SH grupları, Cu 2+, Co 2+, Mn 2+, Fe 2+ gibi birçok ağır metal iyonlarıyla kompleks kelatlar (şelatlar) oluştururlar.

Bazı AA Temel Özellikleri ve İşlevleri Lösin; �Proteinlerin ≈%6 -15 bulunmaktadır. �Jelatinde çok az, tahıl proteinlerin çok miktarda bulunur. İsolösin; �Et, süt ve yumurta proteininde %5 -6. 5 oranında bulunur. �Tahıl ve bitki proteinlerinin çoğu yetersizdir.

Bazı AA Temel Özellikleri ve İşlevleri Glutamik asit; �Proteinlerin tümünün ana yapı taşıdır. �Buğday gluteninde, mısır prolaminlerinde, soyada bulunur. Arjinin; �Protein türevlerinde bulunur �Gıda proteinlerindeki oranı %3 -9 dolaylarındadır. �Proteinlerin %87’sini oluşturur.

Bazı AA Temel Özellikleri ve İşlevleri Lizin; �Kas, süt ve yumurta proteinlerinde çok bulunur. �Tahıl ve diğer bazı bitki proteinlerinde eksiktir. �Patates, muzda hemen hiç bulunmaz; pirinçte yoktur. Metiyonin; �Organizmada metil donörü olmasından dolayı önemlidir. �Hemen hemen tüm proteinlerin yapısında bulunur (Et %3, yumurta %1 -4) �Baklagil ve yağlı tohumlarda eksiktir.

Bazı AA Temel Özellikleri ve İşlevleri Fenilalanin �Proteinlerin tümünde %4 -5 oranında bulunur. , Jelatinde %2, yumurtada %6 oranında bulunur. �Fenilalanin, tirozin dönüşümünü sağlayan enzim sorunu sonucu PKU görülmektedir. Tirozin �Proteinlerin tümünde %2 -6 oranında bulunur. �Süt proteinlerinde çok, jelatinde ise az bulunur.

Bazı AA Temel Özellikleri ve İşlevleri Histidin �Proteinlerde %1 -3 oranın bulunur. �Kan renk maddesi olan globinde arjinin ve lizin ile beraber bulunur. Triptofan; �Tahıl ve ürünlerinde yetersizdir. �Zein, elastin, jelatin ve kollojen gibi proteinler triptofandan zengindir.
- Slides: 55