PROTEIN SERAT DAN GLOBULAR ISMAIL SALEH PENGGOLONGAN PROTEIN
PROTEIN SERAT DAN GLOBULAR ISMAIL SALEH

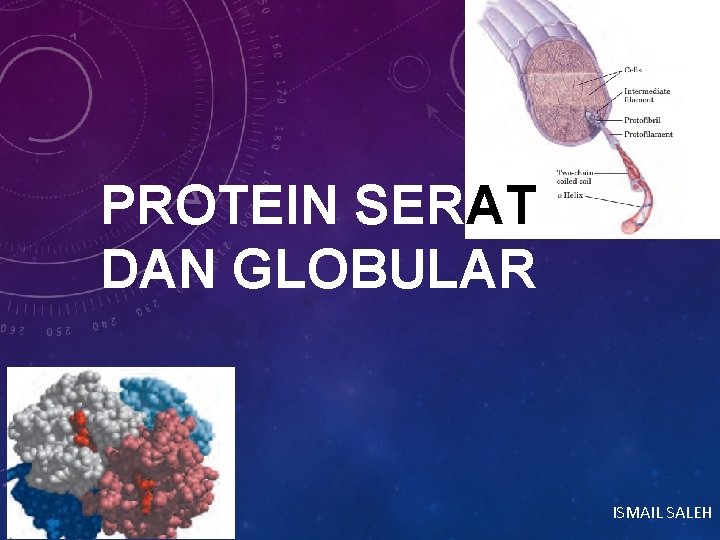
PENGGOLONGAN PROTEIN • PROTEIN SERAT : RANTAI POLIPEPTIDA TERSUSUN DALAM UNTAIAN ATAU LEMBARAN PANJANG • PROTEIN GLOBULAR : RANTAI POLIPEPTIDA YANG BERLIPAT RAPAT MENJADI BENTUK BULAT ATAU GLOBULAR

PROTEIN SERAT

KONFIGURASI VS KONFORMASI • Konfigurasi adalah susunan dalam ruang bagi suatu molekul organik yang ditunjukkan oleh adanya ikatan ganda yang tidak memberikan kebebasan berputar bagi atom di sekelilingnya atau pusat khiral di sekelilingnya gugus substituent tersusun atas deret yang spesifik
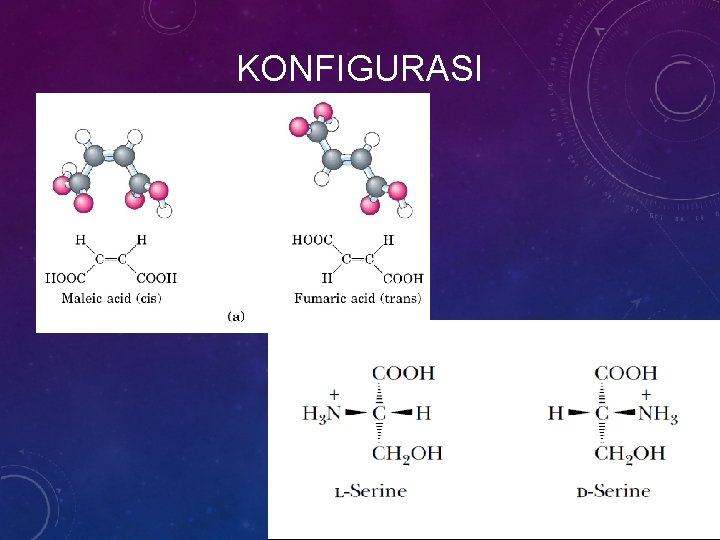
KONFIGURASI

KONFORMASI • Konformasi adalah susunan ruang dari gugus substituen molekul organik yang bebas untuk mencapai posisi yang berbeda-beda di dalam ruang tanpa memutuskan ikatan, karena kebebasan berputar di sekeliling ikatan tunggal karbon.

PARADOKS DALAM KONFORMASI STRUKTUR PROTEIN K A D I ikatan tunggal mampu membentuk sejumlah besar T A konformasi dalam ruang Y N N • Konformasi polipeptida mengalami perubahan terus. A Atermal dan rotasi acak pada bagian menerus karena gerakan T A Y rantai di sekeliling tiap-tiap ikatan tunggal pada kerangka N E polipeptida K • Kerangka kovalen rantai polipeptida mengandung hanya

PARADOKS DALAM KONFORMASI STRUKTUR PROTEIN • Rantai polipeptida protein asli mempunyai hanya satu konformasi (atau sedikit) di dalam ruang pada kondisi biologi normal pada suhu dan p. H tertentu • Konformasi asli ini cukup stabil bagi protein • Ulasan pertama tentang keratin, golongan protein serat yang strukturnya menjadi kunci penelaahan konformasi protein


• Ikatan C-N yang menggabungkan dua asam amino pada ikatan peptida lebih pendek daripada ikatan C-N lainnya • Ikatan C-N ini memiliki sifat ikatan ganda tidak dapat berotasi secara bebas • Keempat atom gugus peptida terletak pada satu bidang sedemikian rupa sehingga atom O (gugus karbonil) dan atom hidrogen (gugus –NH-) bersifat trans satu dengan yang lainnya



• Konformasi ini membiarkan ikatan hidrogen terbentuk di antara setiap atom H yang melekat pada atom nitrogen elektronegatif pada rantai peptida dan atom oksigen karbonil dari asam amino ke empat di belakangnya • Setiap ikatan peptida berpartisipasi dalam membentuk ikatan hidrogen




• Jika terdapat satu atau lebih residu prolin atom nitrogen merupakan bagian dari rantai yang kaku, dan cincin ikatan N-C tidak mungkin berotasi menyebabkan suatu putaran atau belokan

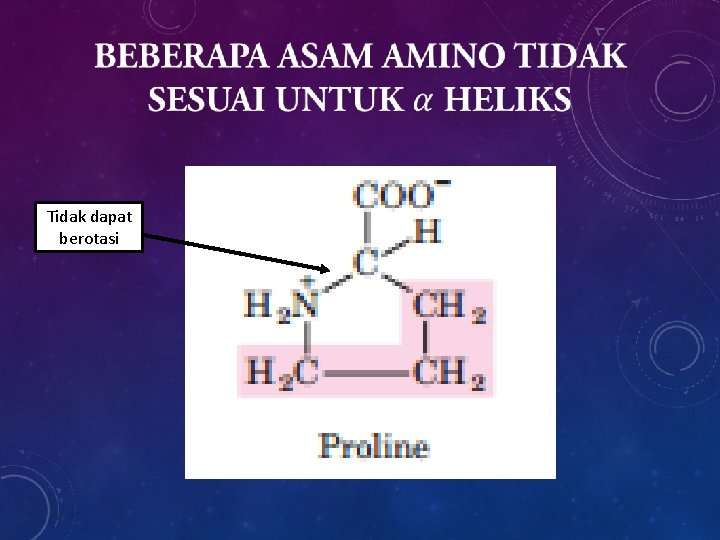
Tidak dapat berotasi

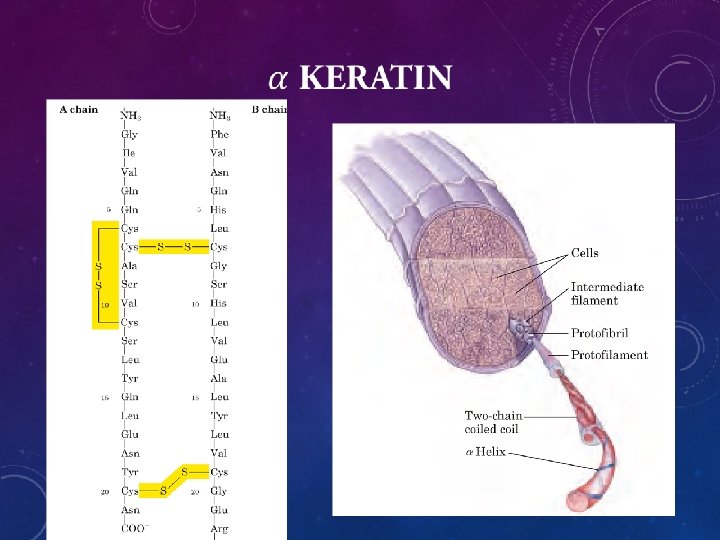




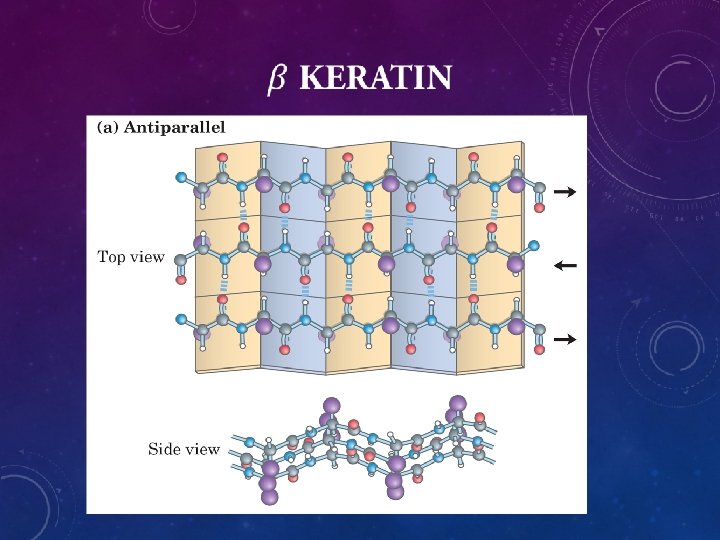
• Bila rambut diberi uap panas, maka akan meregang 2 x lipat → ikatan kovalen rusak • Struktur rambut yang meregang akan nampak sama dengan struktur sutera • Konformasi rambut yang meregang dan sutera disebut konformasi β. • Konformasi ini memperlihatkan struktur “zig zag” yang disusun berdampingan membentuk struktur lipatan • Pada konformasi β tidak terdapat ikatan hidrogen di dalam rantai, yang ada ikatan hidrogen antar-rantai. • Pada β-keratin tidak dijumpai jembatan sistin pada polipeptida yang berdampingan


MENGERITING RAMBUT MERUPAKAN PROSES REKAYASA BIOKIMIA

PROTEIN GLOBULAR

STRUKTUR PROTEIN GLOBULAR • Dalam protein globular, rantai polipeptida berlibat menjadi suatu bentuk globular yang kompak • Konformasi golongan protein globular lebih kompleks dibandingkan dengan golongan protein serat • Hampir semua enzim merupakan protein globular (Enzim akan dibahas pada Bab berikutnya)

STRUKTUR PROTEIN GLOBULAR • Terdapat dua bukti penting yang menunjukkan bahwa rantai polipeptida protein globular berlipat-lipat dengan erat dan bahwa konformasi yang berlipat-lipat ini penting bagi fungsi biologisnya 1. Protein globular mengalami denaturasi dengan pemanasan atau p. H yang ekstrim 2. Perbandingan panjang rantai polipeptida dengan ukuran molekular sebenarnya diperlihatkan oleh pengukuran fisiokimia

STRUKTUR PROTEIN GLOBULAR •

PENGGOLONGAN ASAM AMINO BERDASARKAN POLARITAS DAN LETAK ASAM AMINO YANG SANGAT HIDROFILIK PERMUKAAN LUAR PROTEIN GLOBULAR • Asam aspartate • Asam glutamate • Asparagin • Glutamin • Lisin • Arginin • Histidin

PENGGOLONGAN ASAM AMINO BERDASARKAN POLARITAS DAN LETAK ASAM AMINO YANG SANGAT HIDROFOBIK BAGIAN DALAM PROTEIN GLOBULAR • Fenilalanin • Leusin • Isoleusin • Metionin • Valin • Triptofan

PENGGOLONGAN ASAM AMINO BERDASARKAN POLARITAS DAN LETAK ASAM AMINO DENGAN POLARITAS ANTARA BAGIAN DALAM DAN LUAR PROTEIN GLOBULAR • Prolin • Treonin • Serin • Sistein • Alanin • Glisin • Tirosin

JENIS GAYA YANG MENSTABILKAN STRUKTUR TERSIER 1. Ikatan hidrogen di anatara gugus R residu pada simpul yang berdekatan di dalam rantai 2. Gaya Tarik-menarik ionik di antara gugus R yang muatannya berlawanan 3. Interaksi hidrofobik 4. Jembatan kovalen residu sistin jembatan disulfida

TERIMA KASIH
- Slides: 37