Propionibacterium acnes et infections osseuses Une espce ne

Propionibacterium acnes et infections osseuses Une espèce à ne pas négliger… Pr Anne Jolivet-Gougeon CRIOGO Rennes 12 mars 2015 1
Généralités 2

P. acnes • Bacille Gram + anaérobie • Commensal de la flore cutanée • Lipophile (Ac. G du sebum) 3

Facteurs de virulence (1) Séquençage de génomes : • protéines cytotoxiques • enzymes permettant la phosphorylation oxydative et la respiration anaérobie, marqueurs responsables de la protection de la cellule contre les effets toxiques de la teneur en oxygène réduite • hémolysines ou cytotoxines (Camp factor, hémolysine III) • enzymes ou molécules impliquées dans la dégradation des tissus de l’hôte (lipase Geha, lysophospholipase, hyaluronate lyase, endoglycocéramidase, etc. ) • protéines impliquées dans le métabolisme du fer (Hta. A) Mc. Dowell A, Nagy I, Magyari M, Barnard E, Patrick S. The opportunistic pathogen Propionibacterium acnes: insights into typing, human disease, clonal diversification and CAMP factor evolution. PLo. S One 2013; 8: e 70897. Brüggemann H. Insights in the pathogenic potential of Propionibacteriumacnes from its complete genome. Semin Cutan Med Surg 2005; 24: 67– 72. 4

Facteurs de virulence (2) P. acnes porte des composants sur sa surface agissant comme antigènes, qui peuvent : - déclencher ou médier un processus inflammatoire : - - activation des récepteurs Toll-like (transcription des facteurs NF-k. B et STAT 3), activation de la sécrétion de cytokines par les cellules infectées, comme l'IL-6 ou IL-8 (études du sécrétome) présenter des propriétés de cellules adhérentes (adhésine dermatane-sulfate, type 3 protéines de répétition Thrombospondin) et invasives (PAmce et PAp 60). Variable selon le sérotype (I>II) (si mutations dans gènes) Certaines protéines pourraient donc être : - impliquées dans l'inflammation (cutané, sarcoïdose) en conditions limitées en oxygène essentielles pour l’adhérence aux tissus de la peau ou aux dispositifs médicaux (biofilm) Brzuszkiewicz E, Weiner J, Wollherr A, Thürmer A, Hüpeden J, Lomholt. HB, et al. Comparative genomics and transcriptomics of Propionibacteriumacnes. PLo. S One 2011; 6: e 21581. Achermann Y, Goldstein EJ, Coenye T, Shirtliff ME. Propionibacterium acnes: from commensal to opportunistic biofilm-associated implant pathogen. Clin Microbiol Rev. 2014 Jul; 27(3): 419 -40. 5
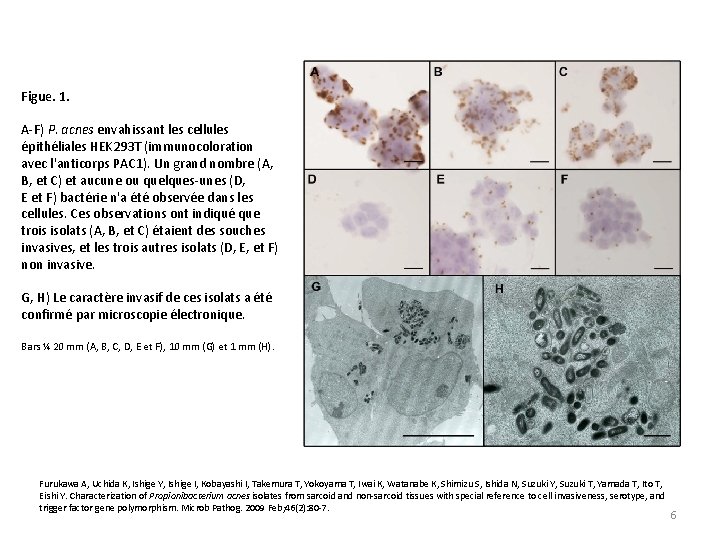
Figue. 1. A-F) P. acnes envahissant les cellules épithéliales HEK 293 T (immunocoloration avec l'anticorps PAC 1). Un grand nombre (A, B, et C) et aucune ou quelques-unes (D, E et F) bactérie n'a été observée dans les cellules. Ces observations ont indiqué que trois isolats (A, B, et C) étaient des souches invasives, et les trois autres isolats (D, E, et F) non invasive. G, H) Le caractère invasif de ces isolats a été confirmé par microscopie électronique. Bars ¼ 20 mm (A, B, C, D, E et F), 10 mm (G) et 1 mm (H). Furukawa A, Uchida K, Ishige Y, Ishige I, Kobayashi I, Takemura T, Yokoyama T, Iwai K, Watanabe K, Shimizu S, Ishida N, Suzuki Y, Suzuki T, Yamada T, Ito T, Eishi Y. Characterization of Propionibacterium acnes isolates from sarcoid and non-sarcoid tissues with special reference to cell invasiveness, serotype, and trigger factor gene polymorphism. Microb Pathog. 2009 Feb; 46(2): 80 -7. 6

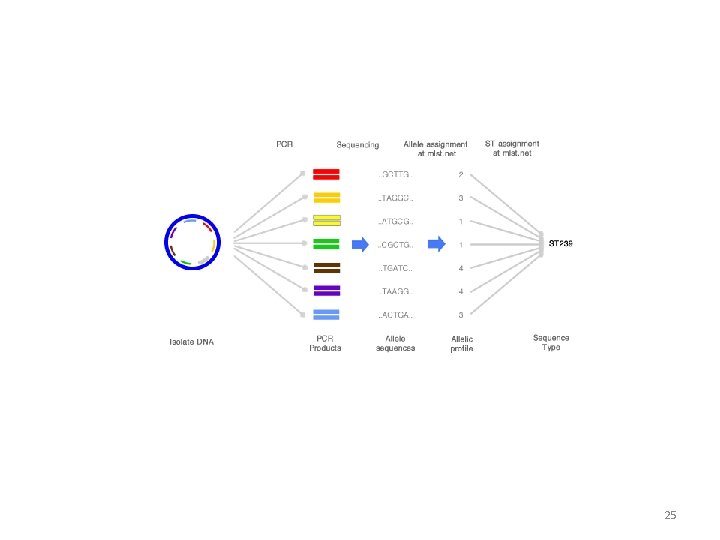
Typage moléculaire À l’origine, 2 sérotypes I et II MLST de 372 isolats de P. acnes. 7

Typage moléculaire PCR multiplex : plus rapide o o o 16 S r. RNA (tous les isolats) ATPase (type IA 1, IA 2, IC) sod. A (type IA 2, IB) atp. D (type II) rec. A (type III) Fic family toxin gene (type IC). 312 P. acnes type IA 1 (n = 145) type IA 2 (n = 20) type IB (n = 65) type CI (n = 7) type II (n = 45) type III (n = 30) 100% de sensibilité 100% de spécificité par rapport à MLST Barnard E, Nagy I, Hunyadkürti J, Patrick S, Mc. Dowell A. Multiplex Touchdown PCR for Rapid Typing of the Opportunistic Pathogen Propionibacterium acnes. J Clin Microbiol. 2015 Jan 28. 8

Epidémiologie 9

P. acnes Responsable d’infections opportunistes et infections ostéoarticulaires (chroniques) - Environ 10% des infections (taux sûrement sous-estimé) Trampuz A, Piper KE, Jacobson MJ, Hanssen AD, Unni KK, Osmon DR, et al. Sonication of removed hip and knee prostheses for diagnosis ofinfection. N Engl J Med 2007; 357(7): 654– 63. - Principalement au niveau de l’épaule Piper KE, Jacobson MJ, Cofield RH, Sperling JW, Sanchez-Sotelo J, Osmon DR, et al. Microbiologic diagnosis of prosthetic shoulder infectionby use of implant sonication. J Clin Microbiol 2009; 47(6): 1878– 84. - Infections tardives, survenant 3 -24 mois ou plus après la pose de la prothèse. 10
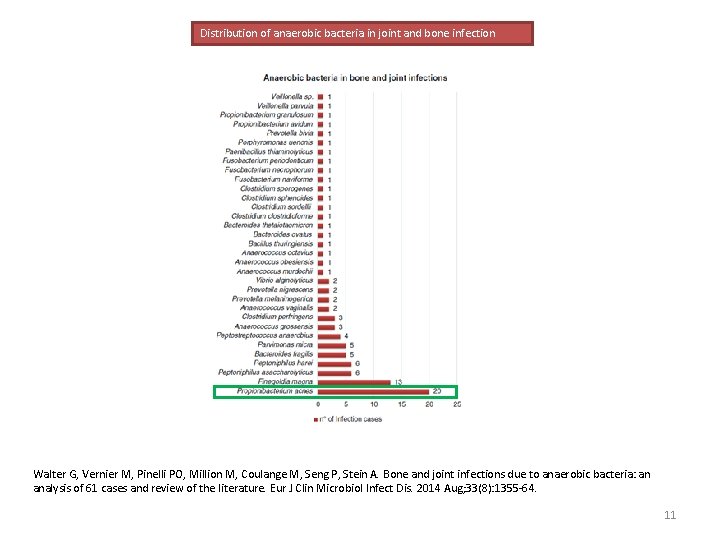
Distribution of anaerobic bacteria in joint and bone infection Walter G, Vernier M, Pinelli PO, Million M, Coulange M, Seng P, Stein A. Bone and joint infections due to anaerobic bacteria: an analysis of 61 cases and review of the literature. Eur J Clin Microbiol Infect Dis. 2014 Aug; 33(8): 1355 -64. 11
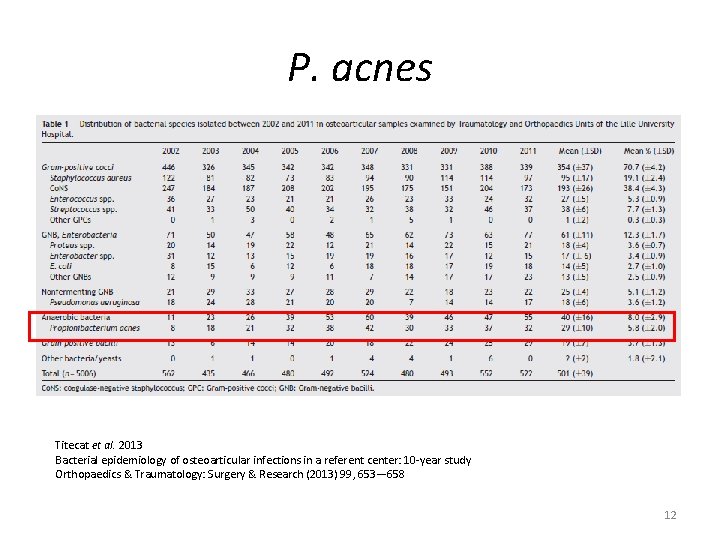
P. acnes Titecat et al. 2013 Bacterial epidemiology of osteoarticular infections in a referent center: 10 -year study Orthopaedics & Traumatology: Surgery & Research (2013) 99, 653— 658 12

Au CHU de Rennes 2011 -2014 50 45 40 35 30 25 Nombre d'isolats de P. acnes dans les liquides articulaires 20 15 10 5 0 2010 -5 2011 2012 2013 2014 2015 Bjerke-Kroll BT, Christ AB, Mc. Lawhorn AS, Sculco PK, Jules-Elysée KM, Sculco TP. Periprosthetic joint infections treated with two-stage revision over 14 years: an evolving microbiology profile. J Arthroplasty. 2014 May; 29(5): 877 -82. 13

Diagnostic 14

Infections osseuses à P. acnes • Souvent peu ou pas de perturbation biologique : leucocytes, CRP, VS…(= faible virulence et/ ou faible inoculum) • Descellement aseptique de prothèse en l'absence d'arguments cliniques et microbiologiques pourrait être lié à une infection de bas grade Nelson CL, Mc. Laren AC, Mc. Laren SG, Johnson JW, Smeltzer MS. Isaseptic loosening truly aseptic? Clin Orthop Relat Res 2005; (437): 25– 30. • Nécessité de prolonger l’incubation des cultures > 13 j 15

But de l’étude : Evaluer l'utilité diagnostique de mesurer les niveaux de l'interleukine-6 (IL-6) dans le liquide synovial d'épaule, pour identifier une infection ostéoarticulaire. q Echantillons provenant de patients : 15 infectés et 20 non infectés q Dosage immunologique de cytokines par détection électrochimiluminescence. q Courbe ROC utilisée pour déterminer l'utilité diagnostique de l’analyse de l’l. L-6 dans le fluide synovial. Aire sous la courbe de 0, 891 (valeur seuil : 359, 3 pg / m. L) 7 patients qui ont subi une révision en une seule étape ont eu des résultats bio négatifs (VS, CRP), mais avec plusieurs cultures de tissus peropératoires positifs. IL-6 élevée chez 5/7 patients (médiane de 1 400 pg / m. L) Significativement plus élevé chez les patients atteints d'une infection due à P. acnes (p = 0, 01). Frangiamore SJ et al. Synovial fluid interleukin-6 as a predictor of periprosthetic shoulder infection. J Bone Joint Surg Am. 2015 Jan 7; 97(1): 63 -70. 16

But de l’étude : Evaluer l'utilité diagnostique de mesurer les niveaux de l’ α-Defensine dans le liquide synovial d'épaule, pour identifier une infection ostéoarticulaire. q. Echantillons provenant de patients : 11 infectés et 22 non infectés q. Dosage par Synovasure (Diagnostic CD, Wynnewood, PA, USA). q. Courbe ROC utilisée pour déterminer l'utilité diagnostique de l’analyse de l’α-defensine dans le fluide synovial. Aire sous la courbe de 0, 78 Niveau de l’α-défensine synoviale élevée en présence d'une culture positive pour P. acnes (médiane 1, 33 S / CO; P = 0, 03); corrélation moyenne avec le nombre de cultures positives). Synovasure™ Test Frangiamore Sj et al. α-Defensin as a predictor of periprosthetic shoulder infection. J Shoulder Elbow Surg. 2015 Feb 8. 95% Confidence Interval Sensitivity 97. 4% Specificity (excluding cases of metallosis) 97. 1% Specificity (including cases of metallosis) 95. 8% 63% 95%, 86. 1% - 99. 6% 93. 0% - 99. 7% 90. 5% - 98. 6% 17
Traitement 18

Mécanismes de résistance Aubin GG, Portillo ME, Trampuz A, Corvec S. Propionibacterium acnes, an emerging pathogen: from acne to implant-infections, from phylotype to resistance. Med Mal Infect. 2014 Jun; 44(6): 241 -50. 19

P. acnes • Pénicillines (Penicilline G) et céphalosporins (ceftriaxone) actives contre les infections cliniques à P. acnes (planctonique et biofilm) in vitro. • Vancomycine, utilisée si allergie • Resistance au métronidazole, fosfomycine et gentamicine 20

Infections sur prothèses à Propionibacterium acnes genou (n = 5), hanche (n = 17), épaule (n = 33) MATERIALS AND METHODS: CMIs de 55 isolats cliniques de P. acnes, mesurées par E tests : benzylpenicillin, clindamycine, métronidazole, acide fusidique, doxycycline, moxifloxacine, linezolide et rifampicine. Tests de synergie entre Rfa et autres ATB RESULTS: 100% resistance to metronidazole 9. 1% diminution de sensibilité à la clindamycine 1. 8% diminution de sensibilité à la moxifloxacin. rifampicin + benzylpenicillin : action synergique sur près de la moitié des isolats. Rares effets antagonistes Khassebaf J et al. 2014. Antibiotic susceptibility of Propionibacterium acnes isolated from orthopaedic implant-associated infections. Anaerobe. 2014 Dec 23; 32 C: 57 -62. 21

P. acnes • Une association rifampicine et daptomycine plus efficace in vivo (biofilm). Treatment activity against biofilm P. acnes. Shown are the cure rates of adherent bacteria from explanted cages. The percentages above the columns indicate the cure rates. *, P < 0. 05; **, P < 0. 01; ***, P < 0. 005. Furustrand Tafin U et al. Role of rifampin against Propionibacterium acnes biofilm in vitro and in an experimental foreign-body infection model. Antimicrob Agents Chemother. 2012 Apr; 56(4): 1885 -91. 22

Conclusion • Prolonger les cultures pour isoler la souche • Traitement antibiotique simple • Infections persistantes (biofilms) 23

24
25
- Slides: 25