PROPIEDADES QUMICAS DE LOS COMPUESTOS AROMTICOS SUSTITUCIN NUCLEOFLICA











- Slides: 28

PROPIEDADES QUÍMICAS DE LOS COMPUESTOS AROMÁTICOS

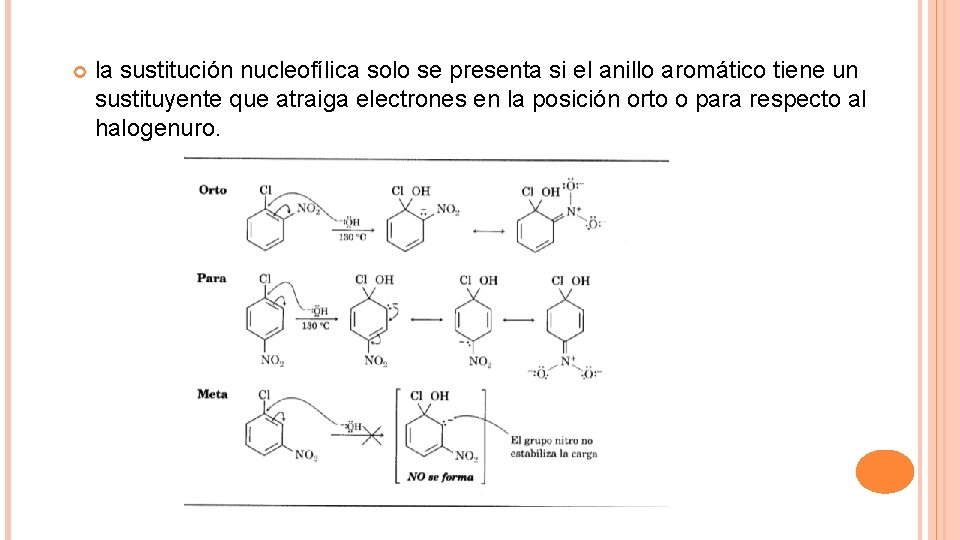
SUSTITUCIÓN NUCLEOFÍLICA AROMÁTICA Las sustituciones nucleofílicas en un anillo aromático se efectúan por un mecanismo de adicción/eliminación. El nucleofílo atacante se suma primero al halogenuro de arilo deficiente en electrones y forma un intermediario con carga negativa estabilizado por resonancia. Llamado complejo de Meisenheimer. El ion halogenuro se elimina en una segunda etapa.

la sustitución nucleofílica solo se presenta si el anillo aromático tiene un sustituyente que atraiga electrones en la posición orto o para respecto al halogenuro.

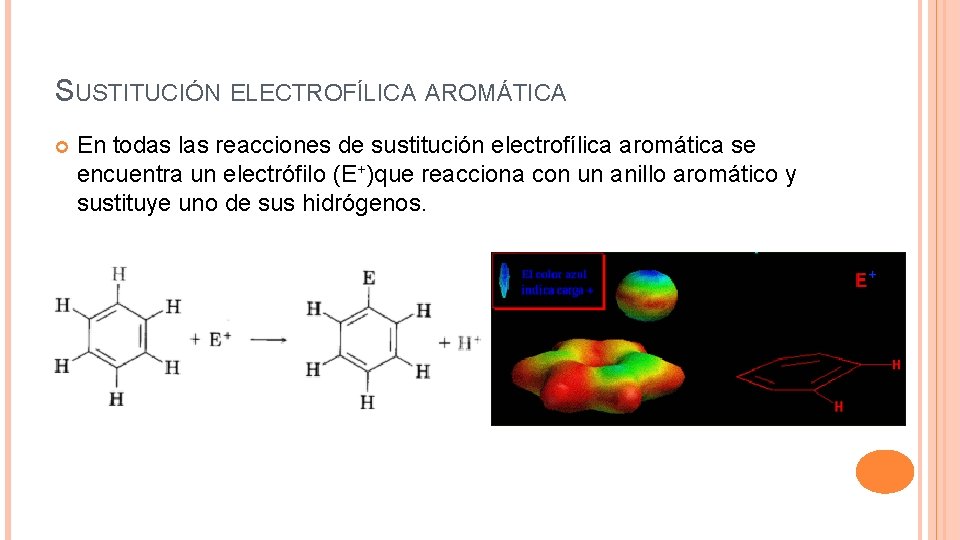
SUSTITUCIÓN ELECTROFÍLICA AROMÁTICA En todas las reacciones de sustitución electrofílica aromática se encuentra un electrófilo (E+)que reacciona con un anillo aromático y sustituye uno de sus hidrógenos.

HALOGENACION DEL BENCENO En la bromacion y cloración del benceno se necesita un acido de Lewis. Reacción completa:

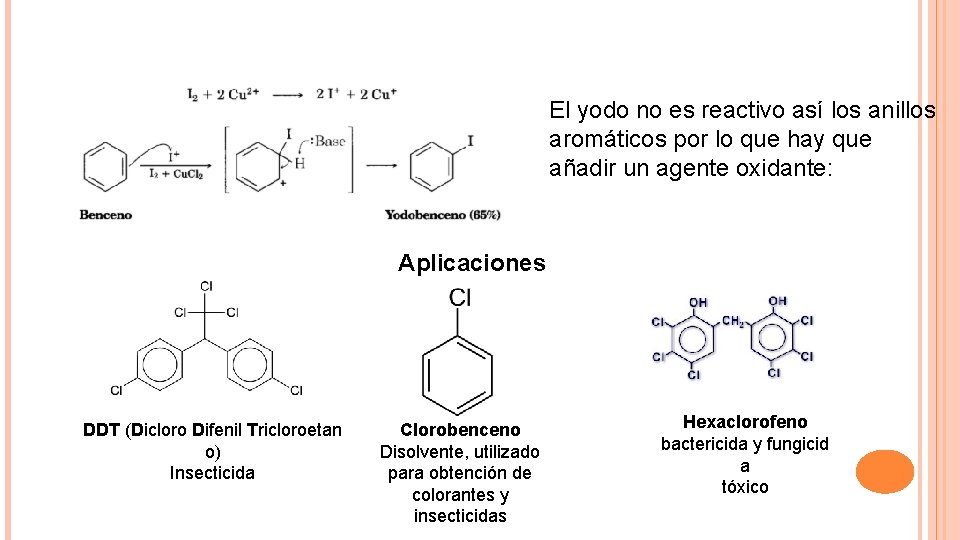
El yodo no es reactivo así los anillos aromáticos por lo que hay que añadir un agente oxidante: Aplicaciones DDT (Dicloro Difenil Tricloroetan o) Insecticida Clorobenceno Disolvente, utilizado para obtención de colorantes y insecticidas Hexaclorofeno bactericida y fungicid a tóxico

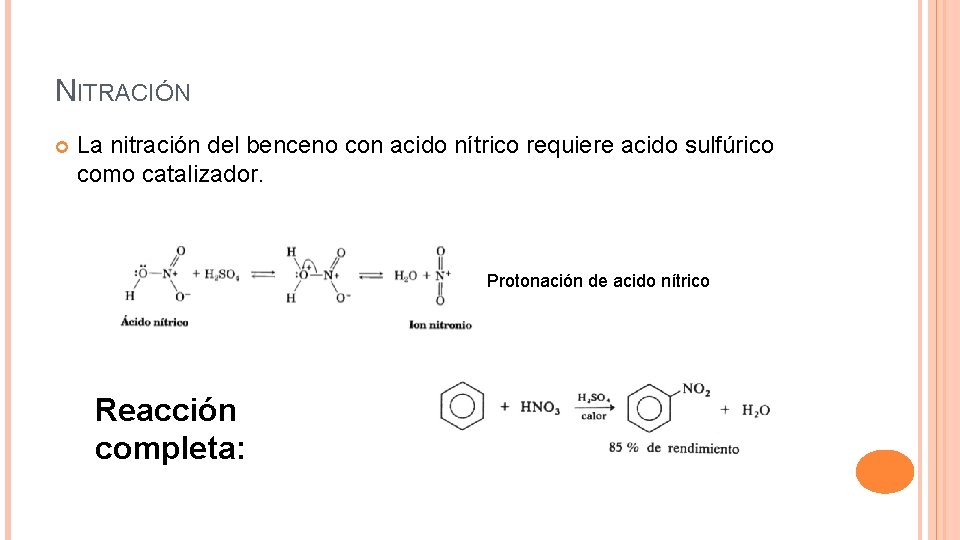
NITRACIÓN La nitración del benceno con acido nítrico requiere acido sulfúrico como catalizador. Protonación de acido nítrico Reacción completa:

APLICACIONES El nitrobenceno es un compuesto de partida importante en la síntesis de diversos productos orgánicos, y aparte de la anilina, para sintetizar la benzidina, el trinitrobenceno, el ácido nitrobenzolsulfónico, la fucsina, la quinolina o fármacos como el acetoaminofeno.

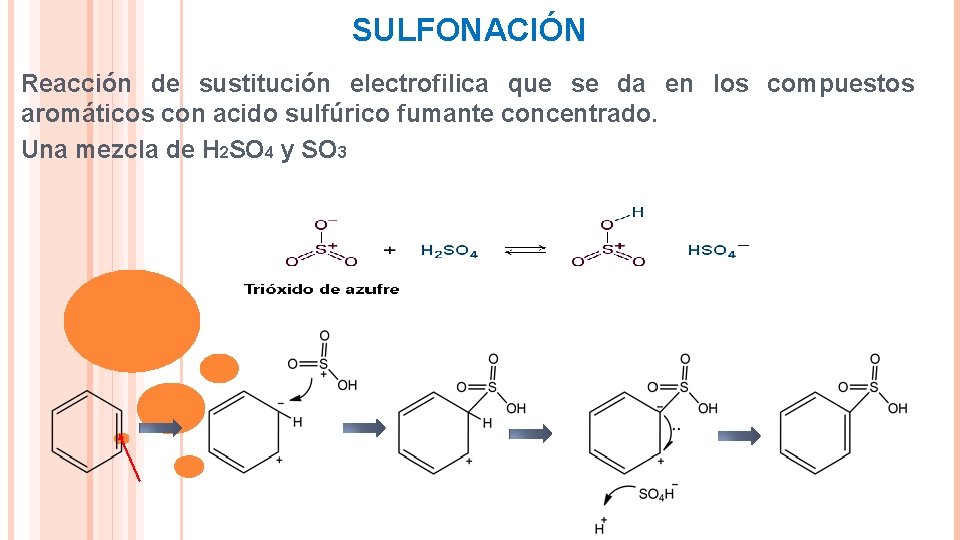
SULFONACIÓN Reacción de sustitución electrofilica que se da en los compuestos aromáticos con acido sulfúrico fumante concentrado. Una mezcla de H 2 SO 4 y SO 3

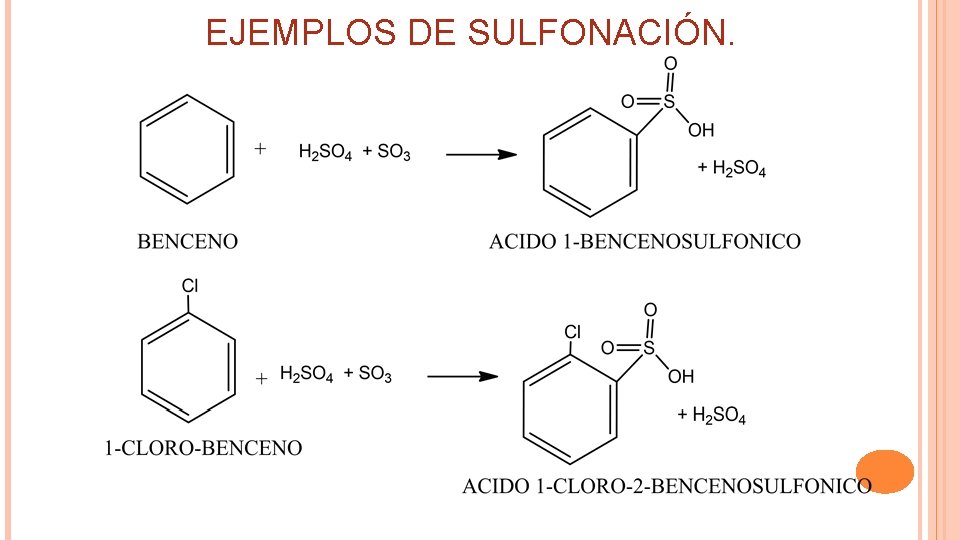
EJEMPLOS DE SULFONACIÓN.

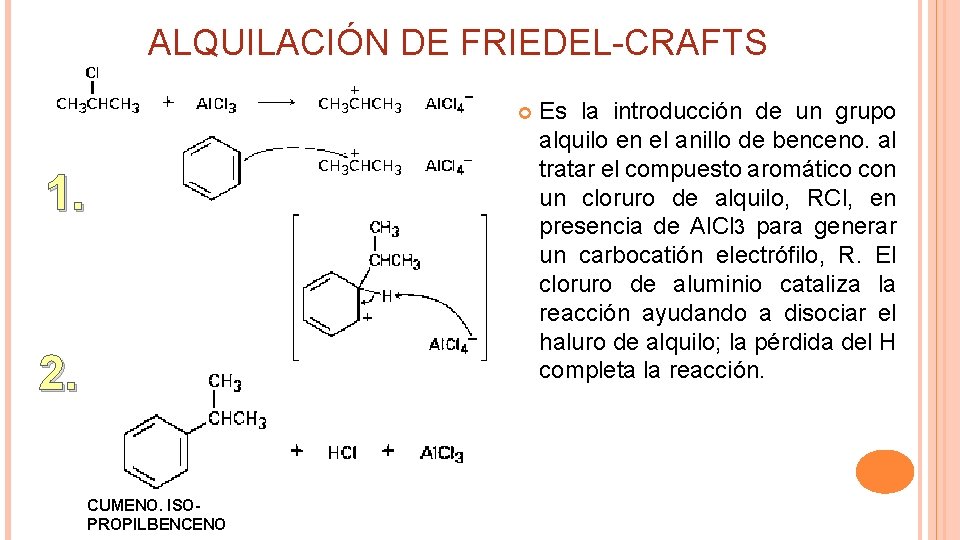
ALQUILACIÓN DE FRIEDEL-CRAFTS 1. 2 CUMENO. ISOPROPILBENCENO Es la introducción de un grupo alquilo en el anillo de benceno. al tratar el compuesto aromático con un cloruro de alquilo, RCl, en presencia de Al. Cl 3 para generar un carbocatión electrófilo, R. El cloruro de aluminio cataliza la reacción ayudando a disociar el haluro de alquilo; la pérdida del H completa la reacción.

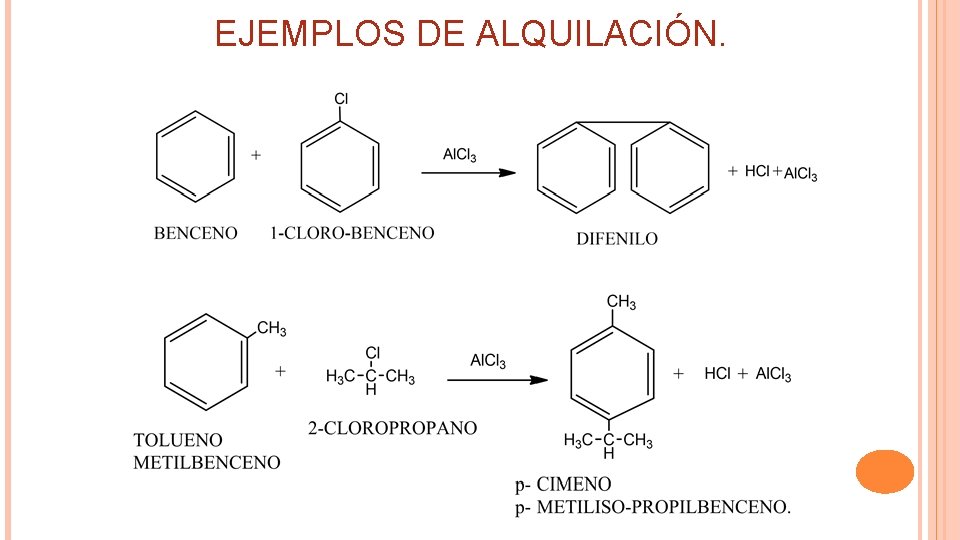
EJEMPLOS DE ALQUILACIÓN.

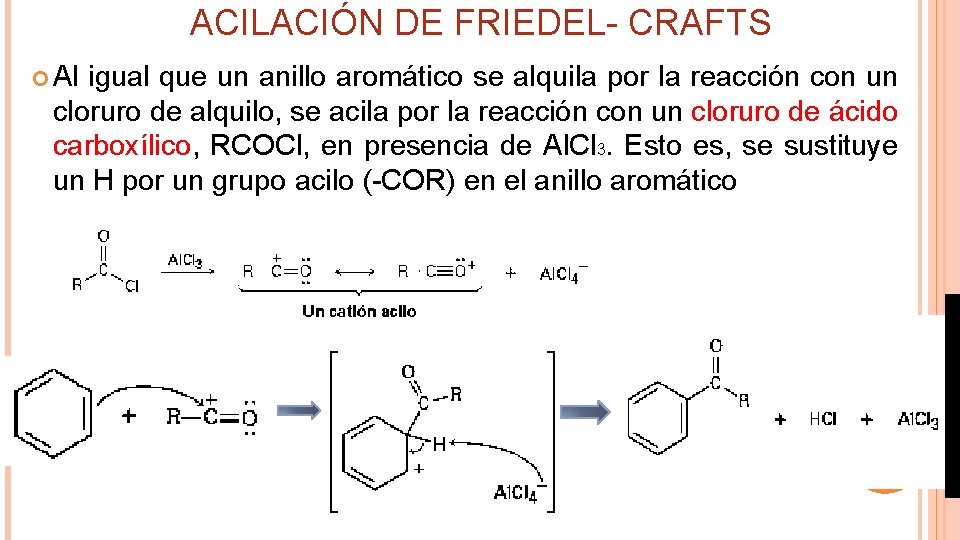
ACILACIÓN DE FRIEDEL- CRAFTS Al igual que un anillo aromático se alquila por la reacción con un cloruro de alquilo, se acila por la reacción con un cloruro de ácido carboxílico, RCOCl, en presencia de Al. Cl 3. Esto es, se sustituye un H por un grupo acilo (-COR) en el anillo aromático

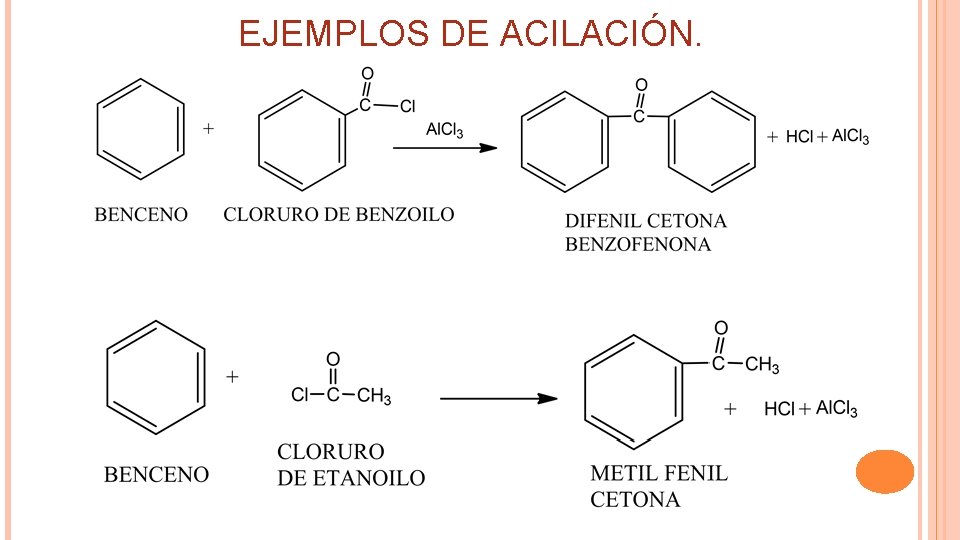
EJEMPLOS DE ACILACIÓN.

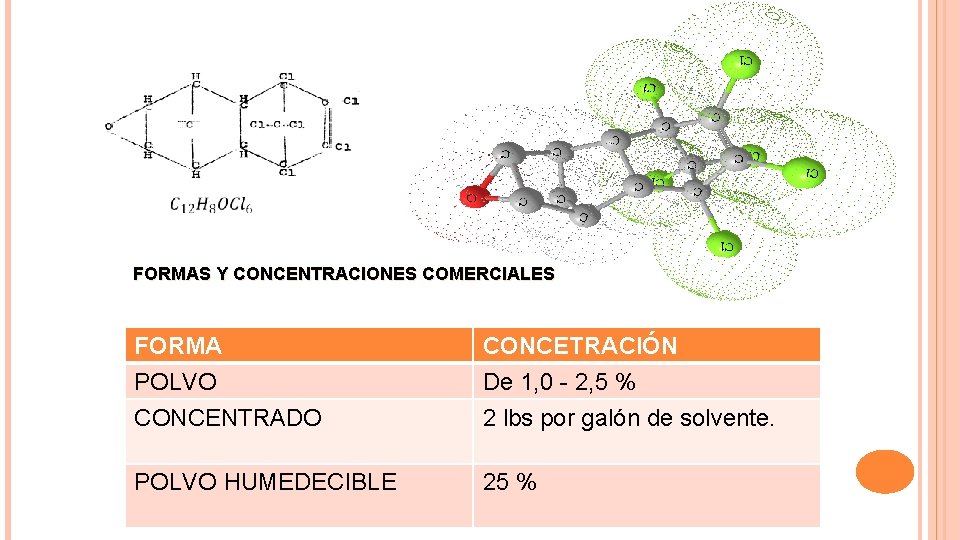
ALDRÍN Hexacloro- hexahidro- dimetanonaftaleno. Insecticidas sintéticos. Sólido, cristalino, de color blancuzco. Su punto de fusión y ebullición es cerca de 104 °C – 145°C. Densidad: 1, 54 g/cc. Una de sus ventajas químicas parece ser su estabilidad con sustancias de alcalinidad relativa.

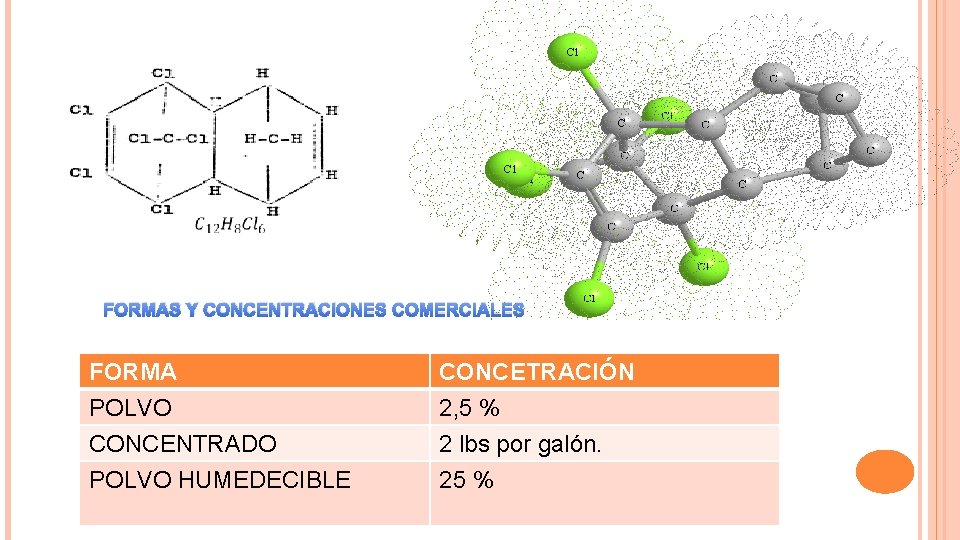
FORMAS Y CONCENTRACIONES COMERCIALES FORMA POLVO CONCENTRADO POLVO HUMEDECIBLE CONCETRACIÓN 2, 5 % 2 lbs por galón. 25 %

CONTROLA… INSECTOS (ANIMALES) INSECTOS (VEGETALES) Hormigas (varias especies) Gorgojos de semilla Piojo humano Moscas de raíces Plagas subterráneas Chinches de la raíz (maíz) Gusano- alambre. Escarabajo cortadores Gorgojos Gusanos cortadores Mosca casera Plagas de la alfalfa Mosquito y zancudos Curculíos o picudos Langostas Cigarras Cucarachas

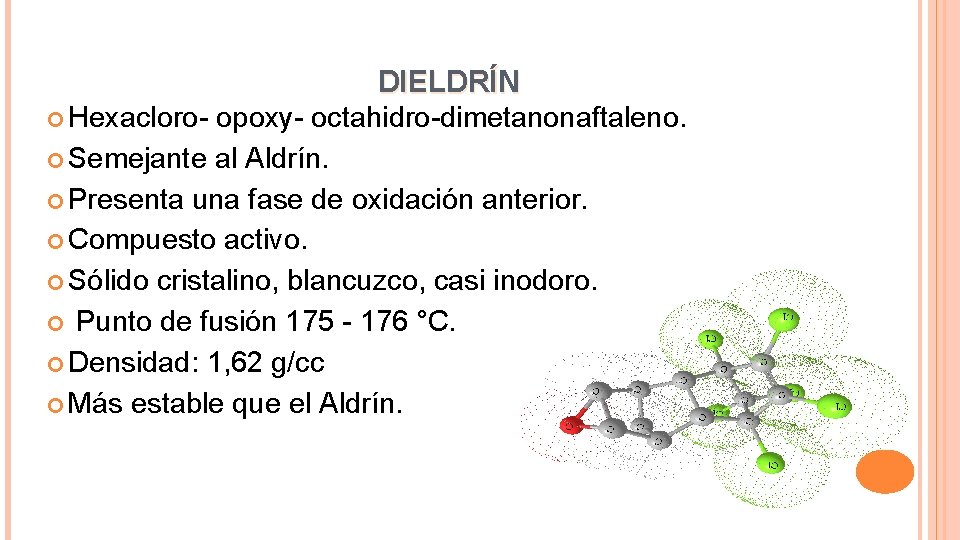
DIELDRÍN Hexacloro- opoxy- octahidro-dimetanonaftaleno. Semejante al Aldrín. Presenta una fase de oxidación anterior. Compuesto activo. Sólido cristalino, blancuzco, casi inodoro. Punto de fusión 175 - 176 °C. Densidad: 1, 62 g/cc Más estable que el Aldrín.

FORMAS Y CONCENTRACIONES COMERCIALES FORMA POLVO CONCENTRADO CONCETRACIÓN De 1, 0 - 2, 5 % 2 lbs por galón de solvente. POLVO HUMEDECIBLE 25 %

CONTROLA… INSECTOS (ANIMALES) INSECTOS (VEGETALES) Polillas y otros Insectos de la madera Insectos de ropero Plagas forestales Cucarachas Plagas subterráneas Comejenes o termitas Áfidos de raíces Hormigas Gusanos cortadores Langostas Gusano - alambre Zancudos Escarabajos cortadores Grillos Chinche de la raíz del maíz

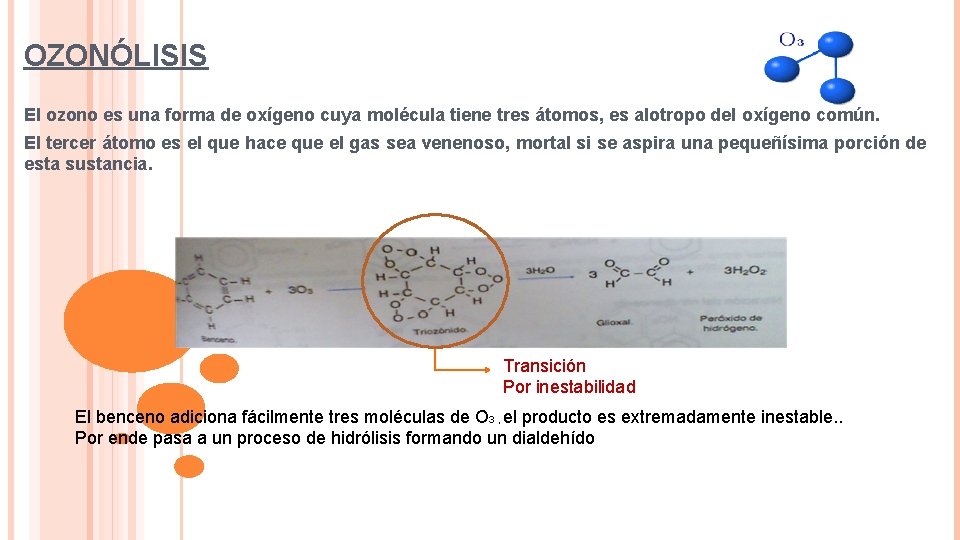
OZONÓLISIS El ozono es una forma de oxígeno cuya molécula tiene tres átomos, es alotropo del oxígeno común. El tercer átomo es el que hace que el gas sea venenoso, mortal si se aspira una pequeñísima porción de esta sustancia. Transición Por inestabilidad El benceno adiciona fácilmente tres moléculas de O 3 , el producto es extremadamente inestable. . Por ende pasa a un proceso de hidrólisis formando un dialdehído

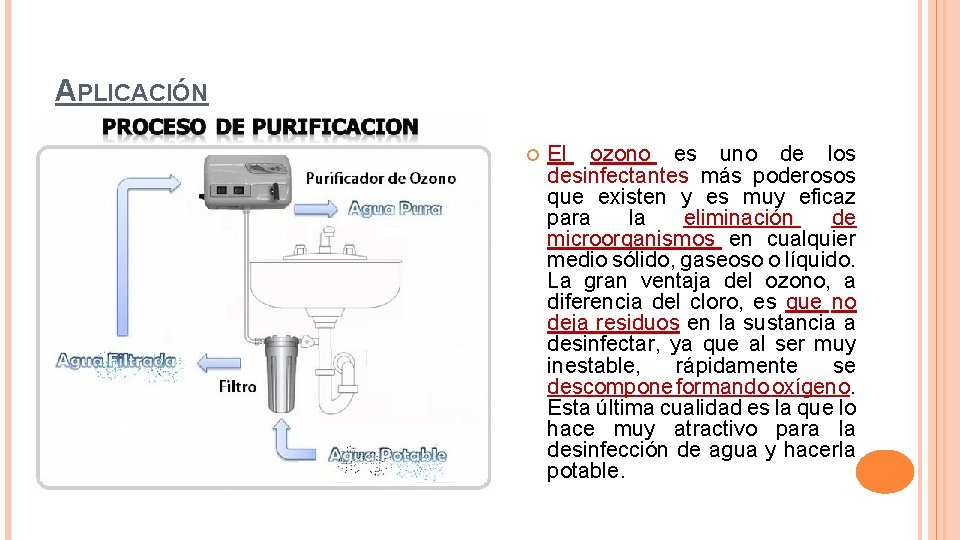
APLICACIÓN El ozono es uno de los desinfectantes más poderosos que existen y es muy eficaz para la eliminación de microorganismos en cualquier medio sólido, gaseoso o líquido. La gran ventaja del ozono, a diferencia del cloro, es que no deja residuos en la sustancia a desinfectar, ya que al ser muy inestable, rápidamente se descompone formando oxígeno. Esta última cualidad es la que lo hace muy atractivo para la desinfección de agua y hacerla potable.

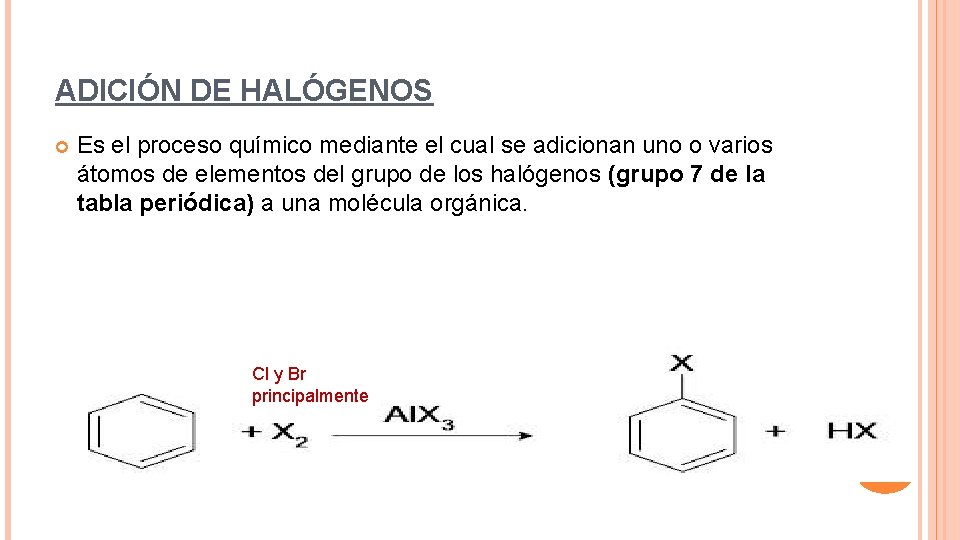
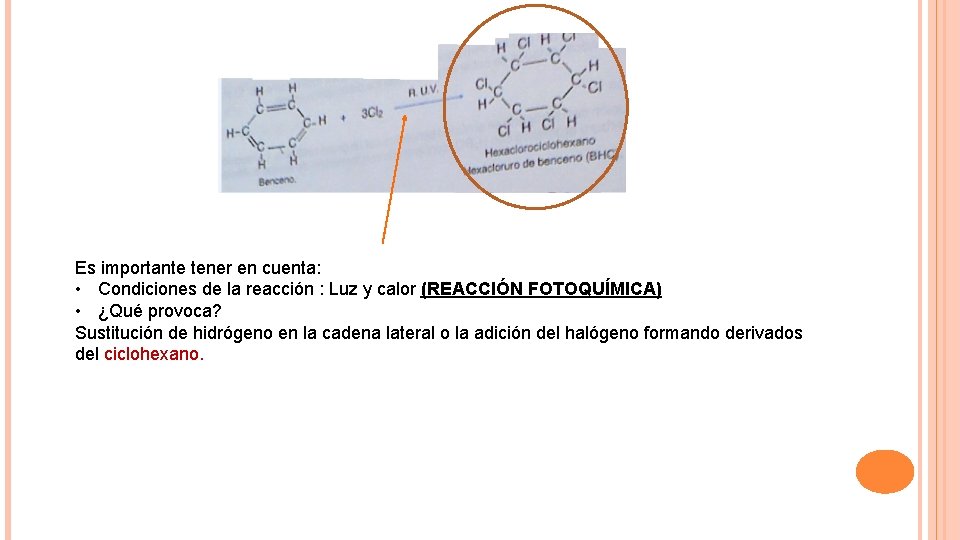
ADICIÓN DE HALÓGENOS Es el proceso químico mediante el cual se adicionan uno o varios átomos de elementos del grupo de los halógenos (grupo 7 de la tabla periódica) a una molécula orgánica. Cl y Br principalmente

Es importante tener en cuenta: • Condiciones de la reacción : Luz y calor (REACCIÓN FOTOQUÍMICA) • ¿Qué provoca? Sustitución de hidrógeno en la cadena lateral o la adición del halógeno formando derivados del ciclohexano.

APLICACIÓN Insecticida BHC (lindano) : El lindano se utiliza para tratar la pediculosis (infestación de piojos) y la sarna, pero puede provocar efectos secundarios graves. En raros casos, el lindano ha ocasionado convulsiones e incluso la muerte.

REACCIÓN DE OXIDACIÓN El benceno tiene estabilidad de núcleo frente a la oxidación, este tipo de reacciones se presenta usualmente a temperaturas elevadas. El oxígeno del aire sobre el benceno, en presencia del catalizador pentóxido de vanadio, a alta temperatura (400ºC) produce el anhidrido maleico.

APLICACIONES El anhídrido maleico también se utiliza para la síntesis de varios plaguicidas (insecticidas y fungicidas, herbicidas, reguladores del crecimiento de las plantas), tales como malatión (ya no está en uso), daminozida (nombre comercial Alar, ya no está en uso), captán y endothal. El anhídrido maleico es muy irritante para los ojos, la piel y el tracto respiratorio.

A PARTIR DE LOS “ARENOS” SE PRODUCE LA OXIDACIÓN DE LAS CADENAS LATERALES ; NO IMPORTA LA COMPLEJIDAD DE LA CADENA , CUANDO HAY UN OXIDANTE FUERTE SE PRESENTA LA PRODUCCIÓN DEL GRUPO CARBOXILO.