Propiedades fsicas y efectos electrnicos Lic en Biotecnologa

Propiedades físicas y efectos electrónicos Lic. en Biotecnología Mariana Bianchi Química orgánica y biológica- Química orgánica

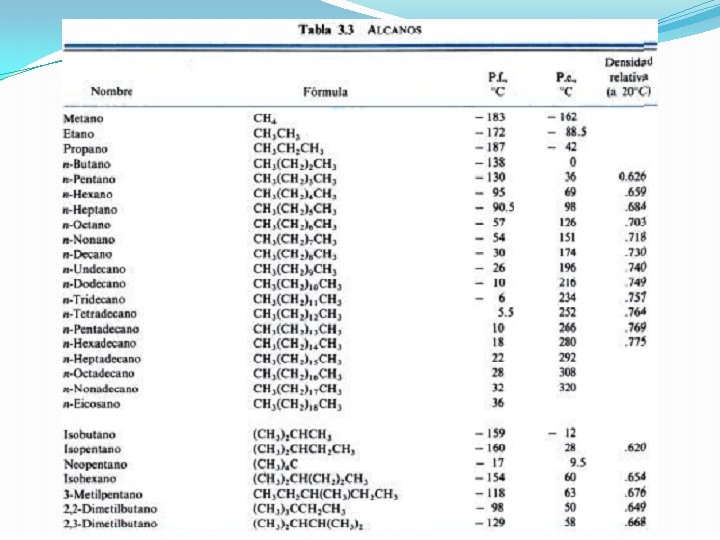
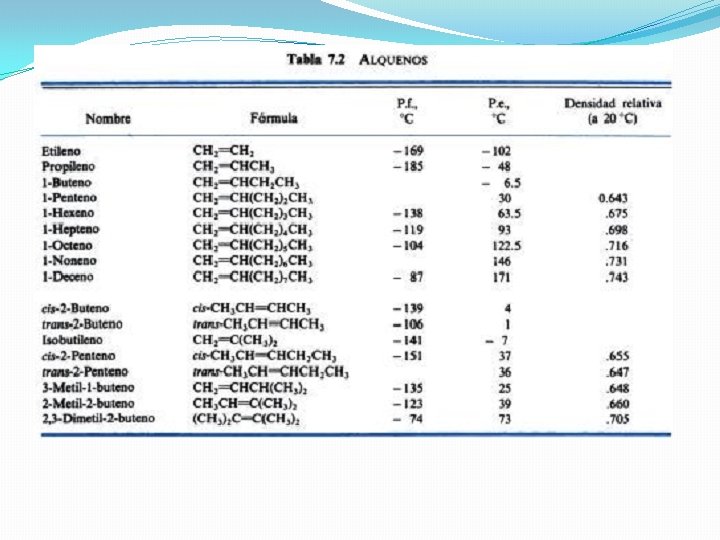
Punto de ebullición: Es la Temperatura a la cual la materia cambia de estado líquido a estado gaseoso Punto de fusión: Es la Temperatura a la cual la materia cambia de estado sólido a estado líquido En general… Para n-alcanos/alquenos/alquinos los PE y PF aumentan a medida que crece el número de C. Los procesos de ebullición y fusión requieren vencer las fuerzas intermoleculares de un líquido y un sólido; los puntos de ebullición y fusión suben porque dichas fuerzas se intensifican a medida que aumenta el tamaño molecular. Un isómero ramificado tiene un punto de ebullición más bajo que uno de cadena recta y además, cuanto más numerosas son las ramificaciones, menor es el punto de ebullición correspondiente.
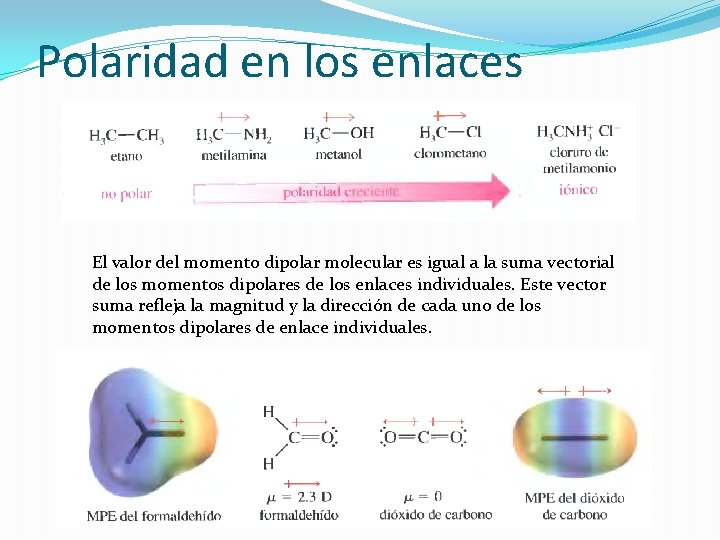
Polaridad en los enlaces El valor del momento dipolar molecular es igual a la suma vectorial de los momentos dipolares de los enlaces individuales. Este vector suma refleja la magnitud y la dirección de cada uno de los momentos dipolares de enlace individuales.
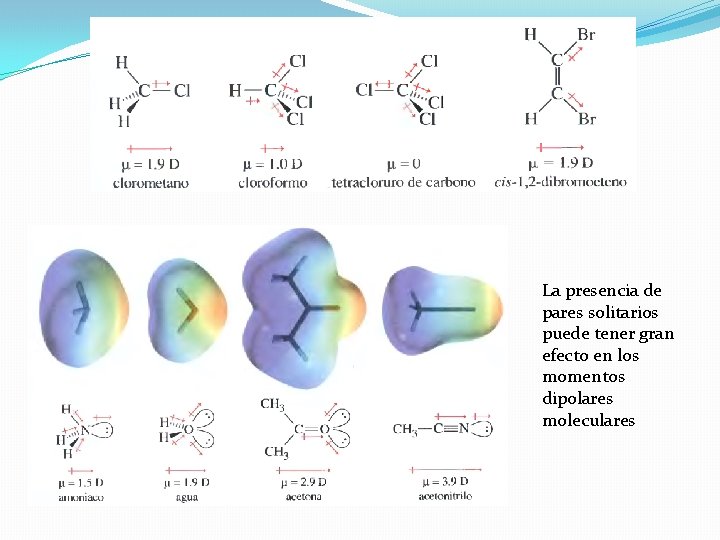
La presencia de pares solitarios puede tener gran efecto en los momentos dipolares moleculares
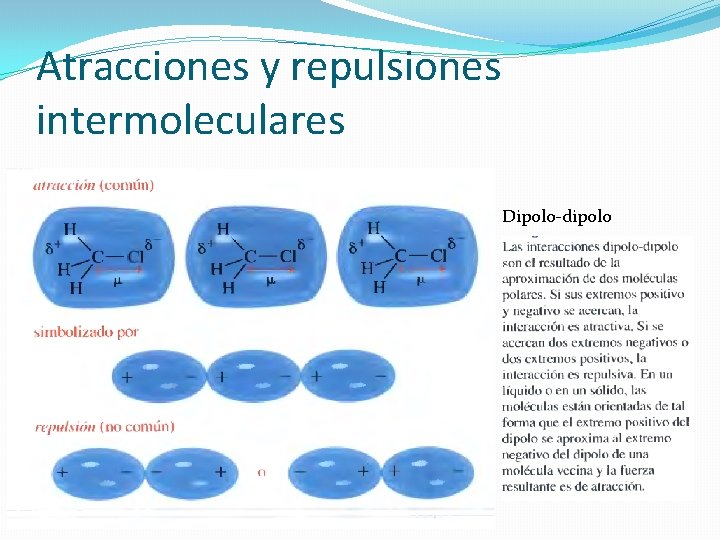
Atracciones y repulsiones intermoleculares Dipolo-dipolo

Fuerzas de dispersión de London
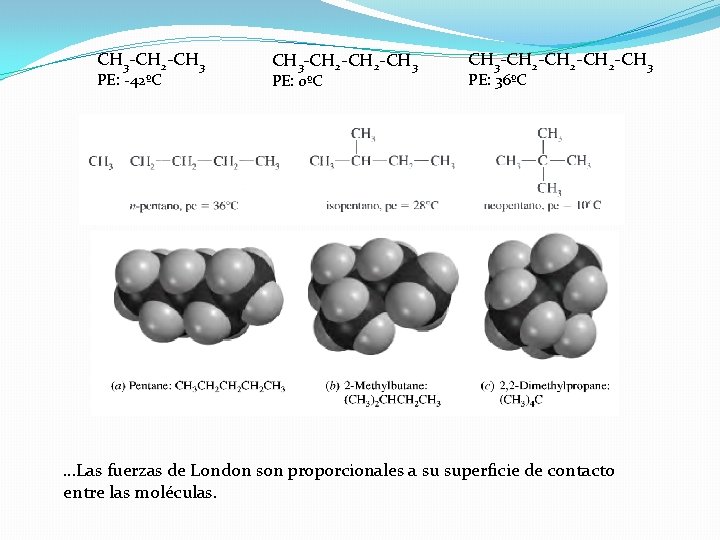
CH 3 -CH 2 -CH 3 PE: -42ºC CH 3 -CH 2 -CH 3 PE: 0ºC CH 3 -CH 2 -CH 3 PE: 36ºC …Las fuerzas de London son proporcionales a su superficie de contacto entre las moléculas.
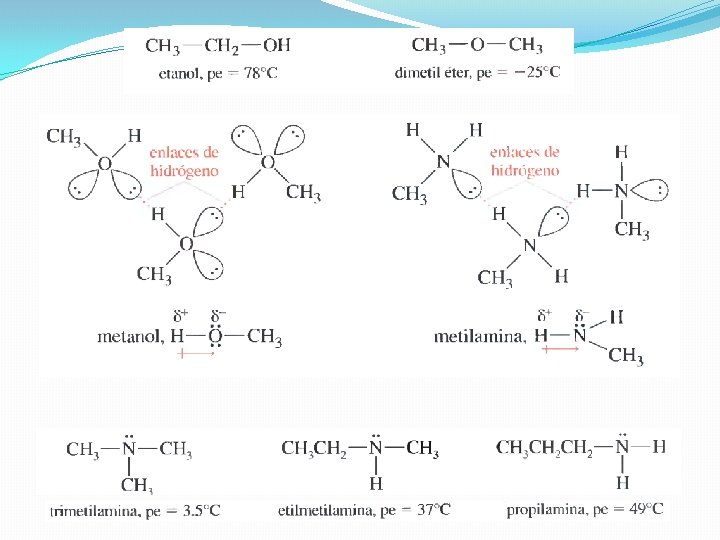
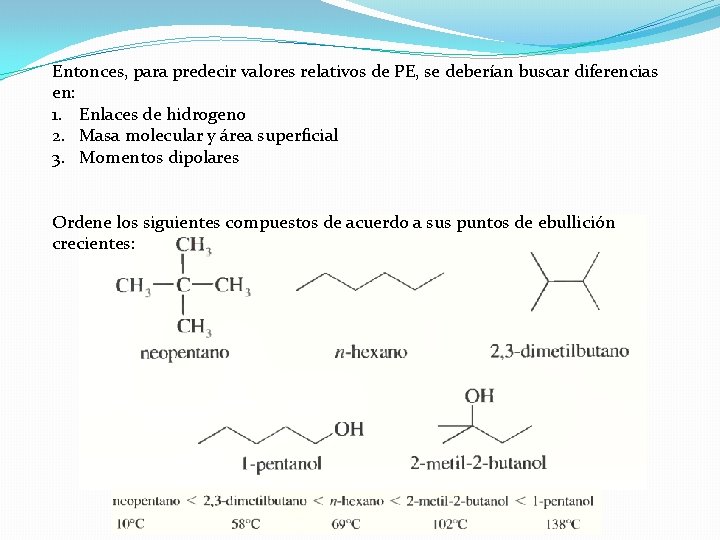
Entonces, para predecir valores relativos de PE, se deberían buscar diferencias en: 1. Enlaces de hidrogeno 2. Masa molecular y área superficial 3. Momentos dipolares Ordene los siguientes compuestos de acuerdo a sus puntos de ebullición crecientes:
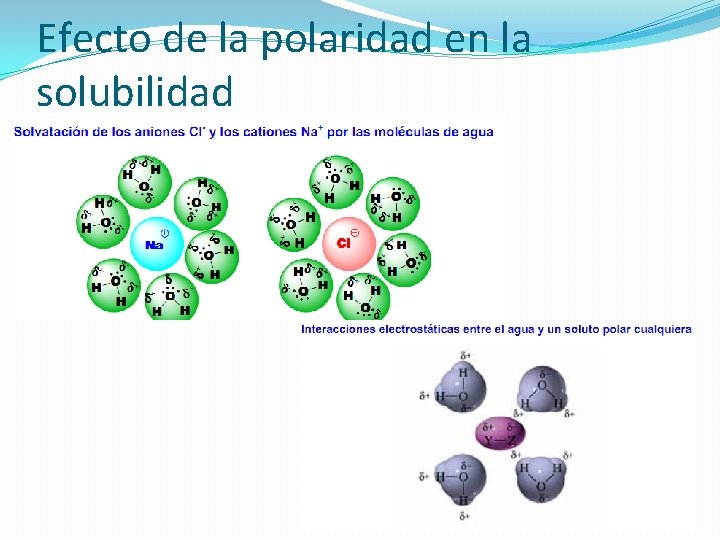
Efecto de la polaridad en la solubilidad
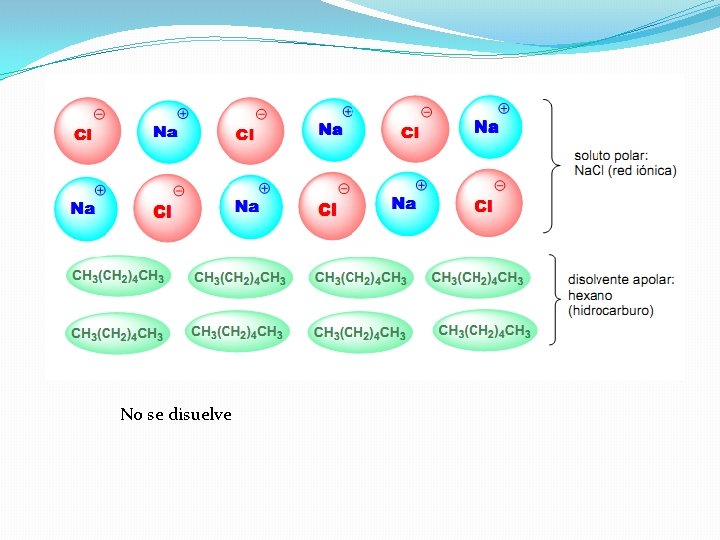
No se disuelve
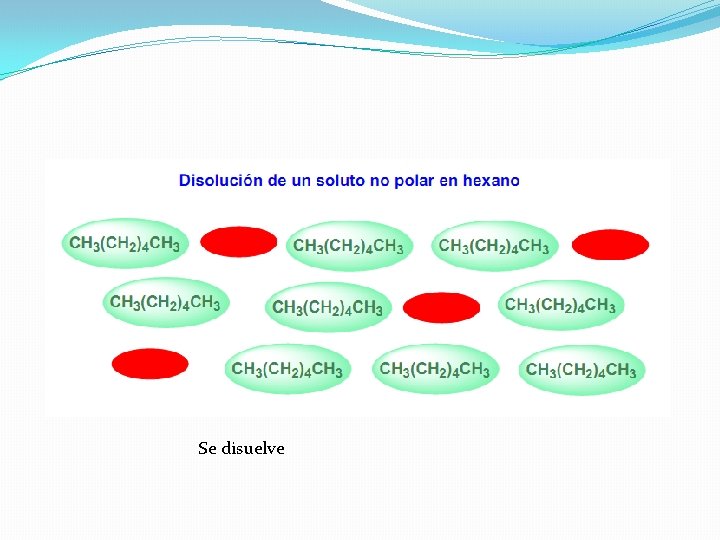
Se disuelve
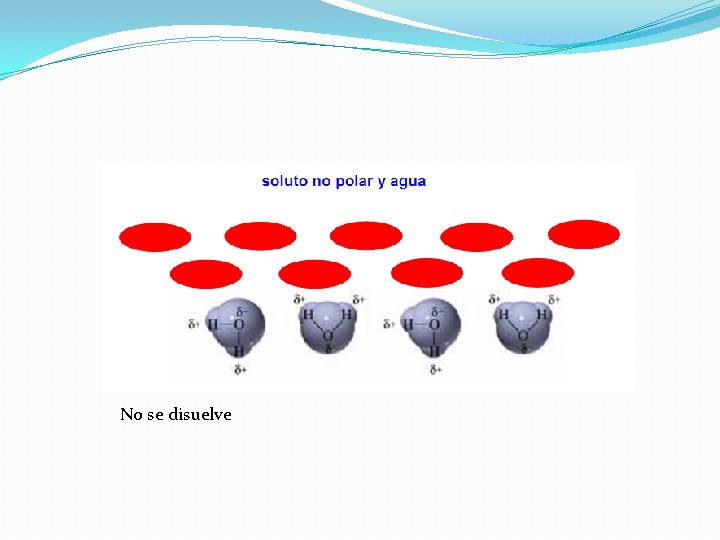
No se disuelve
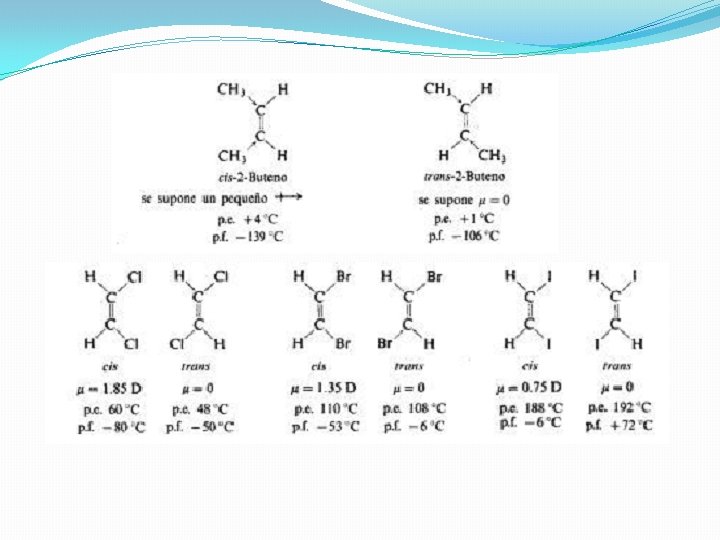
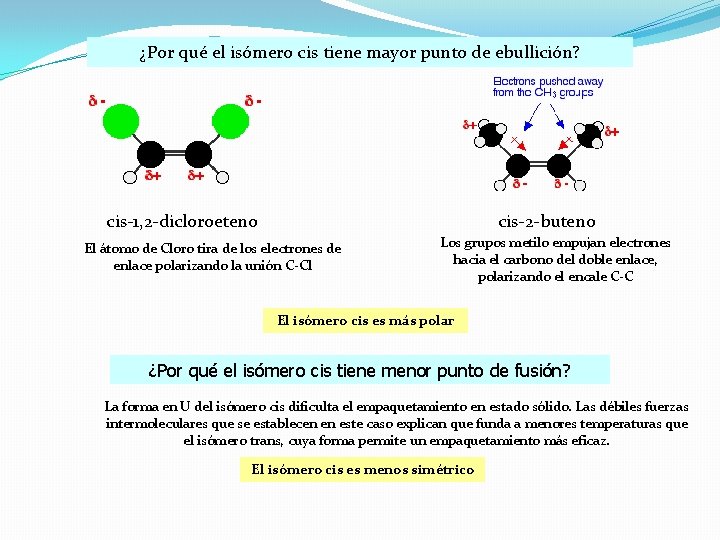
¿Por qué el isómero cis tiene mayor punto de ebullición? cis-1, 2 -dicloroeteno cis-2 -buteno El átomo de Cloro tira de los electrones de enlace polarizando la unión C-Cl Los grupos metilo empujan electrones hacia el carbono del doble enlace, polarizando el encale C-C El isómero cis es más polar ¿Por qué el isómero cis tiene menor punto de fusión? La forma en U del isómero cis dificulta el empaquetamiento en estado sólido. Las débiles fuerzas intermoleculares que se establecen en este caso explican que funda a menores temperaturas que el isómero trans, cuya forma permite un empaquetamiento más eficaz. El isómero cis es menos simétrico
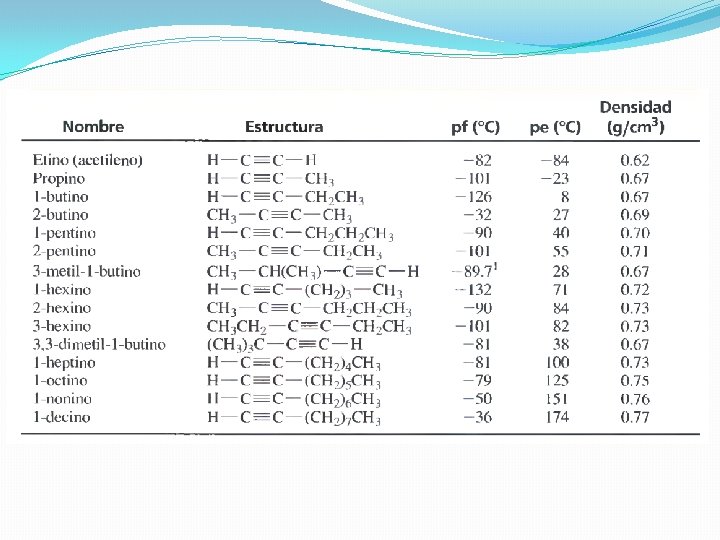
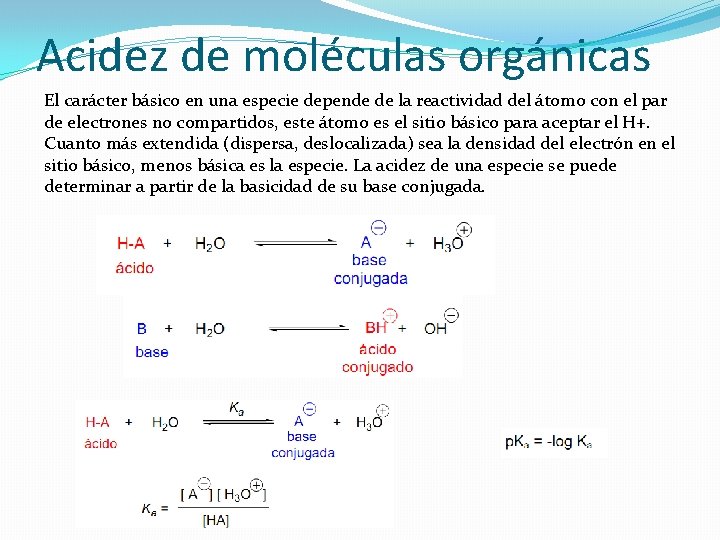
Acidez de moléculas orgánicas El carácter básico en una especie depende de la reactividad del átomo con el par de electrones no compartidos, este átomo es el sitio básico para aceptar el H+. Cuanto más extendida (dispersa, deslocalizada) sea la densidad del electrón en el sitio básico, menos básica es la especie. La acidez de una especie se puede determinar a partir de la basicidad de su base conjugada.

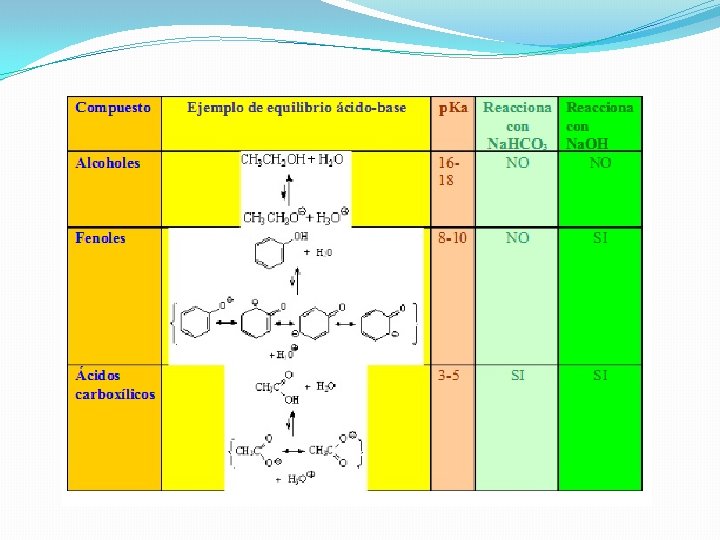
Determinados compuestos orgánicos poseen características ácidas. Los más importantes son: � Los ácidos carboxílicos (RCOOH) con p. Ka del orden de 3 a 5. Estos compuestos son, al igual que el agua, anfotéricos y por tanto capaces de actuar como ácidos o como bases. � Los alcoholes, mucho menos ácidos que los ácidos carboxílicos, con valores de p. Ka alrededor de 16. Son también anfóteros. � Las sales de amonio, ácidos conjugados de las aminas, con valores de pka entre 5 -10. Son más ácidas que los alcoholes.
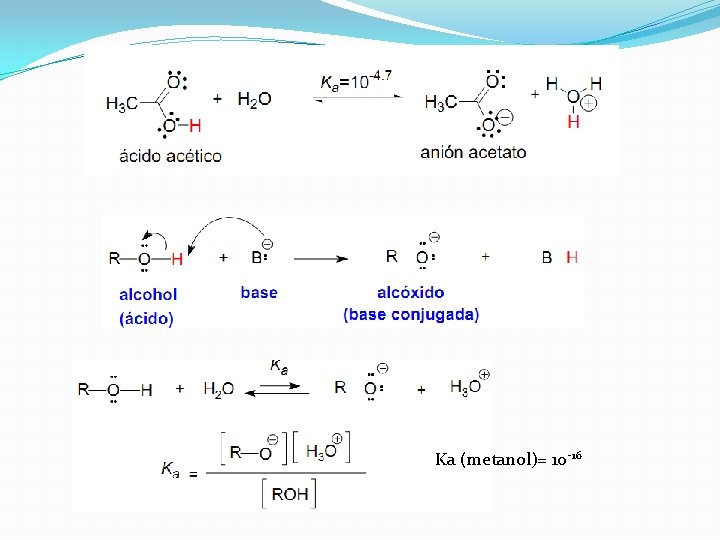
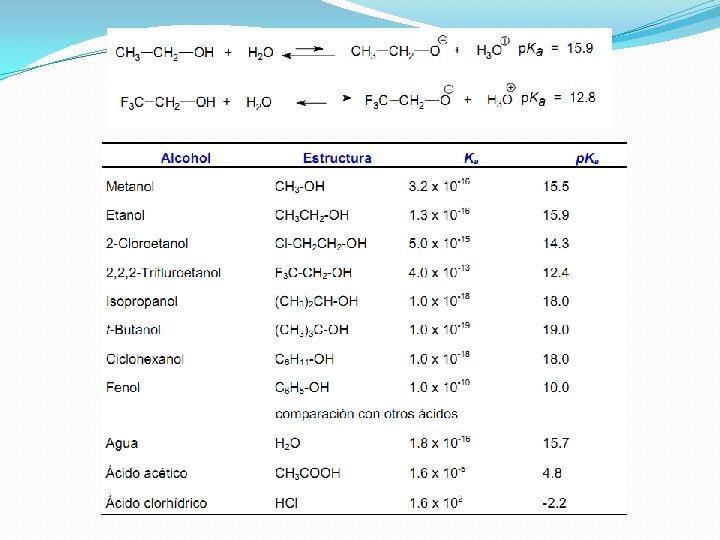
Ka (metanol)= 10 -16
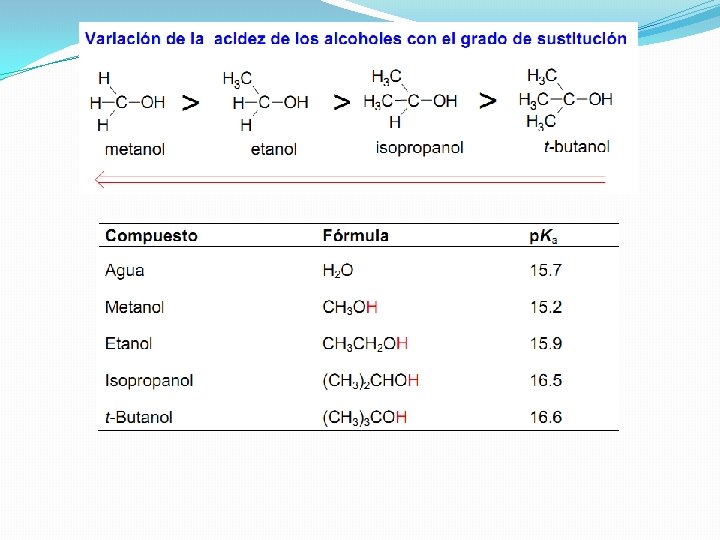
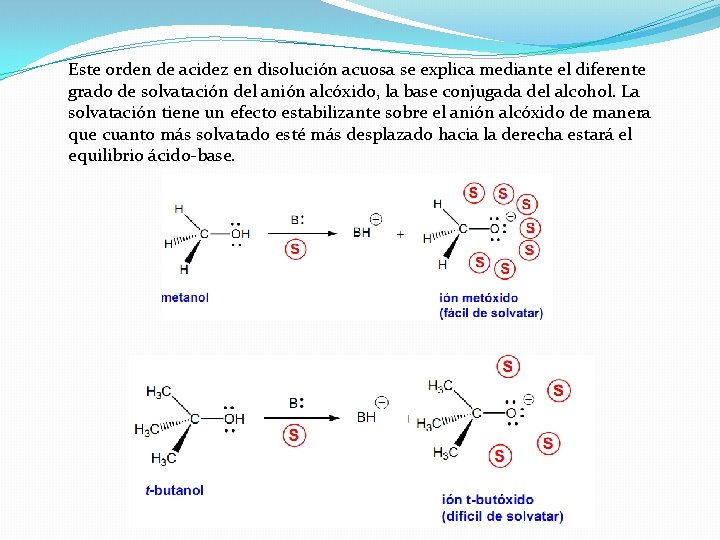
Este orden de acidez en disolución acuosa se explica mediante el diferente grado de solvatación del anión alcóxido, la base conjugada del alcohol. La solvatación tiene un efecto estabilizante sobre el anión alcóxido de manera que cuanto más solvatado esté más desplazado hacia la derecha estará el equilibrio ácido-base.

Efecto Inductivo �polarización de un enlace provocada por un átomo o un grupo atómico a lo largo de una cadena carbonada.

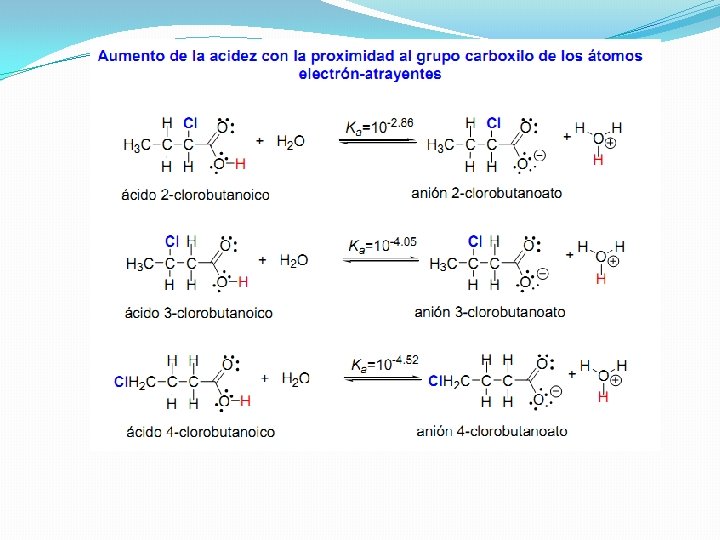
El efecto inductivo es permanente y por tanto no es un fenómeno que ocurra en un momento dado en la molécula. Hay que tener en cuenta que el efecto inductivo decrece rápidamente al aumentar la distancia al origen del desplazamiento electrónico, y en la práctica se puede despreciar a partir del segundo átomo de la cadena. El efecto inductivo puede ser electrón-atrayente, como el del átomo de cloro en el cloroetano, o electrón-dador. El efecto inductivo se representa transformando el enlace en una flecha y se indica como +I o –I según el efecto sea electrón-dador o electrón-atrayente.
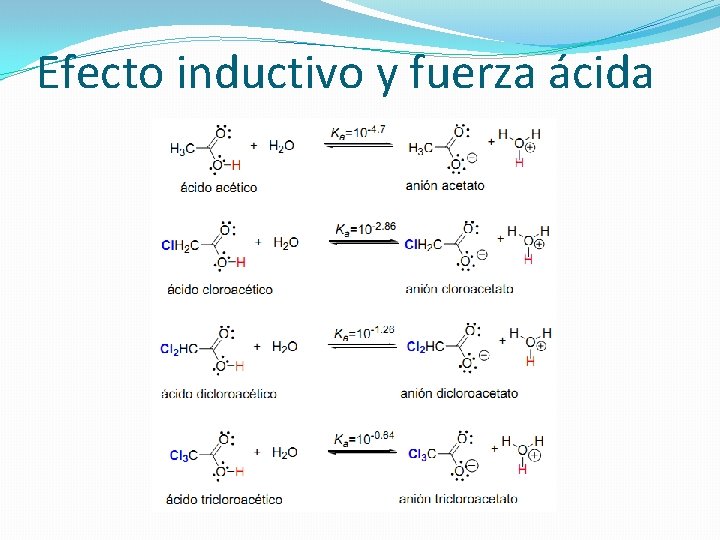
Efecto inductivo y fuerza ácida
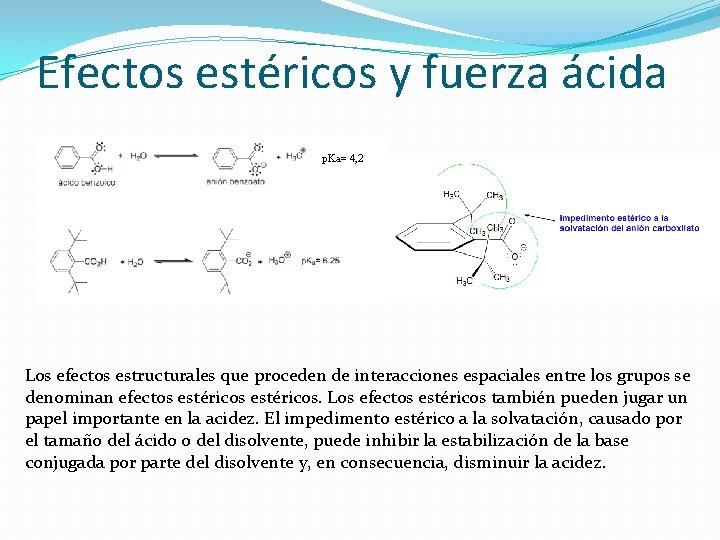
Efectos estéricos y fuerza ácida p. Ka= 4, 2 Los efectos estructurales que proceden de interacciones espaciales entre los grupos se denominan efectos estéricos. Los efectos estéricos también pueden jugar un papel importante en la acidez. El impedimento estérico a la solvatación, causado por el tamaño del ácido o del disolvente, puede inhibir la estabilización de la base conjugada por parte del disolvente y, en consecuencia, disminuir la acidez.
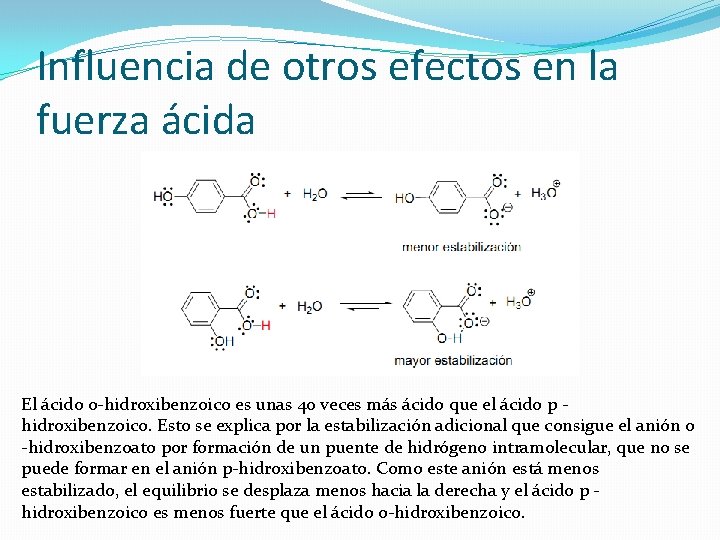
Influencia de otros efectos en la fuerza ácida El ácido o-hidroxibenzoico es unas 40 veces más ácido que el ácido p - hidroxibenzoico. Esto se explica por la estabilización adicional que consigue el anión o -hidroxibenzoato por formación de un puente de hidrógeno intramolecular, que no se puede formar en el anión p-hidroxibenzoato. Como este anión está menos estabilizado, el equilibrio se desplaza menos hacia la derecha y el ácido p - hidroxibenzoico es menos fuerte que el ácido o-hidroxibenzoico.

ENLACES DESLOCALIZADOS. Estructuras de resonancia: algunas moléculas orgánicas se pueden representar mediante dos o más estructuras de Lewis, que difieren entre sí únicamente en la colocación de los electrones y que se denominan estructuras resonantes. En estos casos, la molécula tendrá características de ambas estructuras y se dice que en realidad la molécula es un híbrido de resonancia de las estructuras resonantes. El método de la resonancia permite saber, de forma cualitativa, la estabilización que puede conseguir una molécula por deslocalización electrónica. Cuanto mayor sea el número de estructuras resonantes mediante las que se puede describir una especie química mayor será su estabilidad. En realidad, el nitrometano no es la estructura resonante I ni tampoco la estructura resonante II, sino la estructura que resultaría al mezclar las características asociadas a la estructura I y a la II

La mayor o menor contribución de las estructuras resonantes a la descripción de la molécula se puede relacionar con la mayor o menor estabilidad que teóricamente puede atribuirse a cada estructura. De forma cualitativa se puede evaluar esta mayor o menor estabilidad teniendo en cuenta los siguientes puntos: � Las estructuras con el mayor número de enlaces covalentes son los más estables. Sin embargo, para elementos del segundo periodo (C, O, N) se debe cumplir la regla del octeto. � Con unas pocas excepciones, las estructuras con la menor cantidad de cargas formales son más estables. � Si todas las estructuras tienen carga formal, la más estable (la de energía más baja) tiene - en el átomo mas electronegativo y + en el átomo más electropositivo. � Estructuras con cargas formales similares en átomos adyacentes tienen energías muy altas. � Las estructuras de resonancia con deficiencia de electrones, átomos positivamente cargados, tienen energía muy elevada y, por lo común, no se toman en cuenta.

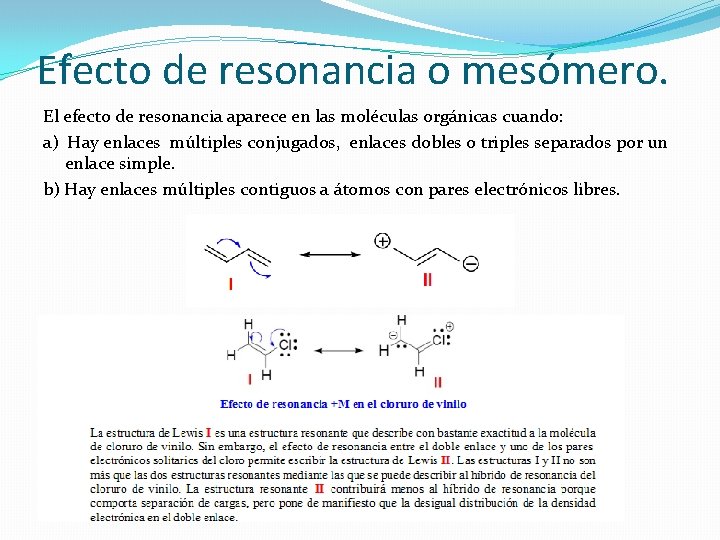
Efecto de resonancia o mesómero. El efecto de resonancia aparece en las moléculas orgánicas cuando: a) Hay enlaces múltiples conjugados, enlaces dobles o triples separados por un enlace simple. b) Hay enlaces múltiples contiguos a átomos con pares electrónicos libres.

El efecto de resonancia se diferencia del efecto inductivo en que hay una cesión, o paso de electrones de un átomo a otro, que se indica mediante flechas curvas. El efecto de resonancia puede ser positivo (+M) si es electrón -dador, o negativo (-M) si es electrón-atrayente. En el caso del cloruro de vinilo se puede considerar que el átomo de cloro ejerce un efecto de resonancia +M (electrón-dador).
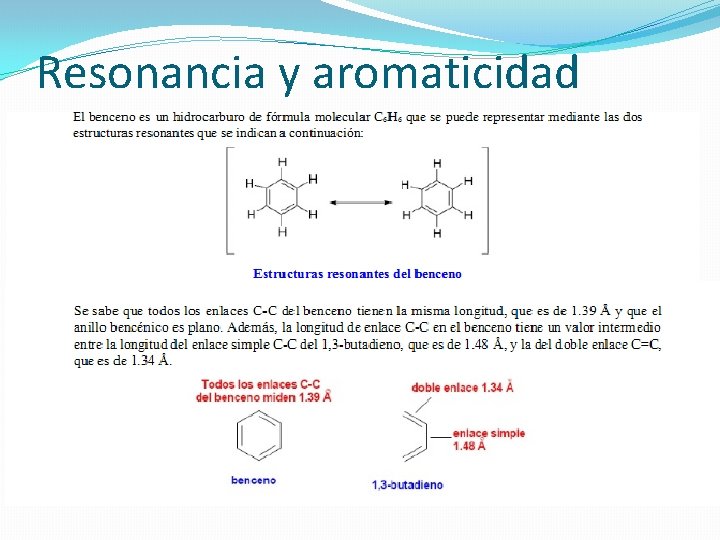
Resonancia y aromaticidad

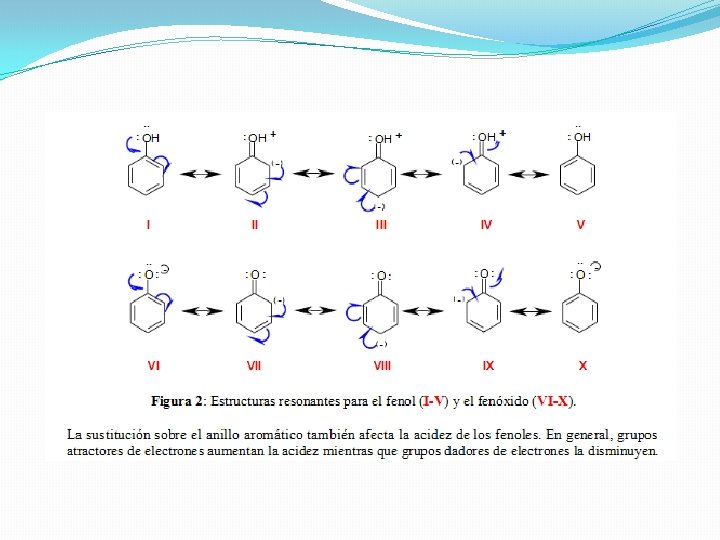
Efecto de la resonancia y acidez El efecto de la resonancia estabiliza más a una base que a un ácido, ya que se produce una deslocalización del par de electrones de la base y, por lo tanto, estos están menos disponibles a captar un protón, con lo cual disminuye el p. Ka. Todo hidrógeno que se encuentre unido o cerca de un átomo o grupo de átomos más electronegativos que el carbono son ácidos. Dentro de las moléculas orgánicas más representativas están los alcoholes(ROH), los fenoles (Ar. OH) y los ácidos carboxílicos (RCOOH), en que un hidrógeno está unido a un oxígeno. La propiedad más llamativa de los fenoles es su acidez: son varios órdenes de magnitud más ácidos que sus homólogos, los alcoholes pero menos ácidos que los ácidos carboxílicos. El ión alcóxido (RO-) está relativamente poco estabilizado porque no se puede deslocalizar la carga negativa por resonancia. El equilibrio está muy poco desplazado hacia el anión y los alcoholes son muy poco ácidos. No reaccionan ni con una base fuerte como el Na. OH. Los ácidos carboxílicos (RCOOH) son mucho más ácidos que los fenoles. A pesar de que el anión carboxilato (RCOO-) sólo se puede describir con dos formas resonantes, éstas son equivalentes y tienen la carga negativa sobre el oxígeno muy electronegativo. Esto explica la elevada estabilidad del anión carboxilato. Los ácidos carboxílicos reaccionan con bases tan débiles como el bicarbonato. El ión fenóxido (Ar. O-) está mucho más estabilizado por medio de la resonancia con el anillo aromático. Aunque las formas resonantes con la carga negativa formal sobre los carbonos contribuirán menos al híbrido de resonancia, su escritura permite entender por qué un fenol es más de un millón de veces más ácido que un alcohol. Por ello reaccionan con Na. OH, que es capaz de desprotonar cuantitativamente a un fenol en medio acuoso.
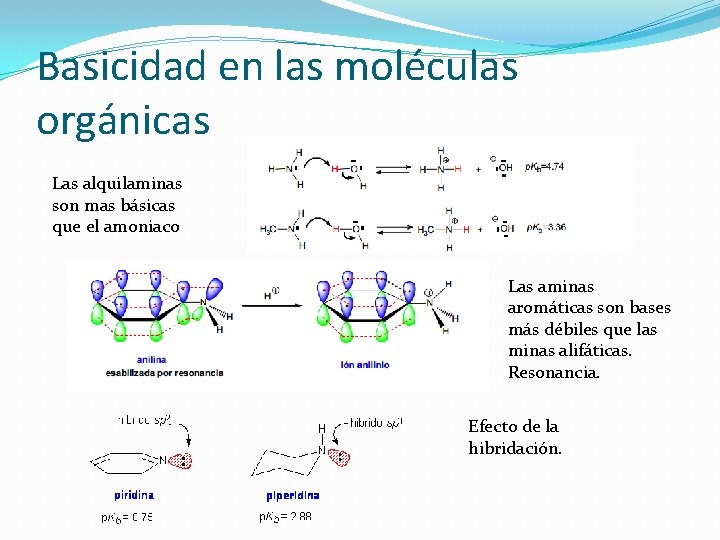
Basicidad en las moléculas orgánicas Las alquilaminas son mas básicas que el amoniaco Las aminas aromáticas son bases más débiles que las minas alifáticas. Resonancia. Efecto de la hibridación.
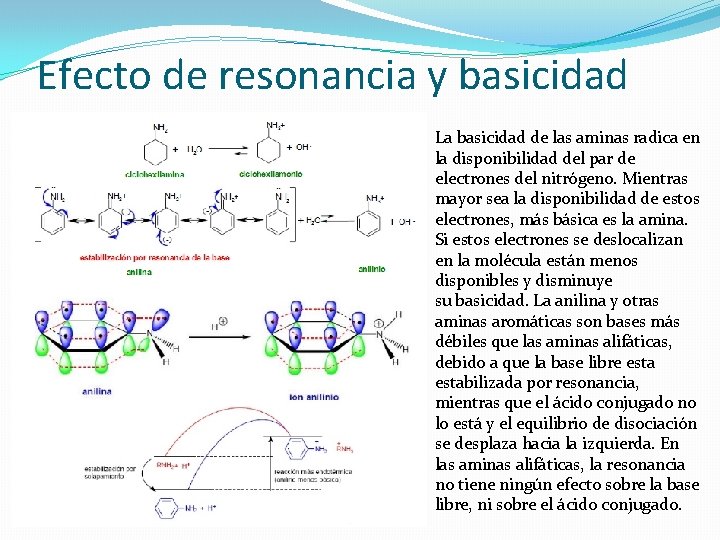
Efecto de resonancia y basicidad La basicidad de las aminas radica en la disponibilidad del par de electrones del nitrógeno. Mientras mayor sea la disponibilidad de estos electrones, más básica es la amina. Si estos electrones se deslocalizan en la molécula están menos disponibles y disminuye su basicidad. La anilina y otras aminas aromáticas son bases más débiles que las aminas alifáticas, debido a que la base libre estabilizada por resonancia, mientras que el ácido conjugado no lo está y el equilibrio de disociación se desplaza hacia la izquierda. En las aminas alifáticas, la resonancia no tiene ningún efecto sobre la base libre, ni sobre el ácido conjugado.
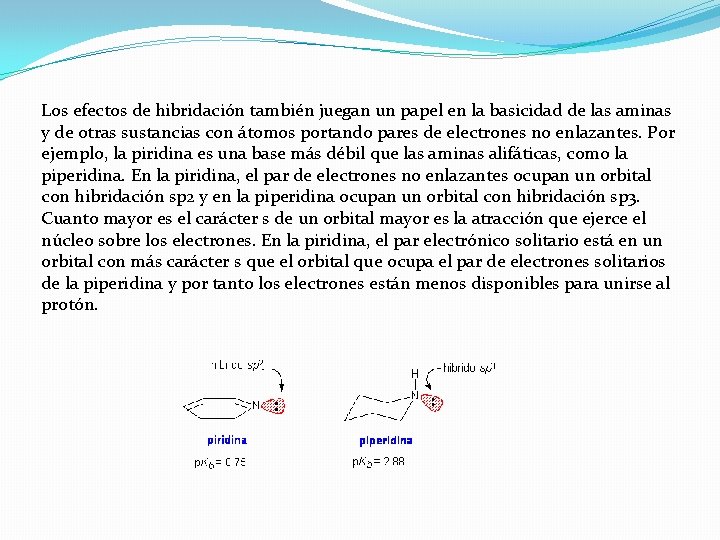
Los efectos de hibridación también juegan un papel en la basicidad de las aminas y de otras sustancias con átomos portando pares de electrones no enlazantes. Por ejemplo, la piridina es una base más débil que las aminas alifáticas, como la piperidina. En la piridina, el par de electrones no enlazantes ocupan un orbital con hibridación sp 2 y en la piperidina ocupan un orbital con hibridación sp 3. Cuanto mayor es el carácter s de un orbital mayor es la atracción que ejerce el núcleo sobre los electrones. En la piridina, el par electrónico solitario está en un orbital con más carácter s que el orbital que ocupa el par de electrones solitarios de la piperidina y por tanto los electrones están menos disponibles para unirse al protón.
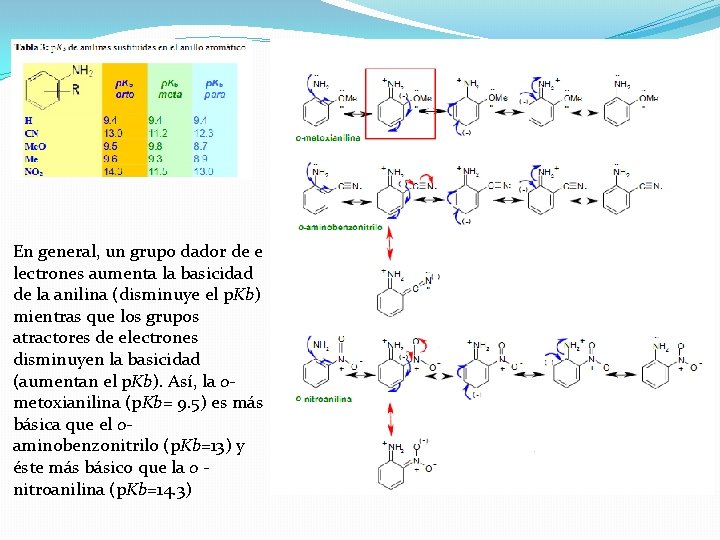
En general, un grupo dador de e lectrones aumenta la basicidad de la anilina (disminuye el p. Kb) mientras que los grupos atractores de electrones disminuyen la basicidad (aumentan el p. Kb). Así, la ometoxianilina (p. Kb= 9. 5) es más básica que el oaminobenzonitrilo (p. Kb=13) y éste más básico que la o nitroanilina (p. Kb=14. 3)
- Slides: 43