PROPIEDADES DEL CARBONO El tomo de Carbono El

PROPIEDADES DEL CARBONO
El Átomo de Carbono. • El átomo de carbono se ubica en el grupo IVA , período 2. • Su número atómico (Z) es 6. • Su configuración electrónica es: ls 22 p 2. • Posee una electronegatividad intermedia igual a 2, 5. Este le confiere al átomo de carbono la propiedad de combinarse con facilidad con otros elementos muy diferentes formando enlaces covalentes. 2

Covalencia: El átomo de carbono se combina con átomos de otros elementos como el C, H, O y N mediante la compartición de electrones, es decir, formando enlaces covalentes. Ejemplo: metano CH 4 Notación Lewis
• Tiene cuatro electrones de valencia. • Tiene la capacidad para formar hasta cuatro enlaces; es tetravalente. • Su numero atómico es 6 y su masa atómica es 12. 4

Tetravalencia del Carbono. • Tetravalencia: • El carbono es tetravalente, forma un total de cuatro enlaces covalentes Cumpliendo su octeto electrónico. • Autosaturación o Concatenación una de las principales propiedades del átomo de carbono el cual se une a otros átomos que también son de carbono para formar cadena carbonada. 5
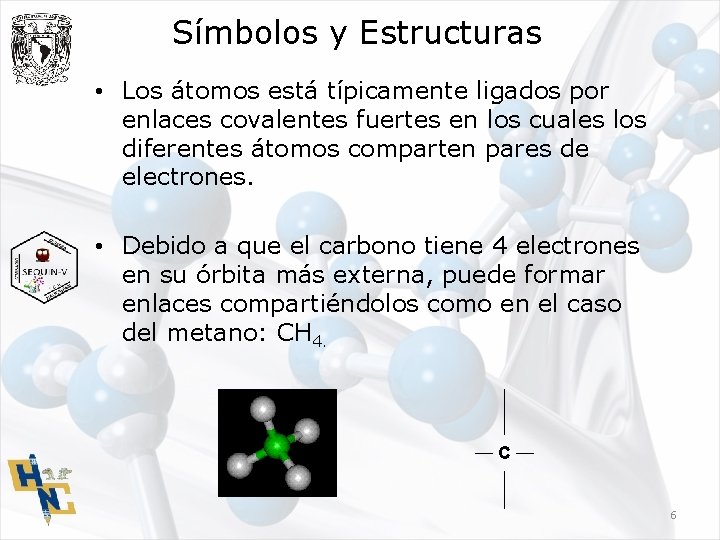
Símbolos y Estructuras • Los átomos está típicamente ligados por enlaces covalentes fuertes en los cuales los diferentes átomos comparten pares de electrones. • Debido a que el carbono tiene 4 electrones en su órbita más externa, puede formar enlaces compartiéndolos como en el caso del metano: CH 4. C 6

Configuración • Configuración normal 1 s 22 p 2 • Tetravalencia 1 s 22 s 12 px 22 py 22 pz 2 En esta nueva configuración , el átomo de carbono posee cuatro electrones desapareados que pueden formar enlaces con otros átomos. La energía desprendida al formarse los enlaces es suficiente para compensar la energía necesaria para desaparear los electrones. Así el átomo de carbono cumplirá con la regla del octeto ; esto lo logra con el proceso de hibridación.

Algunas características estructurales de los compuestos orgánicos • Las moléculas orgánicas pueden tener cadenas lineales o ramificadas, ser cadenas abiertas o cíclicas, saturadas o insaturadas, y ser carbocíclicos o heterocíclicos 8

HIDROCARBUROS • Compuestos por átomos de sólo dos elementos: carbono e hidrógeno • Los enlaces covalentes entre los átomos de carbono pueden ser sencillos, dobles o triples. • Los esqueletos de carbono pueden ser cadenas o anillos 9

Los prefijos, hasta C-10, son los siguientes: met- 1 C hex- 6 C et 2 C hept- 7 C TERMINACIÓN-ano prop- 3 C oct 8 C but- 4 C non- 9 C pent- 5 C dec- 10 C En el caso de los cicloalcanos, la aplicación es así: Ciclopropano, ciclobutano, ciclohexano, etc. 10

• • • • A partir del butano los nombres de los compuestos orgánicos llevan el prefijo: Penta Hexa Hepta Octo 5 átomos de C 6 átomos de C 7 átomos de C 8 átomos de C Nona 9 átomos de C Deca 10 átomos de C Undeca 11 átomos de C Sabias que. . . Al aumentar el número de Carbonos en los alcanos se van modificando sus propiedades físicas, por ejemplo los primeros cuatro alcanos son gases a temperatura ambiente y del Pentano al Decano son líquidos. Además al aumentar el tamaño mole-cular (⇡ Nº de C), se incrementa el punto de ebullición. 11

Tipos de enlace • Enlace simple: Los cuatro pares de electrones se comparten con cuatro átomos distintos. Ejemplo: CH 4, CH 3–CH 3 • Enlace doble: Hay dos pares electrónicos compartidos con el mismo átomo. Ejemplo: H 2 C=CH 2 • Enlace triple: Hay tres pares electrónicos compartidos con el mismo átomo. Ejemplo: HC CH 12

Clasificación de hidrocarburos de cadena abierta • Alcanos: Hidrocarburos saturados, con enlaces sencillos únicamente. • Cn. H 2 n+2 • Alquenos: hidrocarburos insaturados con dobles. Cn. H 2 n • Alquinos: hidrocarburos insaturados con triples ligaduras. Cn. H 2 n-2 13

TIPOS DE FORMULA: • • • Condensada Expresa el tipo y número de átomos de la molécula. Pero no informa de los enlaces que presenta la misma. Ejemplo : C 6 H 6 compuesto formado por seis átomos de carbono y seis átomos de hidrógeno. • • • Semidesarrollada En ella se representa sólo los enlaces carbono-carbono. Ejemplo: HC CH presenta un enlace triple carbono-carbono. • • • Desarrollada o Estructural Se representan todos los enlaces de la molécula. Ejemplo: H - C C - H En la mayor parte de los casos bastará con la fórmula semidesarrollada.

Formulación y nomenclatura: hidrocarburos de cadena abierta. • ALCANOS: Prefijo (nº C) + sufijo “ano” – Ejemplo: CH 3–CH 2–CH 3: propano • ALQUENOS: Prefijo (nº C) + sufijo “eno” indicando la posición del doble enlace si éste puede colocarse en varios sitios. – Ejemplo: CH 3–CH =CH–CH 3: 2 -buteno • ALQUINOS: Prefijo (nº C) + sufijo “ino” indicando la posición del trible enlace si éste puede colocarse en varios sitios. – Ejemplo: CH 3–CH 2–C CH: butino
- Slides: 15