Propiedades del Agua de Importancia Biolgica La mayor
Propiedades del Agua de Importancia Biológica La mayor parte de la masa de cualquier organismo es agua. Cerca de 70 % del peso total del cuerpo humano está formado por agua, pero alcanza hasta 95 % en una medusa o en ciertas plantas. Las propiedades físicas y químicas del agua les han permitido a los seres vivos aparecer, sobrevivir y evolucionar en este planeta Disuelve diferentes tipos de compuestos (propiedad solvente o disolvente) Manifiesta los fenómenos de cohesión y adhesión Tiene un alto grado de tensión superficial Tiene elevado calor específico, debido a puentes de H intermoleculares Alcanza su mayor densidad a los 4°C pero por debajo de esa temperatura la densidad disminuye nuevamente
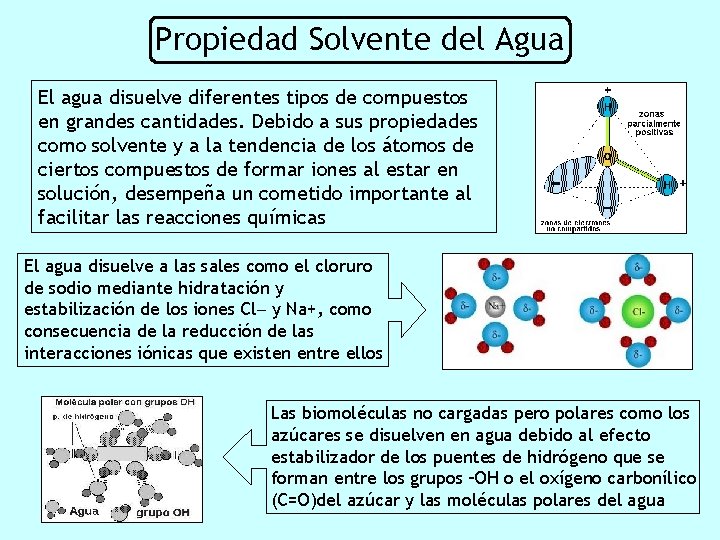
Propiedad Solvente del Agua El agua disuelve diferentes tipos de compuestos en grandes cantidades. Debido a sus propiedades como solvente y a la tendencia de los átomos de ciertos compuestos de formar iones al estar en solución, desempeña un cometido importante al facilitar las reacciones químicas El agua disuelve a las sales como el cloruro de sodio mediante hidratación y estabilización de los iones Cl y Na+, como consecuencia de la reducción de las interacciones iónicas que existen entre ellos Las biomoléculas no cargadas pero polares como los azúcares se disuelven en agua debido al efecto estabilizador de los puentes de hidrógeno que se forman entre los grupos –OH o el oxígeno carbonílico (C=O)del azúcar y las moléculas polares del agua
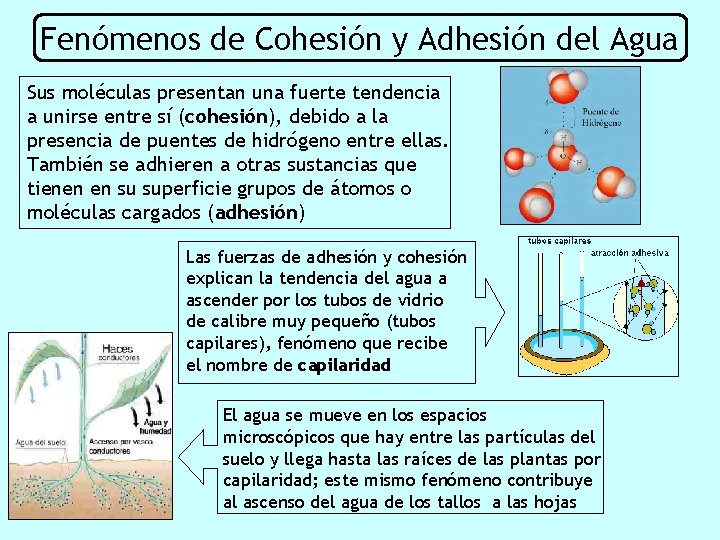
Fenómenos de Cohesión y Adhesión del Agua Sus moléculas presentan una fuerte tendencia a unirse entre sí (cohesión), debido a la presencia de puentes de hidrógeno entre ellas. También se adhieren a otras sustancias que tienen en su superficie grupos de átomos o moléculas cargados (adhesión) Las fuerzas de adhesión y cohesión explican la tendencia del agua a ascender por los tubos de vidrio de calibre muy pequeño (tubos capilares), fenómeno que recibe el nombre de capilaridad El agua se mueve en los espacios microscópicos que hay entre las partículas del suelo y llega hasta las raíces de las plantas por capilaridad; este mismo fenómeno contribuye al ascenso del agua de los tallos a las hojas

Tensión Superficial del Agua El alto grado de tensión superficial del agua es debido a la cohesión de sus moléculas, ya que éstas se atraen entre sí con mayor fuerza que las moléculas del aire. Las moléculas de agua de la superficie libre se agrupan formando una capa debido a la atracción que ejercen sobre ellas otras moléculas de agua situadas por debajo. Este hecho es importante en el caso de las plantas acuáticas y en el desarrollo de las larvas de algunos insectos. Larvas de mosquitos en el agua Loto gigante (Victoria amazonica)

Calor Específico del Agua Hace falta 1 caloría para elevar la temperatura de 1 gramo de agua en 1ºC. El alto calor específico es consecuencia de los puentes de H entre sus moléculas Así, los organismos que viven en los océanos cuentan con un medio de temperatura uniforme. El alto contenido de agua de plantas y animales terrestres les ayuda a mantener una temperatura interna constante El agua tiene también un elevado calor de vaporización. Gracias a ello el cuerpo humano puede disipar el exceso de calor por la evaporación del sudor, y una hoja se mantiene fresca, en presencia de una luz intensa, evaporando agua en su superficie

Densidad del Agua En el hielo los puentes de hidrógeno mantienen a las moléculas de agua más separadas que en el agua líquida (la densidad del hielo es 10 % menor que la densidad del agua); por eso el hielo flota sobre el agua fría, que es más densa. Esta propiedad del agua ha sido esencial en la aparición, supervivencia y evolución de la vida en la Tierra. Si el hielo tuviera una densidad mayor se hundiría y hasta los océanos se congelarían desde el fondo hasta la superficie haciendo imposible la vida. El hielo aísla el agua líquida que se encuentra por debajo, evitando el congelamiento de ésta y permitiendo que animales y plantas sobrevivan por debajo de la superficie de hielo.
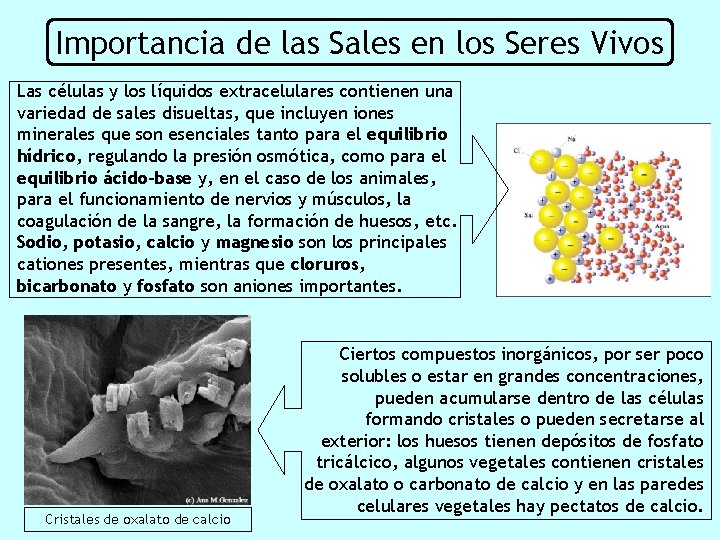
Importancia de las Sales en los Seres Vivos Las células y los líquidos extracelulares contienen una variedad de sales disueltas, que incluyen iones minerales que son esenciales tanto para el equilibrio hídrico, regulando la presión osmótica, como para el equilibrio ácido-base y, en el caso de los animales, para el funcionamiento de nervios y músculos, la coagulación de la sangre, la formación de huesos, etc. Sodio, potasio, calcio y magnesio son los principales cationes presentes, mientras que cloruros, bicarbonato y fosfato son aniones importantes. Cristales de oxalato de calcio Ciertos compuestos inorgánicos, por ser poco solubles o estar en grandes concentraciones, pueden acumularse dentro de las células formando cristales o pueden secretarse al exterior: los huesos tienen depósitos de fosfato tricálcico, algunos vegetales contienen cristales de oxalato o carbonato de calcio y en las paredes celulares vegetales hay pectatos de calcio.
- Slides: 7