Propiedades de las soluciones 2 DO MEDIO 2020




- Slides: 6

Propiedades de las soluciones 2 DO MEDIO 2020

Objetivo Comprender la diferenciación entre soluciones electrolitas y no electrolitas

Propiedades electrolíticas de las soluciones Corresponde a la capacidad de las soluciones químicas para conducir la corriente eléctrica, esto depende de la naturaleza química del soluto de acuerdo al tipo de enlace que presentan y al tipo de compuestos que representan (orgánicas o inorgánicas). Hay soluciones químicas que pueden conducir la electricidad y se denominan conductoras o soluciones electrolíticas, existen otras que no pueden conducir la electricidad y se denominan no conductoras o soluciones no electrolíticas Soluto Soluciones conductoras Soluciones no conductoras Cloruro de Sodio (Na. Cl) Sacarosa (C 12 H 22 O 11) Hidróxido de Sodio (Na. OH) Etanol (C 2 H 5 OH) Sulfato de Cobre (Cu. SO 4) Acetona (CH 3 COCH 3) Ácido Sulfúrico (H 2 SO 4) Éter dimetílico (CH 3 OCH 3) Nitrato de Potasio (KNO 3) Urea (CO(NH 2)2) * La solubilidad de un soluto en un solvente no garantiza la conductividad de las soluciones

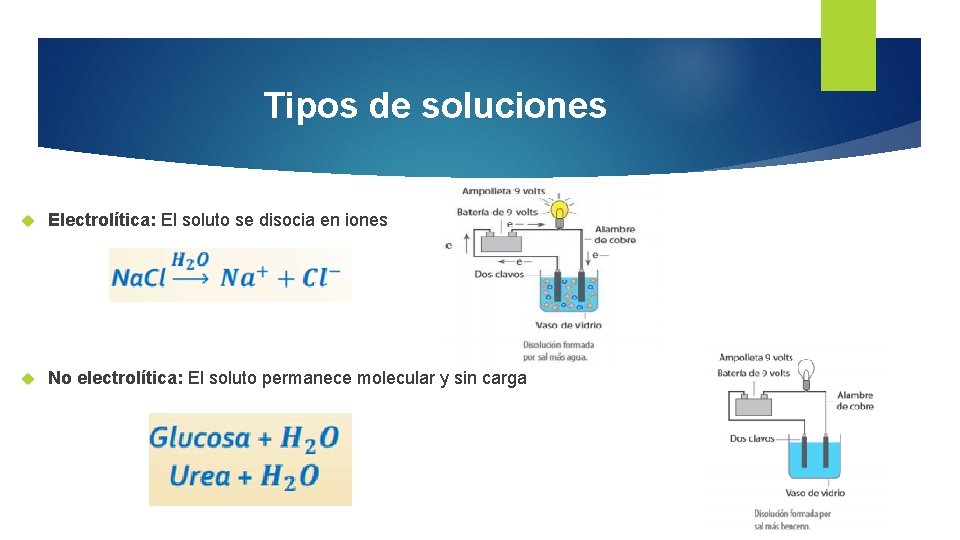
Tipos de soluciones Electrolítica: El soluto se disocia en iones No electrolítica: El soluto permanece molecular y sin carga

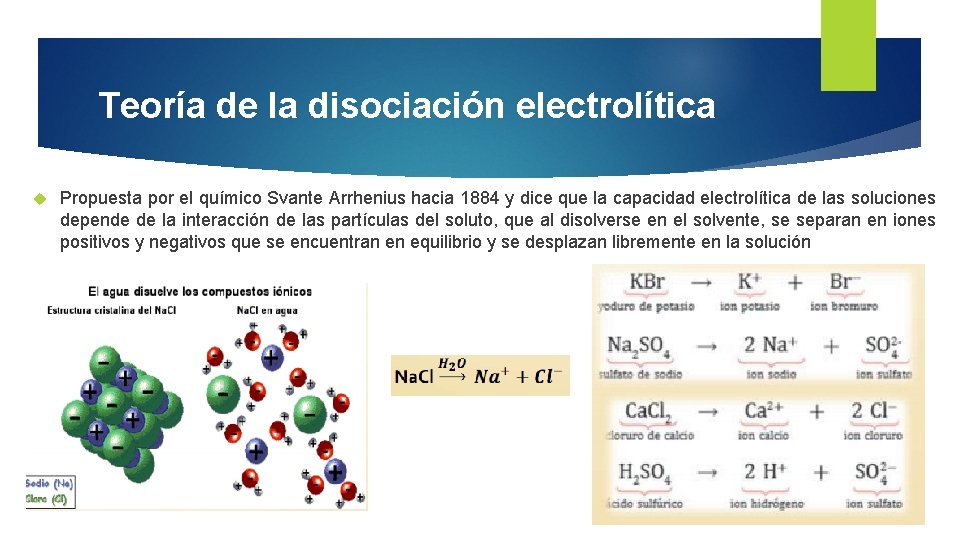
Teoría de la disociación electrolítica Propuesta por el químico Svante Arrhenius hacia 1884 y dice que la capacidad electrolítica de las soluciones depende de la interacción de las partículas del soluto, que al disolverse en el solvente, se separan en iones positivos y negativos que se encuentran en equilibrio y se desplazan libremente en la solución

Tipos de electrolitos y porcentaje de disociación El porcentaje de disolución determina si una solución es mas conductora o no, dependiendo de la cantidad de soluto que logre disociarse. Por eso los científicos acordaron que: Electrolitos fuertes: disociación 40% o mas Electrolitos débiles: disociación 10% o menos