Profesor Bastin Crdenas G Qumica Enlaces y Reacciones

Profesor: Bastián Cárdenas G Química Enlaces y Reacciones 3º Medio E-mail: bastiancardenasnumancia@gmail. com

Ruta de aprendizaje Ruta • • Objetivos de aprendizaje 1. Comprender el funcionamiento de la estructura de Lewis y las reglas establecidas (octeto y dueto) Enlace iónico Enlace covalente Reglas Ejemplos Iones poliatomicos Estructuras resonantes Cierre de la clase

Son Iones de varios átomos que los enlaces entre sus átomos son COVALENTES. Iones poliatomicos amonio carbonato ANION= se suman los e- Las estructuras de LEWIS se escribe igual que para compuestos neutros, pero se considera la carga del ION al determinar el # total de e- de valencia CATION= se restan los e-
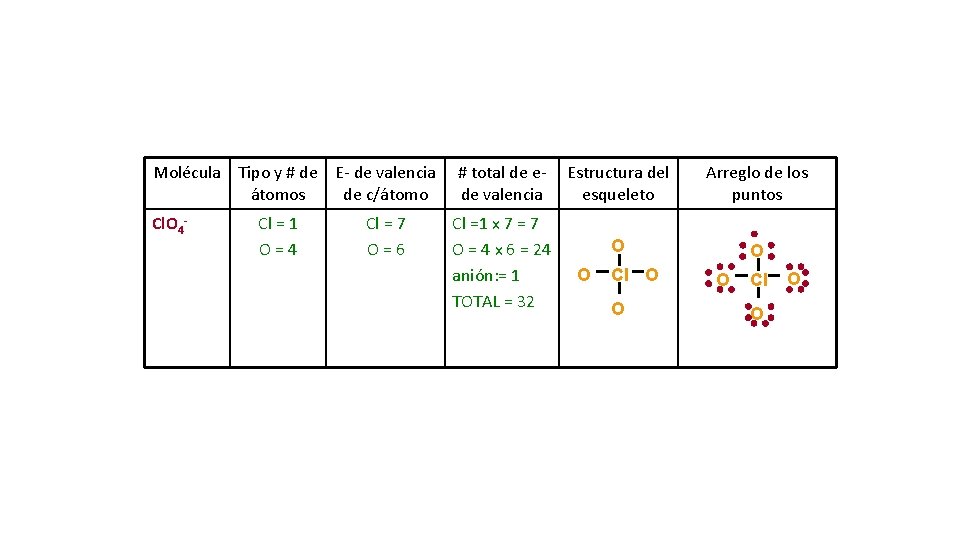
Molécula Tipo y # de E- de valencia átomos de c/átomo # total de ede valencia Cl. O 4 - Cl =1 x 7 = 7 O = 4 x 6 = 24 anión: = 1 TOTAL = 32 Cl = 1 O=4 Cl = 7 O=6 Estructura del esqueleto Arreglo de los puntos O O O Cl O O
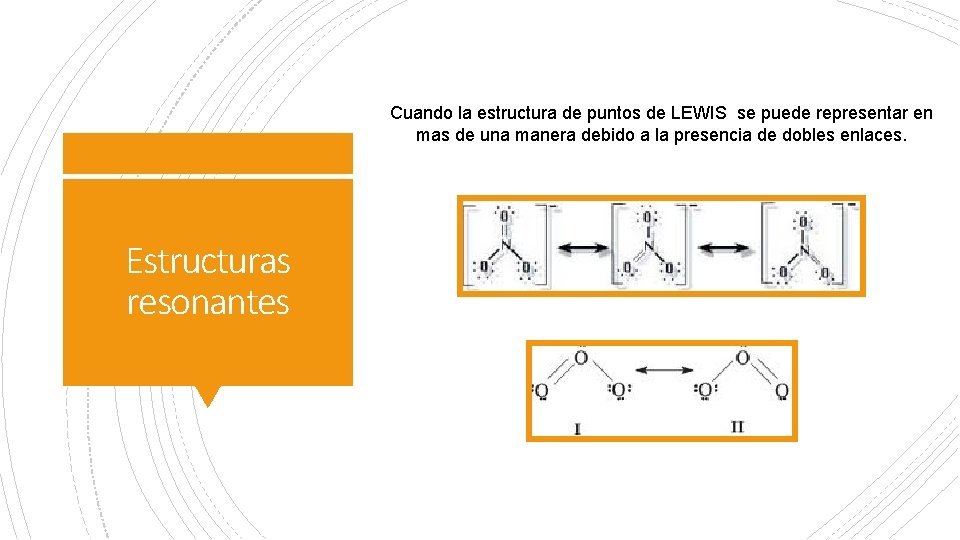
Cuando la estructura de puntos de LEWIS se puede representar en mas de una manera debido a la presencia de dobles enlaces. Estructuras resonantes
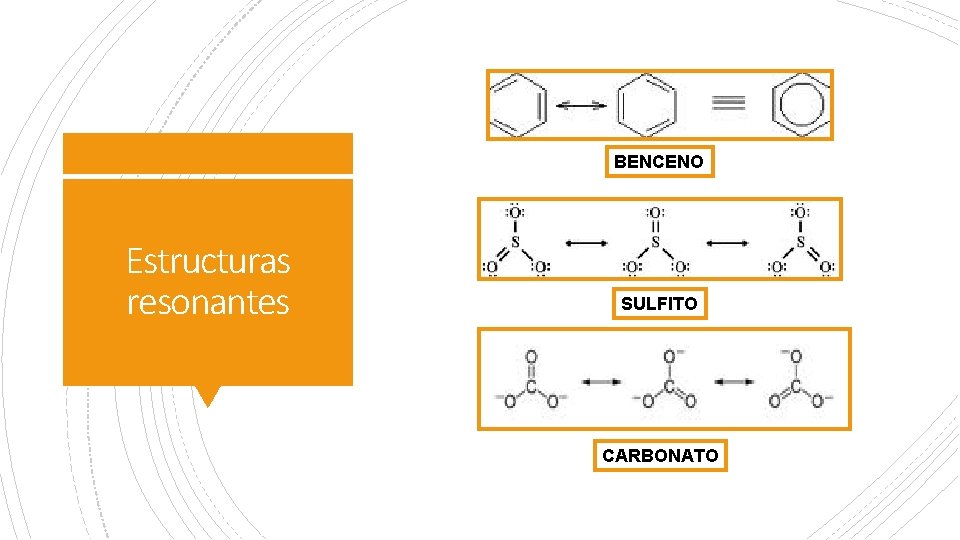
BENCENO Estructuras resonantes SULFITO CARBONATO
Diapo anterior Estructuras resonantes TODAS las estructuras cumplen la regla del octeto. En cuanto a la distancia de los enlaces todos son iguales, no corresponden ni a uno sencillo ni a uno doble, sino a uno intermedio. TODAS las estructuras RESONANTES son posibles. (actividad)

Una reaccio n qui mica es un cambio profundo de la materia, o sea, una o varias sustancias se transforman en otras sustancias diferentes debido a que su composicio n y propiedades se modifican. Las sustancias que se transforman, bajo determinadas condiciones, se llaman reactantes, y las que se producen se denominan productos. Recciones químicas
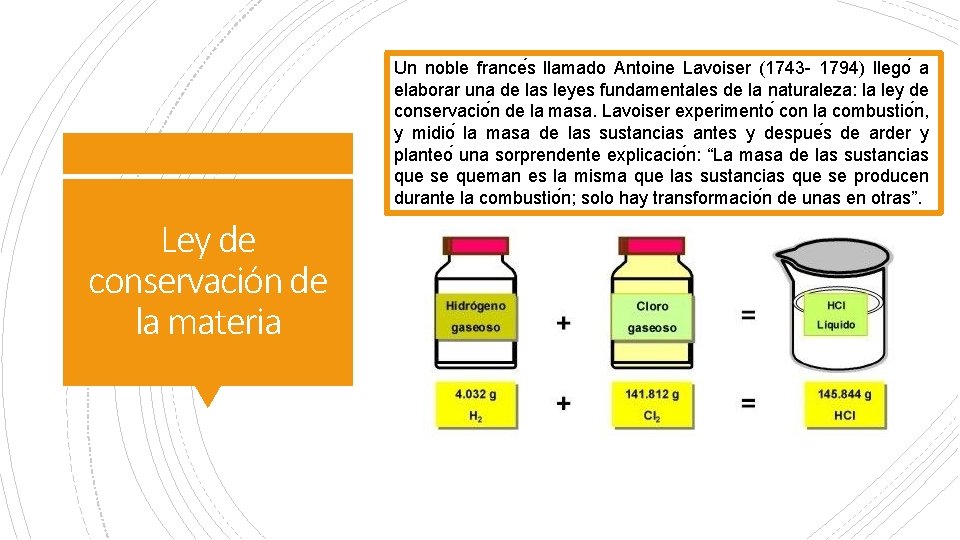
Un noble france s llamado Antoine Lavoiser (1743 - 1794) llego a elaborar una de las leyes fundamentales de la naturaleza: la ley de conservacio n de la masa. Lavoiser experimento con la combustio n, y midio la masa de las sustancias antes y despue s de arder y planteo una sorprendente explicacio n: “La masa de las sustancias que se queman es la misma que las sustancias que se producen durante la combustio n; solo hay transformacio n de unas en otras”. Ley de conservación de la materia

Actividad formativa: Instrucciones 1. Contaran hasta el día domingo 15 de noviembre antes de las 23: 59 horas, para hacer envio de la actividad a mi correo electrónico. 2. La actividad se puede realizar sobre el mismo ppt o bien en su cuaderno y compartir imágenes (claras) a mi correo electrónico. 3. Resolvere dudas por el mail y tambien por instagram.

Realizar la estructura de Lewis de las siguientes moléculas: C 2 H 4 Etileno Ba. Cl 2 Cloruro de Bario H 3 PO 4 Ácido fosfórico Ejercicio con nota formativa
Identificar que tipo de enlace se encuentra presente. ( iónico, covalente polar, covalente apolar y metálico) Molécula Benceno Ejercicios con nota formativa Oxido de magnesio Ioduro de potasio Glucosa Cobre Niquel Sulfuro de hierro Metano Tipo de enlace
Realizar la estructura de Lewis de los siguientes iones presentes: a. NH 4+ b. CO 3 -2 c. CHO 2 - Ejercicios con nota formativa

La calidad nunca es un accidente, siempre es resultado de un esfuerzo de la inteligencia (John Ruskiin) Ya pronto nos volveremos a encontrar, un abrazo gigante a la distancia No se olviden de ponerse al día con sus actividades y notas pendientes
- Slides: 14