Profa Graa Porto Entre vrios tipos de reaes






















![H I H 3 C – OH I H [O] OH I H 3 H I H 3 C – OH I H [O] OH I H 3](https://slidetodoc.com/presentation_image_h/b2567adb39ef3d5d54b16dada09badd2/image-44.jpg)

- Slides: 52

Profa. Graça Porto

Entre vários tipos de reações É quando um átomo ou grupo de átomos é podemos destacar as de substituído por um radical do outro reagente SUBSTITUIÇÃO, ADIÇÃO H H e LUZ H C H H + Cl ELIMINAÇÃO H C Cl H Cl + H Cl

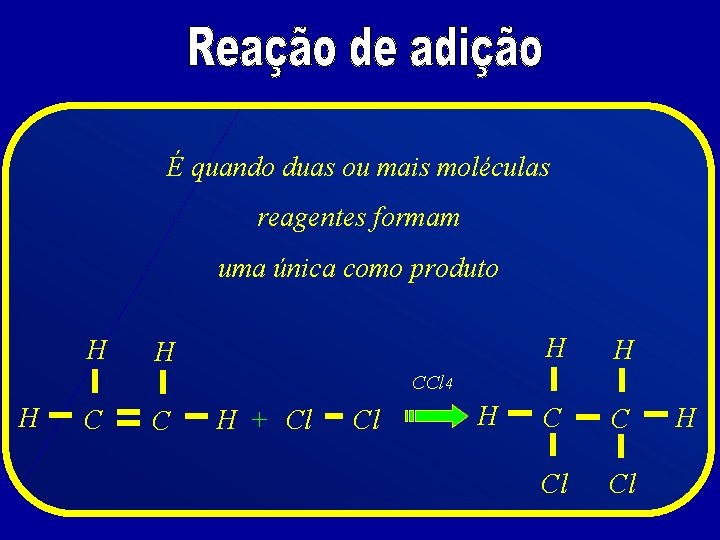
É quando duas ou mais moléculas reagentes formam uma única como produto H H C C Cl Cl CCl 4 H C C H + Cl Cl H H

É quando de uma molécula são retirados dois átomos ou dois grupos de átomos sem que sejam substituídos por outros H H OH C C H H H+ H H C C H + H 2 O

Entre os compostos orgânicos que sofrem reações de substituição destacam-se os alcanos, o benzeno e seus derivados, os haletos de alquila, álcoois e ácidos carboxílicos

É quando substituímos um ou mais átomos de hidrogênio de um alcano por átomos dos halogênios H H LUZ H C H H + Cl Cl H Cl + H Cl

Podemos realizar a substituição dos demais átomos de hidrogênio sucessivamente, resultando nos compostos CH 4 + 2 Cl 2 H 2 CCl 2 + 2 HCl CH 4 + 3 Cl 2 HCCl 3 + 3 HCl CH 4 + 4 Cl 2 CCl 4 + 4 HCl

A reatividade depende do carbono onde ele se encontra; a Nos alcanos de cadeias maiores, teremos vários átomos preferência de substituição segue a de hidrogênios possíveis de serem substituídos seguinte ordem: C terciário > C secundário > C primário H I CH 3 – CH 3 + Cl 2 I CH 3 LUZ Cl I CH 3 – CH 3 + H – Cl I CH 3 produto principal

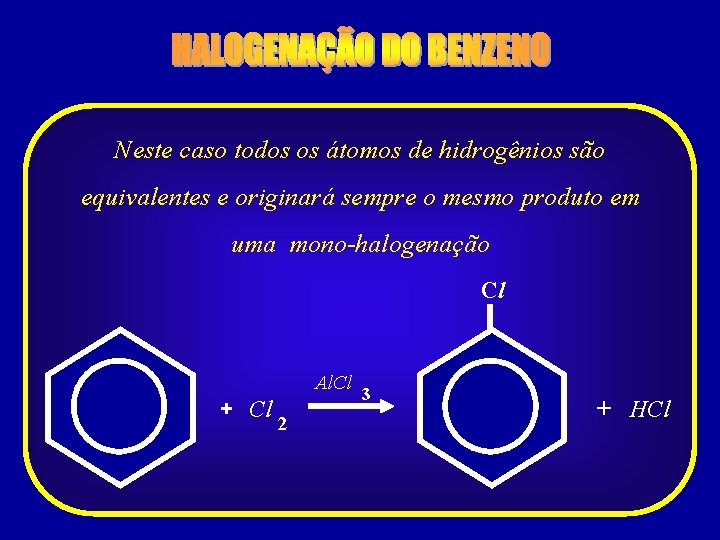
Neste caso todos os átomos de hidrogênios são equivalentes e originará sempre o mesmo produto em uma mono-halogenação Cl Al. Cl + Cl 2 3 + HCl

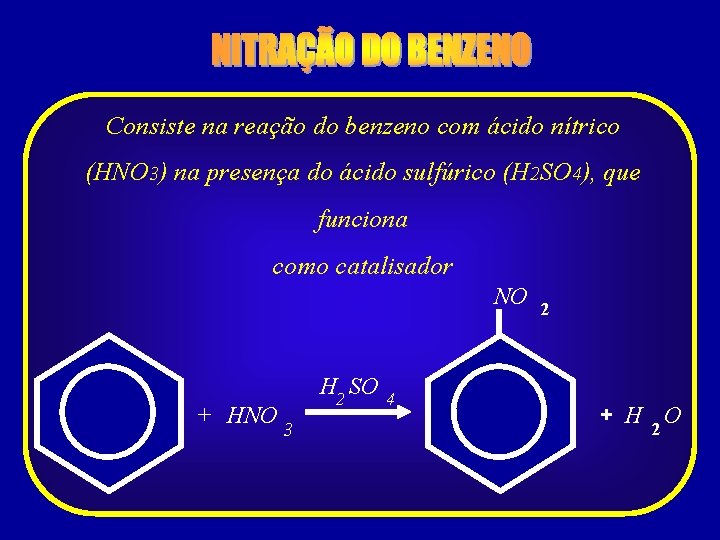
Consiste na reação do benzeno com ácido nítrico (HNO 3) na presença do ácido sulfúrico (H 2 SO 4), que funciona como catalisador NO + HNO H 2 SO 3 4 2 + H O 2

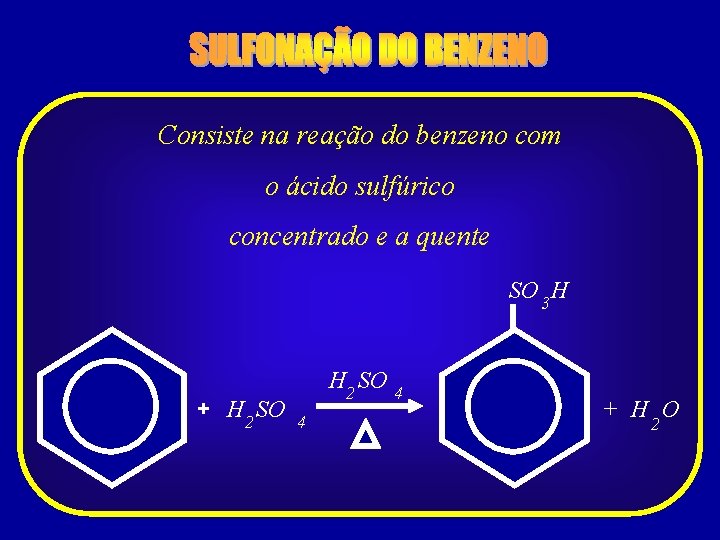
Consiste na reação do benzeno com o ácido sulfúrico concentrado e a quente SO 3 H + H 2 SO 4 4 + H O 2

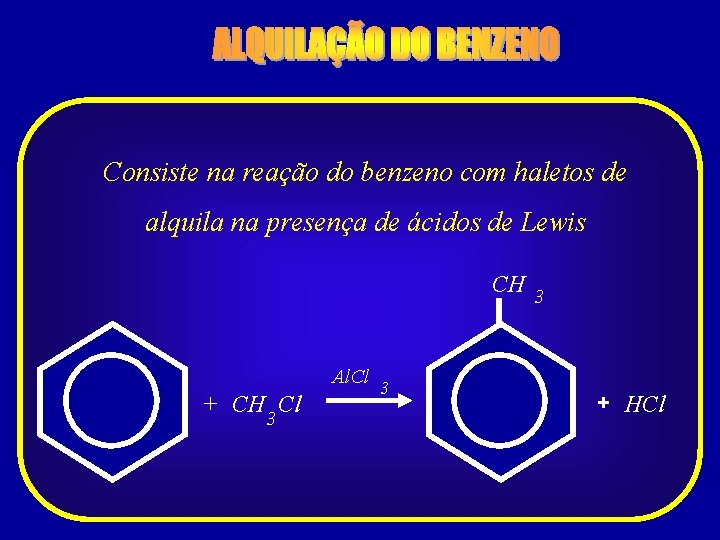
Consiste na reação do benzeno com haletos de alquila na presença de ácidos de Lewis CH 3 Al. Cl + CH Cl 3 3 + HCl

01) No 3 – metil pentano, cuja estrutura está representada a seguir: 1 H 3 C 2 CH 3 4 CH 2 6 CH CH 5 2 CH 3 O hidrogênio mais facilmente substituível por halogênio está situado no carbono de número: a) 1. b) 2. c) 3. d) 4. e) 6. 3

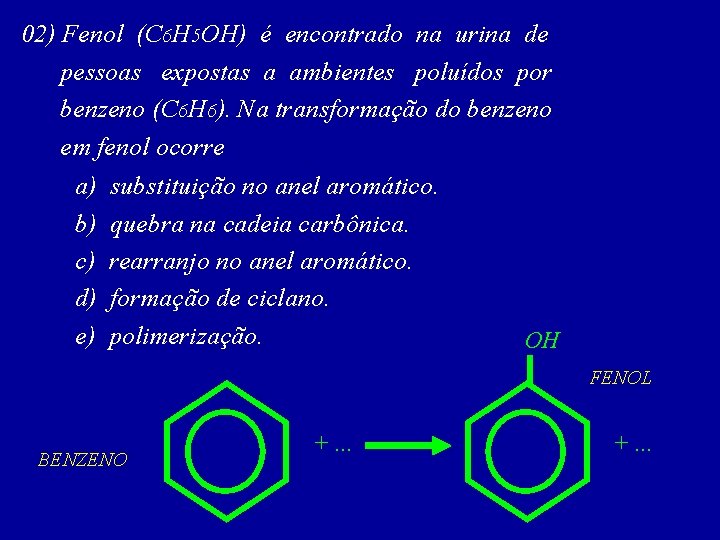
02) Fenol (C 6 H 5 OH) é encontrado na urina de pessoas expostas a ambientes poluídos por benzeno (C 6 H 6). Na transformação do benzeno em fenol ocorre a) b) c) d) e) substituição no anel aromático. quebra na cadeia carbônica. rearranjo no anel aromático. formação de ciclano. polimerização. OH FENOL BENZENO +. . .

03) Considere a reação de substituição do butano: BUTANO + Cl LUZ 2 X + ORG NICO Y INORG NICO O nome do composto X é: a) b) c) d) e) cloreto de hidrogênio. 1 -cloro butano. 2 -cloro butano. 1, 1 -cloro butano. 2, 2 -dicloro butano. CH 3 – CH 2 – CH 3 + Cl 2 carbono secundário é mais reativo que carbono primário 2 – cloro butano LUZ 1 2 3 CH 3 – CH 2 – CH 3 Cl + HCl 4

Assim teremos: ORIENTADORES ORTO META – PARA DESATIVANTES ( ATIVANTES ) ) observadas reações( de substituição Todas as A velocidade da reação e o produto obtido – OH com ocorrem seus – COOH – NO 2 benzeno – SOtambém 3 H – CN com dependem do radical presente no benzeno – NH 2 derivados, porém diferem na velocidade de Os orientadores META possuem um átomo que orientam a entrada dos substituintes – CH 3 ocorrência e nos produtos obtidos com ligação dupla ou tripla ligado ao – Cl – Br –I benzeno ( desativantes )

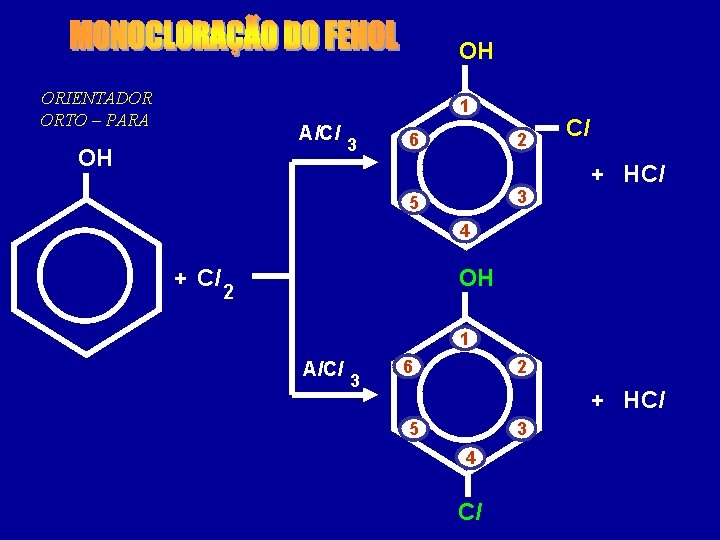
OH ORIENTADOR ORTO – PARA 1 Al. Cl OH 3 6 2 Cl + HCl 3 5 4 + Cl OH 2 1 Al. Cl 3 6 2 + HCl 5 3 4 Cl

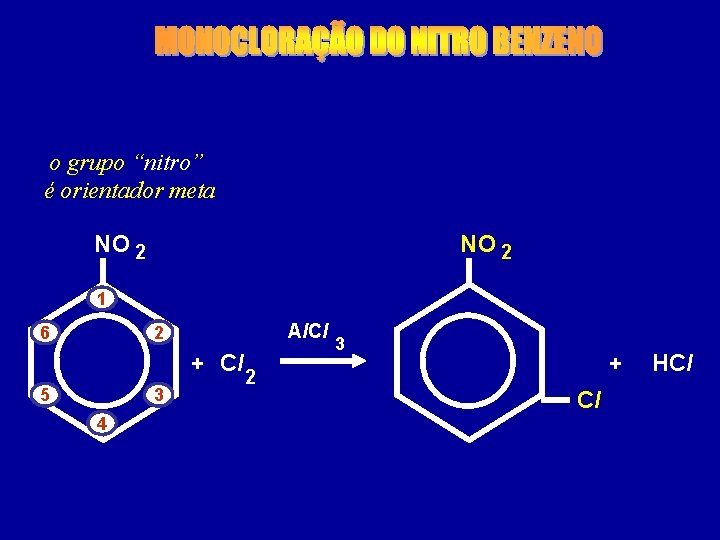
o grupo “nitro” é orientador meta NO 2 1 Al. Cl 2 6 + Cl 5 3 4 2 3 + Cl HCl

01) (UNICAP-98) O clorobenzeno, ao reagir por substituição eletrofílica com: V 0 0 HNO 3, em presença de H 2 SO 4, produz 2 -nitroclorobenzeno. F 1 1 Cl 2, em presença de Fe. Cl 3, produz preferencialmente metadiclorobenzeno V 2 2 CH 3 Cl, em presença de Al. Cl 3, produz 4 -metilclorobenzeno. V 3 3 H 2 SO 4, em presença de SO 3, produz 2 -hidrogenosulfato de clorobenzeno. F 4 4 Br 2, produz preferencialmente, em presença de Fe. Cl 3 3 -bromo, cloro benzeno. Cl 1 6 2 3 5 4 o “cloro” é orientador orto-para e desativante

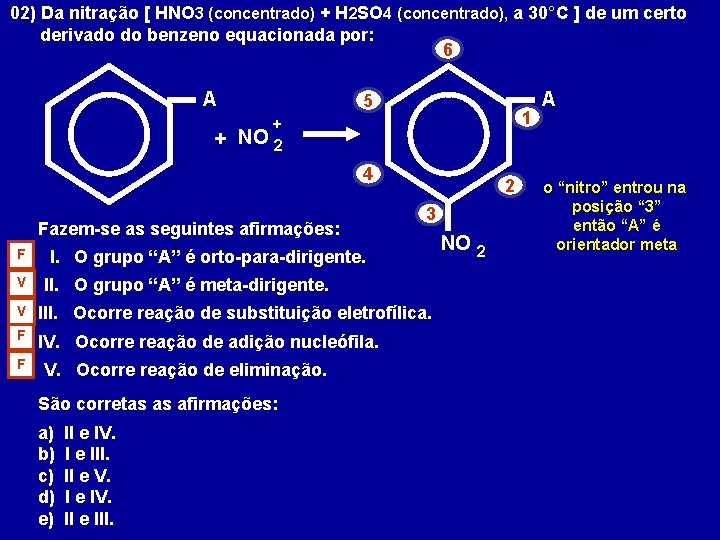
02) Da nitração [ HNO 3 (concentrado) + H 2 SO 4 (concentrado), a 30°C ] de um certo derivado do benzeno equacionada por: 6 A + NO 5 1 + 2 4 Fazem-se as seguintes afirmações: F V 2 3 I. O grupo “A” é orto-para-dirigente. II. O grupo “A” é meta-dirigente. V III. Ocorre reação de substituição eletrofílica. F IV. Ocorre reação de adição nucleófila. F V. Ocorre reação de eliminação. São corretas as afirmações: a) b) c) d) e) II e IV. I e III. II e V. I e IV. II e III. NO 2 A o “nitro” entrou na posição “ 3” então “A” é orientador meta

Os haletos de hidrogênio As reações adição mais importantes reagemde com os alcenos produzindo haletos de alquil ocorrem nos alcenos, nos alcinos, H Hem aldeídos e I I H – C = C – H + H – Cl H nas cetonas I CCl 4 H I H–C – H I I H Cl

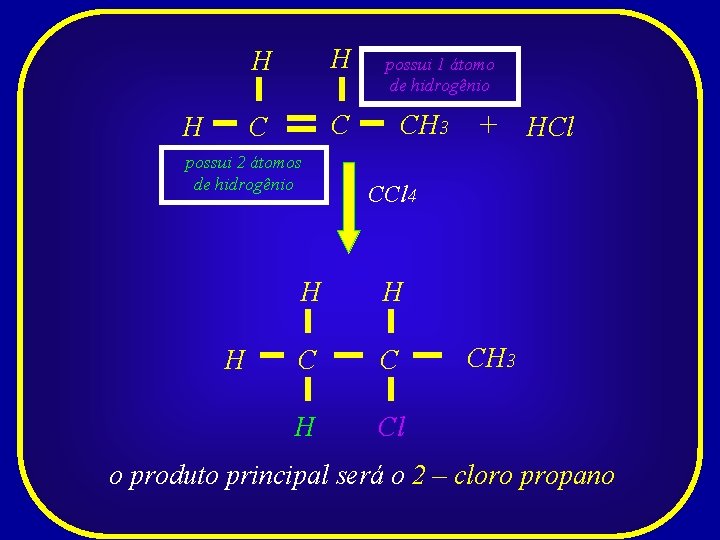
Neste caso, Paradevemos alcenoslevar em consideração com três ou mais átomosade carbono REGRA DE MARKOVNIKOV que diz: a adição do haleto de alquil produzirá dois compostos, + “O hidrogênio (H ) é adicionado sendo um deles em maior proporção ao carbono da dupla ligação (produto principal) mais hidrogenado”

H H H C C possui 2 átomos de hidrogênio H possui 1 átomo de hidrogênio CH 3 + HCl CCl 4 H H C C H Cl CH 3 o produto principal será o 2 – cloro propano

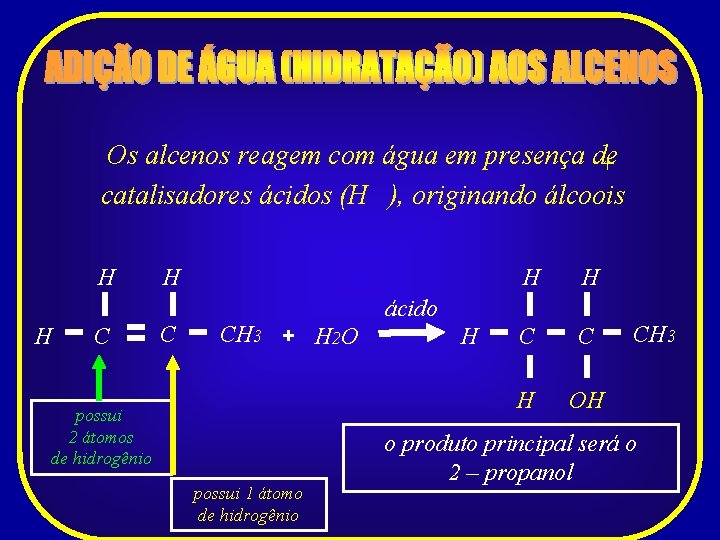
Os alcenos reagem com água em presença de + catalisadores ácidos (H ), originando álcoois H H C CH 3 + H 2 O possui 2 átomos de hidrogênio possui 1 átomo de hidrogênio H H C C H OH ácido H CH 3 o produto principal será o 2 – propanol

Os halogênios reagem com os alcenos, na presença do CCl 4, formando di-haletos de alquil. H H C CH 3 + Cl – Cl H H C C Cl Cl CCl 4 H CH 3

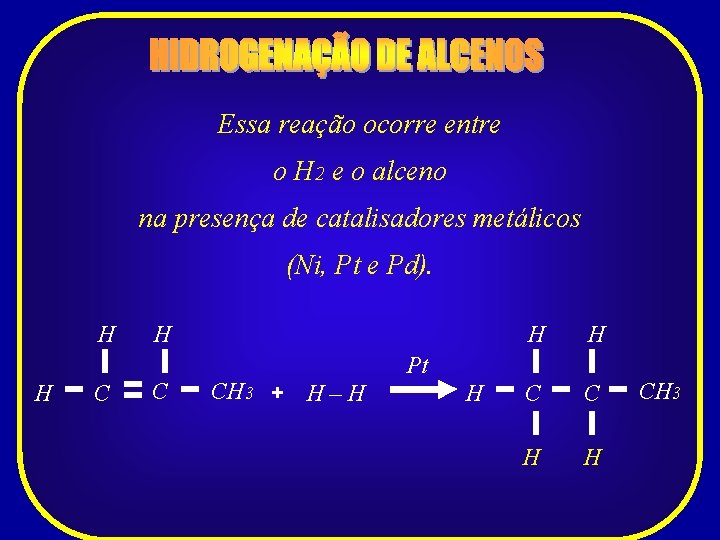
Essa reação ocorre entre o H 2 e o alceno na presença de catalisadores metálicos (Ni, Pt e Pd). H H C CH 3 + H – H H H C C H H Pt H CH 3

01) Com respeito à equação: X + HBr C 6 H 13 Br Pode-se afirmar que X é um: a) b) c) d) e) alcano e a reação é de adição. alceno e a reação de substituição. alceno e a reação é de adição eletrofílica. alcano e a reação é de substituição eletrofílica. alceno e a reação é de substituição.

H–C C – CH 3 + H – Cl H – C = C – CH 3 Ocorre a adição de H Cl 1 mol do haleto de hidrogênio para, em seguida, H Cl ocorrer a adição de H – C = C – CH 3 + H – Cl H – C – CH 3 outro mol do haleto de hidrogênio H Cl

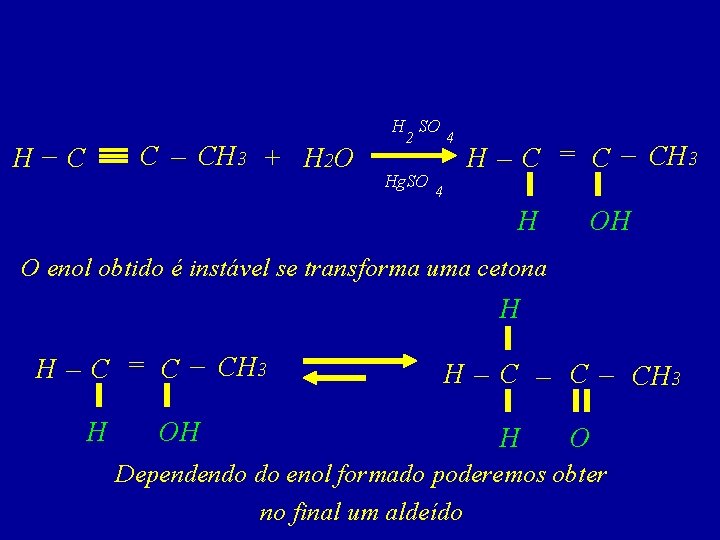
H SO H–C C – CH 3 + H 2 O 2 Hg. SO 4 H – C = C – CH 3 4 A hidratação dos alcinos, H OH O enol obtido é instável se transforma em cetona que é catalisada com H 2 SO 4 e Hg. SO 4, H possui uma seqüência parecida H – C = C – CH 3 H – C – CH 3 com a dos alcenos. H OH H O Dependendo do enol formado poderemos obter no final um aldeído

H SO H–C C – CH 3 + H 2 O 2 Hg. SO 4 H – C = C – CH 3 4 H OH O enol obtido é instável se transforma uma cetona H H – C = C – CH 3 H OH H – C – CH 3 H O Dependendo do enol formado poderemos obter no final um aldeído

O esquema geral do processo é: A adição de reagentes de Grignard (RMg. X), seguida de metanal + RMg. X H 2 O hidrólise, álcool primário a aldeídos ou cetonas é um dos melhores processos aldeído + RMg. X H 2 O para álcool secundário a preparação H 2 Ode álcoois cetona + RMg. X álcool terciário

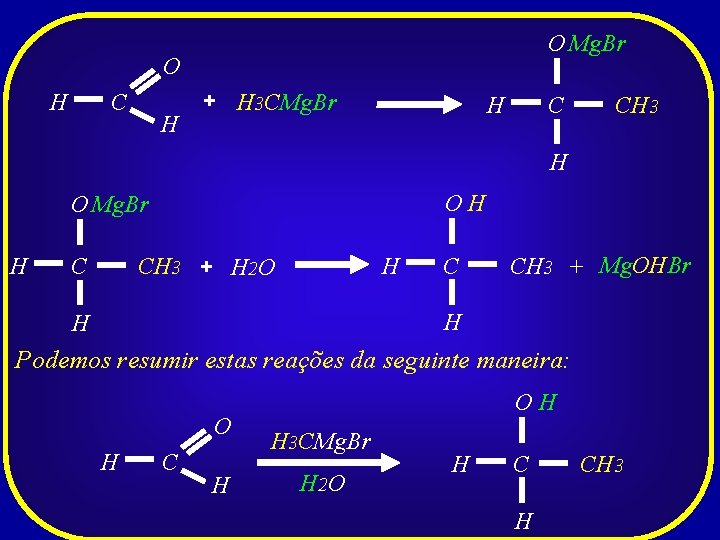
O Mg. Br O H C H + H 3 CMg. Br H C CH 3 H OH O Mg. Br H H CH 3 + H 2 O C C CH 3 + Mg. OHBr H H Podemos resumir estas reações da seguinte maneira: O H C H OH H 3 CMg. Br H 2 O H CH 3

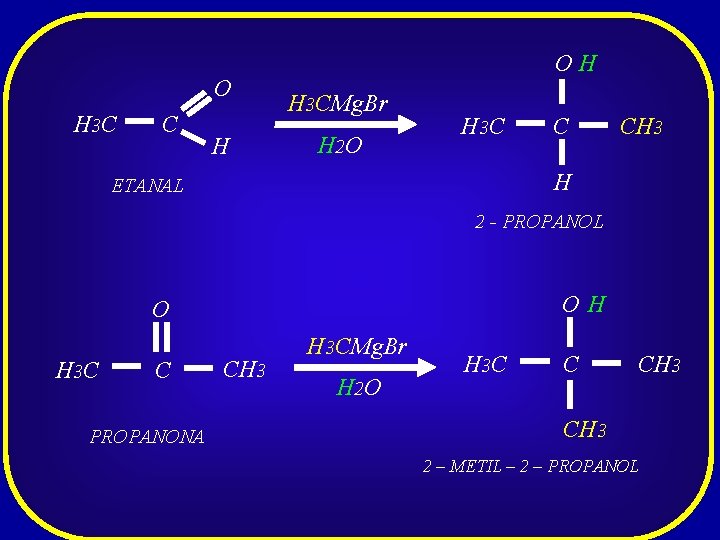
O H 3 C C H OH H 3 CMg. Br H 2 O H 3 C C CH 3 H ETANAL 2 - PROPANOL OH O H 3 C C PROPANONA CH 3 H 3 CMg. Br H 2 O H 3 C C CH 3 2 – METIL – 2 – PROPANOL

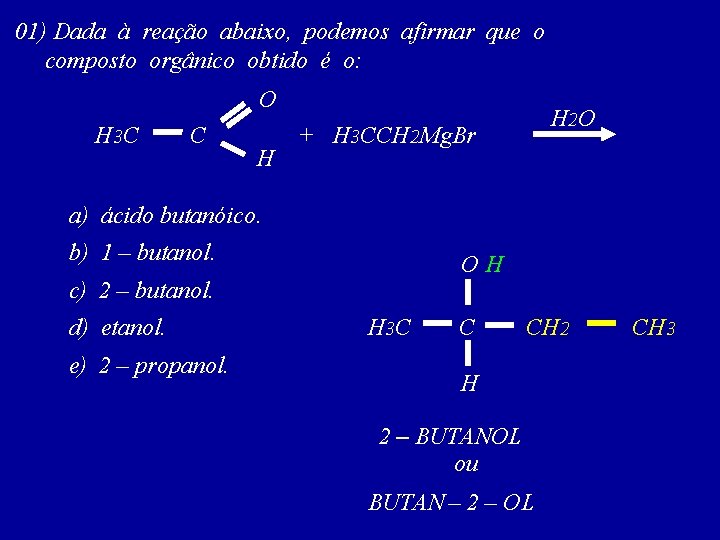
01) Dada à reação abaixo, podemos afirmar que o composto orgânico obtido é o: O H 3 C C H H 2 O + H 3 CCH 2 Mg. Br a) ácido butanóico. b) 1 – butanol. OH c) 2 – butanol. d) etanol. e) 2 – propanol. H 3 C C CH 2 – BUTANOL ou BUTAN – 2 – OL CH 3

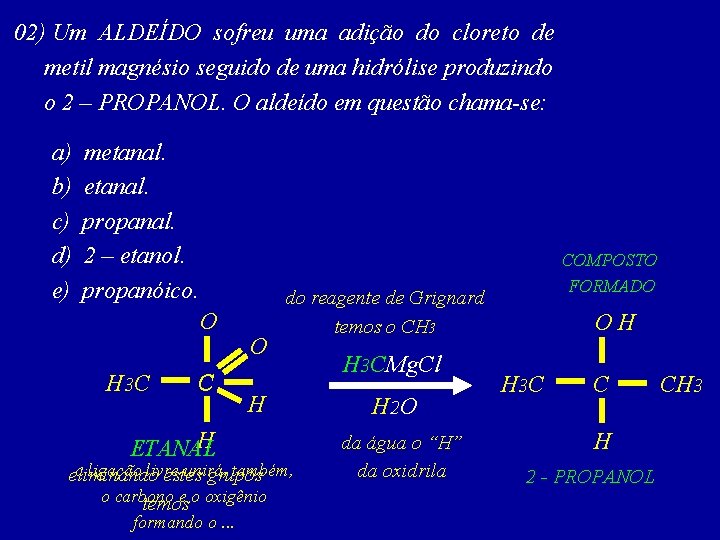
02) Um ALDEÍDO sofreu uma adição do cloreto de metil magnésio seguido de uma hidrólise produzindo o 2 – PROPANOL. O aldeído em questão chama-se: a) b) c) d) e) metanal. propanal. 2 – etanol. propanóico. O H 3 C C H ETANAL O do reagente de Grignard temos o CH 3 H a ligação livre unirá, também, eliminando estes grupos o carbono e o oxigênio temos formando o. . . COMPOSTO FORMADO H 3 CMg. Cl H 2 O da água o “H” da oxidrila OH H 3 C C H 2 - PROPANOL CH 3

As reações de eliminação são processos, em geral, inversos aos descritos para as reações de adição e, constituem métodos de obtenção de alcenos e alcinos

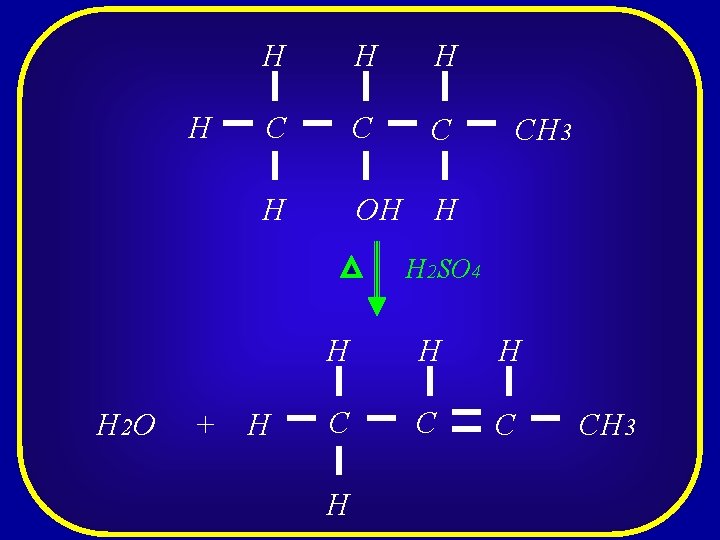
A desidratação dos álcoois segue A desidratação (eliminação de água) a regra de SAYTZEFF, isto é, de um álcool elimina-se oxidrila e deste o hidrogênio carbono ocorre com a aquecimento álcool em do presença de vizinho ao carbono da oxidrila MENOS ácido sulfúrico HIDROGENADO

H H C C C H OH H CH 3 H 2 SO 4 H 2 O + H H C C C H CH 3

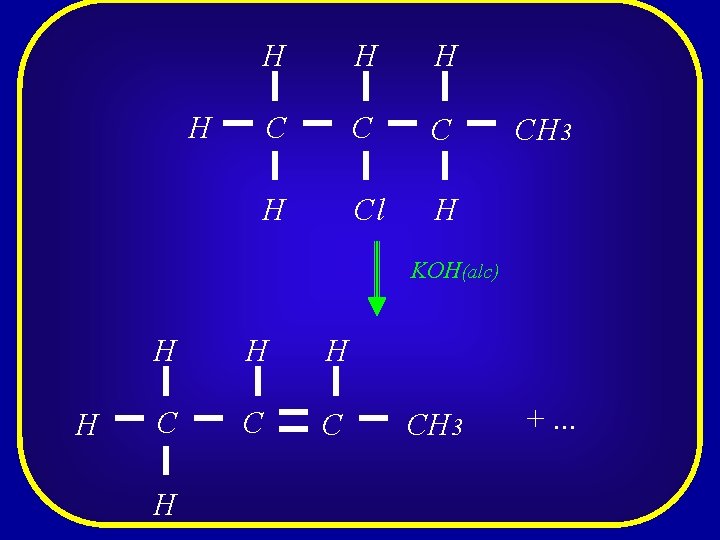
Esta reação, normalmente, ocorre em solução concentrada de KOH em álcool O haleto eliminado reage com o KOH produzindo sal e água

H H H C C C H Cl H H CH 3 KOH(alc) H H C C C H CH 3 +. . .

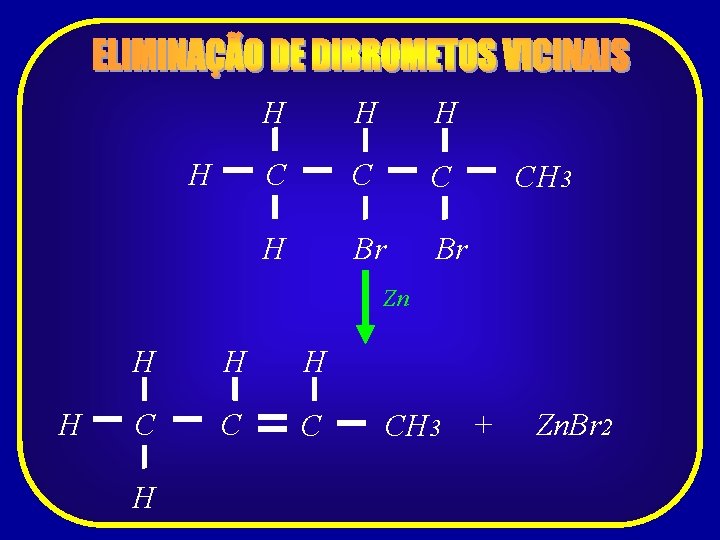
H H C C C H Br Br CH 3 Zn H H C C C H CH 3 + Zn. Br 2

H H H C C C H Br Br H CH 3 KOH (alc) As duas moléculas de HBr eliminadas reagem com o KOH formando sal e água H H C C CH 3 +. . .

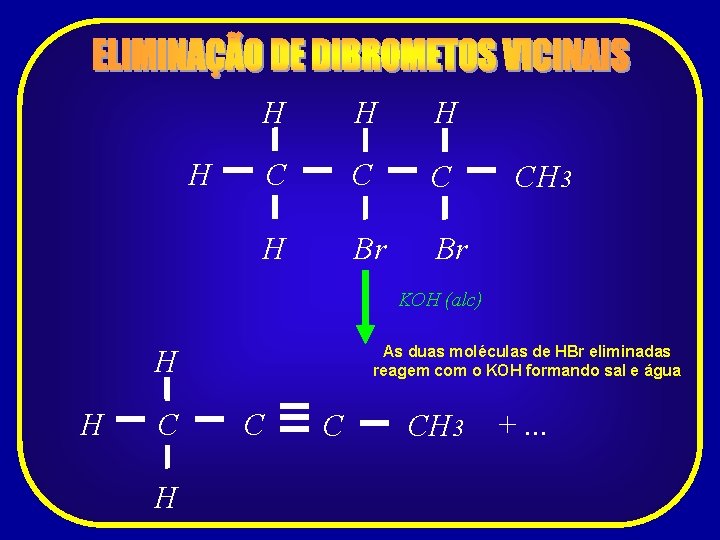
Os álcoois primários, ao sofrerem, As principais reações de O comportamento oxidação, em aldeídos e estes, oxidação redução compostos dos álcooisetransformam-se primários, secundários e orgânicos terciários, se deixados em contato com oxidante, ocorrem com os oxidantes, sãoaldeídos oxidados a álcoois, e alcenos são semelhantes ácidos carboxílicos
![H I H 3 C OH I H O OH I H 3 H I H 3 C – OH I H [O] OH I H 3](https://slidetodoc.com/presentation_image_h/b2567adb39ef3d5d54b16dada09badd2/image-44.jpg)
H I H 3 C – OH I H [O] OH I H 3 C – OH I H – H 2 O O H 3 C – C H ETANAL sofre desidratação ETANOL O H 3 C – C O [O] H 3 C – C ÁCIDO ETANÓICO H OH ETANAL RESUMINDO H I H 3 C – OH I H ETANOL O [O] H 3 C – C ETANAL O [O] H OH ÁCIDO ETANÓICO

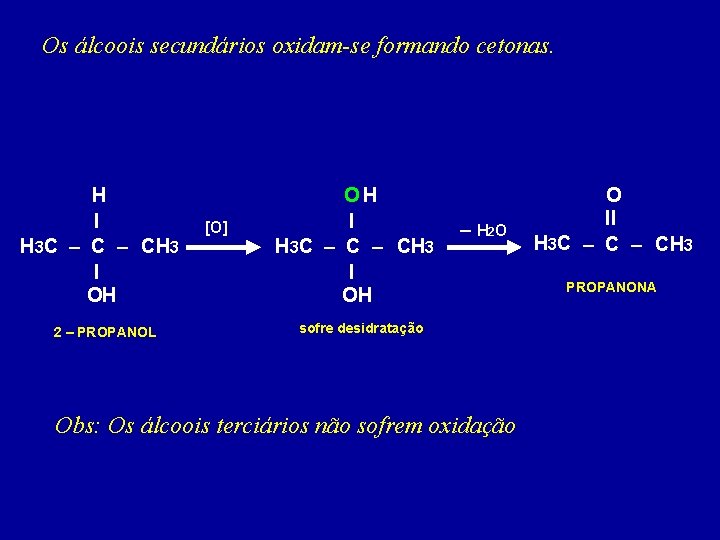
Os álcoois secundários oxidam-se formando cetonas. H I H 3 C – CH 3 I OH 2 – PROPANOL [O] OH I H 3 C – CH 3 I OH – H 2 O sofre desidratação Obs: Os álcoois terciários não sofrem oxidação O II H 3 C – CH 3 PROPANONA

01) Quando um álcool primário sofre oxidação, o produto principal é: a) ácido carboxílico. b) álcool secundário. c) éter. d) álcool terciário. e) cetona.

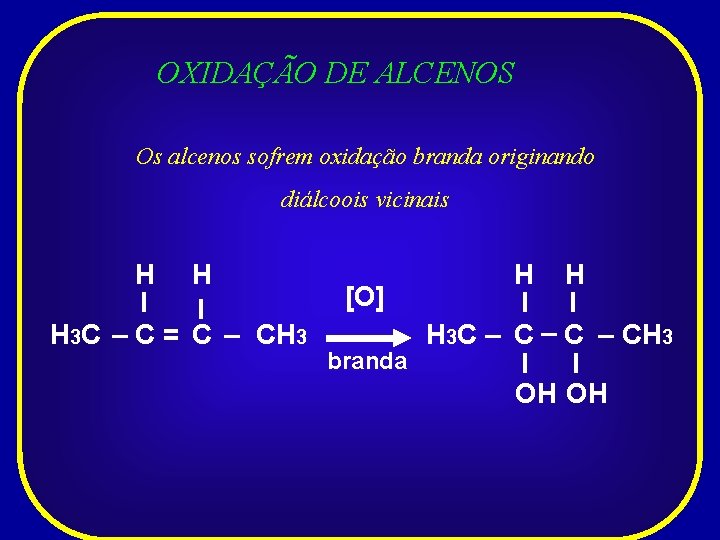
OXIDAÇÃO DE ALCENOS Os alcenos sofrem oxidação branda originando diálcoois vicinais H H I I H 3 C – C = C – CH 3 H H [O] I I H 3 C – C – CH 3 branda I I OH OH

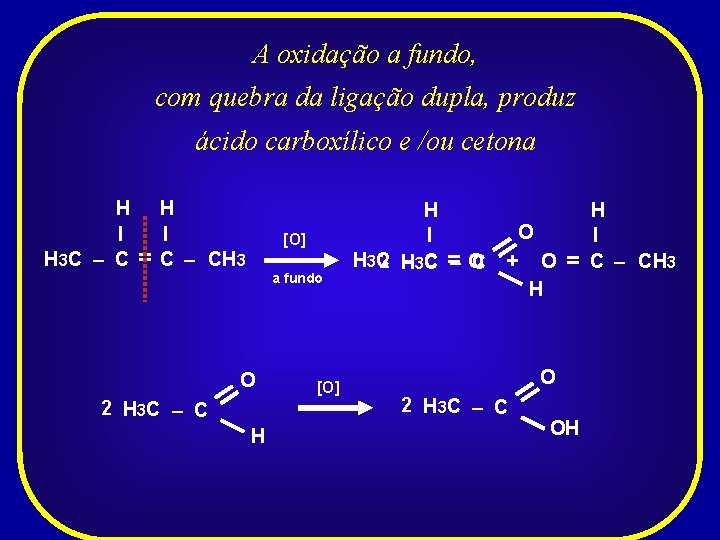
A oxidação a fundo, com quebra da ligação dupla, produz ácido carboxílico e /ou cetona H I H 3 C – C = H I C – CH 3 [O] a fundo O 2 H 3 C – C H [O] H O I H 3 C 2 H – 3 C = –O C + O H = O 2 H 3 C – C OH H I C – CH 3

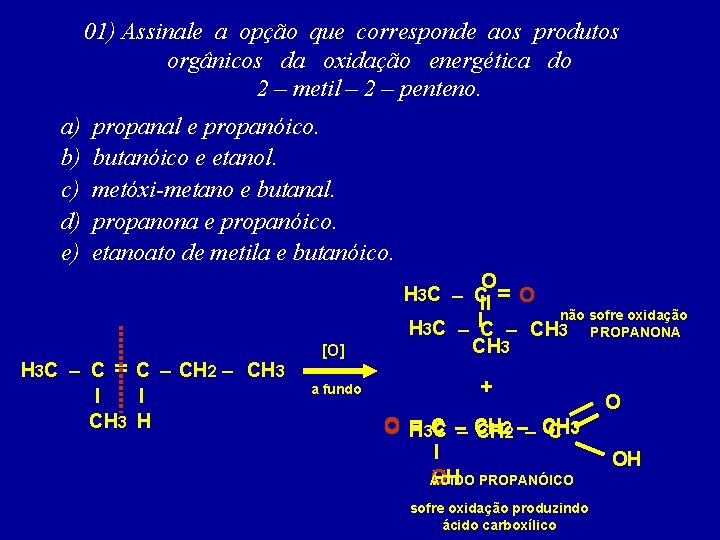
01) Assinale a opção que corresponde aos produtos orgânicos da oxidação energética do 2 – metil – 2 – penteno. a) b) c) d) e) propanal e propanóico. butanóico e etanol. metóxi-metano e butanal. propanona e propanóico. etanoato de metila e butanóico. H 3 C – C = C – CH 2 – CH 3 I I CH 3 H [O] a fundo O H 3 C – CII = O não sofre oxidação H 3 C – IC – CH 3 PROPANONA CH 3 + =3 C O H C –– CH CH 22 –– CH C 3 I OH ÁCIDO PROPANÓICO H sofre oxidação produzindo ácido carboxílico O OH

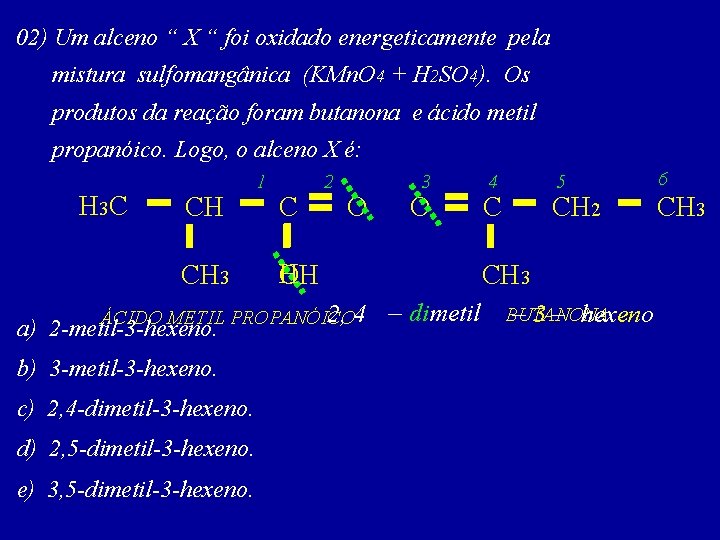
02) Um alceno “ X “ foi oxidado energeticamente pela mistura sulfomangânica (KMn. O 4 + H 2 SO 4). Os produtos da reação foram butanona e ácido metil propanóico. Logo, o alceno X é: H 3 C CH CH 3 1 C 2 O 3 O H OH 2, 4 – dimetil c) 2, 4 -dimetil-3 -hexeno. d) 2, 5 -dimetil-3 -hexeno. e) 3, 5 -dimetil-3 -hexeno. 5 C CH 2 CH 3 ÁCIDO METIL PROPANÓICO a) 2 -metil-3 -hexeno. b) 3 -metil-3 -hexeno. 4 BUTANONA – 3 – hexeno 6 CH 3

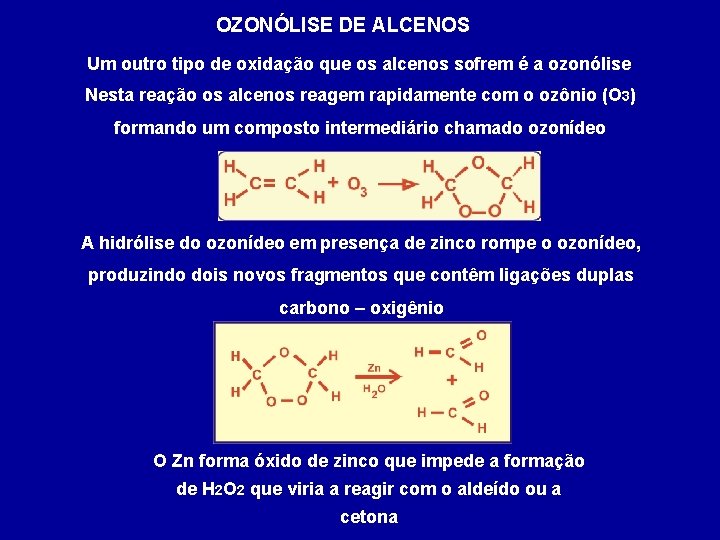
OZONÓLISE DE ALCENOS Um outro tipo de oxidação que os alcenos sofrem é a ozonólise Nesta reação os alcenos reagem rapidamente com o ozônio (O 3) formando um composto intermediário chamado ozonídeo A hidrólise do ozonídeo em presença de zinco rompe o ozonídeo, produzindo dois novos fragmentos que contêm ligações duplas carbono – oxigênio O Zn forma óxido de zinco que impede a formação de H 2 O 2 que viria a reagir com o aldeído ou a cetona

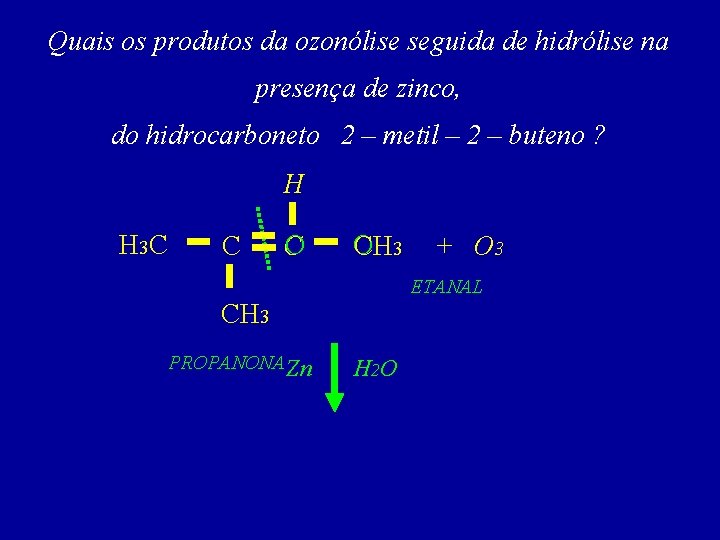
Quais os produtos da ozonólise seguida de hidrólise na presença de zinco, do hidrocarboneto 2 – metil – 2 – buteno ? H H 3 C C O CH 3 + O 3 ETANAL CH 3 PROPANONA Zn H 2 O