Prof Srgio Yoshio Funes Inorgnicas Prof Busato Qumica

Prof. Sérgio Yoshio Funções Inorgânicas Prof. Busato Química

Funções químicas Função química corresponde a um conjunto de substâncias que apresentam propriedades químicas semelhantes. As substâncias inorgânicas podem ser classificadas em quatro funções: §Ácidos §Bases §Sais §Óxidos Assim, numa reação química, todos os ácidos, por exemplo, terão comportamento semelhante. Prof. Busato Química
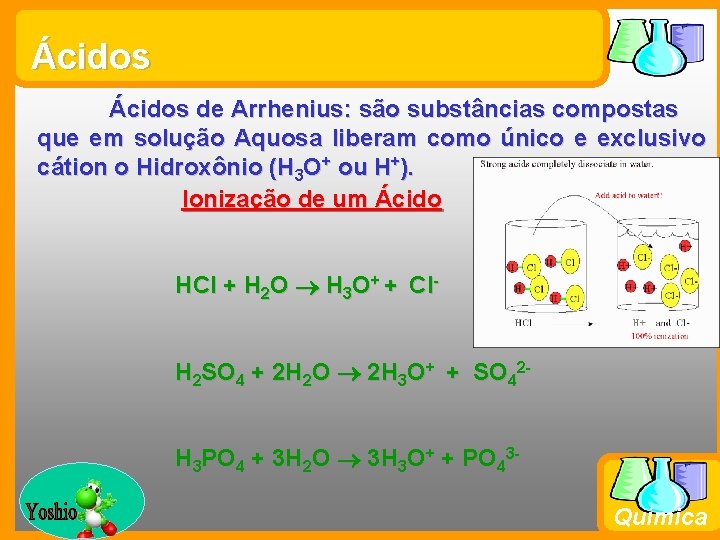
Ácidos de Arrhenius: são substâncias compostas que em solução Aquosa liberam como único e exclusivo cátion o Hidroxônio (H 3 O+ ou H+). Ionização de um Ácido HCl + H 2 O H 3 O+ + Cl. H 2 SO 4 + 2 H 2 O 2 H 3 O+ + SO 42 H 3 PO 4 + 3 H 2 O 3 H 3 O+ + PO 43 Prof. Busato Química

Hidrogênios ionizáveis Os hidrogênios que fornecem H 3 O+ são chamados de hidrogênios ionizáveis. São aqueles que se ligam ao elemento mais eletronegativo na molécula do ácido. Geralmente a quantidade de hidrogênios do ácido é a mesma que pode ionizar, mas existem exceções: H 3 PO 3 + 2 H 2 O 2 H 3 O+ + HPO 32 - apenas 2 H+ H 3 PO 2 + H 2 O H 3 O+ + H 2 PO 21 - apenas 1 H+ Prof. Busato Química

Classificação dos Ácidos Quanto a presença ou ausência de Oxigênio Hidrácidos (HCl, H 2 S, HBr) Oxiácidos (H 2 SO 4, H 3 PO 4, HCl. O 4) Quanto ao número de Hidrogênios Ionizáveis: Monoácidos (HCl, HI, H 3 PO 2) Diácidos (H 2 SO 4, H 2 S, H 3 PO 3) Triácidos (H 3 PO 4, H 3 BO 3, H 3 BO 2) Tetrácidos (H 4 P 2 O 7) Prof. Busato Química

Quanto ao Grau de Ionização (a) Ácidos fracos: 0< a < 5% Ácidos moderados: 5% £ a £ 50% Ácidos fortes : 50% < a < 100% a= Nº de Mol Ionizados Nº Inicial de Mols Ácido fraco: HCl. O Ácido moderado: H 3 PO 4 Ácido forte : H 2 SO 4 HCl. O 4 Prof. Busato Química
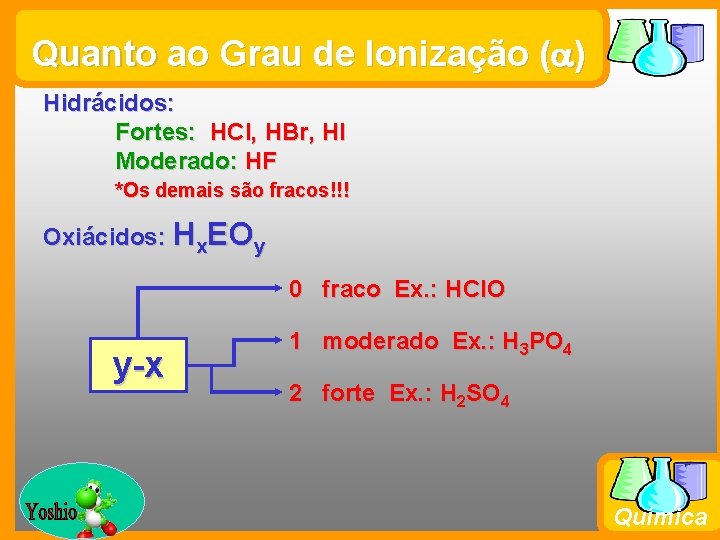
Quanto ao Grau de Ionização (a) Hidrácidos: Fortes: HCl, HBr, HI Moderado: HF *Os demais são fracos!!! Oxiácidos: Hx. EOy 0 fraco Ex. : HCl. O y-x Prof. Busato 1 moderado Ex. : H 3 PO 4 2 forte Ex. : H 2 SO 4 Química
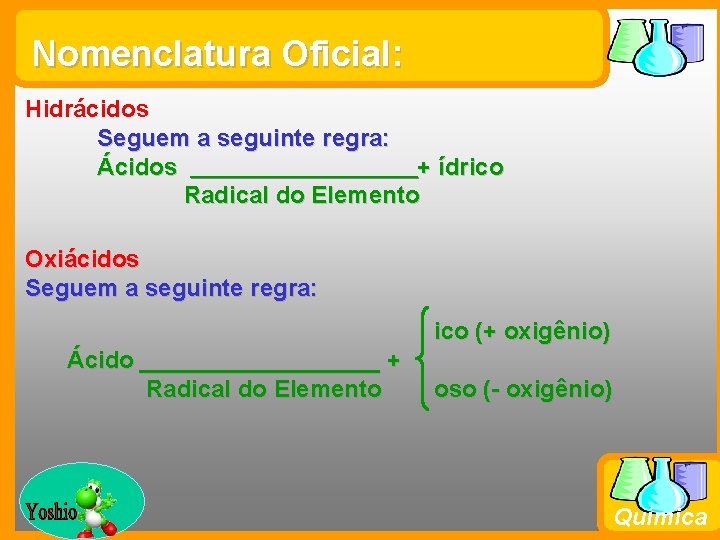
Nomenclatura Oficial: Hidrácidos Seguem a seguinte regra: Ácidos + ídrico Radical do Elemento Oxiácidos Seguem a seguinte regra: ico (+ oxigênio) Ácido _________ + Radical do Elemento Prof. Busato oso (- oxigênio) Química

Nomenclatura Oxiácidos: Ácidos padrões: (Ác. . . ico) -H 3 BO 3 -H 2 CO 3 -HNO 3 -H 3 PO 4 (+1 oxig. )Ác. Per. . . ico (Padrão) Ác. . . ico (-1 oxig. )Ác. . . oso (-2 oxig. )Ác. Hipo. . . oso Ex: HCl. O 4 – ác. Perclórico -H 2 SO 4 HCl. O 2 – ác. Cloroso -HCl. O 3 HCl. O – ác. Hipocloroso Prof. Busato Química

Exemplo: H 2 S Ácido sulfídrico H 2 SO 3 Ácido sulfuroso H 2 SO 4 Ácido sulfúrico Prof. Busato *Para ácidos do enxofre usamos o radical em latim “sulfur”. Química

Características gerais dos ácidos üApresentam sabor azedo; üDesidratam a matéria orgânica; üDeixam incolor a solução alcoólica de fenolftaleína; üNeutralizam bases formando sal e água; Prof. Busato Química

Ácidos importantes: 1) H 2 SO 4 – Ác. Sulfúrico (ácido ou água de bateria) É um líquido incolor e oleoso de densidade 1, 85 g/cm 3, é um ácido forte que reage com metais originando sulfatos além de ser muito higroscópico. Pode ser obtido a partir das seguintes reações: S + O 2 SO 2 + ½O 2 SO 3 + H 2 O H 2 SO 4 *É usado para medir o desenvolvimento industrial de um país. Prof. Busato Química

Ácidos importantes: 2) HCl – Ác. Clorídrico (ácido muriático) Solução de hidreto de cloro em água. Apresenta forte odor, além de ser sufocante. É utilizado na limpeza de peças metálicas e de superfícies de mármore. É encontrado no suco gástrico humano. *A limpeza de superfícies com ácido clorídrico é chamada de decapagem. Prof. Busato Química
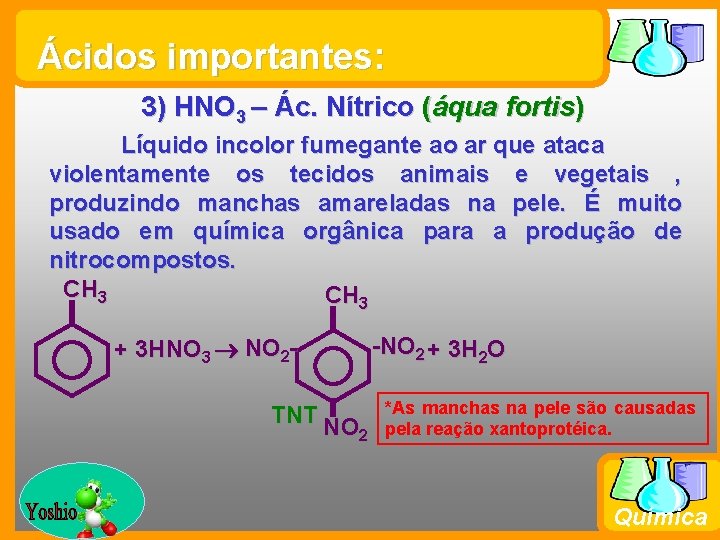
Ácidos importantes: 3) HNO 3 – Ác. Nítrico (áqua fortis) Líquido incolor fumegante ao ar que ataca violentamente os tecidos animais e vegetais , produzindo manchas amareladas na pele. É muito usado em química orgânica para a produção de nitrocompostos. CH 3 + 3 HNO 3 NO 2 TNT NO 2 Prof. Busato -NO 2 + 3 H 2 O *As manchas na pele são causadas pela reação xantoprotéica. Química

Ácidos importantes: 4) H 3 PO 4 – Ác. Fosfórico (Acidulante INS-338) É um líquido xaporoso obtido pela oxidação do fósforo vermelho com ácido nítrico concentrado. É um ácido moderado usado na industria de vidros, preparo de águas minerais e nos refrigerantes de “cola”. Seus fosfatos são usados como adubo. *Seus fosfatos fazem parte da formulação do fertilizante “NPK”. Prof. Busato Química

Bases De acordo com Arrhenius, base ou hidróxido é toda substância que, dissolvida em água, dissocia-se fornecendo como ânion exclusivamente OH- (hidroxila ou oxidrila). Na. OH Na+ + OHCa(OH)2 Ca 2+ + 2 OH- §Possuem OH- (direita); §Metais; §Lig. Iônicas; §Sólidas; §Fixas. Al(OH)3 Al 3+ + 3 OHProf. Busato Química

Bases (exceção) * NH 3 + H 2 O NH 4 OH §Ametais; §Lig. covalentes; §Solução aquosa; §Volátil. Prof. Busato Química

Nomenclatura Hidróxido de _________ Nome do Elemento Na. OH hidróxido de sódio Fe(OH)2 hidróxido de ferro II Fe(OH)3 hidróxido de ferro III Prof. Busato Química

Classificação Quanto ao Número de Hidroxilas - Monobases: - Dibases: - Tribases: - Tetrabases: Na. OH; NH 4 OH Ca(OH)2; Mg(OH)2 Al(OH)3; Fe(OH)3 Pb(OH)4; Sn(OH)4 Quanto ao Grau de Dissociação Iônica - Fortes: Os hidróxidos de metais alcalinos (G 1) e metais alcalinos terrosos (G 2). - Fracas: Nesse grupo incluem-se o hidróxido de amônio (NH 4 OH) e as demais bases. Prof. Busato Química

Classificação Quanto à Solubilidade em Água - Totalmente solúveis: os hidróxidos metais alcalinos (G 1) e o hidróxido de amônio (NH 4 OH). - Parcialmente solúveis: hidróxidos metais alcalino-terrosos (G 2). - Insolúveis: todos os demais hidróxidos. KOH Prof. Busato Monobase Forte Solúvel Al(OH)3 Tribase Fraca Insolúvel Química

Características gerais das bases üApresentam sabor caústico; üEstriam a matéria orgânica; üDeixam vermelha a solução alcoólica de fenolftaleína; üNeutralizam ácidos formando sal e água; Prof. Busato Química

Bases importantes: 1) Na. OH – Hidróxido de sódio (Soda caústica) É um sólido branco floculado muito solúvel em água além de extremamente caústico. É usado na desidratação de gorduras, no branqueamento de fibras (celulose) e na fabricação de sabões e detergentes e como desentupidor de ralos e esgotos. *Sabões e detergentes são chamados de agentes tensoativos e possuem caráter básico. Prof. Busato Química

Bases importantes: 2) Ca(OH)2 – Hidróxido de cálcio (cal apagada, hidratada ou extinta) É uma suspensão aquosa de aparência leitosa, obtida a partir do Ca. O (cal virgem). É usada na caiação de paredes e muros, na neutralização de solos ácidos e na fabricação de doces. Ca. O + H 2 O Ca(OH)2 Cal Virgem Prof. Busato Cal Apagada Química

Bases importantes: 3) Mg(OH)2 – Hidróxido de magnésio (Leite de magnésia) É uma suspensão leitosa, obtida a partir do Mg. O. É usada como antiácido estomacal e também como laxante. Mg(OH)2 + 2 HCl Mg. Cl 2 + 2 H 2 O *Antigamente era aplicada nas axilas para impedir a ação dos ácidos que causam odores indesejáveis. Prof. Busato Química

Bases importantes: 4) Al(OH)3 – Hidróxido de alumínio (Maalox) É uma suspensão gelatinosa que pode adsorver moléculas orgânicas que por ventura estejam em solução aquosa (no tratamento da água). É usada como antiácido estomacal, para tingimentos e na preparação de lacas (resina ou verniz) para pintura artística. *Como antiácido estomacal recebe os nomes de Mylantha plus e Gelmax. Prof. Busato Química
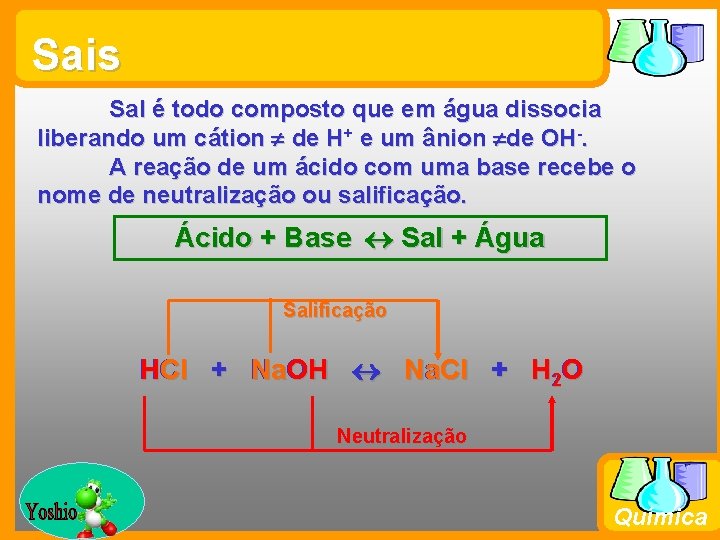
Sais Sal é todo composto que em água dissocia liberando um cátion de H+ e um ânion de OH-. A reação de um ácido com uma base recebe o nome de neutralização ou salificação. Ácido + Base Sal + Água Salificação HCl + Na. OH Na. Cl + H 2 O Neutralização Prof. Busato Química

Nomenclatura Obedece à expressão: (nome do ânion) de (nome do cátion) Sufixo do ácido ídrico oso Sufixo do ânion eto ato ito H 2 SO 4 + Ca(OH)2 Ca. SO 4 + 2 H 2 O Sulfato de cálcio (gesso) Prof. Busato Química
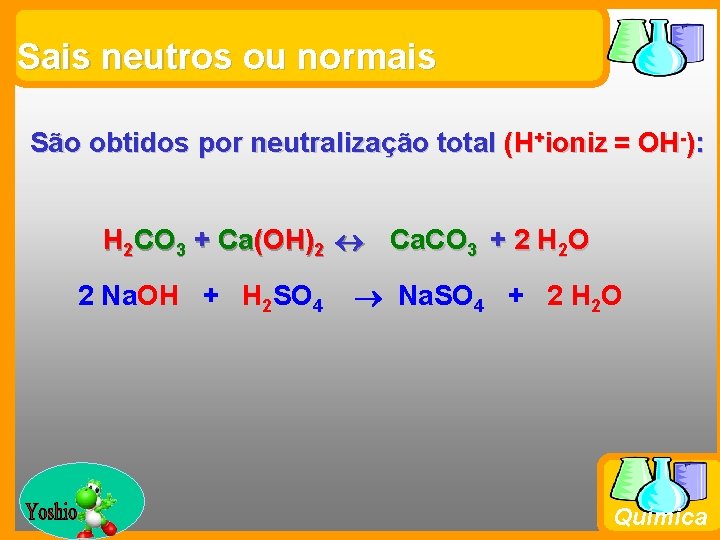
Sais neutros ou normais São obtidos por neutralização total (H+ioniz = OH-): H 2 CO 3 + Ca(OH)2 Ca. CO 3 + 2 H 2 O 2 Na. OH + H 2 SO 4 Prof. Busato Na. SO 4 + 2 H 2 O Química

Sais Ácidos e Sais Básicos São obtidos por neutralização parcial (H+ioniz ≠ OH-): H 2 CO 3 + Na Na. OH OH Na. HCO 3 + H 2 O Sal ácido ou hidrogenossal HCl + Mg HCl Mg(OH)2 Mg(OH)Cl + H 2 O Sal básico ou hidróxissal Prof. Busato Química

Classificação Quanto à Presença de Água - Hidratados: Cu. SO 4. 5 H 2 O; Ca. SO 4. 2 H 2 O - Anidro: KCl; Na. Cl; Ca. SO 4 Quanto à Natureza - Neutros ou normais: Na. Br; Ca. CO 3 - Ácidos ou Hidrogenossais: Na. HCO 3; Ca. HPO 4 - Básicos ou Hidroxissais: Ca(OH)Br - Duplos ou mistos: Na. KSO 4; Ca. Cl. Br Prof. Busato Química

Sais importantes: 1) Na. HCO 3 – Bicarbonato de sódio (ENO, Sonrisal) É um pó branco que perde CO 2 com facilidade (efervescência). É usado como antiácido estomacal , fermento químico e nos extintores de incêndio. H 2 CO 3 Na. HCO 3 + H 2 O Na. OH + H 2 O+ CO 2 *Pode ser usado para neutralizar os ácidos graxos na manteiga rançosa. Prof. Busato Química

Sais importantes: 2) Ca. CO 3 – Carbonato de cálcio (mármore, calcáreo) É um sólido branco que por aquecimento perde CO 2 e produz Ca. O (calcinação). É usado na fabricação de cimentos(Portland), como corretivo do solo e como fundente em metalurgia. Ca. CO 3 Ca. O + CO 2 *Na Espanha é encontrado na região de Aragón, daí seu nome mineral (aragonita). Na forma de estalagmites pode ser chamado de calcita (mármore Carrara). Prof. Busato Química

Sais importantes: 3) Na. NO 3 – Nitrato de sódio (Salitre do Chile) É um sólido cristalizado no sistema cúbico, além de ser um ótimo oxidante para reações químicas. É usado na fabricação de fertilizantes e explosivos. *Nos Andes era higroscópico. Prof. Busato utilizado na conservação da carne por ser Química

Sais importantes: 4) NH 4 Cl – Cloreto de amônio (Sal amoníaco) É um sólido granulado obtido do líquido amoniacal das fábricas de gás. É usado na fabricação de pilhas secas, na soldagem , na galvanização do ferro e na fabricação de tecidos. *Por ser higroscópico é utilizado na fabricação de bolachas. Prof. Busato Química

Óxidos Óxido é todo composto binário oxigenado, no qual o oxigênio é o elemento mais eletronegativo. Fórmula geral dos óxidos: x+ E 2 2 O X Exemplos: CO 2, H 2 O, Mn 2 O 7, Fe 2 O 3 Prof. Busato Química

Nomenclatura Regra geral: (Prefixo) + óxido de (prefixo) + elemento CO -monóxido de monocarbono N 2 O 5 -pentóxido de dinitrogênio P 2 O 3 -trióxido de difosforo H 2 O -monóxido de dihidrogênio Nox fixo(g 1 e g 2)- óxido de elemento Para metais: Nox - óxido de elemento+valência Na 2 O -óxido de sódio Al 2 O 3 -óxido de alumínio Fe. O -óxido de ferro II (óxido ferroso) Fe 2 O 3 -óxido de ferro III (óxido férrico) Prof. Busato Química

Classificação • Óxidos Ácidos • Óxidos Básicos • Óxidos Anfóteros • Óxidos Neutros • Óxidos Duplos • Peróxidos Prof. Busato • Superóxidos Química
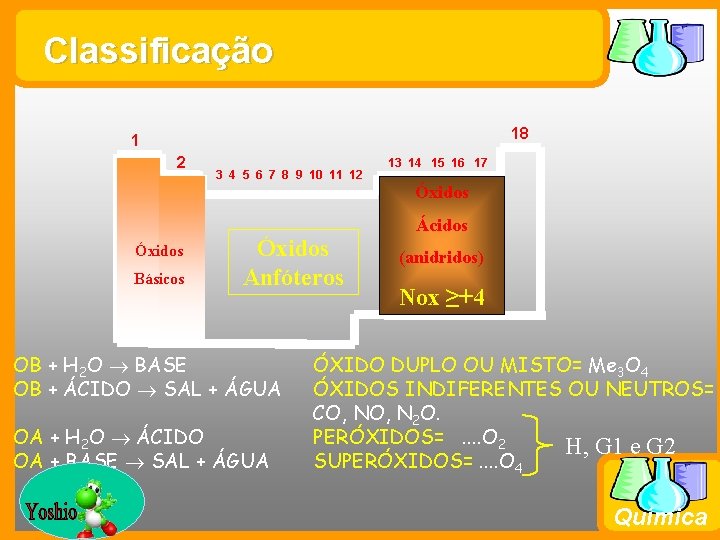
Classificação 18 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 Óxidos Básicos Óxidos Anfóteros OB + H 2 O BASE OB + ÁCIDO SAL + ÁGUA OA + H 2 O ÁCIDO OA + BASE SAL + ÁGUA Prof. Busato Ácidos (anidridos) Nox ≥+4 ÓXIDO DUPLO OU MISTO= Me 3 O 4 ÓXIDOS INDIFERENTES OU NEUTROS= CO, N 2 O. PERÓXIDOS=. . O 2 H, G 1 e G 2 SUPERÓXIDOS=. . O 4 Química

Óxidos Básicos (metálicos) São formados por metais alcalinos e alcalinos terrosos e reagem com água formando bases e com ácidos formando sal e água. Óxido básico + H 2 O base 2 Na. O + H 2 O 2 Na. OH Ca. O + H 2 O Ca(OH)2 Ca. O (cal virgem, cal viva ) Óxido básico + ácido sal + H 2 O Mg. O + 2 HCl Mg. Cl 2 + H 2 O Prof. Busato Química

Óxidos Ácidos (anidridos) São formados por ametais e reagem com água formando ácidos e com bases formando sal e água. Óxido ácido + H 2 O ácido CO 2 + H 2 O H 2 CO 3 (gás carbônico) – EFEITO ESTUFA N 2 O 5 + H 2 O 2 HNO 3 SO 3 + H 2 O H 2 SO 4 “chuva ácida” Óxido ácido + base sal + H 2 O CO 2 + Ca(OH)2 Ca. CO 3 + H 2 O Prof. Busato Química
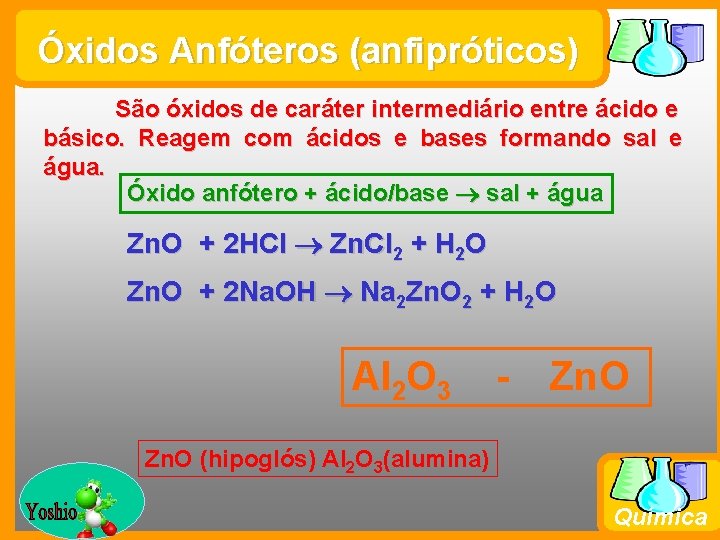
Óxidos Anfóteros (anfipróticos) São óxidos de caráter intermediário entre ácido e básico. Reagem com ácidos e bases formando sal e água. Óxido anfótero + ácido/base sal + água Zn. O + 2 HCl Zn. Cl 2 + H 2 O Zn. O + 2 Na. OH Na 2 Zn. O 2 + H 2 O Al 2 O 3 - Zn. O (hipoglós) Al 2 O 3(alumina) Prof. Busato Química

Óxidos Neutros (indiferentes) São todos covalentes e não reagem com base, ácido ou água; mas podem reagir com oxigênio. CO + H 2 O Não ocorre reação NO + HCl Não ocorre reação Óxido Neutro + O 2 Oxidação CO + ½O 2 CO 2 CO Prof. Busato - NO Química
Óxidos Duplos (mistos) São óxidos que, quando aquecidos, originam dois outros óxidos. M 3 O 4 Fe, Pb, Mn Fe. O + Fe 2 O 3 Fe 3 O 4 (magnetita , imã) Fe 3 O 4; Pb 3 O 4; Mn 3 O 4 Prof. Busato Química
Peróxidos São formados por metais alcalinos, alcalinos terrosos e hidrogênio e possuem oxigênio com Nox = -1. M 2 O 2 - MO 2 M. Alcalinos M. Alc. Terrosos Ex. : Na 2 O 2, Li 2 O 2, Ca. O 2, Mg. O 2 H 2 O 2 - Ag. Oxidante e Bactericida Prof. Busato Química

Superóxidos (polióxidos) São formados por metais alcalinos, alcalinos terrosos e hidrogênio e possuem oxigênio com Nox = - ½. M 2 O 4 - MO 4 M. Alcalinos M. Alc. Terrosos Ex. : Na 2 O 4, Li 2 O 4, Ca. O 4, Mg. O 4 Prof. Busato Química

Óxidos importantes: 1) Zn. O – óxido de Zinco (Hipoglós) É um sólido branco de caráter anfótero (anfiprótico). É usado na fabricação de cremes dermatológicos, na industria de tintas galvanização do ferro. e na *A proteção de superfícies metálicas com tintas ou metais de sacrifício é chamada de proteção anódica. Prof. Busato Química

Óxidos importantes: 2) Al 2 O 3 – óxido de Alumínio (Bauxita, Alumina) É um sólido muito duro (dureza 9) de onde é extraído por eletrólise o alumínio metálico. Na forma cristalizada é encontrado nas safiras e nos rubis. *É um óxido anfótero abrasivo que também pode ser chamado de Coríndon. Prof. Busato Química

Óxidos importantes: 3) H 2 O 2 – Peróxido de hidrogênio (água oxigenada) É uma solução aquosa que se decompõe facilmente em presença de luz (fotólise). É utilizada como agente oxidante e bactericida. H 2 O 2 H 2 O + ½ O 2 *Os recipientes que guardam a água oxigenada são opacos para impedir a entrada de luz. Prof. Busato Química

Óxidos importantes: 4) Fe 3 O 4 – Tetróxido de triferro (magnetita, imã) É um sólido escuro que apresenta características ferromagnéticas. É utilizado na fabricação de caixas de som e aparelhos eletrônicos em geral. Fe. O + Fe 2 O 3 Fe 3 O 4 *A tarja dos cartões magnéticos é constituída por este óxido. Prof. Busato Química

p. H e indicadores Prof. Busato Química
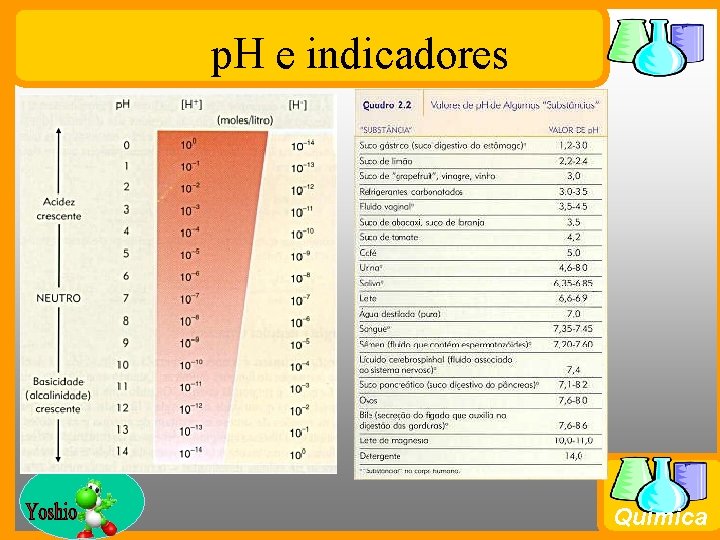
p. H e indicadores Prof. Busato Química
- Slides: 51