Prof Paolo Abis Lic Classico D A Azuni

Prof. Paolo Abis Lic. Classico “D. A. Azuni” SASSARI Come assegnare un nome ad una sostanza chimica e/o come, noto il nome, scrivere al sua formula Nomenclatura Chimica 1. Il numero di Ossidazione

Nomenclatura Chimica La materia è formata da sostanze semplici (elementi) che si ritrovano in natura da sole o in unione fra loro per formare composti (molecole). l Attualmente i chimici hanno classificato più di 10 milioni di composti (naturali e sintetici) l I composti chimici sono distinguibili l'uno dall'altro per le loro proprietà particolari, pertanto è necessario imparare a conoscerli, attribuendo loro un nome che non possa ingenerare confusione con qualche altra sostanza similare. l

Nomenclatura Chimica l Una nomenclatura sistematica dei vari composti deve tener conto delle caratteristiche chimiche generali e degli elementi che li costituiscono. l Insieme delle regole che consente di attribuire un nome a ciascun composto di cui si conosca la formula o, viceversa, di ricavare la formula se è noto il nome del composto.
Nomenclatura Chimica Tradizionale In chimica generale continua ad avere maggior diffusione la nomenclatura tradizionale, anche perché legata a composti chimici comuni e diffusi. I nomi tradizionali sono legati agli albori della chimica, spesso (in chimica organica) derivano dal nome della fonte naturale da cui questi composti sono stati isolati. IUPAC International Union of Pure and Applied Chemistry Commissione internazionale costituita con lo scopo di aggiornare e uniformare le regole riguardanti la nomenclatura chimica. I nomi IUPAC si basano sulla corrispondenza, il più possibile esatta e univoca, tra nome e formula chimica del composto.

Molecola Si definisce molecola (dal latino scientifico "molecula", derivato a sua volta da "moles": mole, "piccola quantità") la più piccola unità strutturale di un composto chimico non ionico che può esistere allo stato libero e che ne mantiene le medesime proprietà chimiche. l Può essere monoatomica, cioè costituita da un solo atomo (è il caso dei cosiddetti gas nobili elio, argon, xeno, neon) o poliatomica, cioè costituita da più atomi, uguali o diversi. l Le singole parti, gli atomi, hanno proprietà differenti da quelle dell’intera molecola. l
Formula chimica l La formula chimica di una molecola indica la composizione: qualitativa quantitativa Gli elementi che la compongono In quali rapporti quantitativi Viene espressa utilizzando i simboli chimici degli elementi che la compongono
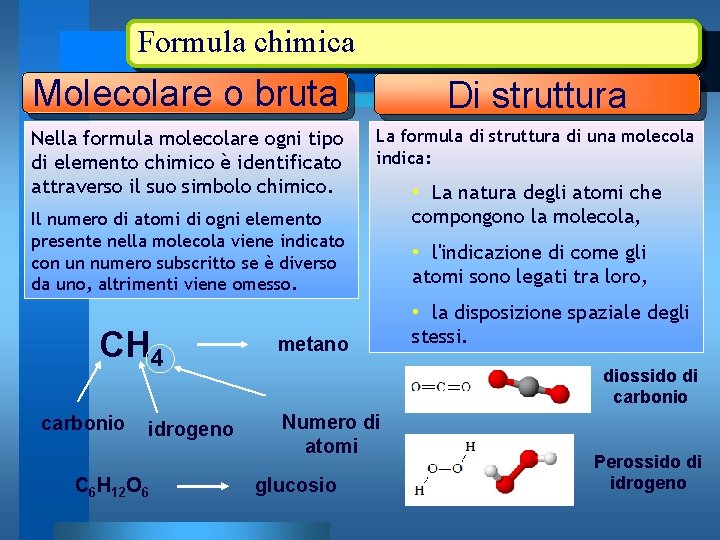
Formula chimica Molecolare o bruta Di struttura Nella formula molecolare ogni tipo di elemento chimico è identificato attraverso il suo simbolo chimico. La formula di struttura di una molecola indica: Il numero di atomi di ogni elemento presente nella molecola viene indicato con un numero subscritto se è diverso da uno, altrimenti viene omesso. CH 4 carbonio idrogeno C 6 H 12 O 6 metano • La natura degli atomi che compongono la molecola, • l'indicazione di come gli atomi sono legati tra loro, • la disposizione spaziale degli stessi. diossido di carbonio Numero di atomi glucosio Perossido di idrogeno

Valenza e Numero di Ossidazione Per scrivere la formula chimica di un composto dobbiamo prestare particolare attenzione a due caratteristiche: • Posizione nel Sistema Periodico Distinguere fra metalli e non metalli • Configurazione elettronica Per valutare gli elettroni in eccesso o in difetto rispetto alla configurazione più stabile (ottetto)

Posizione nel Sistema Periodico Ø tenere in considerazione la distinzione metallo/non-metallo
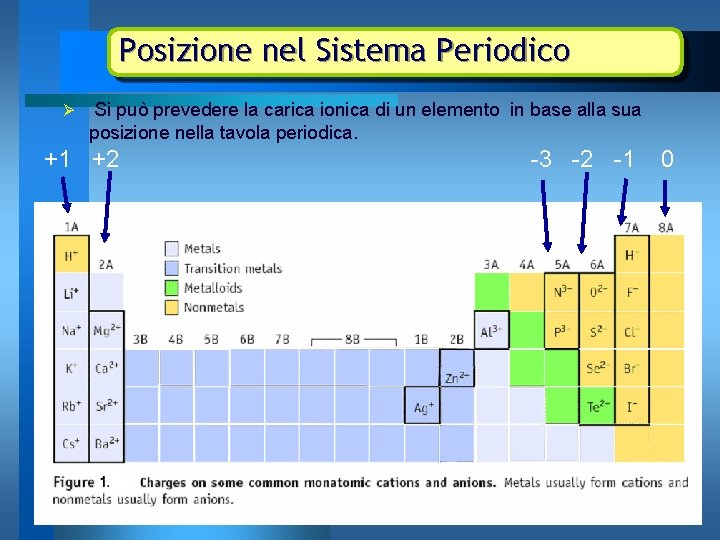
Posizione nel Sistema Periodico Ø Si può prevedere la carica ionica di un elemento in base alla sua posizione nella tavola periodica. +1 +2 -3 -2 -1 0
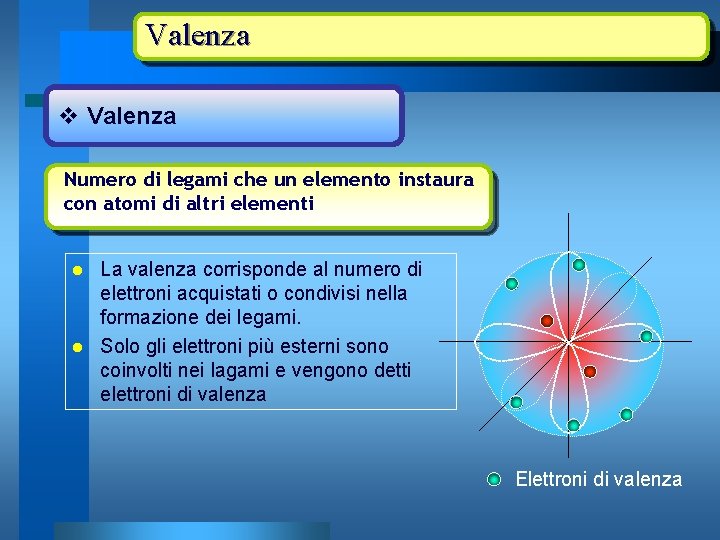
Valenza v Valenza Numero di legami che un elemento instaura con atomi di altri elementi La valenza corrisponde al numero di elettroni acquistati o condivisi nella formazione dei legami. l Solo gli elettroni più esterni sono coinvolti nei lagami e vengono detti elettroni di valenza l Elettroni di valenza
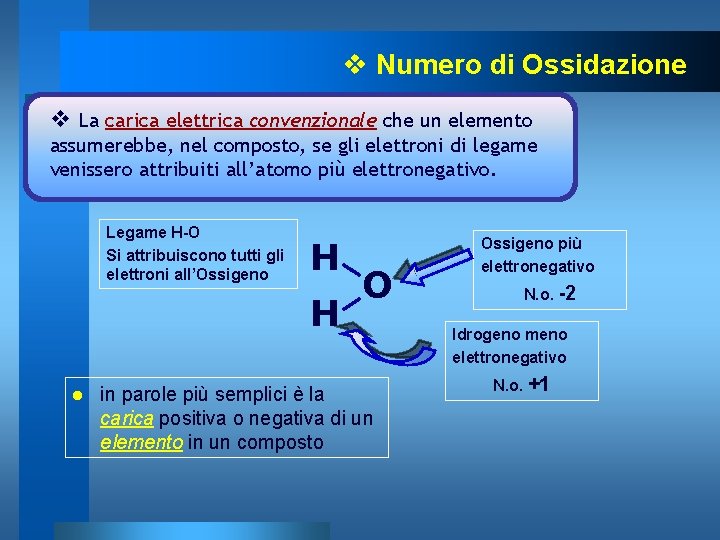
v Numero di Ossidazione v La carica elettrica convenzionale che un elemento assumerebbe, nel composto, se gli elettroni di legame venissero attribuiti all’atomo più elettronegativo. Legame H-O Si attribuiscono tutti gli elettroni all’Ossigeno H H l O in parole più semplici è la carica positiva o negativa di un elemento in un composto Ossigeno più elettronegativo N. o. -2 Idrogeno meno elettronegativo N. o. +1
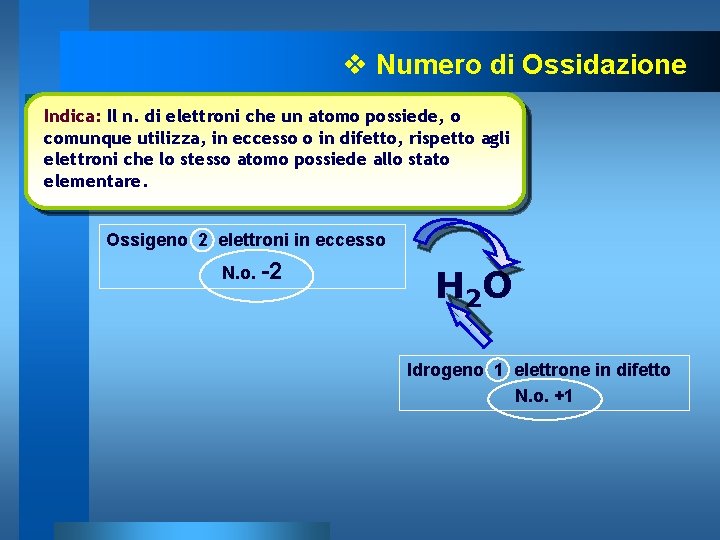
v Numero di Ossidazione Indica: Il n. di elettroni che un atomo possiede, o comunque utilizza, in eccesso o in difetto, rispetto agli elettroni che lo stesso atomo possiede allo stato elementare. Ossigeno 2 elettroni in eccesso N. o. -2 H 2 O Idrogeno 1 elettrone in difetto N. o. +1

v Numero di Ossidazione I numeri di ossidazione di O, H, F e Cl sono i seguenti F -1 O -2 H +1 Cl -1 (con alcune eccezioni). Agli atomi, nelle loro forme elementari, vengono attribuiti numeri di ossidazione uguali a zero. Ad esempio, in H 2, O 3, P 4, Mg, Ne, ecc. , il n. o. di ogni singolo elemento è 0 (zero).

v Numero di Ossidazione l La somma algebrica dei numeri di ossidazione di tutti gli atomi presenti in una molecola neutra deve essere zero; N. di Ossidazione del C in CO 2? ? – 4=0 ? = +4 Aggiungi il +! F -1 O -2 H +1 Cl -1

v Numero di Ossidazione l La somma algebrica dei numeri di ossidazione di tutti gli atomi presenti in una molecola neutra deve essere zero; N. di Ossidazione del Mg in Mg. Cl 2? +2 F -1 O -2 H +1 Cl -1

v Numero di Ossidazione l La somma algebrica dei numeri di ossidazione di tutti gli atomi presenti in una molecola neutra deve essere zero; N. di ossidazione dell’ N in NH 3? -3 F -1 O -2 H +1 Cl -1

v Numero di Ossidazione La somma algebrica dei numeri di ossidazione di tutti gli atomi presenti in una molecola neutra deve essere zero; F -1 O -2 N. di Ossidazione dello S in SO 42 - ? H +1 ? – 8 = -2 Cl -1 Ø mentre, in uno ione, assume il valore della carica elettrica da esso posseduta. ? = +6

v Numero di Ossidazione La somma algebrica dei numeri di ossidazione di tutti gli atomi presenti in una molecola neutra deve essere zero; Ø mentre, in uno ione, assume il valore della carica elettrica da esso posseduta. N. di Ossidazione dello S in S 2 - ? -2 F -1 O -2 H +1 Cl -1

v Numero di Ossidazione La somma algebrica dei numeri di ossidazione di tutti gli atomi presenti in una molecola neutra deve essere zero; Ø mentre, in uno ione, assume il valore della carica elettrica da esso posseduta. N. di Ossidazione N in NH 4+ ? -3 F -1 O -2 H +1 Cl -1

N. O. di alcuni atomi coinvolti in legami covalenti Acido cloridrico, HCl Acqua, H 2 O Acqua ossigenata, H 2 O 2 Idrogeno, H 2 Ossido di fluoro, F 2 O Formula di Lewis N. O. H: Cl -1(Cl) +1(H) H: O: H -2(O) +1(H) H: O: O: H -1(O) +1(H) H: H 0(H) F: O: F -1(F) +2(O) Un elemento viene considerato tanto più ossidato quanto più elevato è il suo N. O.

N. O. di alcuni atomi coinvolti in legami ionici N. O. Na. Cl (Na+ Cl-) +1(Na) -1(Cl) Ca. F 2 (Ca 2+ 2 F-) +2(Ca) -1(F) Na 2 SO 4 (2 Na+ SO 42 -) +1(Na) -2(SO 42 -) [-2 = N. O. (S) + 4 N. O. (O)]

Regole per la determinazione del numero di ossidazione

Regole per la determinazione del numero di ossidazione N. O. v Atomi allo stato elementare 0 (Es. He, H 2, N 2, P 4, S 8, …): v elementi del I° gruppo in tutti i loro composti +1 (metalli alcalini) v elementi del II° gruppo in tutti i loro composti +2 (metalli alcalino-terrosi) v l’idrogeno Ø eccetto che negli idruri dei metalli del I e II gruppo del blocco s (Li. H, Na. H, Mg. H 2, Ca. H 2, . . . ) +1 -1

v Regole per la determinazione del numero di ossidazione N. O. l’Ossigeno -2 eccetto che (a) nei perossidi (H 2 O 2): (b) nei superossidi (KO 2): (c) nel fluoruro di ossigeno (F 2 O): v Elementi di ioni monoatomici Na+ S 2 - -1 -1/2 +2 +1 -2 6) La sommatoria dei N. O. degli elementi presenti a) in una molecola neutra: 0 -2 b) in uno ione poliatomico tipo SO 42 -:

v Esempi di determinazione del N. O. Sostanza Mn. O 4 (ione permanganato) PO 43(ione ortofosfato) N. O. (Mn) + 4 (-2) = -1 N. O. (Mn) = - 1 + 8 = +7 N. O. (P) + 4 (-2) = -3 N. O. (P) = - 3 + 8 = +5

v Esempi di determinazione del N. O. Sostanza H 2 SO 4 (acido solforico) K 2 Cr 2 O 7 (bicromato potassico) Na 2 CO 3 (soda Solvay) 2 (+1) + N. O. (S) + 4 (-2) = 0 N. O. (S) = + 8 - 2 = + 6 2 (+1) + 2 N. O. (Cr) + 7 (-2) = 0 N. O. (Cr ) = (+ 14 - 2) / 2 = + 6 2 (+1) + N. O. (C) + 3 (-2) = 0 N. O. (C) = 6 - 2 = 4

v Esempi di determinazione del N. O. H 2, O 3, He 0 n° ossidazione = _______ Osserviamo prima di tutto che He è un elemento, mentre H 2, O 3, pur essendo molecole, sono formate dagli stessi atomi. In questo caso, alla luce della regola "il n. o. degli elementi neutri è pari a zero così come il n. o. per gli elementi costituiti nella realtà da molecole", il n. o. è zero. Si precisa che O 3 è una forma allotropica di ossigeno che è conosciuta con il nome di ozono. Na. H n° ossidazione H = -1 Na = +1 = _______ Na. H è l'idruro di sodio, pertanto l'idrogeno si trova legato ad un atomo meno elettronegativo. In base alla regola il suo n. o. è -1. Il sodio è un metallo alcalino (gruppo I della tavola periodica). Il suo n. o. è +1. Tuttavia allo stesso risultato si poteva arrivare applicando la regola della conservazione della carica 0 (molecola neutra) = -1 (n. o. idrogeno) + x (n. o. sodio, incognito) => x = +1.

v Esempi di determinazione del N. O. S -Cu+ Fe+++ I- n° ossidazione -2 = _______ =+1 _______ +3_______ = -1 = _______ Per gli ioni monoatomici S-- , Cu+, Fe+++, I-, è sufficiente contare le cariche e anteporre al numero il loro segno. Si hanno nell'ordine i seguenti n. o. -2, +1, +3, -1.

v Esempi di determinazione del N. O. NH 3 n° ossidazione -3 = _______ Nell'ammoniaca, NH 3, l'idrogeno si trova legato ad un metallo più elettronegativo. Quindi, in base alla regola, l'idrogeno ha n. o. pari a +1. Il n. o. dell'azoto si trova facilmente scrivendo 0 = 3 x 1 + x, da cui x = -3. NH+4 n° ossidazione -3 = _______ Quando l'azoto si lega ad un quarto atomo d'idrogeno, andando a formare un legame dativo, si ha lo ione ammonio. In questo caso, ogni atomo d'idrogeno ha carica +1. Quindi +1 = 4 x 1 + x, da cui x = -3. Os. O 4 n° ossidazione +8 = _______ Nell'osmio tetrossido non essendoci il fluoro, ogni atomo d'ossigeno ha n. o. -2. Ne segue che 0 = 4 x(-2) + x, e quindi x = +8. Si tratta del più alto n. o. possibile.

v Esempi di determinazione del N. O. Mg. Cl 2, n° ossidazione Mg = -1 = _______ Il cloro è un alogeno e quindi il n. o. di ogni atomo di cloro è -1. Il magnesio, un metallo alcalino terroso, ha n. o. +2. H 2 SO 4 n° ossidazione +6 = _______ idrogeno +1, ossigeno -2, zolfo +6. Infatti esso si ricava dall'equazione: 0 = 2 x 1 + 4 x(-2) + x. Cl. On° ossidazione =+1_______ Nello ione monossoclorato, il cloro ha n. o. pari a: -1 = x + (-2) => x = +1. Li. NO 2 n° ossidazione =+3_______ Nel litio diossonitrato, considerando che il litio è un metallo alcalino (n. o. +1) e che il n. o. dell'ossigeno è -2, si ha che l'atomo di azoto ha n. o. pari a +3. Infatti si ricava da 0 = 1 + x + 2 x(-2).

v Esempi di determinazione del N. O. Na. IO 3 n° ossidazione =+5_______ Nel sodio triossoiodato, il n. o. dello iodio è +5. Infatti 0 = 1 + x + 3 x(-2), da cui x = +5. +6 Na 2 Cr 2 O 7, n° ossidazione = _______ Nel disodioeptaossodicromato, Na 2 Cr 2 O 7, il n. o. di ogni atomo di cromo è +6. Infatti si imposta l'equazione 0 = 2 x 1 + 2 x + 7 x(2), da cui x = +6. L'unica difficoltà è scrivere 2 x, dal momento che di atomi di cromo ce ne sono 2. PF 5, +5 n° ossidazione = _______ il fluoro è l'elemento più elettronegativo Il suo n. o. è -1. Quindi : 0 = x + 5 x(-1) => x = +5.

v Esempi di determinazione del N. O. Ca(Mn. O 4)2, n° ossidazione +7 = _______ Per quanto riguarda il calciotetraossomanganato si possono seguire due strade equivalenti. La prima consiste nel considerare il sale nel suo insieme e impostare l'equazione 0 = 2 + 2[x + 4 x(-2)], da cui x = +7, oppure smembrare il sale osservando che lo ione negativo (anione) ha una sola carica, essendo il calcio bivalente. Si imposta allora l'equazione -1 = x + 4 x(-2), da cui ovviamente x = +7. Mo. S 2. n° ossidazione =+4_______ Nei solfuri l'atomo di zolfo ha n. o. -2. Quindi molibdenodisolfuro l'atomo di molibdeno ha n. o. +4. nel
- Slides: 33