Produzione Idrogeno Combustibili fossili petroli e carboni 80

Produzione Idrogeno Combustibili fossili (petroli e carboni) → 80% energia utilizzata. Criticità: • non rinnovabilità (tempi lunghi) • produzione di inquinanti (anche da additivi): • Anidride solforosa SO 2 • Ossidi d’azoto • Anidride carbonica → effetto serra? (reazione teorica: Cx. Hy + O 2 → CO 2 + H 2 O) • Polveri Combustibili alternativi → idrogeno; H 2 +1/2 02 → H 2 O (emissioni teoriche nulle) Attualmente l’idrogeno copre ≈ 3% dell’energia utilizzata, usato solo nel settore industriale.

Fonti di idrogeno attuali 1. Combustibili fossili (gas naturali e frazioni leggere del petrolio) ≈ 90% 2. Acqua Scarti di produzioni agricole o industriali o appositamente 3. Biomasse Metodi termochimici o elettrochimici con uso di combustibili fossili (!!!) come fonte di energia o materia prima: inquinanti e costosi coltivate + microrganismi da deiezioni, fanghi, effluenti Produttori di idrogeno: 1. Batteri chemioeterotrofi fermentanti (fermentazione al ‘buio’, da composti organici) 2. Batteri fotosintetici (batteri/cianobatteri) ed eucarioti (microalghe) = FOTOPRODUZIONE (luce) • Eucarioti = biofotolisi (dell’acqua) diretta ossigenica (o a due fasi) • Procarioti: • Fotofermentazione anossigenica da batteri anaerobi (da substrati organici e/o inorganici) • Biofotolisi (acqua) indiretta da cianobatteri eterocistati (spaziale) • Biofotolisi (acqua) indiretta a due fasi (temporale) da cianobatteri Presenza di idrogeno in natura: scarsa perché utilizzato da altri microbi (sintrofici) come fonte di potere riducente. Esempio: metanogenesi 1. Biomassa (anaerobiosi)→ H 2 2. CO 2 +H 2 → CH 4
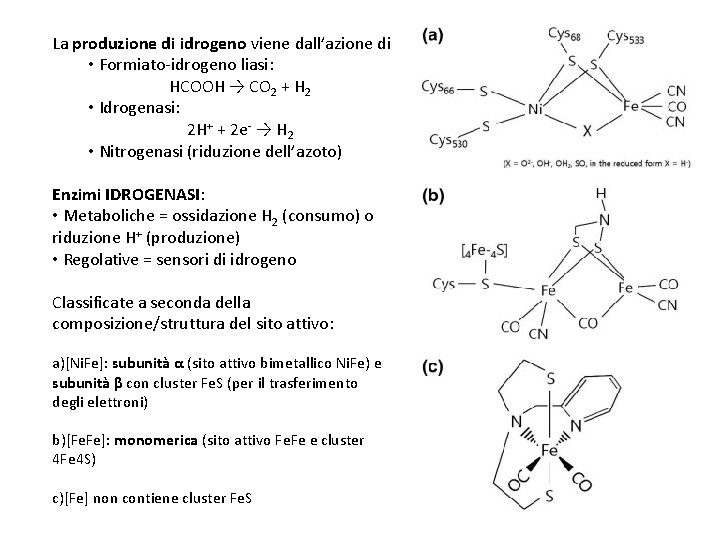
La produzione di idrogeno viene dall’azione di • Formiato-idrogeno liasi: HCOOH → CO 2 + H 2 • Idrogenasi: 2 H+ + 2 e- → H 2 • Nitrogenasi (riduzione dell’azoto) Enzimi IDROGENASI: • Metaboliche = ossidazione H 2 (consumo) o riduzione H+ (produzione) • Regolative = sensori di idrogeno Classificate a seconda della composizione/struttura del sito attivo: a)[Ni. Fe]: subunità α (sito attivo bimetallico Ni. Fe) e subunità β con cluster Fe. S (per il trasferimento degli elettroni) b)[Fe. Fe]: monomerica (sito attivo Fe. Fe e cluster 4 Fe 4 S) c)[Fe] non contiene cluster Fe. S
![Idrogenasi [Ni. Fe]: • Gruppo più numeroso; in batteri e Archea • Poco sensibili Idrogenasi [Ni. Fe]: • Gruppo più numeroso; in batteri e Archea • Poco sensibili](http://slidetodoc.com/presentation_image_h/81a4b002b99fc25f7d6fabddb57bcea0/image-4.jpg)
Idrogenasi [Ni. Fe]: • Gruppo più numeroso; in batteri e Archea • Poco sensibili all’inibizione da CO e O 2 • Subunità α e β (modulo dimerico) • Suddivisione in 4 gruppi: determinati dall’analisi della sequenza e dalle funzioni Accettore (ox) H 2 α 2 e. Fe. S Accettore (red) β Ni. Fe 2 H+ Gruppo Funzione Caratteristiche Organismo I consumo Membrana (peptide segnale); riduzione anaerobia di nitrati, solfati, fumarato, CO 2; riduzione aerobia di O 2 accoppiate a energia da gradiente H+ (H 2→ 2 H+ + 2 e-) Batteri, archea IIa sensore H 2 Citoplasma; attivazione cascata del segnale; insensibili a O 2 Batteri IIb consumo Citoplasma; indotte in condizioni di fissazione N 2; uptake di H 2 per ridurre l’azoto Cianobatteri IIIa consumo Citoplasma; eteromultimerica (idrogenasi + diaforasi); cofattore redox F 420 Metanogeni IIIb bidirezionale Citoplasma; eteromultimerica (idrogenasi + diaforasi); cofattore redox NADP+ Batteri, metanogeni IIIc consumo Citoplasma; eteromultimerica (idrogenasi + diaforasi); non F 420 Metanogeni IIId bidirezionale Citoplasma; eteromultimerica (idrogenasi + diaforasi); cofattore redox NADP+/NAD+ Batteri, cianobatteri IV produzione Membrana; ossidazione del carbonile da acetil-Co. A (metanogeni) → Fd (red) → H 2 (esempio Ech/Vho metanogeni); ossidazione CO/formiato (batteri) → H 2 Archea, batteri
![Idrogenasi [Ni. Fe] gruppo III: • eteromultimeriche • 2 enzimi: idrogenasi e diaforasi • Idrogenasi [Ni. Fe] gruppo III: • eteromultimeriche • 2 enzimi: idrogenasi e diaforasi •](http://slidetodoc.com/presentation_image_h/81a4b002b99fc25f7d6fabddb57bcea0/image-5.jpg)
Idrogenasi [Ni. Fe] gruppo III: • eteromultimeriche • 2 enzimi: idrogenasi e diaforasi • bidirezionali • citoplasmatiche Accettore (ox) NAD+/NADP+/F 420(ox) H 2 α NADH+/NADPH+/F 420(red) Fe. S 2 e- Fe. S β Ni. Fe 2 H+ Idrogenasi (modulo dimerico) Fe. S diaforasi Accettore (red)
![Idrogenasi [Fe. Fe]: • Monomeriche (solo la subunità catalitica) o dimeriche • Presente in Idrogenasi [Fe. Fe]: • Monomeriche (solo la subunità catalitica) o dimeriche • Presente in](http://slidetodoc.com/presentation_image_h/81a4b002b99fc25f7d6fabddb57bcea0/image-6.jpg)
Idrogenasi [Fe. Fe]: • Monomeriche (solo la subunità catalitica) o dimeriche • Presente in procarioti (clostridi e riduttori di solfato) ed eucarioti (esempio in alghe verdi Chlorella, Chlamydomonas): uniche idrogenasi presenti negli eucarioti • Utilizzate principalmente per la produzione di H 2 in condizioni anaerobiche (valvola di scarico del potere riducente, elettroni attivati dalla luce) • Localizzate nel citoplasma, periplasma o cloroplasti (alghe) • Utilizzano ferredoxine, flavodoxine o citocromi per scambiare elettroni Produzione ossigenica di H 2 (microalghe) Chlamydomonas reinhardtii
![Idrogenasi [Fe]: • Idrogenasi particolare chiamata Hmd • Presente negli archea metanogeni (non tutti) Idrogenasi [Fe]: • Idrogenasi particolare chiamata Hmd • Presente negli archea metanogeni (non tutti)](http://slidetodoc.com/presentation_image_h/81a4b002b99fc25f7d6fabddb57bcea0/image-7.jpg)
Idrogenasi [Fe]: • Idrogenasi particolare chiamata Hmd • Presente negli archea metanogeni (non tutti) • Permette la riduzione della CO 2 a metano [riduzione reversibile di metenil-tetraidrometanopterina (methenyl-H 4 MPT+) con H 2 a metilen-H 4 MPT e H+ (∆Go′=− 5. 5 k. J mol− 1); vedi metanogeni] • Il ferro non è catalizzatore redox • Non catalizza la reazione H+ + e - ½ H 2
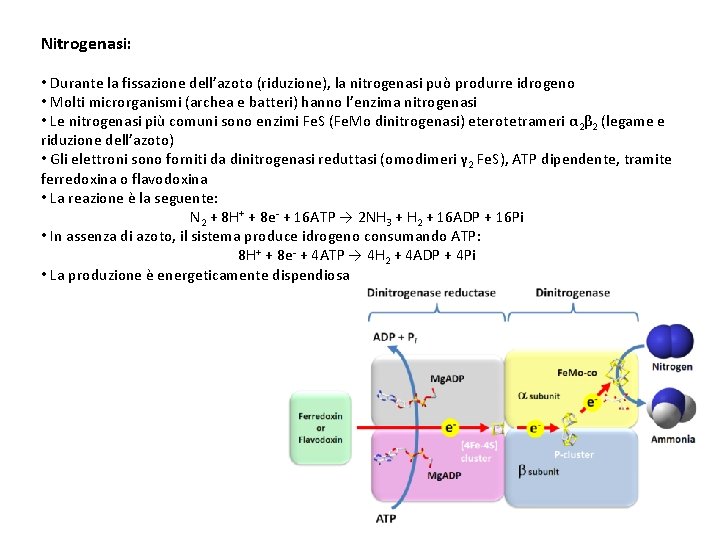
Nitrogenasi: • Durante la fissazione dell’azoto (riduzione), la nitrogenasi può produrre idrogeno • Molti microrganismi (archea e batteri) hanno l’enzima nitrogenasi • Le nitrogenasi più comuni sono enzimi Fe. S (Fe. Mo dinitrogenasi) eterotetrameri α 2β 2 (legame e riduzione dell’azoto) • Gli elettroni sono forniti da dinitrogenasi reduttasi (omodimeri γ 2 Fe. S), ATP dipendente, tramite ferredoxina o flavodoxina • La reazione è la seguente: N 2 + 8 H+ + 8 e- + 16 ATP → 2 NH 3 + H 2 + 16 ADP + 16 Pi • In assenza di azoto, il sistema produce idrogeno consumando ATP: 8 H+ + 8 e- + 4 ATP → 4 H 2 + 4 ADP + 4 Pi • La produzione è energeticamente dispendiosa

Produzione di idrogeno per via fermentativa, al buio, da biomasse Molti vantaggi: • microrganismi fermentanti H 2 -produttori sono diffusi in natura • grande varietà di vie metaboliche consentono l’accumulo di H 2 • produzione continua (non luce-dipendente) • riciclo di biomasse (subsatrati) • produzioni elevate → nuovo interesse sul processo Metabolismi interessati: • Fermentazione acido-mista • Fermentazione butanolo/propanolo
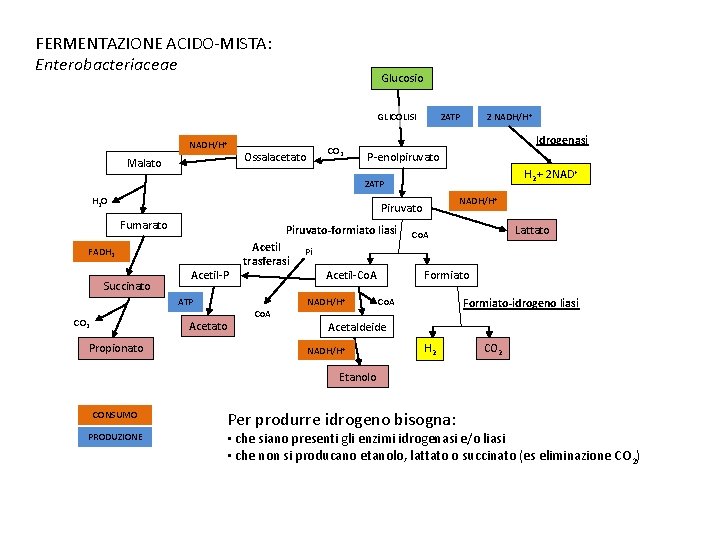
FERMENTAZIONE ACIDO-MISTA: Enterobacteriaceae Glucosio GLICOLISI NADH/H+ Malato CO 2 Ossalacetato 2 ATP 2 NADH/H+ Idrogenasi P-enolpiruvato H 2 + 2 NAD+ 2 ATP H 2 O NADH/H+ Piruvato Fumarato Piruvato-formiato liasi FADH 2 Succinato Acetil-P ATP CO 2 Acetato Propionato Acetil trasferasi Co. A Lattato Co. A Pi Acetil-Co. A NADH/H+ Formiato-idrogeno liasi Co. A Acetaldeide NADH/H+ H 2 CO 2 Etanolo CONSUMO PRODUZIONE Per produrre idrogeno bisogna: • che siano presenti gli enzimi idrogenasi e/o liasi • che non si producano etanolo, lattato o succinato (es eliminazione CO 2)
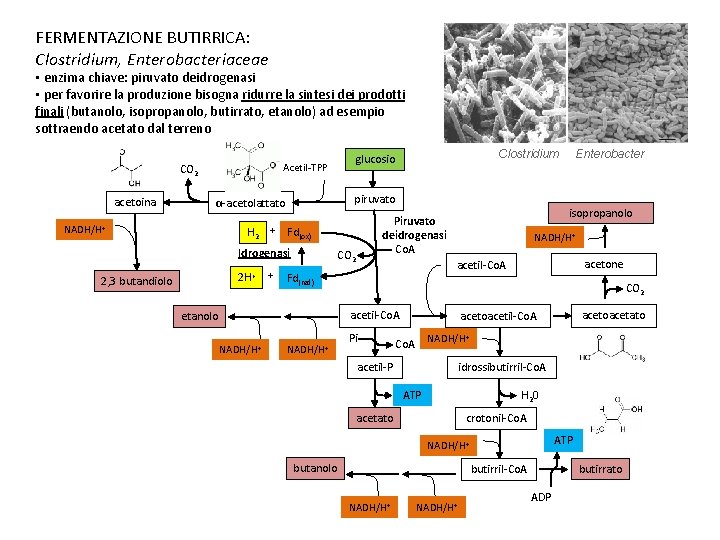
FERMENTAZIONE BUTIRRICA: Clostridium, Enterobacteriaceae • enzima chiave: piruvato deidrogenasi • per favorire la produzione bisogna ridurre la sintesi dei prodotti finali (butanolo, isopropanolo, butirrato, etanolo) ad esempio sottraendo acetato dal terreno CO 2 acetoina piruvato α-acetolattato Idrogenasi 2 H+ 2, 3 butandiolo + isopropanolo Piruvato deidrogenasi Co. A H 2 + Fd(ox) NADH/H+ Clostridium Enterobacter glucosio Acetil-TPP CO 2 NADH/H+ CO 2 acetil-Co. A etanolo NADH/H+ acetone acetil-Co. A Fd(red) Pi NADH/H+ Co. A acetil-P idrossibutirril-Co. A ATP H 20 acetato crotonil-Co. A ATP NADH/H+ butanolo butirrato butirril-Co. A NADH/H+ acetoacetato acetoacetil-Co. A NADH/H+ ADP

Processi fermentativi (dark fermentation) per produzione di idrogeno: • Mesofili o termofili • Colture pure o consorzi • Processi più avanzati utilizzano Clostridium sp (alte rese: 1. 6 -2. 4 mol/mol glucosio e alte produttività: 15 L/L reattore/h) • Fino a 100 volte più produttivo della foto-produzione (vedi dopo) • Uso di materiali di scarto industriale e/o inquinanti (lavorazione alimenti, scarti lignocellulosici, scarichi, fanghi) Sistema biologico Produttività (L/h) Coltura pura mesofila (Clostridium sp) 20 Consorzio mesofilo 60 -120 Coltura pura termofila 8 Consorzio termofilo 8
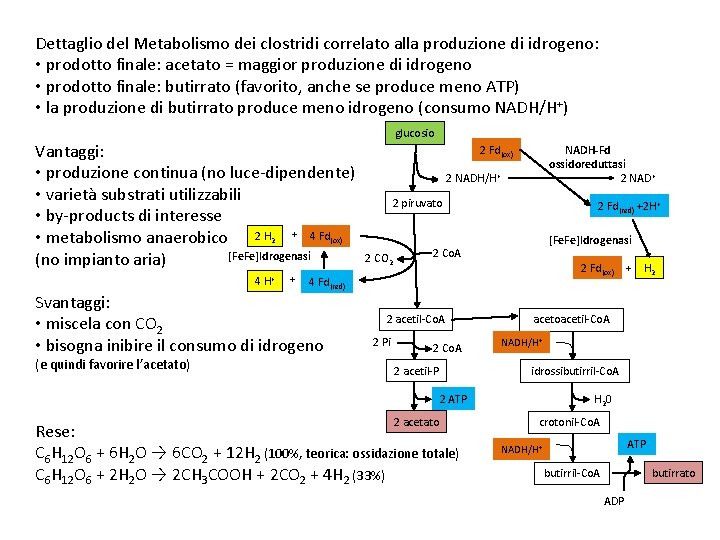
Dettaglio del Metabolismo dei clostridi correlato alla produzione di idrogeno: • prodotto finale: acetato = maggior produzione di idrogeno • prodotto finale: butirrato (favorito, anche se produce meno ATP) • la produzione di butirrato produce meno idrogeno (consumo NADH/H+) Vantaggi: • produzione continua (no luce-dipendente) • varietà substrati utilizzabili • by-products di interesse • metabolismo anaerobico 2 H 2 + 4 Fd(ox) [Fe. Fe]Idrogenasi (no impianto aria) 4 H+ + NADH-Fd ossidoreduttasi 2 NAD+ 2 Fd(ox) 2 NADH/H+ 2 piruvato 2 CO 2 2 Fd(red) +2 H+ [Fe. Fe]Idrogenasi 2 Co. A 2 Fd(ox) + H 2 4 Fd(red) Svantaggi: • miscela con CO 2 • bisogna inibire il consumo di idrogeno (e quindi favorire l’acetato) glucosio 2 acetil-Co. A 2 Pi 2 Co. A 2 acetil-P acetoacetil-Co. A NADH/H+ idrossibutirril-Co. A 2 ATP 2 acetato Rese: C 6 H 12 O 6 + 6 H 2 O → 6 CO 2 + 12 H 2 (100%, teorica: ossidazione totale) C 6 H 12 O 6 + 2 H 2 O → 2 CH 3 COOH + 2 CO 2 + 4 H 2 (33%) H 20 crotonil-Co. A ATP NADH/H+ butirrato butirril-Co. A ADP
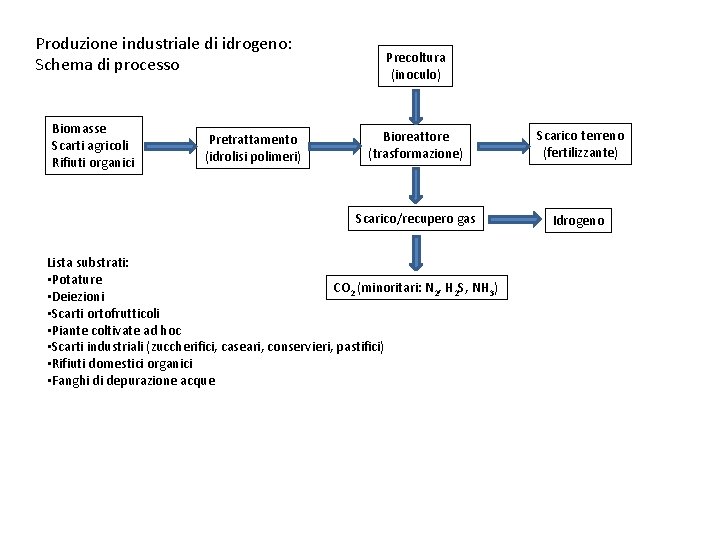
Produzione industriale di idrogeno: Schema di processo Biomasse Scarti agricoli Rifiuti organici Pretrattamento (idrolisi polimeri) Precoltura (inoculo) Bioreattore (trasformazione) Scarico terreno (fertilizzante) Scarico/recupero gas Idrogeno Lista substrati: • Potature CO 2 (minoritari: N 2, H 2 S, NH 3) • Deiezioni • Scarti ortofrutticoli • Piante coltivate ad hoc • Scarti industriali (zuccherifici, caseari, conservieri, pastifici) • Rifiuti domestici organici • Fanghi di depurazione acque

Fattori che influenzano il processo 1. 2. 3. 4. Microrganismi: capacità metabolica elevata (velocità catabolica) e attività idrogenasica elevata Consorzi microbici selezionati per il substrato: substrato eterogeneo = colture pure non sono ottimali Substrati polimerici: consorzio con microrganismi depolimerizzanti Aggiunta di microrganismi fermentanti selezionati (clostridi) ai consorzi 5. 6. 7. Natura del substrato: deve essere sufficientemente ridotto per fornire elettroni Substrati preferiti: carboidrati e polisaccaridi (glucosio nelle sperimentazioni di laboratorio) Importanza del Ferro (cofattore delle idrogenasi) 8. p. H: tra 5 e 7 9. 10. 11. 12. Pressione parziale di idrogeno (p. H 2): deve essere ridotta per favorire la produzione Rimozione del biogas durante la fermentazione Alte p. H 2 favoriscono la produzione di etanolo, lattato, butanolo (etc) a scapito di H 2 Sottrazione di CO 2 → riduzione del succinato (carbossilazione del PEP nelle enterobatteriacee) → potere riducente più disponibile 13. Sottrazione acidi grassi volatili → salvaguardia NAD(P)H/H+ → potere riducente più disponibile RCOOH → RCHO → RCH 2 OH 14. Sottrazione di CO (inibitore di Fe-idrogenasi) 15. Temperatura adeguata (mesofili e termofili)
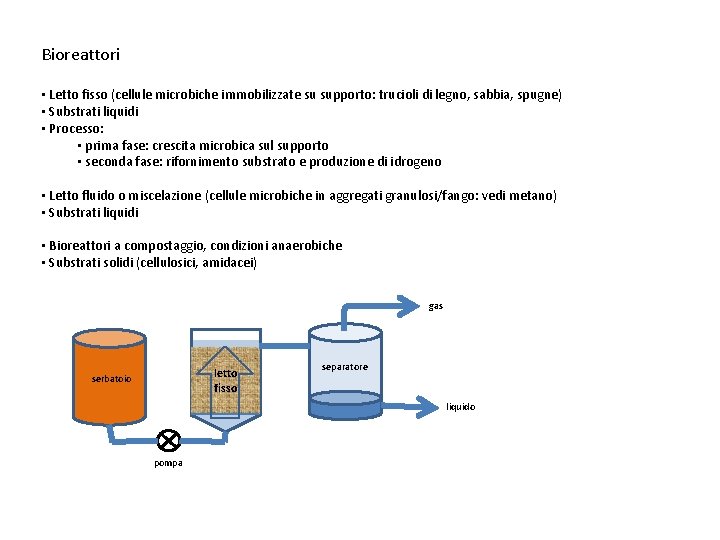
Bioreattori • Letto fisso (cellule microbiche immobilizzate su supporto: trucioli di legno, sabbia, spugne) • Substrati liquidi • Processo: • prima fase: crescita microbica sul supporto • seconda fase: rifornimento substrato e produzione di idrogeno • Letto fluido o miscelazione (cellule microbiche in aggregati granulosi/fango: vedi metano) • Substrati liquidi • Bioreattori a compostaggio, condizioni anaerobiche • Substrati solidi (cellulosici, amidacei) gas letto fisso serbatoio separatore liquido pompa

Miglioramento della produzione Manipolazione genetica dei microrganismi produttori: 1. Introduzione/miglioramento di enzimi litici per polimeri organici (chitina, cellulosa, emicellulosa, lignina etc) → uso diretto dei substrati 2. Sovraespressione/sovradosaggio dei geni per idrogenasi Conversione degli impianti di produzione anaerobica del metano: il metano viene prodotto per riduzione della CO 2: CO 2 + 4 H 2 → CH 4 + H 2 O Si può produrre idrogeno disaccoppiando la riduzione della CO 2, sottraendo gas (CO 2, H 2) dal reattore

Fotoproduzione di idrogeno • Produzione di idrogeno da microrganismi fotosintetici dimostrata fin dagli anni 40 • Produzione da eucarioti (alghe) e procarioti • Decomposizione dell’acqua a idrogeno e ossigeno senza produzione di gas serra: 2 H 2 O + hν → 2 H 2 + O 2 (ΔG=+237 k. J/mol) • Reazione fortemente endoergonica, velocità di produzione lenta • Gli enzimi produttori di idrogeno sono: 1. Idrogenasi classiche 2. Idrogenasi unidirezionali 3. Nitrogenasi Gli elettroni attivati dalla luce vengono trasferiti alla ferredoxina. Da qui si può avere: • La produzione diretta di idrogeno tramite idrogenasi [Fe-Fe] (alghe) o nitrogenasi (cianobatteri) e tramite idrogenasi [Ni-Fe] NADH/H+ dipendente (cianobatteri). • La produzione indiretta, dove il potere riducente passa attraverso la sintesi di carboidrati (ciclo di Calvin) e successiva ossidazione. In questo caso si sfrutta l’attività nitrogenasica e la capacità di fissare azoto (alghe e cianobatteri).

Fotoproduzione di idrogeno Gli enzimi produttori di idrogeno sono: 1. Idrogenasi classiche 2. Idrogenasi unidirezionali 3. Nitrogenasi Tutti enzimi sensibili a O 2 (>0, 1%): si ha produzione solo in ambiente anaerobico 1 – Idrogenasi classiche: • Enzimi reversibili • K 2 = 5 -6 K 1 • Metalli: Nickel e Ferro • Reazione: H+ + e- k 1 k 2 1/2 H 2 H+ 2 – Idrogenasi unidirezionali: • Lavorano principalmente nella riduzione di accettori di elettroni • Non producono idrogeno ma lo ossidano • Metalli: Nickel e Ferro • Reazione: 1/2 H 2 + NAD+ → [H+ + e- ] → NADH/H+ 3 – Nitrogenasi: • Enzimi coinvolti nella fissazione dell’azoto (riduzione di azoto ad ammoniaca) • In mancanza di azoto si ha la riduzione dei protoni ad idrogeno • Processo ad elevata richiesta energetica (ATP) • Reazione: N 2 + 8 H+ + 8 e- + 16 ATP → 2 NH 3 + H 2 + 16 ADP + 16 Pi + e- k 1 k 2 1/2 H 2

Fotosintesi ossigenica e produzione di idrogeno (microalghe, eucarioti) • Il sistema FOTOSINTETICO produce energia e potere riducente per l’organicazione della CO 2 (ciclo di Calvin) • In condizioni particolari si può ottenere idrogeno: • Direttamente (simultanea produzione di ossigeno) • Indirettamente (produzione di ossigeno disaccoppiata nello spazio o nel tempo)
![CO 2 ciclo di Calvin [CH 2 O]n NAD(P)+ hν PSII P 680+ + CO 2 ciclo di Calvin [CH 2 O]n NAD(P)+ hν PSII P 680+ +](http://slidetodoc.com/presentation_image_h/81a4b002b99fc25f7d6fabddb57bcea0/image-21.jpg)
CO 2 ciclo di Calvin [CH 2 O]n NAD(P)+ hν PSII P 680+ + e. OEC 2 H+ + ½O 2 H 2 O ox red F Co. Q PQ cyt. B 6 -F red ox periplasma PSII = Photo System II; OEC = Oxygen Evolving Complex; LHC = Light Harvesting protein Complex (contiene clorifille e carotenoidi: cattura fotoni e li trasferisce a P 680); P 680 = Pigmento fotoreattivo a 680 nm (centro di reazione, contiene due coppie - PD 1 e PD 2 - di clorofille); F = Feofitina (clorofilla a senza Mg); Co. Q = Coenzima Q o ubichinone (derivato del benzochinone); PQ = Plastochinone (derivato del benzochinone); FNR H 2 citoplasma ox LHC → P 680 HYD Ru. BP NAD(P)H/H+ NDH NADP+ 2 H+ hν ox ox ox red Fd LHC → NADPH/H+ P 700 e- P 700+ PSI ATP ADP PC red cyt. B 6 -F = Complesso [Fe-S] di citocromi b 6 ed f e altre sei subunità); PC = Plastocianina (proteina Cu+/Cu 2+); riduce P 700+ PSI = Photo System I; P 700 = Pigmento fotoreattivo a 700 nm (contiene clorofilla a); Fd = Ferredoxina (proteina [Fe-S]); HYD = idrogenasi; FNR = Fd/NADP ossido-reduttasi; NDH = NAD deidrogenasi
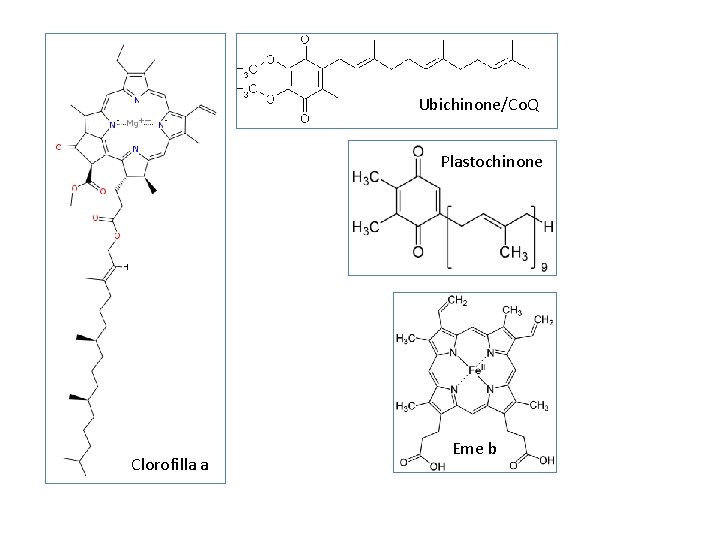
Ubichinone/Co. Q Plastochinone Clorofilla a Eme b
![Produzione di idrogeno da Chlamydomonas reinhardtii • Microalga con idrogenasi reversibile classe [Fe. Fe] Produzione di idrogeno da Chlamydomonas reinhardtii • Microalga con idrogenasi reversibile classe [Fe. Fe]](http://slidetodoc.com/presentation_image_h/81a4b002b99fc25f7d6fabddb57bcea0/image-23.jpg)
Produzione di idrogeno da Chlamydomonas reinhardtii • Microalga con idrogenasi reversibile classe [Fe. Fe] • Biofotolisi diretta dell’acqua • Studi pioneristici di produzione di idrogeno • Indirizzamento elettroni verso la riduzione dei protoni (IDROGENASI) piuttosto che Ciclo di Calvin (OSSIDOREDUTTASI FNR) • Necessaria la sottrazione dell’ossigeno prodotto (sotto i livelli inibitori) • Processo a due fasi: 1. Fase al buio anaerobica → sintesi di idrogenasi 2. Fase alla luce → produzione di idrogeno • La fase 2 viene rapidamente sopraffatta dall’assimilazione di CO 2 (Calvin) e produzione di O 2 (inibizione idrogenasi): necessario quindi reiterare il ciclo • Miglioramento del processo lavorando sull’attività di PSII per ridurre lo svolgimento dell’ossigeno: La riduzione dei composti solforati nel terreno porta all’inibizione progressiva di PSII → riduzione di ossigeno → stato di anaerobiosi alla luce → produzione sostenuta di idrogeno
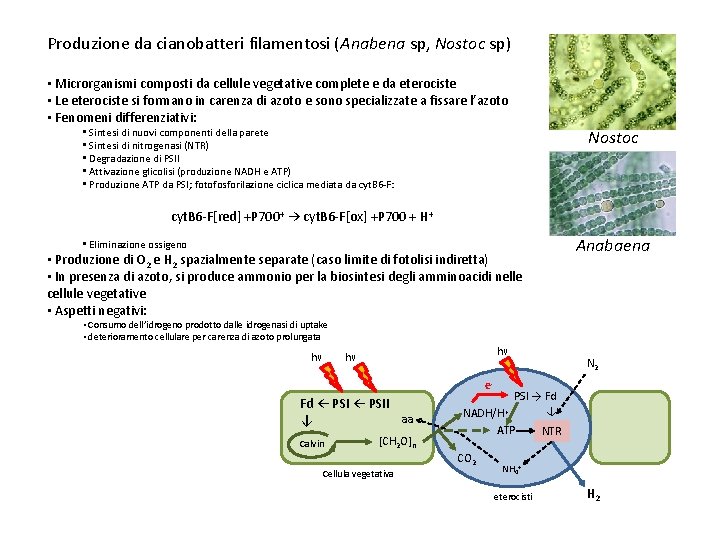
Produzione da cianobatteri filamentosi (Anabena sp, Nostoc sp) • Microrganismi composti da cellule vegetative complete e da eterociste • Le eterociste si formano in carenza di azoto e sono specializzate a fissare l’azoto • Fenomeni differenziativi: • Sintesi di nuovi componenti della parete • Sintesi di nitrogenasi (NTR) • Degradazione di PSII • Attivazione glicolisi (produzione NADH e ATP) • Produzione ATP da PSI; fotofosforilazione ciclica mediata da cyt. B 6 -F: Nostoc cyt. B 6 -F[red] +P 700+ → cyt. B 6 -F[ox] +P 700 + H+ Anabaena • Eliminazione ossigeno • Produzione di O 2 e H 2 spazialmente separate (caso limite di fotolisi indiretta) • In presenza di azoto, si produce ammonio per la biosintesi degli amminoacidi nelle cellule vegetative • Aspetti negativi: • Consumo dell’idrogeno prodotto dalle idrogenasi di uptake • deterioramento cellulare per carenza di azoto prolungata hν hν hν e- Fd ← PSII aa ↓ Calvin NADH/H+ PSI → Fd ↓ ATP [CH 2 O]n CO 2 Cellula vegetativa N 2 NTR NH 4+ eterocisti H 2
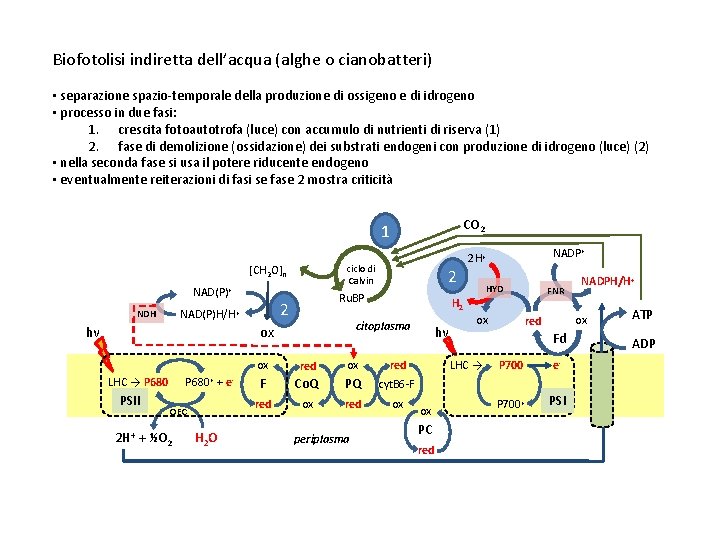
Biofotolisi indiretta dell’acqua (alghe o cianobatteri) • separazione spazio-temporale della produzione di ossigeno e di idrogeno • processo in due fasi: 1. crescita fotoautotrofa (luce) con accumulo di nutrienti di riserva (1) 2. fase di demolizione (ossidazione) dei substrati endogeni con produzione di idrogeno (luce) (2) • nella seconda fase si usa il potere riducente endogeno • eventualmente reiterazioni di fasi se fase 2 mostra criticità CO 2 1 ciclo di Calvin [CH 2 O]n NAD(P)+ NDH hν Ru. BP 2 NAD(P)H/H+ PSII P 680+ + e. OEC 2 H+ + ½O 2 H 2 O ox red F Co. Q PQ cyt. B 6 -F red ox periplasma HYD FNR H 2 citoplasma ox LHC → P 680 2 NADP+ 2 H+ hν ox ox PC red ox red Fd LHC → NADPH/H+ P 700 e- P 700+ PSI ATP ADP
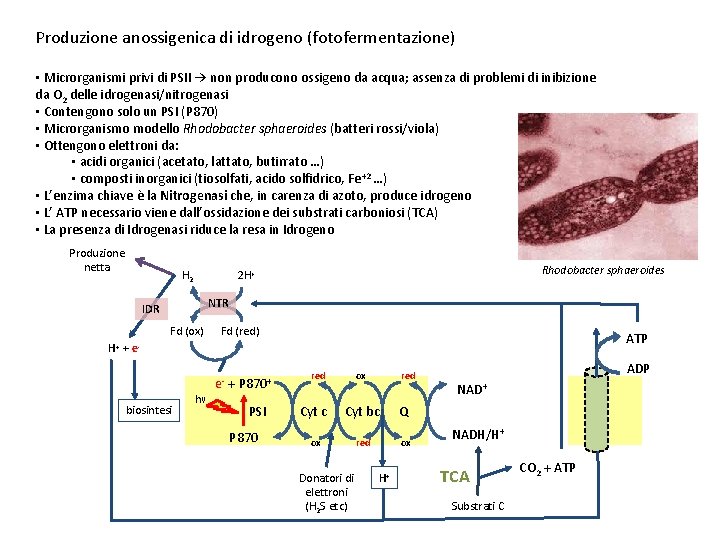
Produzione anossigenica di idrogeno (fotofermentazione) • Microrganismi privi di PSII → non producono ossigeno da acqua; assenza di problemi di inibizione da O 2 delle idrogenasi/nitrogenasi • Contengono solo un PSI (P 870) • Microrganismo modello Rhodobacter sphaeroides (batteri rossi/viola) • Ottengono elettroni da: • acidi organici (acetato, lattato, butirrato …) • composti inorganici (tiosolfati, acido solfidrico, Fe+2 …) • L’enzima chiave è la Nitrogenasi che, in carenza di azoto, produce idrogeno • L’ ATP necessario viene dall’ossidazione dei substrati carboniosi (TCA) • La presenza di Idrogenasi riduce la resa in Idrogeno Produzione netta H 2 Rhodobacter sphaeroides 2 H+ NTR IDR Fd (ox) Fd (red) ATP H+ + e- biosintesi hν e- + P 870+ PSI P 870 red ox red Cyt c Cyt bc Q ox red ox Donatori di elettroni (H 2 S etc) H+ ADP NAD+ NADH/H+ TCA Substrati C CO 2 + ATP

Microrganismi fotosintetici produttori di idrogeno Microalghe verdi: • Eucarioti fotoautotrofi (usano CO 2 e due fotosistemi PSI e PSII) • Contengono clorofilla a e b • Hanno solo Idrogenasi • Esempio: Chlamydomonas reinhardtii Cianobatteri: • Procarioti fotoautotrofi azotofissatori • Ampia diversità ecofisiologica, biochimica e morfologica • Contengono cloroifilla a, carotenoidi e ficobiliproteine (esempio ficocianina) • Possono contenere sia nitrogenasi che idrogenasi (reversibili e di uptake) • Esempio: batteri eterocistati • Eterociste: cellule prive di PSII, assenza di ossigeno svolto (naturalmente anaerobico), nitrogenasi attiva Batteri rossi non-sulfurei: • Procarioti fotoeterotrofi (non usano CO 2) • Morfologicamente eterogenei • Fotositema singolo incapace di scindere l’acqua ma capace di produrre ATP (donatori di elettroni organici) • Contengono batterioclorofille a e b, carotenoidi • Contengono nitrogenasi e idrogenasi (reversibili e di uptake) • Esempio Rhodobacter sphaeroides
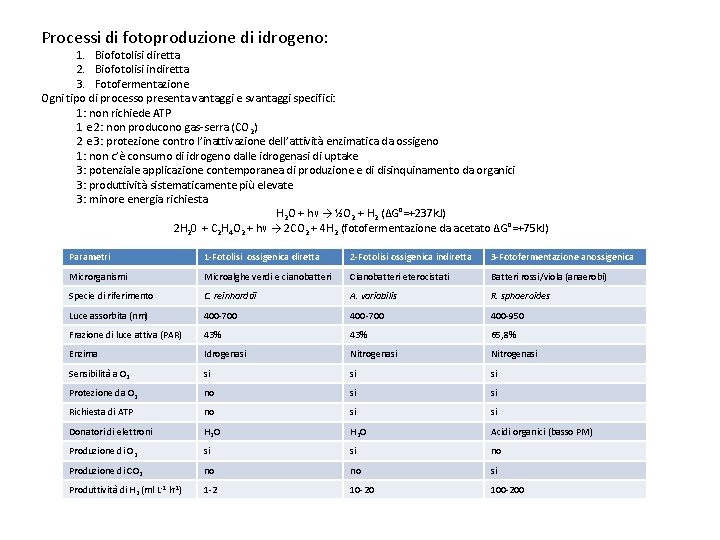
Processi di fotoproduzione di idrogeno: 1. Biofotolisi diretta 2. Biofotolisi indiretta 3. Fotofermentazione Ogni tipo di processo presenta vantaggi e svantaggi specifici: 1: non richiede ATP 1 e 2: non producono gas-serra (CO 2) 2 e 3: protezione contro l’inattivazione dell’attività enzimatica da ossigeno 1: non c’è consumo di idrogeno dalle idrogenasi di uptake 3: potenziale applicazione contemporanea di produzione e di disinquinamento da organici 3: produttività sistematicamente più elevate 3: minore energia richiesta H 2 O + hν → ½O 2 + H 2 (ΔG°=+237 k. J) 2 H 20 + C 2 H 4 O 2 + hν → 2 CO 2 + 4 H 2 (fotofermentazione da acetato ΔG°=+75 k. J) Parametri 1 -Fotolisi ossigenica diretta 2 -Fotolisi ossigenica indiretta 3 -Fotofermentazione anossigenica Microrganismi Microalghe verdi e cianobatteri Cianobatteri eterocistati Batteri rossi/viola (anaerobi) Specie di riferimento C. reinhardtii A. variabilis R. sphaeroides Luce assorbita (nm) 400 -700 400 -950 Frazione di luce attiva (PAR) 43% 65, 8% Enzima Idrogenasi Nitrogenasi Sensibilità a O 2 si si si Protezione da O 2 no si si Richiesta di ATP no si si Donatori di elettroni H 2 O Acidi organici (basso PM) Produzione di O 2 si si no Produzione di CO 2 no no si Produttività di H 2 (ml L-1 h-1) 1 -2 10 -20 100 -200

Finora solo produzioni su scale di laboratorio Problemi: • Mancanza di un sistema ottimale su cui puntare • Alta efficienza di conversione (luce→H 2) solo a basse intensità luminose (laboratorio) • Alta intensità luminosa (luce solare) → basse efficienze dei fotosistemi → basse efficienze di conversione: 0, 04 -0, 2% (fotosintesi ossigenica) e 0, 3 -0, 5% (fotofermentazione, escluso contributo dell’energia chimica) • Le rese in H 2 sono sensibilmente più basse delle rese in biomassa (conversione luce → biomassa) che raggiungono il 4%
- Slides: 29