Processamento de Materiais Reviso sobre ligao qumica Classificao

Processamento de Materiais Revisão sobre ligação química Classificação dos Materiais Aplicações de materiais biomédicos Mestrado em Engenharia Biomédica
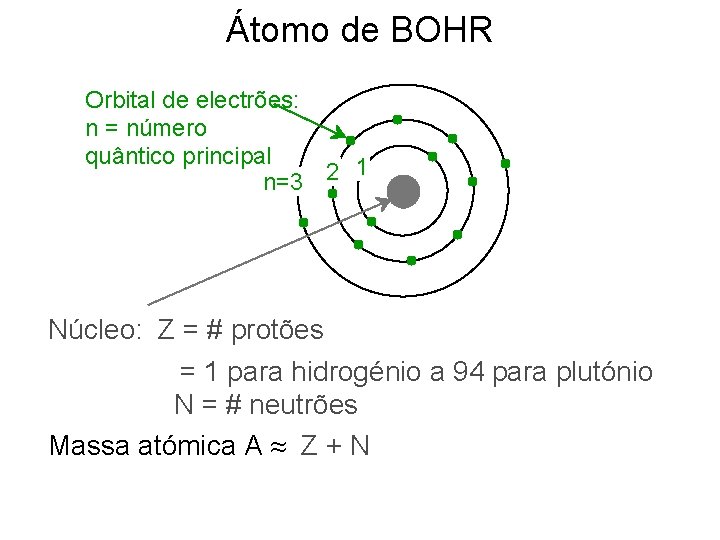
Átomo de BOHR Orbital de electrões: n = número quântico principal 1 2 n=3 Núcleo: Z = # protões = 1 para hidrogénio a 94 para plutónio N = # neutrões Massa atómica A ≈ Z + N

Átomo de BOHR Mprotão = Mneutrão = 1. 66 x 10 -24 g = 1 amu = atomic mass unit (unidade de massa atómica) Num grama teremos 1 g / 1. 66 x 10 -24 g = 6. 023 x 1023 amu NA= Número de Avogadro Melectrão = 0. 911 x 10 -27 g Mprotão = 1822 Meletrão praticamente toda a massa do átomo está no núcleo.

Exercício Comparar o número de areais que existem nas praias portuguesas com o número de átomos na cabeça de um alfinete (Fe) Dados: Costa portuguesa ~1000 km Largura das praias ~0, 2 km Profundidade de areia ~50 m Forma do grão de areia ~ cubo de 1 mm de lado Cabeça de um alfinete ~ esfera de 1 mm de raio Densidade do Fe ~ 8 gr/cm 3 Massa atómica do Fe ~ 56 u. m. a Resultado: Existem cerca de 40 x mais átomos que areias
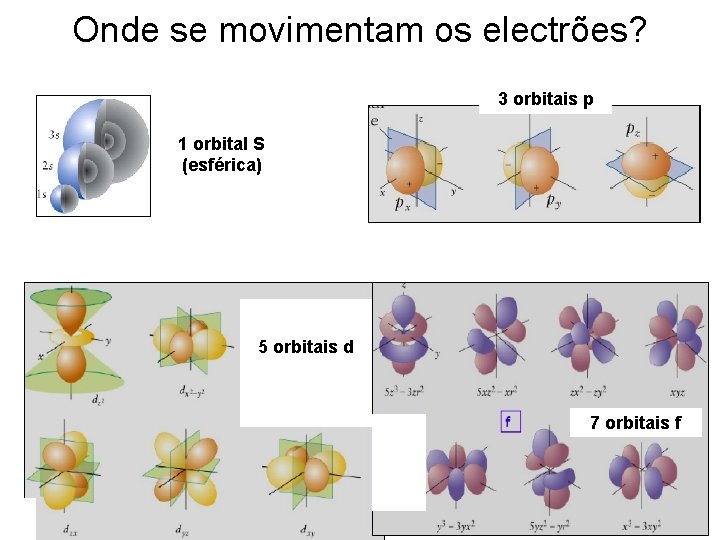
Onde se movimentam os electrões? 3 orbitais p 1 orbital S (esférica) 5 orbitais d 7 orbitais f
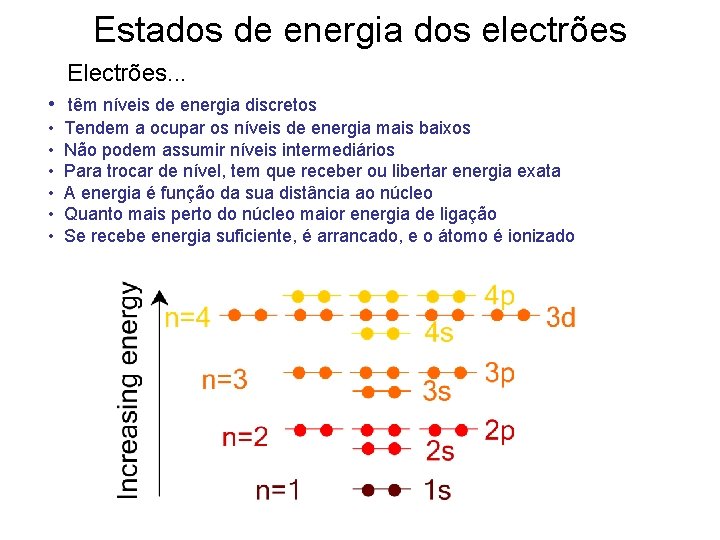
Estados de energia dos electrões Electrões. . . • têm níveis de energia discretos • • • Tendem a ocupar os níveis de energia mais baixos Não podem assumir níveis intermediários Para trocar de nível, tem que receber ou libertar energia exata A energia é função da sua distância ao núcleo Quanto mais perto do núcleo maior energia de ligação Se recebe energia suficiente, é arrancado, e o átomo é ionizado
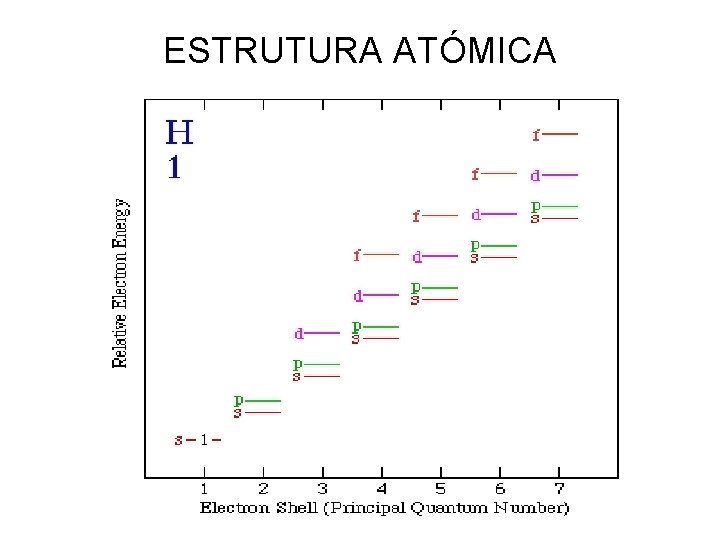
ESTRUTURA ATÓMICA

Configurações estáveis • ter as subcamadas s e p completas • tendem a ser não reactivos. Z Elemento 2 He 10 18 Ne Ar 36 Kr Configuração 1 s 2 2 s 2 2 p 6 3 s 2 3 p 6 3 d 10 4 s 2 4 p 6

Exemplos de elementos • A maioria dos elementos: Não têm configurações electrónicas estáveis • Valência - camada exterior não está completamente preenchida

TABELA PERIÓDICA • Colunas: Estrutura de Valência similar Elementos electropositivos: Fácilmente fornecem electrões para se tornarem iões +. Elementos electronegativos: Fácilmente recebem electrões para se tornarem iões -.
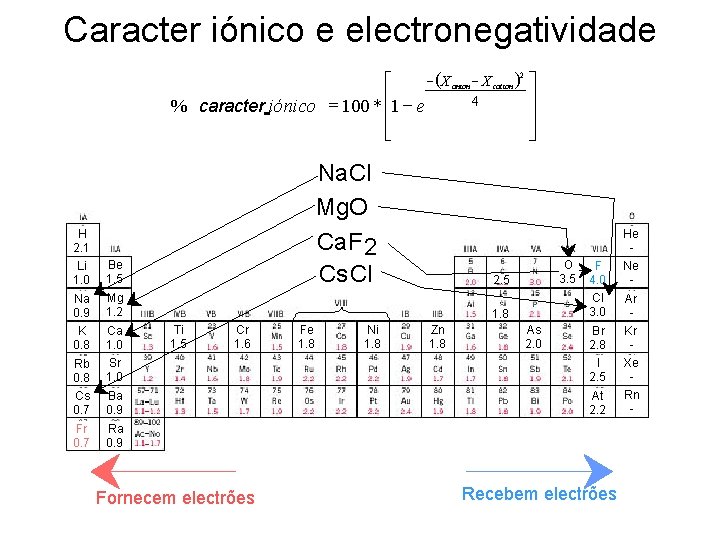
Caracter iónico e electronegatividade - (X anion - X cation )2 ù é 4 ú % caracter iónico = 100 * ê 1 - e ê ú ë û H 2. 1 Li 1. 0 Na 0. 9 K 0. 8 Rb 0. 8 Cs 0. 7 Fr 0. 7 Na. Cl Mg. O Ca. F 2 Cs. Cl Be 1. 5 2. 5 Mg 1. 2 Ca 1. 0 Sr 1. 0 1. 8 Ti 1. 5 Cr 1. 6 Fe 1. 8 Ni 1. 8 Zn 1. 8 As 2. 0 Ba 0. 9 Ra 0. 9 O 3. 5 F 4. 0 Cl 3. 0 Br 2. 8 I 2. 5 At 2. 2 ELECTRONEGATIVIDADE Fornecem electrões Recebem electrões He Ne Ar Kr Xe Rn -

Processamento de Materiais LIGAÇÃO QUIMICA Mestrado em Engenharia Biomédica
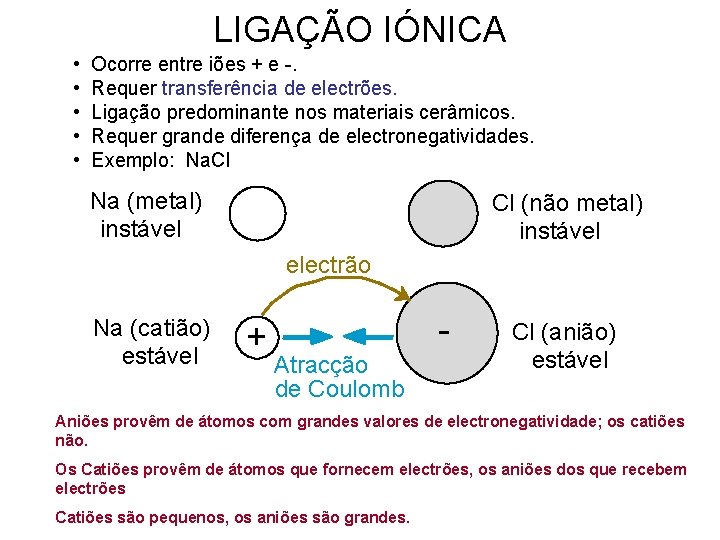
LIGAÇÃO IÓNICA • • • Ocorre entre iões + e -. Requer transferência de electrões. Ligação predominante nos materiais cerâmicos. Requer grande diferença de electronegatividades. Exemplo: Na. Cl Na (metal) instável Cl (não metal) instável electrão Na (catião) estável + Atracção de Coulomb Cl (anião) estável Aniões provêm de átomos com grandes valores de electronegatividade; os catiões não. Os Catiões provêm de átomos que fornecem electrões, os aniões dos que recebem electrões Catiões são pequenos, os aniões são grandes.
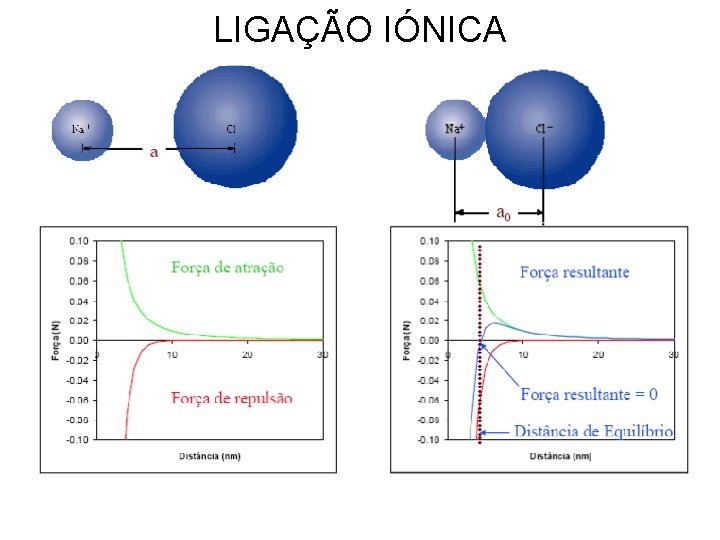
LIGAÇÃO IÓNICA

LIGAÇÃO IÓNICA Z 1 e Z 2 – Número de electrões recebidos ou transferidos e – carga do electrão r – distância internuclear A, B, n - constantes
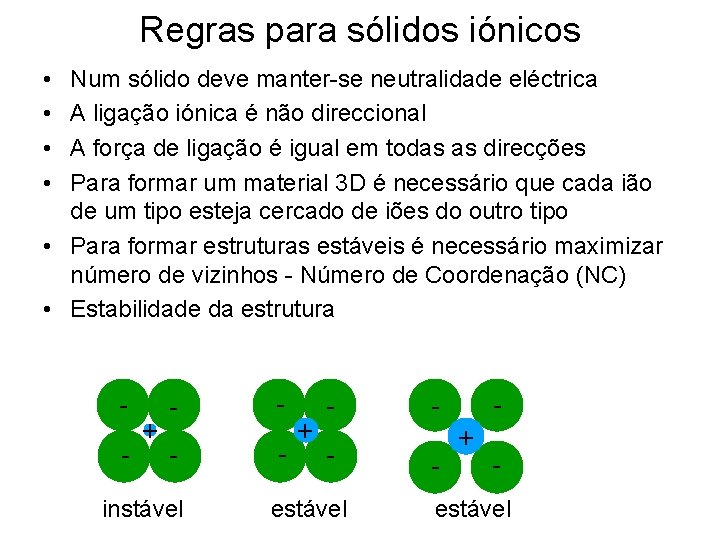
Regras para sólidos iónicos • • Num sólido deve manter-se neutralidade eléctrica A ligação iónica é não direccional A força de ligação é igual em todas as direcções Para formar um material 3 D é necessário que cada ião de um tipo esteja cercado de iões do outro tipo • Para formar estruturas estáveis é necessário maximizar número de vizinhos - Número de Coordenação (NC) • Estabilidade da estrutura - + - - instável + - estável - - + - estável
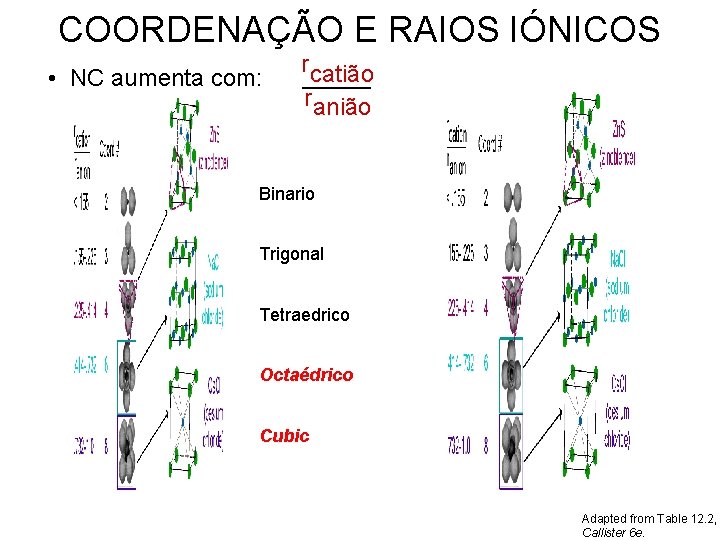
COORDENAÇÃO E RAIOS IÓNICOS • NC aumenta com: r catião r anião Binario Trigonal Tetraedrico Octaédrico Cubic Adapted from Table 12. 2, Callister 6 e.
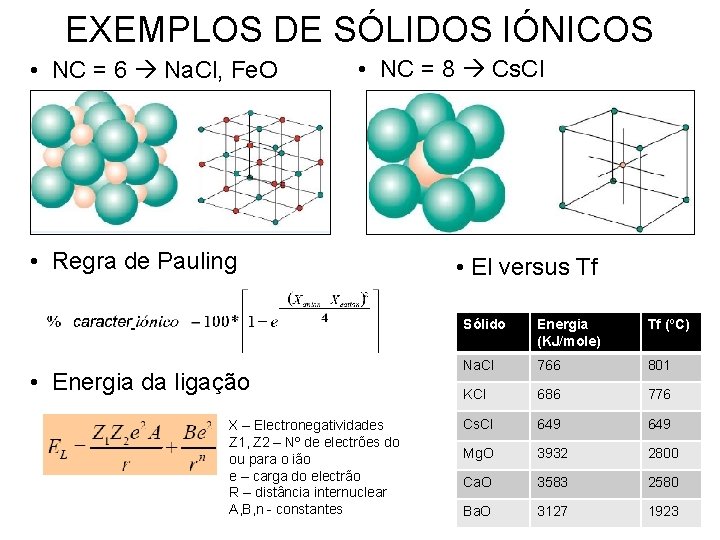
EXEMPLOS DE SÓLIDOS IÓNICOS • NC = 6 Na. Cl, Fe. O • NC = 8 Cs. Cl • Regra de Pauling • Energia da ligação X – Electronegatividades Z 1, Z 2 – Nº de electrões do ou para o ião e – carga do electrão R – distância internuclear A, B, n - constantes • El versus Tf Sólido Energia (KJ/mole) Tf (ºC) Na. Cl 766 801 KCl 686 776 Cs. Cl 649 Mg. O 3932 2800 Ca. O 3583 2580 Ba. O 3127 1923
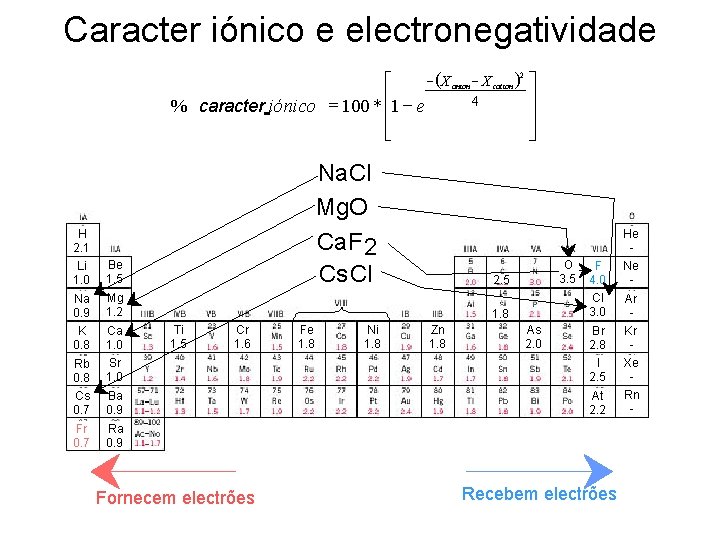
Caracter iónico e electronegatividade - (X anion - X cation )2 ù é 4 ú % caracter iónico = 100 * ê 1 - e ê ú ë û H 2. 1 Li 1. 0 Na 0. 9 K 0. 8 Rb 0. 8 Cs 0. 7 Fr 0. 7 Na. Cl Mg. O Ca. F 2 Cs. Cl Be 1. 5 2. 5 Mg 1. 2 Ca 1. 0 Sr 1. 0 1. 8 Ti 1. 5 Cr 1. 6 Fe 1. 8 Ni 1. 8 Zn 1. 8 As 2. 0 Ba 0. 9 Ra 0. 9 O 3. 5 F 4. 0 Cl 3. 0 Br 2. 8 I 2. 5 At 2. 2 ELECTRONEGATIVIDADE Fornecem electrões Recebem electrões He Ne Ar Kr Xe Rn -
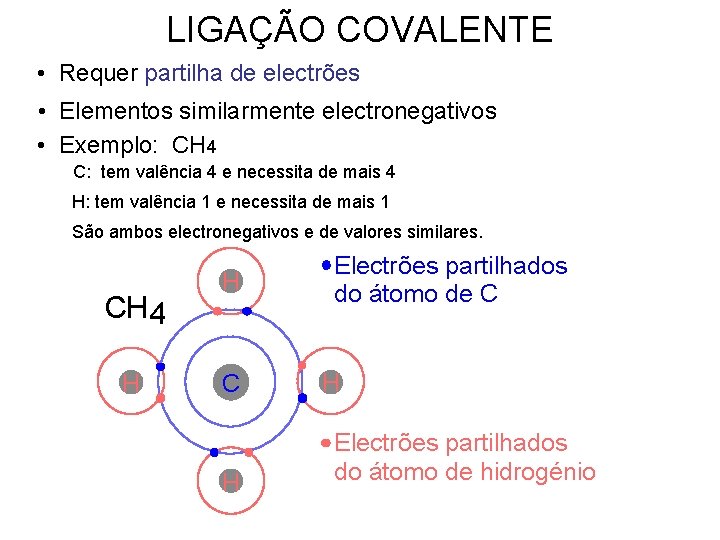
LIGAÇÃO COVALENTE • Requer partilha de electrões • Elementos similarmente electronegativos • Exemplo: CH 4 C: tem valência 4 e necessita de mais 4 H: tem valência 1 e necessita de mais 1 São ambos electronegativos e de valores similares. CH 4 H H C H Electrões partilhados do átomo de hidrogénio
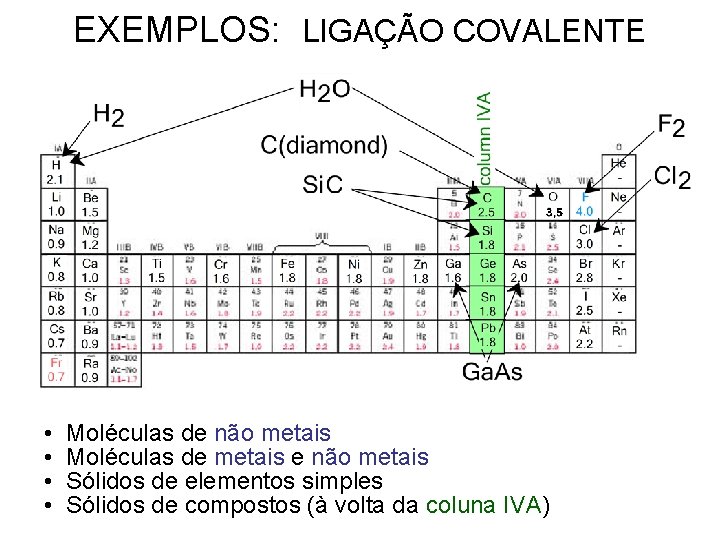
EXEMPLOS: LIGAÇÃO COVALENTE • • Moléculas de não metais Moléculas de metais e não metais Sólidos de elementos simples Sólidos de compostos (à volta da coluna IVA)
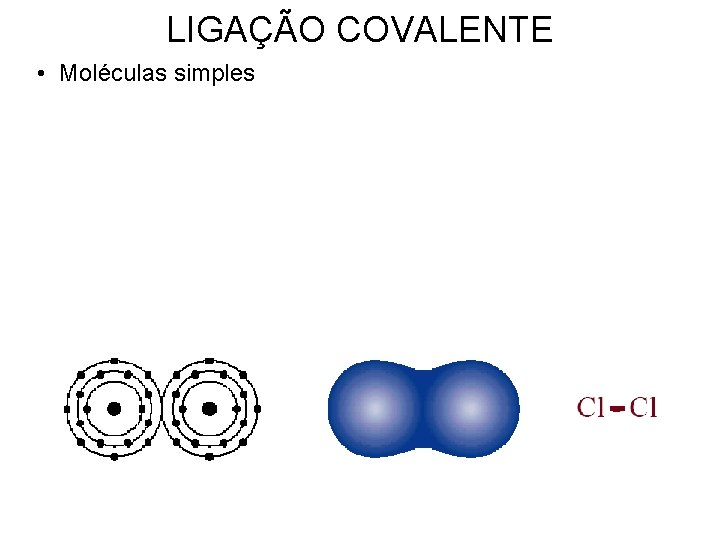
LIGAÇÃO COVALENTE • Moléculas simples
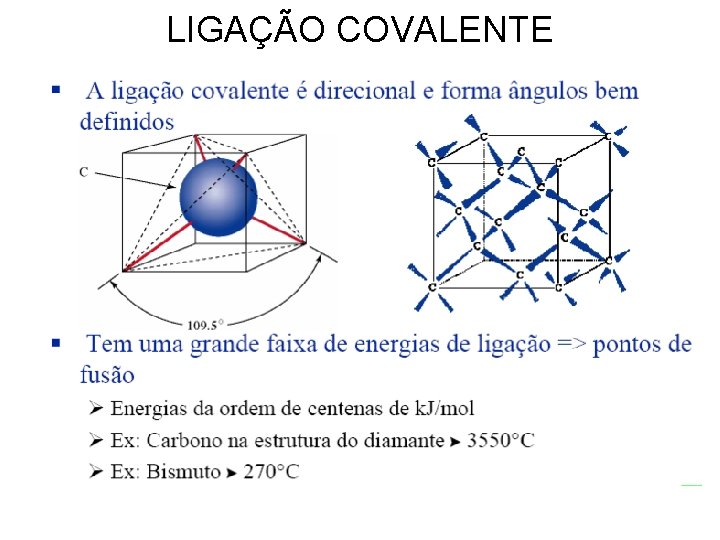
LIGAÇÃO COVALENTE

LIGAÇÃO COVALENTE

LIGAÇÃO METÁLICA - A ligação metálica ocorre entre elementos electropositivos, que fácilmente perdem um electrão - Pode ser imaginada como um aglomerado de iões positivos rodeados por uma nuvem de electrões - Os electrões não ligados especificamente a um determinado átomo são “livres”, electrões de condução. - Estes electrões são partilhados por todos os átomos em geral, formando uma nuvem eletrónica, responsável pela elevada condutividade eléctrica e térmica destes materiais. - A ligação metálica não é direccional, semelhante à ligação Iónica, podendo os iões serem empilhados sem restrições de posição. - As energias de ligação são também da ordem de centenas de k. J/mol.

LIGAÇÃO METÁLICA

LIGAÇÃO SECUNDÁRIA - É possível obter ligação sem troca ou partilha de electrões nas denominada ligações secundárias ou de van der Waals. - A ligação é gerada por pequenas assimetrias na distribuição de cargas nos átomos, que criam dipolos. -Um dipolo é um par de cargas opostas que mantém uma distância entre si. 1. Dipolo permanente 2. Dipolo induzido
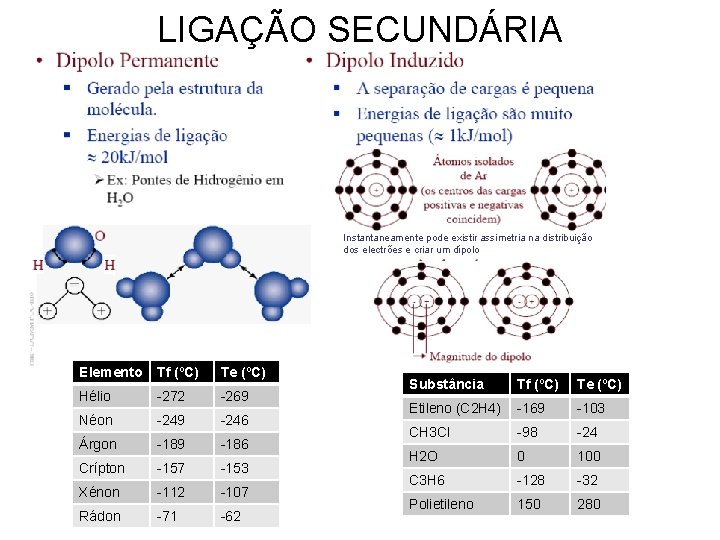
LIGAÇÃO SECUNDÁRIA Instantaneamente pode existir assimetria na distribuição dos electrões e criar um dípolo Elemento Tf (ºC) Te (ºC) Hélio -272 -269 Néon -249 -246 Árgon -189 -186 Crípton -157 -153 Xénon -112 -107 Rádon -71 -62 Substância Tf (ºC) Te (ºC) Etileno (C 2 H 4) -169 -103 CH 3 Cl -98 -24 H 2 O 0 100 C 3 H 6 -128 -32 Polietileno 150 280

LIGAÇÃO SECUNDÁRIA

Exercício Em relação a cada um dos compostos seguintes, indique qual é o tipo de ligação predominante: -Ni -Zr. O 2 -Grafite -Kr sólido -Si -BN -Si. C -Fe 2 O 3 -Mg. O -W -H 2 O na molécula -H 2 O – entre as moléculas
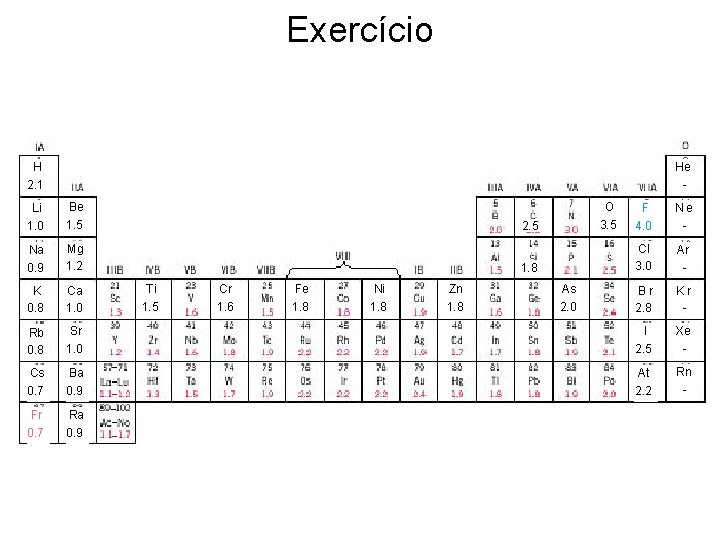
Exercício H 2. 1 He - Li 1. 0 Be 1. 5 Na 0. 9 Mg 1. 2 K 0. 8 Ca 1. 0 Rb 0. 8 O 3. 5 F 4. 0 Ne - Cl 3. 0 Ar - Br 2. 8 Kr - Sr 1. 0 I 2. 5 Xe - Cs 0. 7 Ba 0. 9 At 2. 2 Rn - Fr 0. 7 Ra 0. 9 2. 5 1. 8 Ti 1. 5 Cr 1. 6 Fe 1. 8 Ni 1. 8 Zn 1. 8 ELECTRONEGATIVIDADE As 2. 0
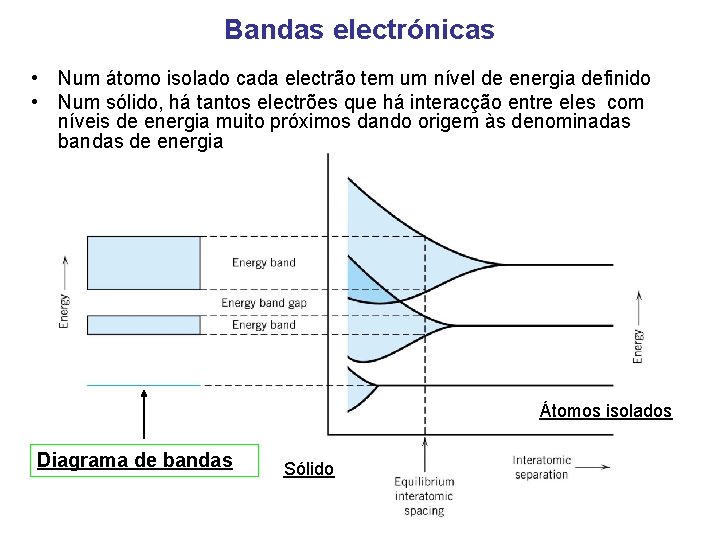
Bandas electrónicas • Num átomo isolado cada electrão tem um nível de energia definido • Num sólido, há tantos electrões que há interacção entre eles com níveis de energia muito próximos dando origem às denominadas bandas de energia Átomos isolados Diagrama de bandas Sólido
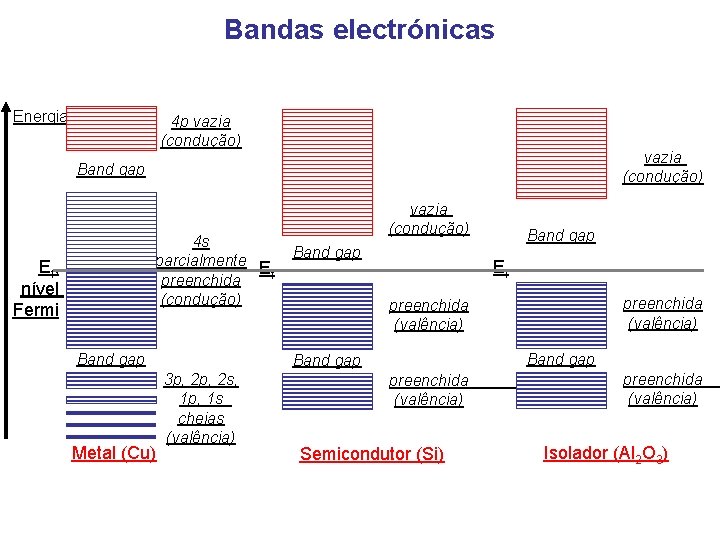
Bandas electrónicas Energia 4 p vazia (condução) Band gap 4 s parcialmente E f preenchida (condução) Ef, nível Fermi Band gap Metal (Cu) vazia (condução) Band gap Ef preenchida (valência) Band gap 3 p, 2 s, 1 p, 1 s cheias (valência) Band gap preenchida (valência) Semicondutor (Si) preenchida (valência) Isolador (Al 2 O 3)

Processamento de Materiais CLASSIFICAÇÃO DOS MATERIAIS Mestrado em Engenharia Biomédica

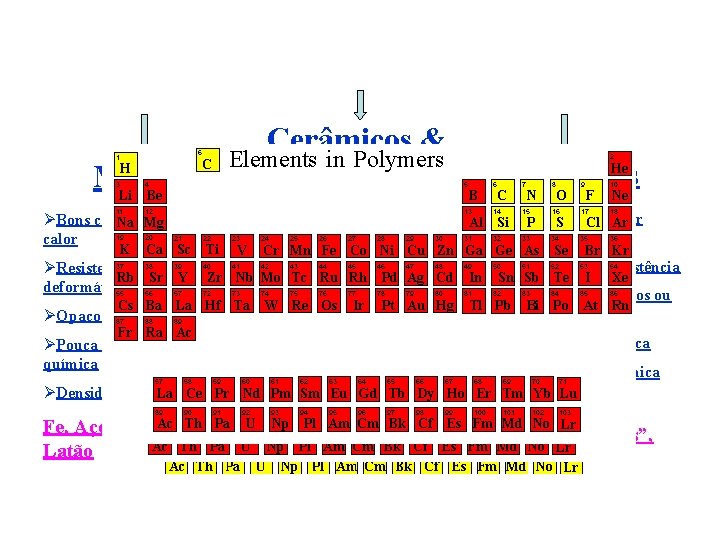
Metais ØBons condutores de e- e calor ØResistentes e deformáveis ØOpacos ØPouca resistência química ØDensidade elevada Fe, Aço, Cu, Al, Latão Cerâmicos & Vidros Polimeros ØIsoladores de e- e calor ØDuros, frágeis e não deformáveis ØFlexíveis, facilmente deformáveis, baixa resistência ØMuitos são translúcidos ou transparentes ØBoa resistência química ØBoa resistência térmica ØBaixa resistência térmica Si. C, Si 3 N 4, Al 2 O 3, Ba. Ti. O 3, ØBaixa densidade YBCO Supercondutores Todos os “plásticos”, Nylon, Borracha

Compósitos Materiais de Engenharia que combinam as melhores propriedades dos Metais, Cerãmicos e polímeros (ex. PRFV, PRFC, WC+Co São muitas vezes considerados na classificação anterior Semi-Condutores Propriedades entre condutor e isolante que podem ser modificadas com a adição de elementos dopantes, tais como, Si, Ga. As Materiais Inteligentes Ligas de memória de forma (Ni. Ti), ligas com efeito piezoeléctrico (PZT) Materiais Avançados Magnéticos, LCDs, fibras ópticas, filmes finos, materiais nanoestruturados …

Processamento de Materiais APLICAÇÃO DE MATERIAIS BIOMÉDICOS Mestrado em Engenharia Biomédica
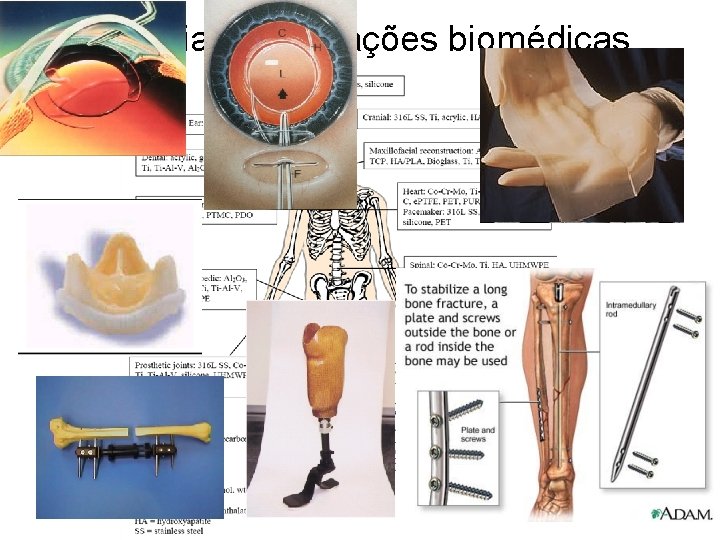
Materias e aplicações biomédicas

Materias e aplicações biomédicas Metais e ligas – Reparação do esqueleto : - Osteosintese (fixação interna de fracturas) - Próteses de articulações (anca, joelho…) - Cirurgia vertebral – Próteses e implantes dentários. - Stents Polímeros – Fios de sutura – Vasos artificiais, – Lentes de contacto, córnea artificial. Cerâmicos – Próteses de articulações – Revestimentos de implantes metálicos – Reparação do esqueleto – Ouvido interno – Próteses oculares: “Olho de vidro". Hidrogéis – Encapsulação : - Células - Medicamentos.
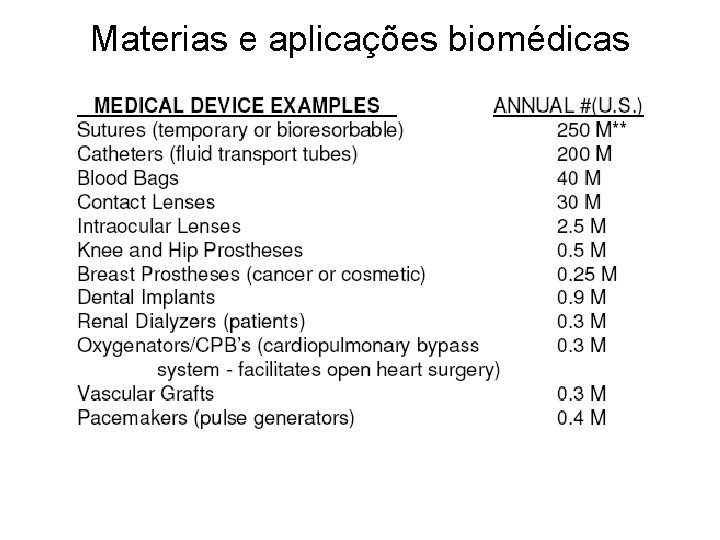
Materias e aplicações biomédicas
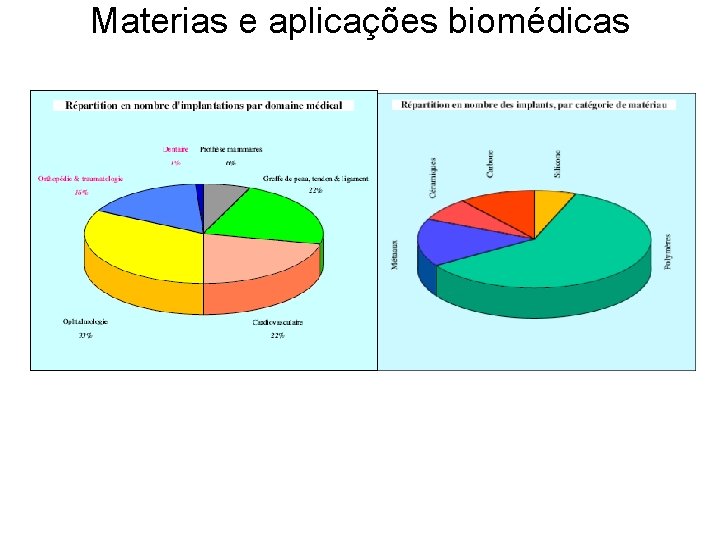
Materias e aplicações biomédicas

Desenvolvimentos relacionados com biomateriais: Ano 1790 -1810 1860 -1870 1886 1893 -1912 Investigadores Desenvolvimento Fe, Au, Ag, and Pt metal devices for fracture fixation J. Lister Aseptic surgical techniques H. Hansmann Ni-plated steel bone fracture plate W. A. Lane Steel screws and plates (Lane fracture plate) W. D. Sherman Vanadium steel plates – lower stress concentration and corrosion (Sherman Plate) 1924 A. A. Zierold Introduced Stellites (Co-Cr-Mo alloys) 1926 M. Z. Lange Introduced 18 -8 s. Mo SS (better than standard 18 -8 SS) 1926 E. W. Hey-Goves Used carpenter’s screws for femoral neck fracture 1931 M. N. Sith-Petersen First femoral neck fracture device made of SS 1936 C. S. Venable, W. G. Stuck Introduced Vitallium (19 -9 SS) – became Co-Cr alloys 1938 P. Wiles First total hip replacement prosthesis 1939 J. C. Burch, H. M. Carney Introduced tantalum (Ta) 1946 J. Judet, R. Judet First biomechanically designed femoral head replacement; first plastics (PMMA) used in joint replacement 1940 s M. J. Dorzee, A. Franceschetti First used acrylics (PMMA) for corneal replacement 1947 J. Cotton Introduced Titanium and its alloys 1952 A. B. Voorhees, A. Jaretzta, A. B. Blackmore First successful blood vessel replacement made of cloth for tissue in-growth 1958 S. Furman, G. Robinson First successful direct heart stimulation 1958 J. Charnley First use of acrylic bone cement in total hip replacement on the advice of Dr. D. Smith 1960 A. Starr, M. L. Edwards First commercial heart valves 1970 W. J. Kolff Total heart replacement
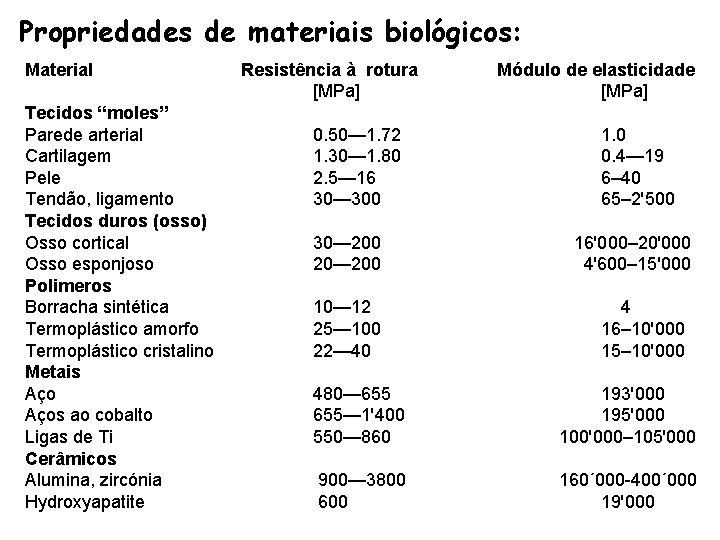
Propriedades de materiais biológicos: Material Tecidos “moles” Parede arterial Cartilagem Pele Tendão, ligamento Tecidos duros (osso) Osso cortical Osso esponjoso Polimeros Borracha sintética Termoplástico amorfo Termoplástico cristalino Metais Aços ao cobalto Ligas de Ti Cerâmicos Alumina, zircónia Hydroxyapatite Resistência à rotura [MPa] 0. 50— 1. 72 1. 30— 1. 80 2. 5— 16 30— 300 30— 200 20— 200 10— 12 25— 100 22— 40 Módulo de elasticidade [MPa] 1. 0 0. 4— 19 6– 40 65– 2'500 16'000– 20'000 4'600– 15'000 4 16– 10'000 15– 10'000 480— 655— 1'400 550— 860 193'000 195'000 100'000– 105'000 900— 3800 600 160´ 000 -400´ 000 19'000
- Slides: 44