PROCEDIMIENTO PARA CALCULAR LA MOLARIDAD DE UNA DISOLUCIN






- Slides: 8

PROCEDIMIENTO PARA CALCULAR LA MOLARIDAD DE UNA DISOLUCIÓN Profechore Masterisco Rosao

¿Qué es la Molaridad? • Debido a que muchos de los fenómenos químicos tienen que ver con la concentración de un soluto en un disolvente, es decir la cantidad de masa o materia de una sustancia disuelta en un disolvente, es necesario calcularla correctamente, para lo cuál necesitamos aplicar su relación mediante la siguiente fórmula:

Fórmula de la Molaridad • • M= -----------Litros de disolución • • El No. De Moles, que es la cantidad de masa, se obtiene aplicando la ecuación Base del mol • El volúmen de la disolución es necesario tenerlo siempre en litros. No. de Moles

Ejemplo práctico • ¿Cuál será la concentración molar de una disolución que contiene 2. 0 g de HCl contenidos en 250 ml de disolución?

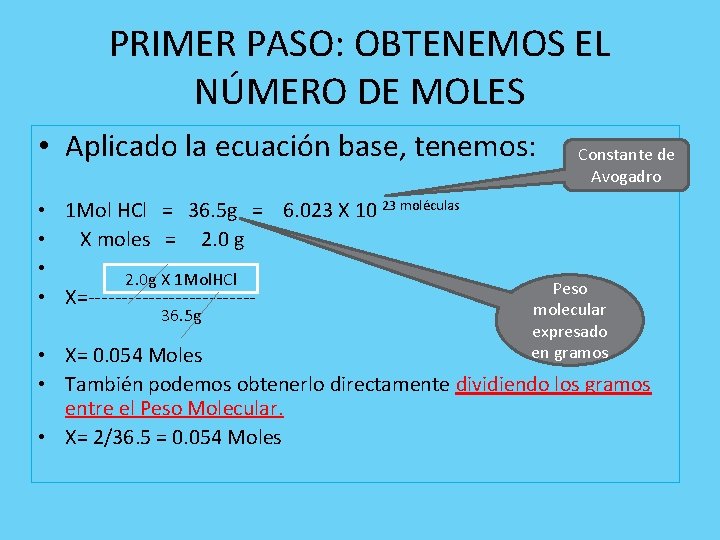
PRIMER PASO: OBTENEMOS EL NÚMERO DE MOLES • Aplicado la ecuación base, tenemos: • 1 Mol HCl = 36. 5 g = 6. 023 X 10 23 moléculas • X moles = 2. 0 g • 2. 0 g X 1 Mol. HCl • X=------------36. 5 g Constante de Avogadro Peso molecular expresado en gramos • X= 0. 054 Moles • También podemos obtenerlo directamente dividiendo los gramos entre el Peso Molecular. • X= 2/36. 5 = 0. 054 Moles

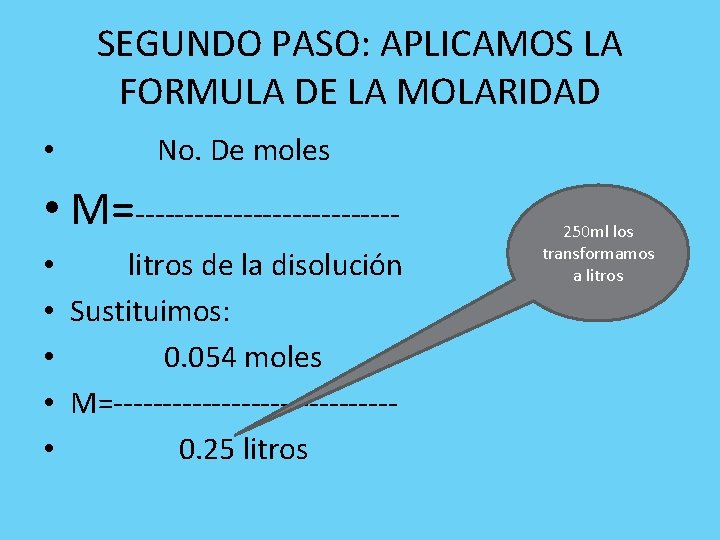
SEGUNDO PASO: APLICAMOS LA FORMULA DE LA MOLARIDAD • No. De moles • M=------------- • litros de la disolución • Sustituimos: • 0. 054 moles • M=-------------- • 0. 25 litros 250 ml los transformamos a litros

TERCER PASO: OBTENEMOS EL RESULTADO • 0. 054 moles • M=--------------- = 0. 216 moles/litro • 0. 25 litros • Por tanto, la concentración molar de ésta solución problema es de 0. 216 moles/litro

Anexo. -¿Cómo transformamos ml a litros? • Para hacer transformaciones basta solo aplicar REGLAS DE TRES SENCILLAS y ya lo tenemos: veamos… • Si 1000 ml = 1 litro • Entonces 250 ml = X • 250 ml x 1 litro • X=------------- = 0. 25 ml • 1000 ml • Es igual si le recorres el punto decimal 3 lugares a la izquierda de la cantidad dada.