Problmes de chimie Cours de sciences de 4

Problèmes de chimie Cours de sciences de 4 ième par C. Hovelaque Création de la mascotte : S. Christiaens (6 G)
Exercice 1 Exercice 2 Exercice 3 Exercice 4 Exercice 5 Exercice 6 Exercice 7 Exercice 8 Exercice 9 Exercice 10

Combien de moles d’aluminium (Al) sont nécessaire pour fabriquer 10 moles de sulfure d’aluminium (Al 2 S 3)? 2 Al Données + demandes ? mol Lect. molaire 2 mol Réponses en moles 5 mol Phrase + 3 S Al 2 S 3 10 mol 3 mol 10 mol 5 moles d’Al sont nécessaire à la fabrication de 10 moles de Al 2 S 3 Clique n’importe où pour obtenir la correction. Clique ici pour retourner au sommaire des exercices

L’acide chlorhydrique est fabriqué à partir de H 2 et Cl 2. Combien de moles de H 2 et de Cl 2 sont nécessaires à la fabrication de 15 moles de HCl? H 2 + Cl 2 2 HCl Données + demandes ? mol Lect. molaire 1 mol 2 mol Réponses en moles 7, 5 mol 15 mol Phrase ? mol 15 mol Il faut 7, 5 mol de H 2 et 7, 5 mol de Cl 2 pour fabriquer 15 mol de HCl Clique n’importe où pour obtenir la correction. Clique ici pour retourner au sommaire des exercices

Combien de moles de SO 2 obtient-on quand on fait réagir dans des conditions NTP 127, 8 litres de O 2 avec suffisamment de sulfure de fer 11 O 2 + 4 Fe. S 2 Données + demandes 127, 8 l Données en moles 5, 7 (127, 8/22, 4) Lect. molaire 11 mol Réponses en moles 5, 7 Phrase 2 Fe 2 O 3 + 8 SO 2 ? mol 4 mol 2 mol 8 mol 4, 15 (8/11 x 5, 7) On obtient 4, 15 mol de SO 2à partir de 127, 8 litres de O 2 Clique n’importe où pour obtenir la correction. Clique ici pour retourner au sommaire des exercices

Quel volume de CO 2 (CNTP)est libéré par la combustion de 100 g de méthane? CH 4 Données + demandes 100 g Données en moles 6, 25 Lect. molaire 1 mol Réponses en moles 6, 25 Réponses + 2 O 2 CO 2 + 2 H 2 O ? l 2 mol 1 mol 2 mol 6, 25 140 l (unités demandées) Phrase 140 litres de CO 2 seront libérés par la combustion de 100 g de méthane. Clique n’importe où pour obtenir la correction. Clique ici pour retourner au sommaire des exercices
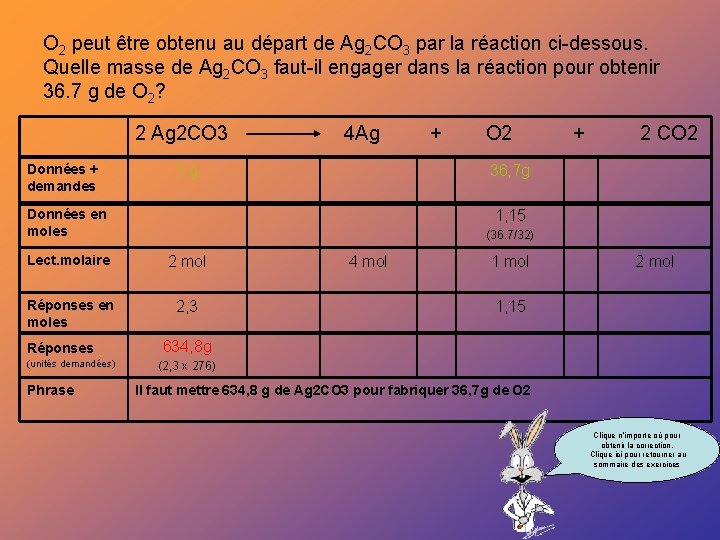
O 2 peut être obtenu au départ de Ag 2 CO 3 par la réaction ci-dessous. Quelle masse de Ag 2 CO 3 faut-il engager dans la réaction pour obtenir 36. 7 g de O 2? 2 Ag 2 CO 3 Données + demandes 4 Ag ? g 2 CO 2 (36. 7/32) 2 mol Réponses en moles 2, 3 Phrase + 1, 15 Lect. molaire (unités demandées) O 2 36, 7 g Données en moles Réponses + 4 mol 1 mol 2 mol 1, 15 634, 8 g (2, 3 x 276) Il faut mettre 634, 8 g de Ag 2 CO 3 pour fabriquer 36, 7 g de O 2 Clique n’importe où pour obtenir la correction. Clique ici pour retourner au sommaire des exercices
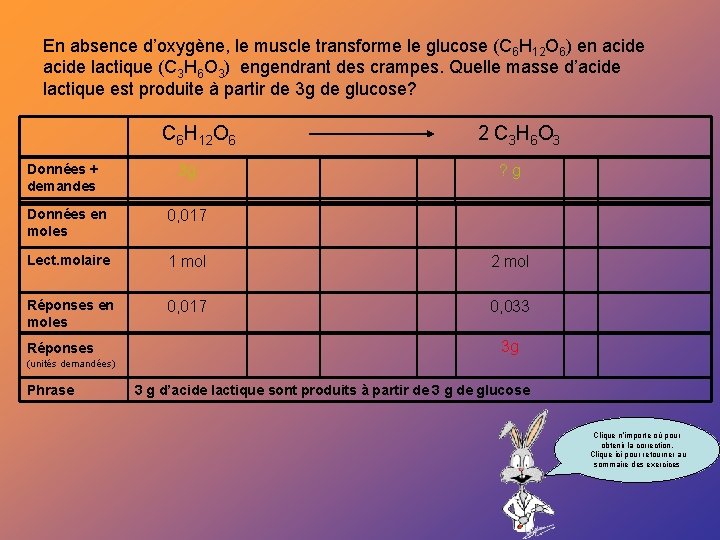
En absence d’oxygène, le muscle transforme le glucose (C 6 H 12 O 6) en acide lactique (C 3 H 6 O 3) engendrant des crampes. Quelle masse d’acide lactique est produite à partir de 3 g de glucose? C 6 H 12 O 6 2 C 3 H 6 O 3 Données + demandes 3 g Données en moles 0, 017 Lect. molaire 1 mol 2 mol Réponses en moles 0, 017 0, 033 Réponses ? g 3 g (unités demandées) Phrase 3 g d’acide lactique sont produits à partir de 3 g de glucose Clique n’importe où pour obtenir la correction. Clique ici pour retourner au sommaire des exercices
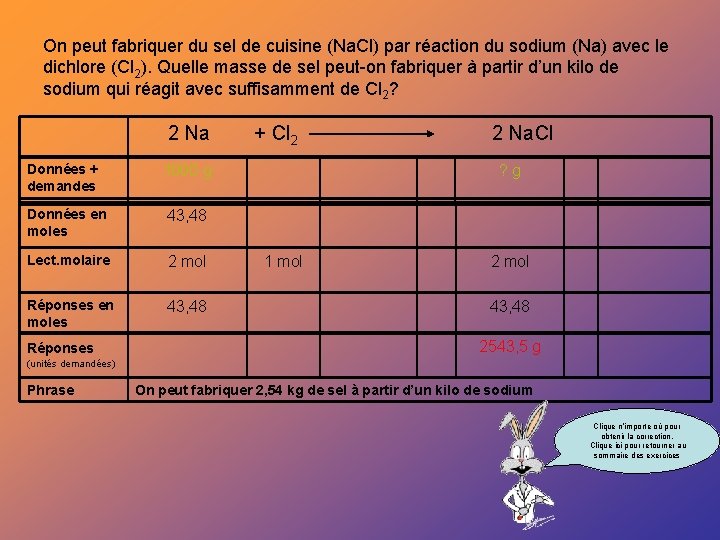
On peut fabriquer du sel de cuisine (Na. Cl) par réaction du sodium (Na) avec le dichlore (Cl 2). Quelle masse de sel peut-on fabriquer à partir d’un kilo de sodium qui réagit avec suffisamment de Cl 2? 2 Na Données + demandes 1000 g Données en moles 43, 48 Lect. molaire 2 mol Réponses en moles 43, 48 Réponses + Cl 2 2 Na. Cl ? g 1 mol 2 mol 43, 48 2543, 5 g (unités demandées) Phrase On peut fabriquer 2, 54 kg de sel à partir d’un kilo de sodium Clique n’importe où pour obtenir la correction. Clique ici pour retourner au sommaire des exercices

Quelle masse de soufre (S) obtient-on si on fait réagir 1, 2 litre de sulfure d’hydrogène (H 2 S) avec suffisamment de SO 2 (CNTP)? 2 H 2 S Données + demandes 1, 2 l Données en moles 0, 054 Lect. molaire 2 mol Réponses en moles 0, 054 Réponses + SO 2 3 S + 2 H 2 O ? g 1 mol 3 mol 2 mol 0, 08 2, 6 g (unités demandées) Phrase 2, 6 g de soufre seront fabriqués à partir de 1, 2 l de H 2 S Clique n’importe où pour obtenir la correction. Clique ici pour retourner au sommaire des exercices

Le fer (Fe) se fabrique dans les haut-fourneaux à partir de minerai (Fe 2 O 3) selon l’équation ci-dessous. Quelle masse de fer obtient-on à partir d’une tonne de minerai? Fe 2 O 3 + 3 CO Données + demandes 1000 g Données en moles 6250 Lect. molaire 1 mol Réponses en moles 6250 3 CO 2 + 2 Fe ? g 3 mol 2 mol 12500 700000 g Réponses (unités demandées) Phrase On obtient 700 kg de fer à partir d’une tonne de minerai Clique n’importe où pour obtenir la correction. Clique ici pour retourner au sommaire des exercices
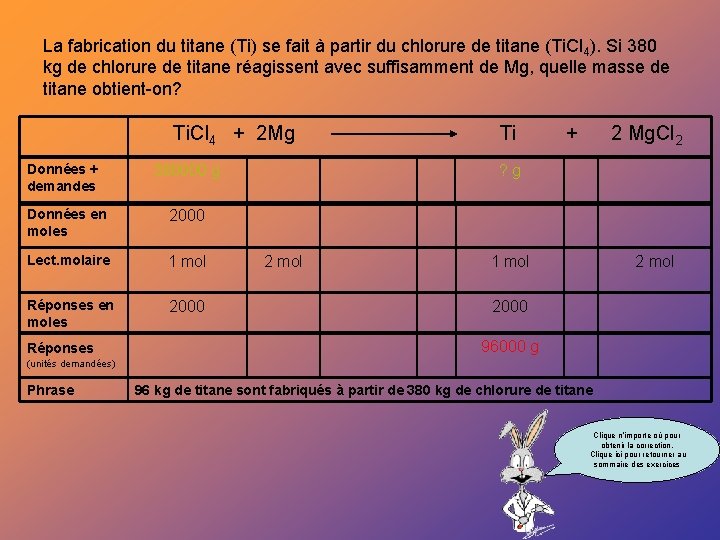
La fabrication du titane (Ti) se fait à partir du chlorure de titane (Ti. Cl 4). Si 380 kg de chlorure de titane réagissent avec suffisamment de Mg, quelle masse de titane obtient-on? Ti. Cl 4 + 2 Mg Données + demandes 380000 g Données en moles 2000 Lect. molaire 1 mol Réponses en moles 2000 Réponses Ti + 2 Mg. Cl 2 ? g 2 mol 1 mol 2000 96000 g (unités demandées) Phrase 96 kg de titane sont fabriqués à partir de 380 kg de chlorure de titane Clique n’importe où pour obtenir la correction. Clique ici pour retourner au sommaire des exercices
- Slides: 12