Problmatique Lutilisation excessive des colorants par certaines industries

Problématique? L’utilisation excessive des colorants par certaines industries génèrent une pollution importante en eaux résiduaires et cause un effet néfaste sur l’environnement: cas des colorants textiles de la région de la Soummam (persistance, pouvoir d’accumulation dans le milieu naturel, …). La valorisation et l’amélioration des performances des phosphates naturels Algériens dont le potentiel de réserves est considérable est devenue une nécessité absolue du fait de l’augmentation constante du taux de rejets qui restent à présent inexploités. 1

Objectifs? Les objectifs sont d’ordre scientifique, économique et environnemental : ØDéfinir une nouvelle approche d’exploitation et de valorisation du minerai de phosphate naturel en se basant sur ses propriétés de surface et d’interface, de façon à diversifier sa gamme de production. ØContribuer à la protection de l’environnement du fait de la toxicité des différents polluants contenus dans les eaux rejetées par les diverses industries de la région. 2
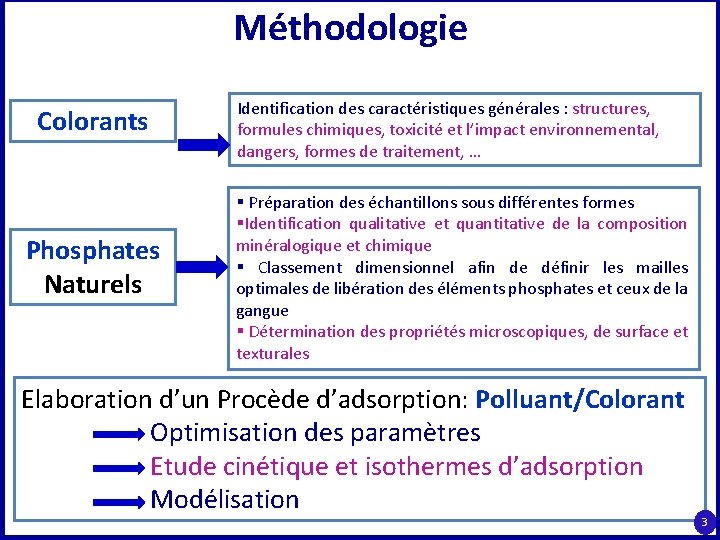
Méthodologie Colorants Phosphates Naturels Identification des caractéristiques générales : structures, formules chimiques, toxicité et l’impact environnemental, dangers, formes de traitement, … § Préparation des échantillons sous différentes formes §Identification qualitative et quantitative de la composition minéralogique et chimique § Classement dimensionnel afin de définir les mailles optimales de libération des éléments phosphates et ceux de la gangue § Détermination des propriétés microscopiques, de surface et texturales Elaboration d’un Procède d’adsorption: Polluant/Colorant Optimisation des paramètres Etude cinétique et isothermes d’adsorption Modélisation 3
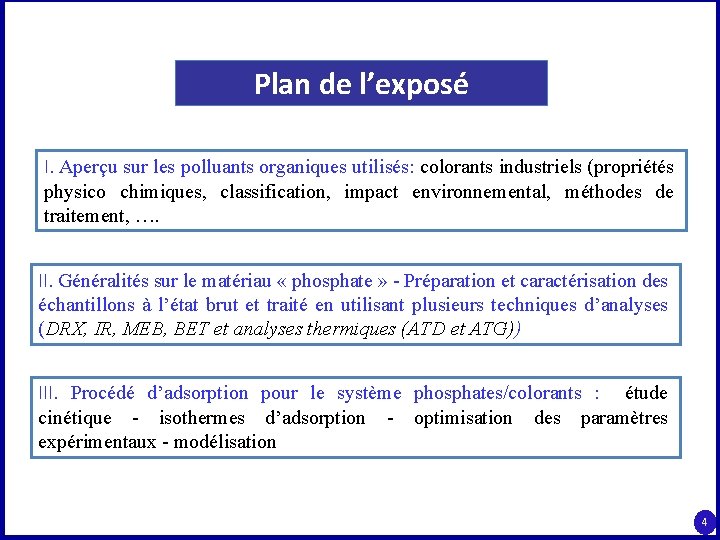
Plan de l’exposé I. Aperçu sur les polluants organiques utilisés: colorants industriels (propriétés physico chimiques, classification, impact environnemental, méthodes de traitement, …. II. Généralités sur le matériau « phosphate » - Préparation et caractérisation des échantillons à l’état brut et traité en utilisant plusieurs techniques d’analyses (DRX, IR, MEB, BET et analyses thermiques (ATD et ATG)) III. Procédé d’adsorption pour le système phosphates/colorants : étude cinétique - isothermes d’adsorption - optimisation des paramètres expérimentaux - modélisation 4
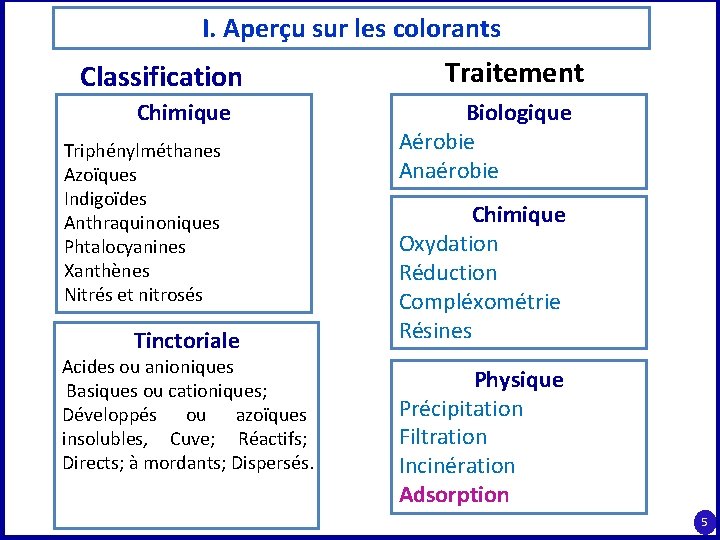
I. Aperçu sur les colorants Classification Chimique Triphénylméthanes Azoïques Indigoïdes Anthraquinoniques Phtalocyanines Xanthènes Nitrés et nitrosés Tinctoriale Acides ou anioniques Basiques ou cationiques; Développés ou azoïques insolubles, Cuve; Réactifs; Directs; à mordants; Dispersés. Traitement Biologique Aérobie Anaérobie Chimique Oxydation Réduction Compléxométrie Résines Physique Précipitation Filtration Incinération Adsorption 5
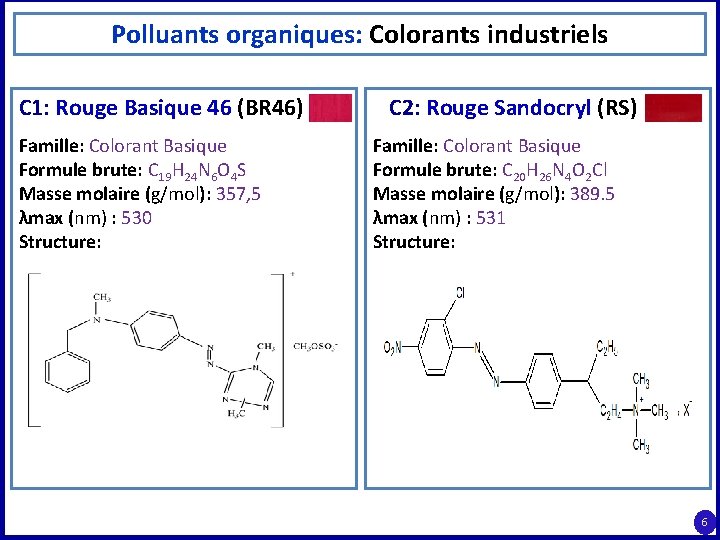
Polluants organiques: Colorants industriels C 1: Rouge Basique 46 (BR 46) Famille: Colorant Basique Formule brute: C 19 H 24 N 6 O 4 S Masse molaire (g/mol): 357, 5 λmax (nm) : 530 Structure: C 2: Rouge Sandocryl (RS) Famille: Colorant Basique Formule brute: C 20 H 26 N 4 O 2 Cl Masse molaire (g/mol): 389. 5 λmax (nm) : 531 Structure: 6
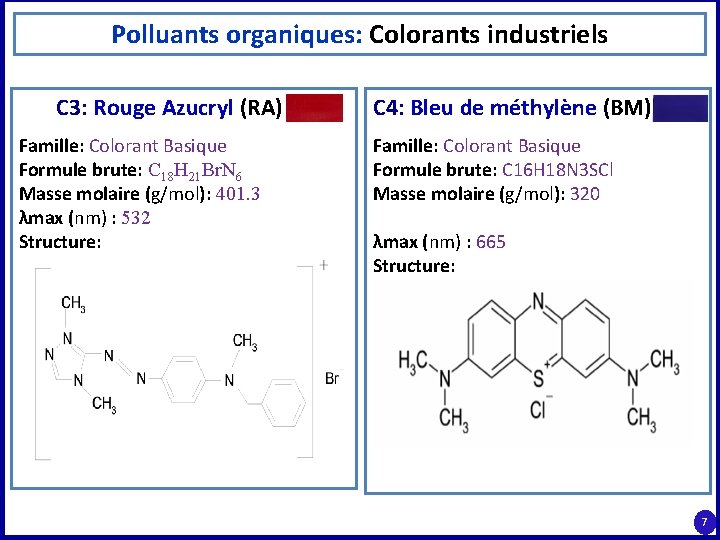
Polluants organiques: Colorants industriels C 3: Rouge Azucryl (RA) Famille: Colorant Basique Formule brute: C 18 H 21 Br. N 6 Masse molaire (g/mol): 401. 3 λmax (nm) : 532 Structure: C 4: Bleu de méthylène (BM) Famille: Colorant Basique Formule brute: C 16 H 18 N 3 SCl Masse molaire (g/mol): 320 λmax (nm) : 665 Structure: 7

II. Phosphates Naturels de Djebel Onk Réserves: 02 Milliards de tonnes avec un taux de production de 2 Millions de tonnes/an Phosphates de calcium: M 5 (XO 4)3 Y Apatite (Ca 5(PO 4)3 F, OH et Cl) Gangue: Dolomite, calcite, (carbonates), Quartz, Gypse, Silicates, Eléments en traces, … Djebel Onk Tébessa Traitements: granulométrie, lavage, calcination, flottation, magnétisme, … Domaines d’utilisation: Engrais-acide phosphorique (90%) …. Pollution. 8
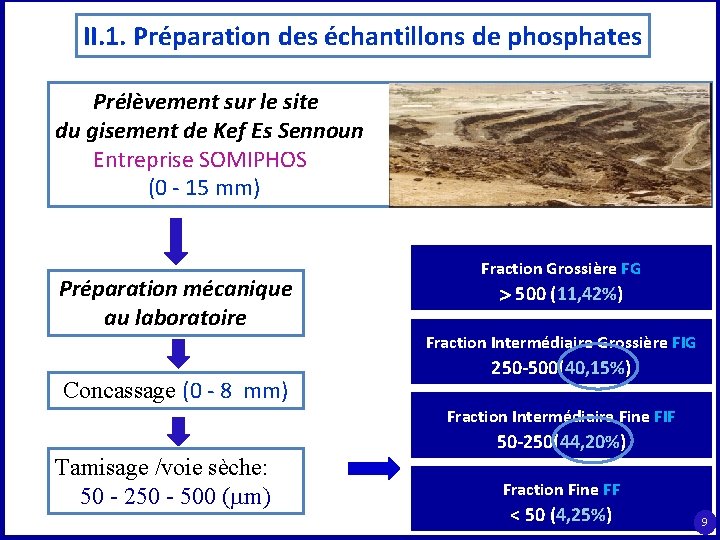
II. 1. Préparation des échantillons de phosphates Prélèvement sur le site du gisement de Kef Es Sennoun Entreprise SOMIPHOS (0 - 15 mm) Préparation mécanique au laboratoire Concassage (0 - 8 mm) Fraction Grossière FG 500 (11, 42%) Fraction Intermédiaire Grossière FIG 250 -500(40, 15%) Fraction Intermédiaire Fine FIF 50 -250(44, 20%) Tamisage /voie sèche: 50 - 250 - 500 ( m) Fraction Fine FF < 50 (4, 25%) 9
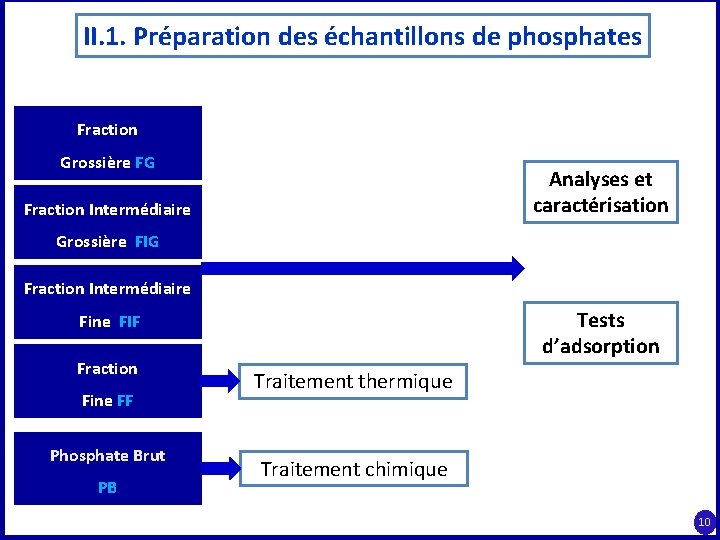
II. 1. Préparation des échantillons de phosphates Fraction Grossière FG Analyses et caractérisation Fraction Intermédiaire Grossière FIG Fraction Intermédiaire Tests d’adsorption Fine FIF Fraction Fine FF Phosphate Brut PB Traitement thermique Traitement chimique 10

II. 1. Préparation des échantillons de phosphates a. Traitement Chimique • HCl ou H 2 SO 4: 250 ml, 1 N Sortie d’eau Réfrigérant à boules • Masse phosphate: de Pince Bague m = f (T. activation) Entrée d’eau • Température : 80°C Ballon Chauffe Ballon • Temps d’agitation: 1 heure Support Lavages pour éliminer H 3 O+, NO 3 - et SO 42 -, restants en solution (on élimine SO 42 - par ajout de Ba. Cl 2). La détection des NO 3 - se fait par des mesures de la conductivité jusqu’à une valeur < 20 µS. m-1. 11
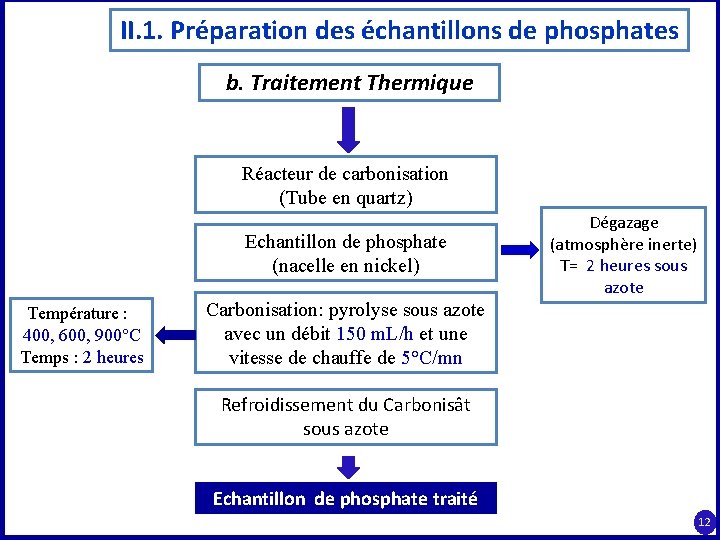
II. 1. Préparation des échantillons de phosphates b. Traitement Thermique Réacteur de carbonisation (Tube en quartz) Echantillon de phosphate (nacelle en nickel) Température : 400, 600, 900°C Temps : 2 heures Dégazage (atmosphère inerte) T= 2 heures sous azote Carbonisation: pyrolyse sous azote avec un débit 150 m. L/h et une vitesse de chauffe de 5°C/mn Refroidissement du Carbonisât sous azote Echantillon de phosphate traité 12
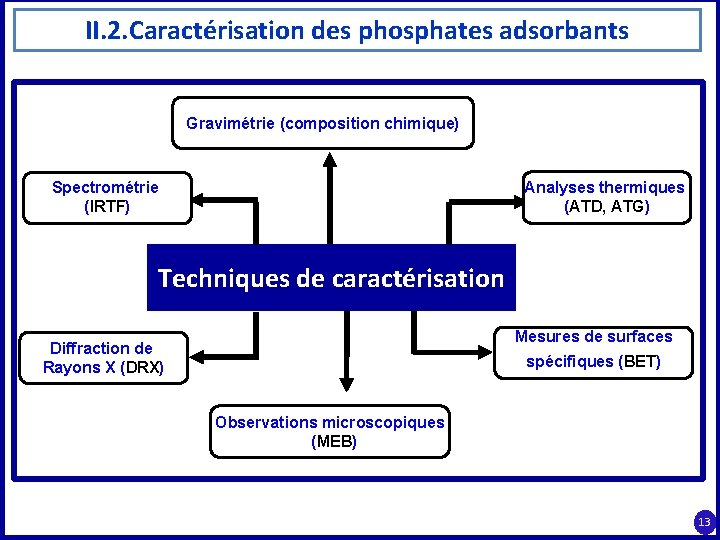
II. 2. Caractérisation des phosphates adsorbants Gravimétrie (composition chimique) Analyses thermiques (ATD, ATG) Spectrométrie (IRTF) Techniques de caractérisation Mesures de surfaces Diffraction de Rayons X (DRX) spécifiques (BET) Observations microscopiques (MEB) 13
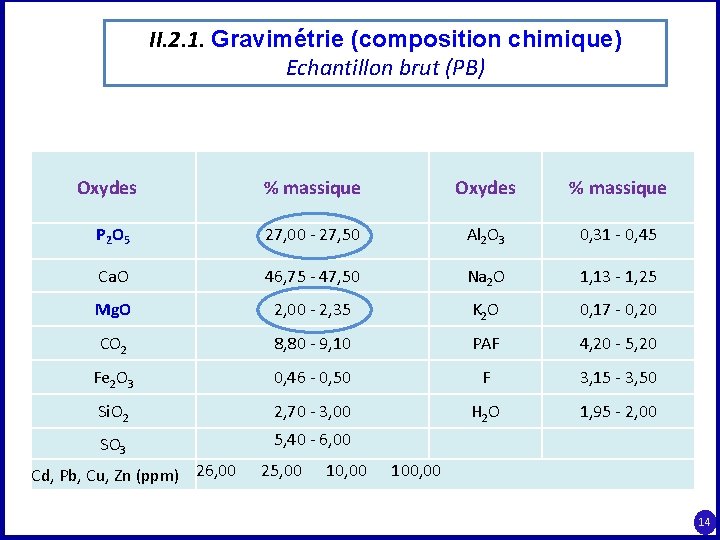
II. 2. 1. Gravimétrie (composition chimique) Echantillon brut (PB) Oxydes % massique P 2 O 5 27, 00 - 27, 50 Al 2 O 3 0, 31 - 0, 45 Ca. O 46, 75 - 47, 50 Na 2 O 1, 13 - 1, 25 Mg. O 2, 00 - 2, 35 K 2 O 0, 17 - 0, 20 CO 2 8, 80 - 9, 10 PAF 4, 20 - 5, 20 Fe 2 O 3 0, 46 - 0, 50 F 3, 15 - 3, 50 Si. O 2 2, 70 - 3, 00 H 2 O 1, 95 - 2, 00 SO 3 5, 40 - 6, 00 Cd, Pb, Cu, Zn (ppm) 26, 00 25, 00 100, 00 14
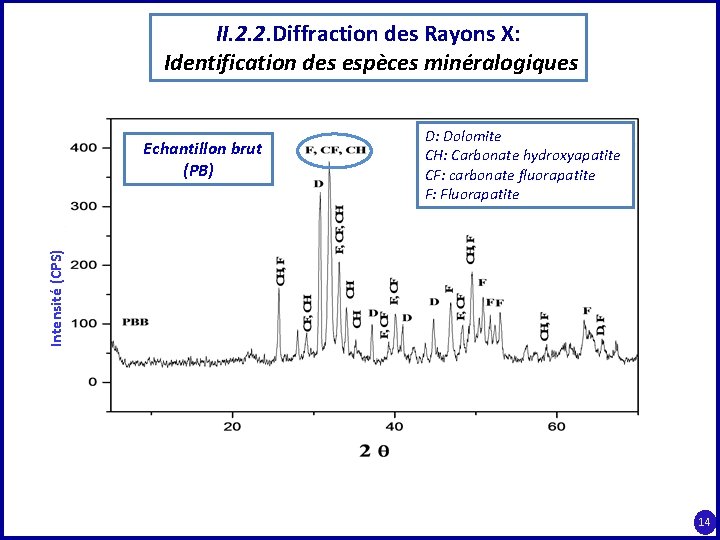
II. 2. 2. Diffraction des Rayons X: Identification des espèces minéralogiques D: Dolomite CH: Carbonate hydroxyapatite CF: carbonate fluorapatite F: Fluorapatite Intensité (CPS) Echantillon brut (PB) 14
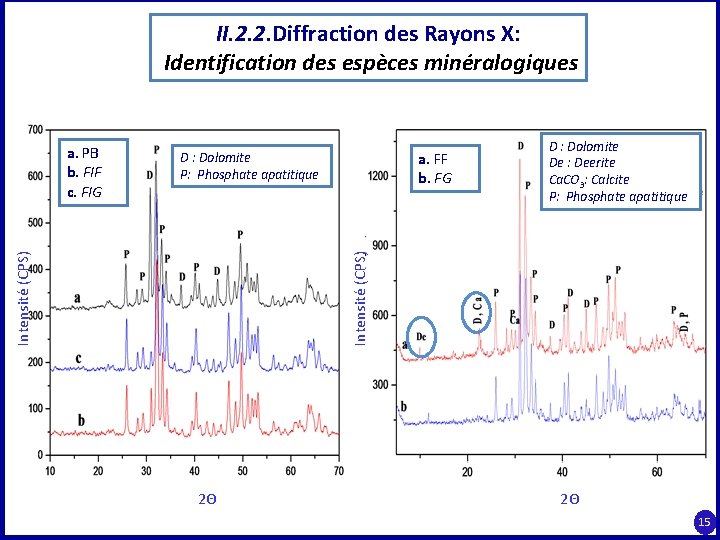
II. 2. 2. Diffraction des Rayons X: Identification des espèces minéralogiques a. FF b. FG D : Dolomite De : Deerite Ca. CO 3: Calcite P: Phosphate apatitique Intensité (CPS) D : Dolomite P: Phosphate apatitique Intensité (CPS) a. PB b. FIF c. FIG 2Θ 2Θ 15
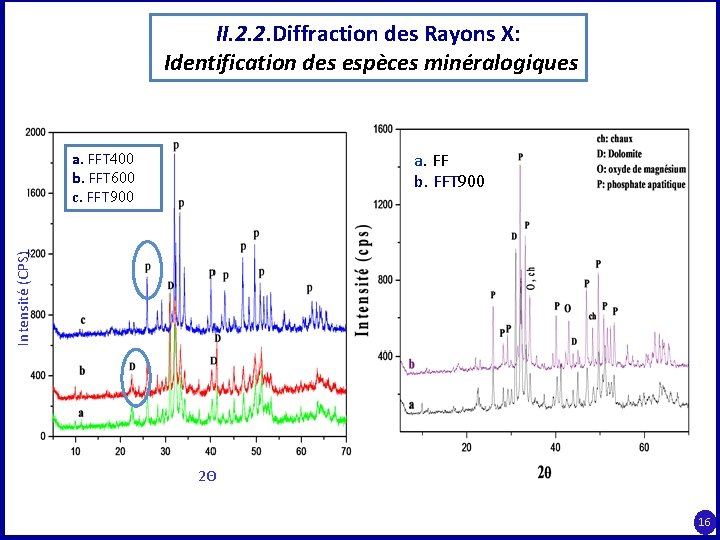
II. 2. 2. Diffraction des Rayons X: Identification des espèces minéralogiques a. FF b. FFT 900 Intensité (CPS) a. FFT 400 b. FFT 600 c. FFT 900 2Θ 16
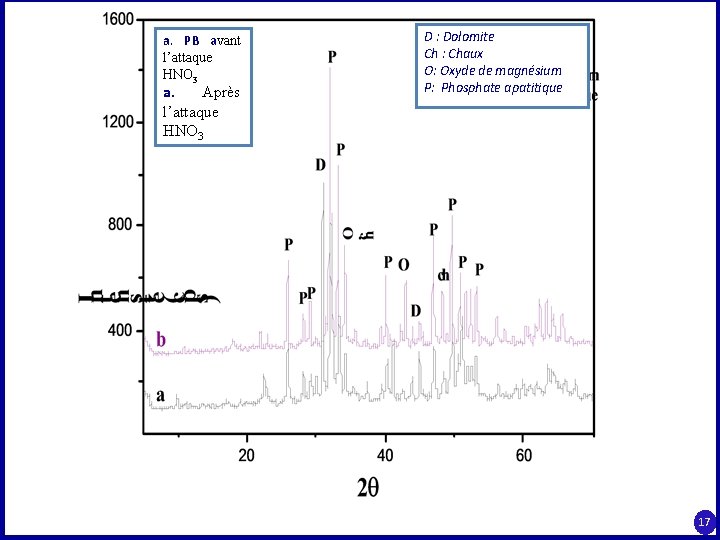
a. PB avant l’attaque HNO 3 a. Après l’attaque HNO 3 D : Dolomite Ch : Chaux O: Oxyde de magnésium P: Phosphate apatitique 17
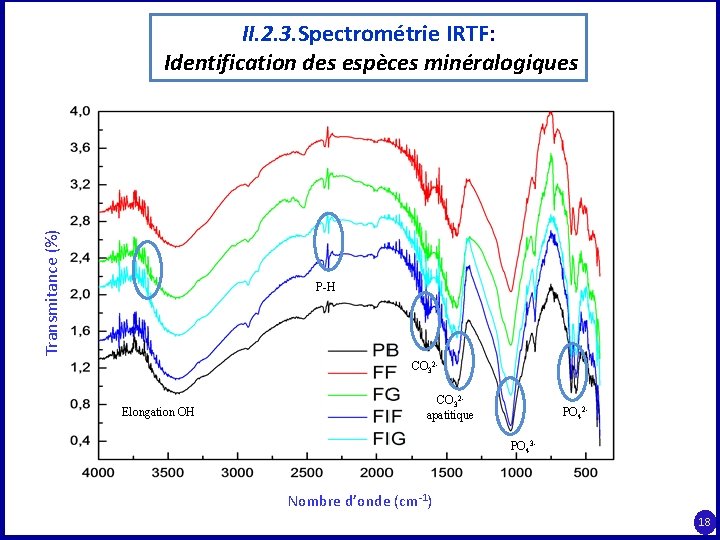
Transmitance (%) II. 2. 3. Spectrométrie IRTF: Identification des espèces minéralogiques P-H CO 32 - Elongation OH CO 32 - apatitique PO 42 PO 43 - Nombre d’onde (cm-1) 18
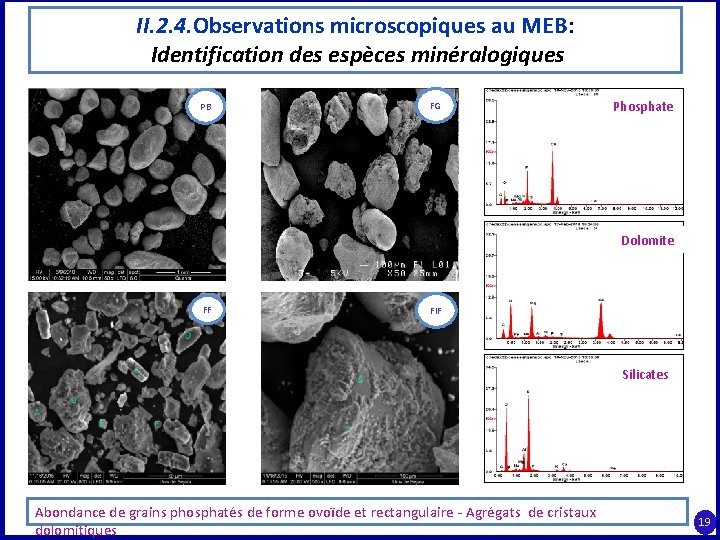
II. 2. 4. Observations microscopiques au MEB: Identification des espèces minéralogiques PB FG Phosphate Dolomite FF FIF Silicates Abondance de grains phosphatés de forme ovoïde et rectangulaire - Agrégats de cristaux dolomitiques 19
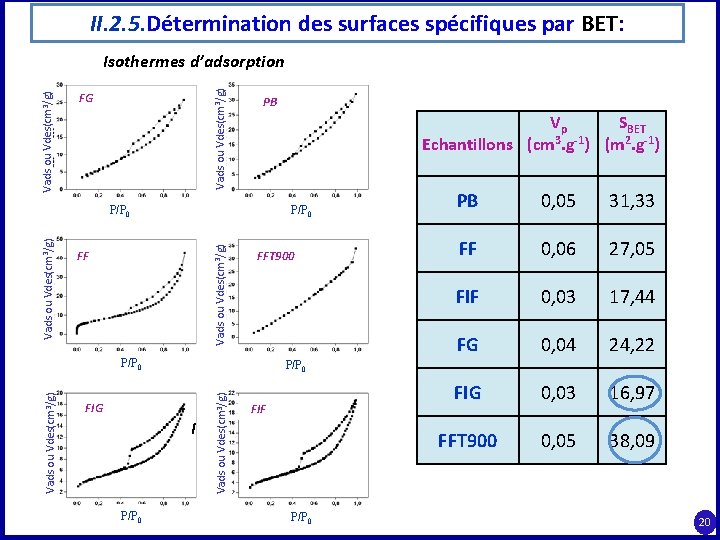
II. 2. 5. Détermination des surfaces spécifiques par BET: Vads ou Vdes(cm 3/g) Isothermes d’adsorption FG PB Vp SBET Echantillons (cm 3. g-1) (m 2. g-1) P/P 0 Vads ou Vdes(cm 3/g) P/P 0 FF FFT 900 FIG I P/P 0 0, 05 31, 33 FF 0, 06 27, 05 FIF 0, 03 17, 44 FG 0, 04 24, 22 FIG 0, 03 16, 97 FFT 900 0, 05 38, 09 P/P 0 Vads ou Vdes(cm 3/g) P/P 0 PB FIF P/P 0 20
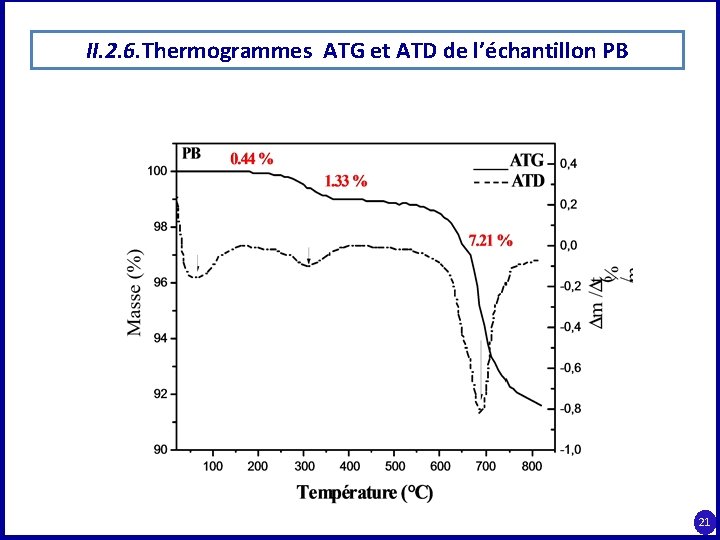
II. 2. 6. Thermogrammes ATG et ATD de l’échantillon PB 21
III. Tests d’adsorption du système: Colorants/Phosphates Isothermes d’adsorption Cinétique d’adsorption • Concentration en colorant • Concentration en phosphate Optimisation des paramètres expérimentaux Paramètres thermodynamiques Modélisation des résultats • Vitesse d’agitation • Température • p. H 22
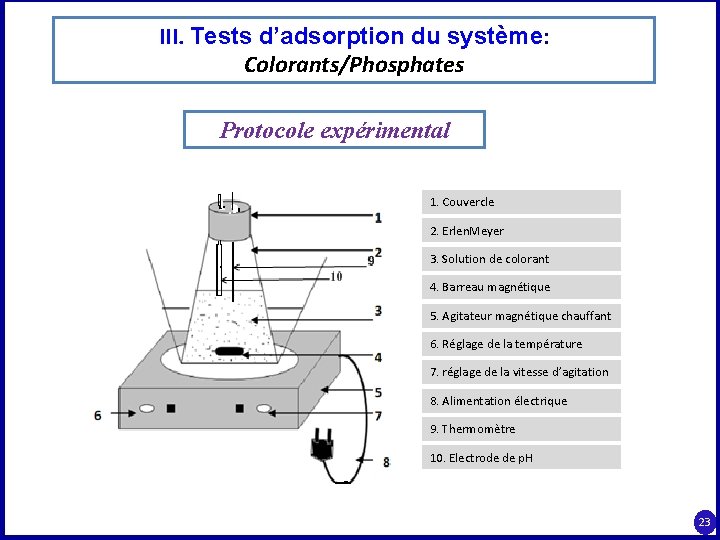
III. Tests d’adsorption du système: Colorants/Phosphates Protocole expérimental 1. Couvercle 2. Erlen. Meyer 3. Solution de colorant 4. Barreau magnétique 5. Agitateur magnétique chauffant 6. Réglage de la température 7. réglage de la vitesse d’agitation 8. Alimentation électrique 9. Thermomètre 10. Electrode de p. H 23
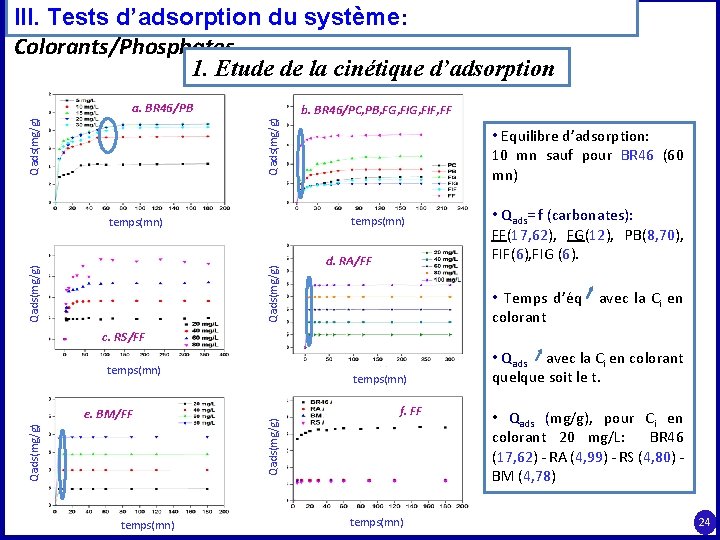
III. Tests d’adsorption du système: Colorants/Phosphates 1. Etude de la cinétique d’adsorption b. BR 46/PC, PB, FG, FIF, FF Qads(mg/g) a. BR 46/PB temps(mn) Qads(mg/g) • Equilibre d’adsorption: 10 mn sauf pour BR 46 (60 mn) d. RA/FF • Qads= f (carbonates): FF(17, 62), FG(12), PB(8, 70), FIF(6), FIG (6). • Temps d’éq avec la Ci en colorant c. RS/FF temps(mn) f. FF Qads(mg/g) e. BM/FF temps(mn) • Qads avec la Ci en colorant quelque soit le t. • Qads (mg/g), pour Ci en colorant 20 mg/L: BR 46 (17, 62) - RA (4, 99) - RS (4, 80) - BM (4, 78) 24
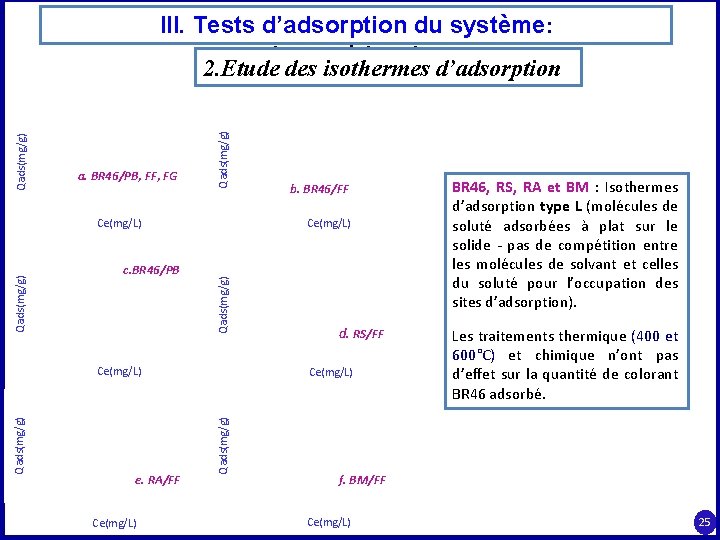
a. BR 46/PB, FF, FG Qads(mg/g) III. Tests d’adsorption du système: Colorants/Phosphates 2. Etude des isothermes d’adsorption c. BR 46/PB Ce(mg/L) Qads(mg/g) Ce(mg/L) d. RS/FF Ce(mg/L) Qads(mg/g) Ce(mg/L) e. RA/FF b. BR 46/FF BR 46, RS, RA et BM : Isothermes d’adsorption type L (molécules de soluté adsorbées à plat sur le solide - pas de compétition entre les molécules de solvant et celles du soluté pour l’occupation des sites d’adsorption). Les traitements thermique (400 et 600°C) et chimique n’ont pas d’effet sur la quantité de colorant BR 46 adsorbé. f. BM/FF Ce(mg/L) 25

III. Tests d’adsorption du système: Colorants/Phosphates 3. Optimisation des paramètres expérimentaux a. Influence de la concentration en colorant (Ci) a. BR 46/PB Qads(mg/g) b. RS/FF Concentration(mg/L) d. BM/FF Qads(mg/g) c. RA/FF Concentration(mg/L) 26

III. Tests d’adsorption du système: Colorants/Phosphates 3. Optimisation des paramètres expérimentaux a. BR 46/PB Taux d’élimination (%) b. Influence de la concentration de la suspension de phosphate R (g/L) Concentration R(g/L) Taux d’élimination (%) Concentration R(g/L) c. RA/FF b. RS/FF Taux d’élimination (%) BR 46: R (g/L): 0, 25 - 4 g/L 16, 1 -91, 52 % RS, RA et BM: R (g/L): 1 - 4 g/L 85, 81 - 99, 37 % pour RS 87, 16 -99, 81 % pour RA 87 % -99, 44 % pour BM. d. BM/FF Concentration R(g/L) 27

III. Tests d’adsorption du système: Colorants/Phosphates 3. Optimisation des paramètres expérimentaux c. Influence de la vitesse d’agitation b. RS/FF Qads(mg/g) a. BR 46/PB Vitesse d’agitation (trs/min) 28
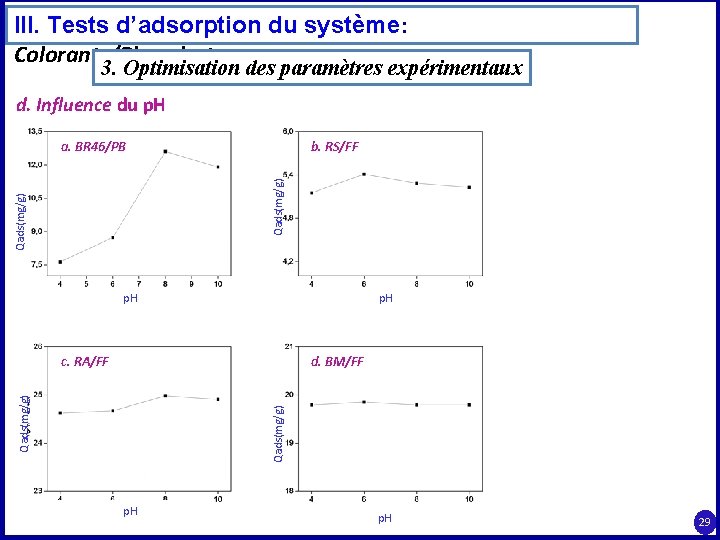
III. Tests d’adsorption du système: Colorants/Phosphates 3. Optimisation des paramètres expérimentaux d. Influence du p. H b. RS/FF Qads(mg/g) a. BR 46/PB p. H d. BM/FF Qads(mg/g) c. RA/FF p. H 29

III. Tests d’adsorption du système: Colorants/Phosphates 4. Paramètres thermodynamiques b. RS/FF Ln(Kd) Ln(Kd) a. BR 46/PB 1/T*1000(k-1) d. BM/FF Ln(Kd) c. RA/FF 1/T*1000(k-1) T: 293 - 298 - 303 - 308 - 313 - 323 (K). BR 46/ PB : ∆H°=-2, 579 k. J/mol< 0 et < 50 k. J/mol: Caractère exothermique-physisorption. ∆S° = -0, 006 k. J/mol. K < 0: Accroissement de l’ordre moléculaire des molécules de soluté en passant de la solution à la surface de l’adsorbant. ∆G° < 0 : Processus spontané. RS, RA et BM/ FF: ∆H°: k. J/mol RS (39, 880); RA (5, 20) et BM (17, 60) ∆H° > 0 et < 50 k. J/mol: Caractère endothermiquephysisorption. ∆S°: k. J/mol. K RS (0, 156), RA (0, 05) et BM (0, 101) ∆S° > 0: Diminution de l’ordre moléculaire des molécules de soluté en passant de la solution à la surface de l’adsorbant. ∆G° < 0 : Processus spontané. 30
III. Tests d’adsorption du système: Colorants/Phosphates 5. Modélisation des résultats expérimentaux Modèles cinétiques: 1 er et 2ème ordre Diffusion intra-particulaire Modèles mathématiques: Langmuir Freundlich Temkin 31
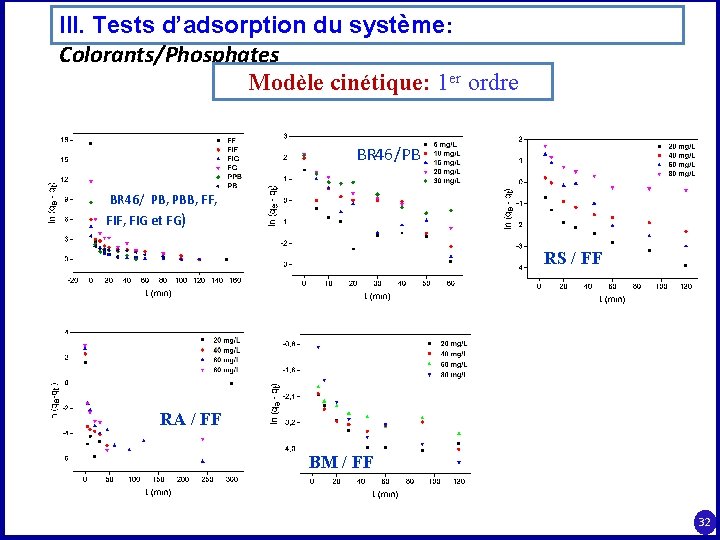
III. Tests d’adsorption du système: Colorants/Phosphates Modèle cinétique: 1 er ordre BR 46/PB BR 46/ PB, PBB, FF, FIF, FIG et FG) RS / FF RA / FF BM / FF 32
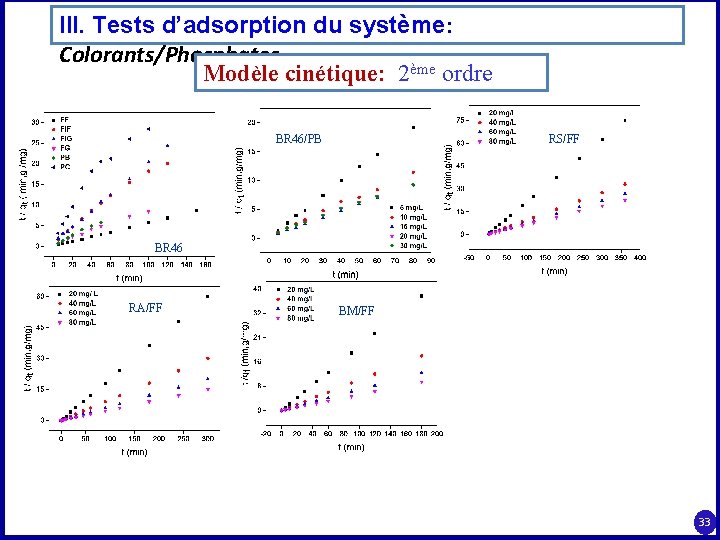
III. Tests d’adsorption du système: Colorants/Phosphates Modèle cinétique: 2ème ordre BR 46/PB RS/FF BR 46 RA/FF BM/FF 33
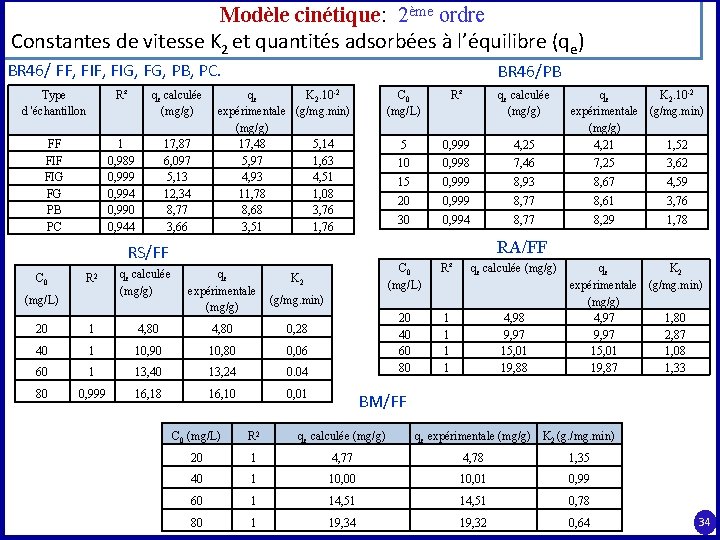
Modèle cinétique: 2ème ordre Constantes de vitesse K 2 et quantités adsorbées à l’équilibre (qe) BR 46/ FF, FIG, FG, PB, PC. BR 46/PB Type d 'échantillon FF FIG FG PB PC R² qe calculée (mg/g) 1 0, 989 0, 994 0, 990 0, 944 17, 87 6, 097 5, 13 12, 34 8, 77 3, 66 qe K 2. 10 -2 expérimentale (g/mg. min) (mg/g) 17, 48 5, 14 5, 97 1, 63 4, 93 4, 51 11, 78 1, 08 8, 68 3, 76 3, 51 1, 76 R 2 qe calculée (mg/g) 20 1 4, 80 0, 28 40 1 10, 90 10, 80 0, 06 60 1 13, 40 13, 24 0. 04 80 0, 999 16, 18 16, 10 0, 01 (mg/L) R² qe calculée (mg/g) qe K 2. 10 -2 expérimentale (g/mg. min) (mg/g) 4, 21 1, 52 5 0, 999 4, 25 10 0, 998 7, 46 7, 25 3, 62 15 0, 999 8, 93 8, 67 4, 59 20 0, 999 8, 77 8, 61 3, 76 30 0, 994 8, 77 8, 29 1, 78 RA/FF RS/FF C 0 (mg/L) qe K 2 expérimentale (g/mg. min) (mg/g) C 0 (mg/L) R² qe calculée (mg/g) 20 40 60 80 1 1 4, 98 9, 97 15, 01 19, 88 qe K 2 expérimentale (g/mg. min) (mg/g) 4, 97 1, 80 9, 97 2, 87 15, 01 1, 08 19, 87 1, 33 BM/FF C 0 (mg/L) R 2 qe calculée (mg/g) qe expérimentale (mg/g) K 2 (g. /mg. min) 20 1 4, 77 4, 78 1, 35 40 1 10, 00 10, 01 0, 99 60 1 14, 51 0, 78 80 1 19, 34 19, 32 0, 64 34
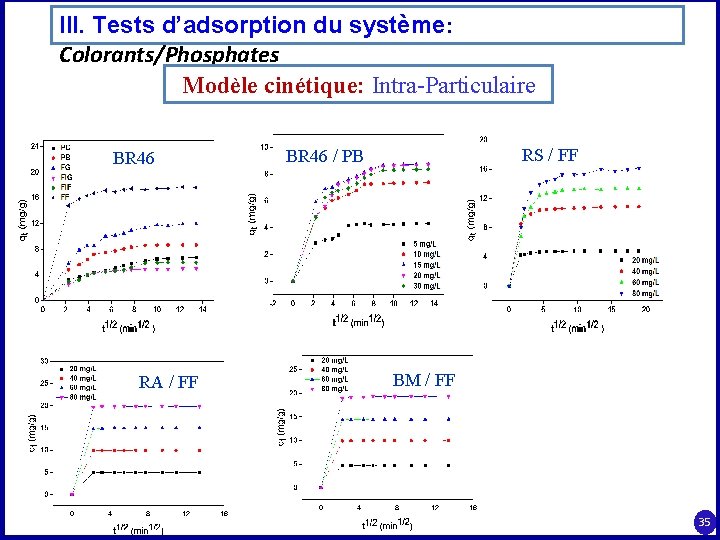
III. Tests d’adsorption du système: Colorants/Phosphates Modèle cinétique: Intra-Particulaire BR 46 RA / FF RS / FF BR 46 / PB BM / FF 35
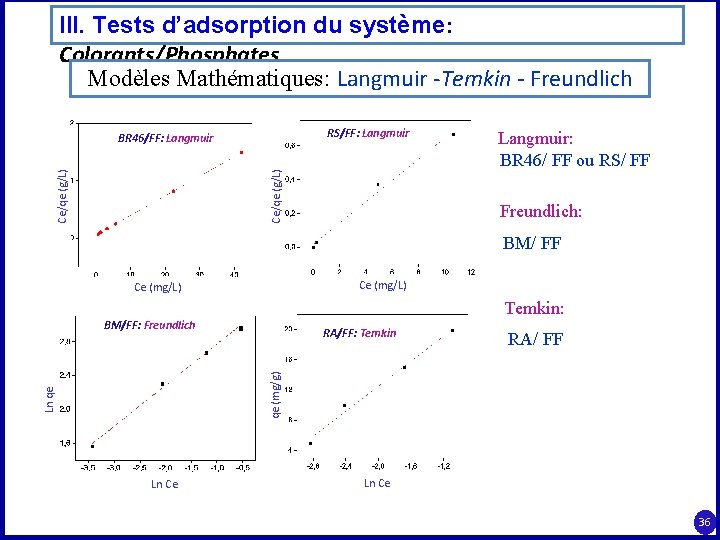
III. Tests d’adsorption du système: Colorants/Phosphates Modèles Mathématiques: Langmuir -Temkin - Freundlich RS/FF: Langmuir Ce/qe (g/L) BR 46/FF: Langmuir: BR 46/ FF ou RS/ FF Freundlich: BM/ FF Ce (mg/L) Temkin: BM/FF: Freundlich RA/ FF Ln qe qe (mg/g) RA/FF: Temkin Ln Ce 36

III. Tests d’adsorption du système: Colorants/Phosphates Modèles Mathématiques Non Linéarisés Langmuir -Temkin - Freundlich BR 46/FF qe(mg/g) BR 46/PB Ce(mg/L) Valeurs de RMSE pour les différents modèles et les différents adsorbants dans le cas de l’adsorption de BR 46 Modèles des isothermes Langmuir Freundlich Temkin qe(mg/g) BR 46/FFT 600 Adsorbants FF PB FFT 600 3, 105 1, 840 1, 310 5, 953 2, 365 2, 105 4, 448 1, 956 1, 558 Adsorption Colorant BR 46/Différents adsorbants utilisés obéit au modèle de Langmuir (faibles valeurs de RMSE) Ce(mg/L) 37
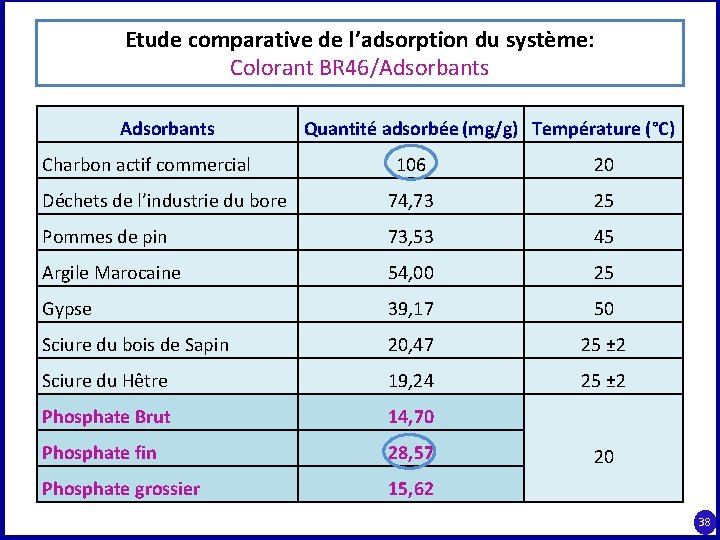
Etude comparative de l’adsorption du système: Colorant BR 46/Adsorbants Charbon actif commercial Quantité adsorbée (mg/g) Température (°C) 106 20 Déchets de l’industrie du bore 74, 73 25 Pommes de pin 73, 53 45 Argile Marocaine 54, 00 25 Gypse 39, 17 50 Sciure du bois de Sapin 20, 47 25 ± 2 Sciure du Hêtre 19, 24 25 ± 2 Phosphate Brut 14, 70 Phosphate fin 28, 57 20 Phosphate grossier 15, 62 38

Conclusion générale 1. La caractérisation granulo-chimique et minéralo-texturale du phosphate naturel de Djebel Onk, à l’état brut et traité, réalisée par différentes techniques d’analyses qualitative et quantitative (DRX, MEB, IR, BET, …) a mis en évidence : ü les espèces minéralogiques en éléments phosphatés : carbonate hydroxyapatite, fluorapatite et carbonate fluorapatite et en éléments de la gangue: dolomite, calcite, silicates et déerite. ü les mailles de libération des éléments phosphatés: fractions granulométriques ( m): 50 -250 (44, 20%) et 250 -500 (40, 15%), et des éléments de la gangue: fraction < 50 (04, 25%) et 500 (11, 42%). ü la disparition de la dolomite et de la deerite et l’apparition de nouvelles phases Mg. O et Ca. O après traitement thermique à 900°C. ü la disparition totale de la dolomite après traitement chimique du phosphate brut (PB) par HNO 3 ou H 2 SO 4. ü Les surfaces spécifiques déterminées par la méthode B. E. T, en m 2/g, varient de 16, 97 pour FIG à 38, 09 pour l’échantillon FFT 900. L’écart observé, est lié essentiellement à la finesse des grains et à la composition minéralogique. les isothermes d’adsorption pour tous les échantillons, sont de Type II, caractéristiques de solides macroporeux sauf pour 39

Conclusion générale l’échantillon FFT 900 où l’isotherme est de type III. La boucle d’hystérésis est de Type (H 3), qui apparait sur les isothermes de type II ne présentant pas de palier de saturation. ü Trois pertes de masse attribuées respectivement au départ de l'eau d'absorption(0, 44 % , Tambiante - 150°C), de l'eau structurale et à la décomposition de la matière organique (1, 3%, 220 - 490 °C) et à la décomposition des carbonates (7, 21%, 600 – 900°C) 2. Les tests d’adsorption effectués pour une série de systèmes: Colorants/Phosphates, ont porté sur l’étude cinétique, thermodynamique, sur l’optimisation des principaux paramètres opératoires, et sur la modélisation des résultats expérimentaux: ü Sur le plan cinétique, la vitesse d’adsorption est très rapide au début du processus d’adsorption: 10 mn/RS, RA, BM et 60 mn pour BR 46. Les quantités adsorbées (mg/g) sont plus élevées pour les fractions riches en carbonates (FF et FG) que pour celles des phosphates (PB, FIF et FIG) : FF (17, 62), FG (11, 95), PB (8, 70), FIF (5, 95) et FIG (4, 98). Ceci démontre l’affinité du colorant aux groupements carbonates. 40

Conclusion générale ü la quantité maximale de colorant adsorbée (mg/g), pour une concentration de 20 mg/L a révélé une différence appréciable entre BR 46 et les autres colorants utilisés : BR 46 (17, 62) - RA(4, 99) - RS (4, 80) - BM (4, 78). La quantité de colorant adsorbée augmente avec l’accroissement de sa concentration. ü le taux d’élimination du BR 46/PB augmente avec l’accroissement de la concentration en phosphate, il passe de 16, 1 à 91, 52 % quand la concentration du phosphate en suspension passe de 0, 25 à 3 g/L, ensuite il devient constant. Il passe de 85, 81 à 99, 37 % pour RS, de 87, 16 à 99, 81 % pour RA et de 87 % à 99, 44 % pour BM, quand la concentration de phosphate en suspension passe de 1 à 4 g/L, au-delà, il se stabilise. ü le traitement chimique effectué sur le phosphate brut (PB) et thermique effectué à 400 et 600°C, sur la fraction fine (FF), ont influé négativement sur leur capacité d’adsorption du colorant BR 46. L’activation chimique a provoqué la dissolution des carbonates or le colorant BR 46 a plus d’affinité pour ces groupements. 41

Conclusion générale ü l’adsorption des colorants est fortement influencée par la vitesse d’agitation, elle est optimale pour une vitesse de 300 trs/min. La quantité de colorant observée à cette vitesse d’agitation est due à une bonne dispersion des particules de phosphate, ce qui a pour conséquence d’augmenter la surface totale d’échange entre le phosphate et la solution de colorant. ü l’adsorption est optimale à p. H 8 pour les colorants BR 46 et RA: surface de l’adsorbant de charge négative favorisant l’adsorption des cations. Pour RS et BM, l’adsorption est optimale à p. H 6: les colorants sont sous forme cationique. ü Sur le plan thermodynamique l’adsorption est spontanée et de type physique: endothermique pour RS, RA et BM et exothermique pour BR 46. ü le traitement des valeurs expérimentales par les différents modèles cinétiques a donné un coefficient de corrélation hautement significatif pour le modèle de second ordre. 42

Conclusion générale ü les isothermes d’adsorption de l’ensemble des systèmes colorants/phosphates étudiés correspondent au type L. Ce qui démontre que les molécules de colorants s’adsorbent en position horizontale (plat) et les isothermes dont de type I. ü l’application des modèles d’adsorption aux résultats expérimentaux a montré que : l’adsorption des colorants BR 46 et RS se rapproche plus du modèle de Langmuir. En revanche, le modèle qui est adapté à l’adsorption du colorant RA, est celui de Temkin. Pour l’adsorption du colorant BM, le modèle de Freundlich est le mieux adapté. D’une façon globale, l’utilisation des rejets de phosphate de Djebel Onk comme adsorbant de ces colorants, a donné des résultats satisfaisants. Ce sont alors des matériaux alternatifs prometteurs pour la dépollution des eaux chargées en colorants cationiques. Leurs utilisations dans ce domaine, donnera une nouvelle approche à l’exploitation et à la valorisation de ce matériau par l’entreprise Somiphos. 43

Perspectives ü L’utilisation des rejets de phosphate sur d’autres types de colorants (anioniques et neutres). ü Elargir cette étude sur d’autres types de rejets de phosphates issus des autres procédés d’enrichissement comme la flottation, la calcination … ü Prévoir d’autres types de traitements capables d’améliorer leur capacité d’adsorption (dopage). 44

Travaux scientifiques • Publication internationale: Influence of adsorption parameters of basic red dye 46 by the rough and treated Algerian natural phosphates - Zahra Graba, Souaad Hamoudi, Djebar Bekka, Nacer Bezzi, Rabah Boukherroub -Journal of Industrial and Engineering Chemistry. 25 (2015) 229 -238. Impact factor 3. 54. • Communications nationales et internationales -Z. Graba, N. Bezzi, Elimination d’un colorant textile par des phosphates naturels algériens, 8ème Symposium National de Chimie Organique Industrielle et pharmaceutique du 07 au 09 Novembre 2012, Sidi Fredj (Alger). Z. Graba, N. Bezzi, Etude comparative de l’élimination d’un polluant organique par les phosphates beige et noir de Djebel-Onk (Tebessa- Algérie), 1 er Congrès International : Substances Naturelles Modélisation : Applications Thérapeutique, Environnementale, Développement Durable, 15 – 16 Décembre 2014, Taza (Maroc). Z. Graba, N. Bezzi, Etude cinétique de l’adsorption d’un colorant par des phosphates noirs de Djebel Onk (Tebessa. Algérie), Journées Internationales de Cinétique, Catalyse et Calorimétrie, 2 -4 Mai 2015, Alger (Algérie). Z. Graba, N. Bezzi, Influence of adsorption parameters of basic red Cl 18 dye by Algerian natural phosphate, International Congress on Energy and Environment Engineering and Management, 22 - 24 Juillet 2015, Paris (France). Z. Graba, N. Bezzi, Elimination d’un colorant cationique par des rejets de phosphates de Djebel-Onk (Tébessa-Algérie), ERVD’ 4, 26 - 27 Octobre 2016, Al Akhawayn Ifrane (Maroc). • Projet de recherche CNEPRU Code E 00620100012, sur le thème «Utilisation des phosphates naturels de Djebel Onk pour éliminer les polluants organiques en milieu aqueux par adsorption» . • Memoire de Magister : 03 soutenus • Memoires de Master : 08 soutenus

Merci pour votre attention
- Slides: 47