Problematika vzcnch onemocnn a lk pro vzcn onemocnn

Problematika vzácných onemocnění a léků pro vzácná onemocnění Kateřina Kubáčková FN Motol, Praha

Vzácná onemocnění • Nesourodá skupina chorob • Dědičná, vrozená • 4%-5% novorozenců • Vývojové vady, dědičné poruchy metabolismu, geneticky podmíněná onemocnění

Vzácná onemocnění • Výskyt u méně než 5 osoba na 10 000 • 6000 -8000 onemocnění • 20% výskytu všech nádorů (ledviny, vaječníky, krevní nádory) • Nádory dětí • 50% úmrtnosti na nádory

Vzácná onemocnění • Příčina často není známa • Nádory dětského a dospělého věku • 80% genetický podklad
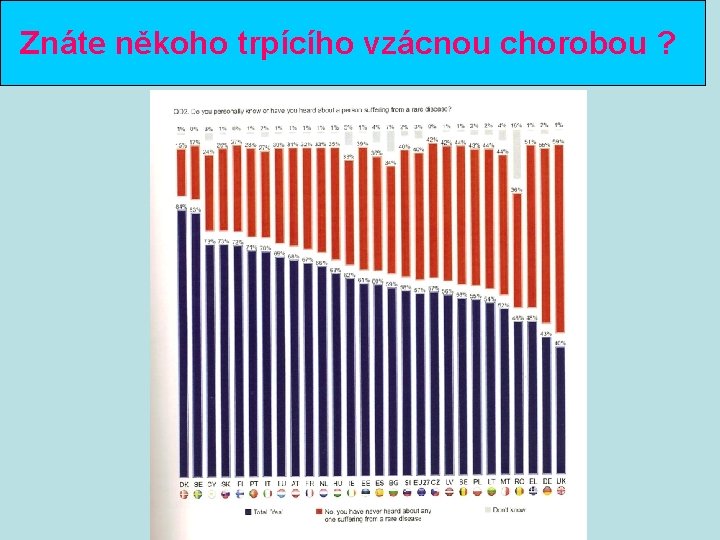
Znáte někoho trpícího vzácnou chorobou ?


Legislativa Nařízení (ES) č. 141/2000 Evropského parlamentu a Rady ze dne 16. prosince 1999 o léčivých přípravcích pro vzácná onemocnění • kritéria designace LPVO Nařízení komise (ES) č. 847/2000 • koncepce „podobných léčivých přípravků“ • koncepce „klinické superiority“

Nařizení (ES) č. 141/2000 Kritéria designace léčivého přípravku jako léku pro vzácné onemocnění ( orphan drug): • Pro diagnostiku, prevenci a léčbu • Prevalence 5/10 000 obyvatel EU • Život ohrožující, chronicky invalidizující či závažná a chronická onemocnění • Ustanovení komise expertů- COMP

Nařízení (ES) č. 141/2000 • Zajistit přístup nemocných trpících vzácnými chorobami k léčbě • Podporovat výzkum, vývoj a uvedení na trh OD • Pobídky (incentives) • USA 1983, Japonsko 1993, Austrálie, Singapur • Snaha o koordinaci podpory na úrovni EU

Legislativa Doporučení Rady o akci v oblasti vzácných onemocnění-2009 Ø Plány a strategie Ø Definice, kodifikace Ø Výzkum Ø Odborná centra a evropské referenční sítě Ø Posílení úlohy pacientů

Doporučení Rady o evropské akci v oblasti vzácných onemocnění 8. 6. 2009: ØNárodní plány pro vzácná onemocnění 2013 ØRegistr vzácných onemocnění - ORPHANET ØEvropské referenční onemocnění sítě pro vzácná


Přeshraniční lékařská péče Směrnice EP a Rady o uplatňování práv pacientů v přeshraniční péči • 19. 1. 2011 • MS 30 měsíců na implementaci • Vzácné onemocnění- samostatný dodatek, síť evropských referenčních center • Vznik národních kontaktních center, úřad evropského ochránce práv pacientů
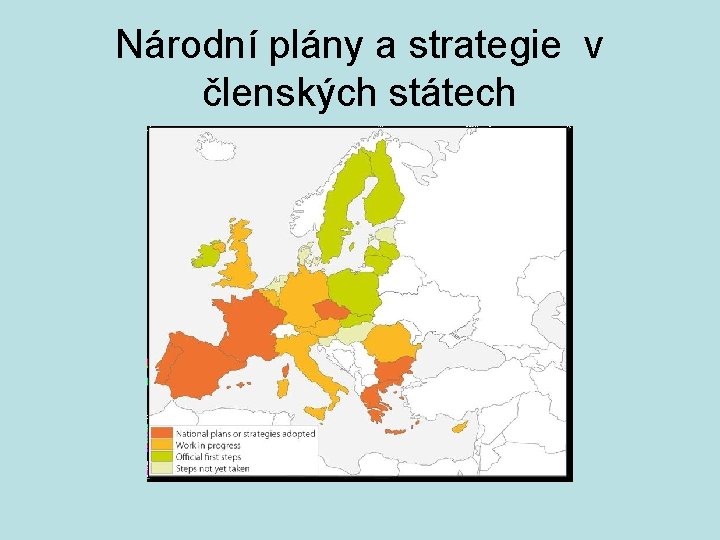
Národní plány a strategie v členských státech


Národní strategie (NS) pro vzácná onemocnění 2010 -2020 • Přijata v roce 2010 • Dalším krokem je její naplnění formou Národního akčního plánu • Hlavní cíle NS: - včasná diagnostika a dostupnost adekvátní léčby vzácných onemocnění - koordinace a centralizace efektivní péče o pacienty se vzácným onemocněním - zlepšení vzdělání a informovanosti odborné i laické veřejnosti - spolupráce na národní i mezinárodní úrovni se zapojením pacientských organizací - zlepšení identifikace vzácných onemocnění v rámci systému Mezinárodní klasifikace nemocí Říjen 2011(MKN).

Národní strategie pro vzácná onemocnění na léta 2010 -2020 • Mezi hlavní cíle Národní strategie proto patří včasná diagnostika a dostupnost adekvátní léčby vzácných onemocnění, koordinace a centralizace efektivní péče o pacienty se vzácným onemocněním, zlepšení vzdělání a informovanosti odborné i laické veřejnosti v dané oblasti a spolupráce na národní i mezinárodní úrovni se zapojením pacientských organizací a také zlepšení identifikace vzácných onemocnění v rámci systému Mezinárodní klasifikace nemocí (MKN).

Národní strategie 2010 -2020 -Cíle • Zlepšení kvality života a sociálního začlenění ØZavedení ICF( International Classification of Functioning, Disability and Health) ØZlepšení meziresortní spolupráce • Podpora výzkumu • Sběr dat • Rozvoj zahraniční spolupráce


Novorozenecký skríning Ø Rychlá diagnostika a včasná léčba Ø Metabolické a endokrinní poruchy Ø Hrazení z prostředků veřejného zdravotnictví Ø Národní koordinační centrum pro novorozenecký skríning VFN Praha

13 nemocí pro novorozenecký screening 2009

E-health

Národní strategie 2010 -2020 -Cíle • Podpora a posílení role organizací pacientů • Meziresortní pracovní skupina pro vzácná onemocnění
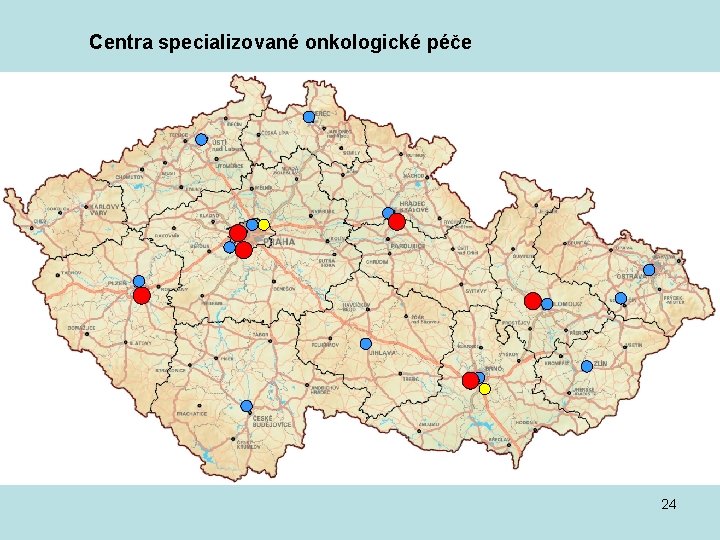
Centra specializované onkologické péče 24

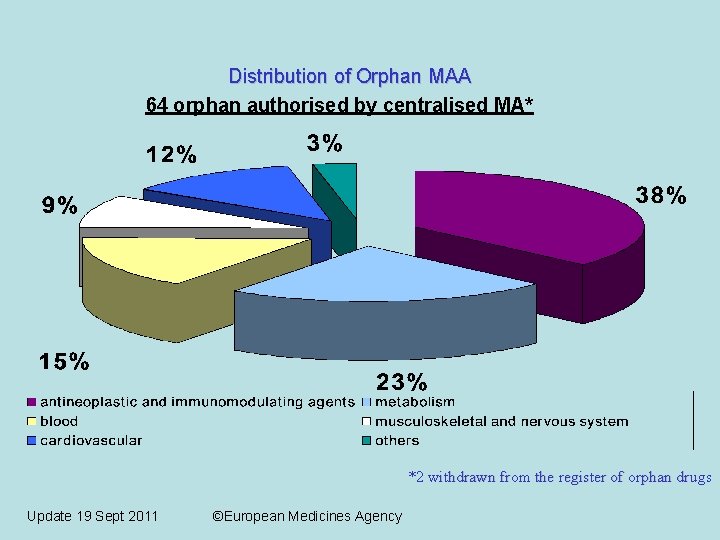
Distribution of Orphan MAA 64 orphan authorised by centralised MA* *2 withdrawn from the register of orphan drugs Update 19 Sept 2011 ©European Medicines Agency
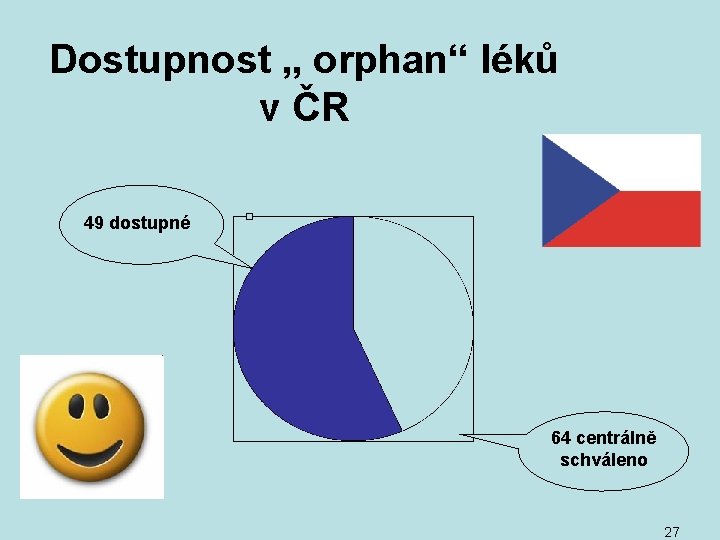
Dostupnost „ orphan“ léků v ČR 49 dostupné 64 centrálně schváleno 27
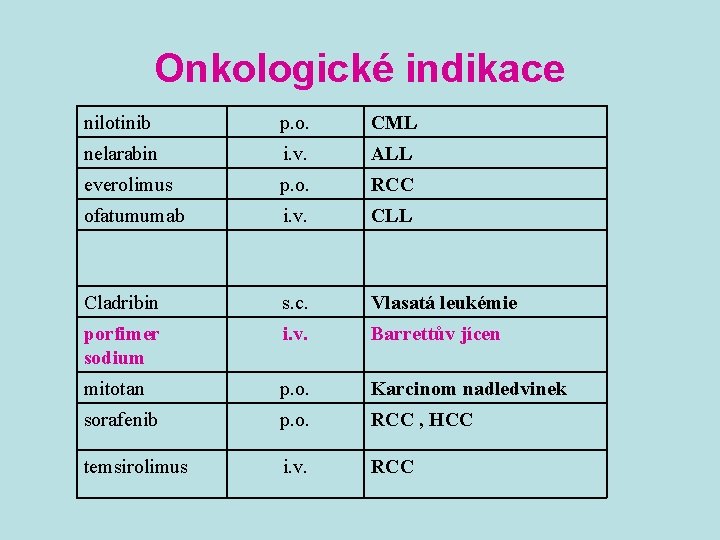
Onkologické indikace nilotinib p. o. CML nelarabin i. v. ALL everolimus p. o. RCC ofatumumab i. v. CLL Celecoxib p. o. Familiární adenomatózní polypóza Cladribin s. c. Vlasatá leukémie porfimer sodium i. v. Barrettův jícen mitotan p. o. Karcinom nadledvinek sorafenib p. o. RCC , HCC temsirolimus i. v. RCC
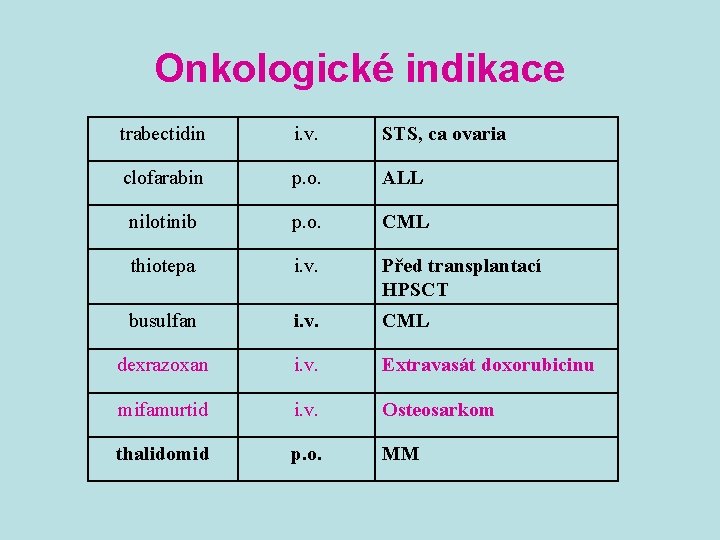
Onkologické indikace trabectidin i. v. STS, ca ovaria clofarabin p. o. ALL nilotinib p. o. CML thiotepa i. v. Před transplantací HPSCT busulfan i. v. CML dexrazoxan i. v. Extravasát doxorubicinu mifamurtid i. v. Osteosarkom thalidomid p. o. MM
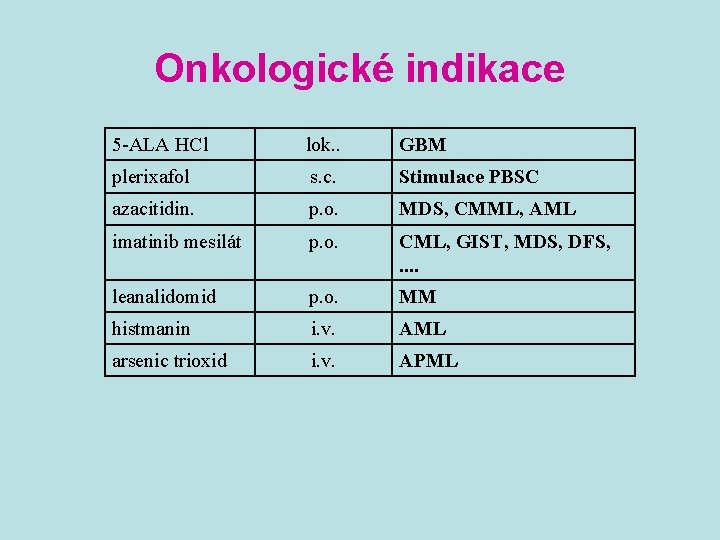
Onkologické indikace 5 -ALA HCl lok. . GBM plerixafol s. c. Stimulace PBSC azacitidin. p. o. MDS, CMML, AML imatinib mesilát p. o. CML, GIST, MDS, DFS, . . leanalidomid p. o. MM histmanin i. v. AML arsenic trioxid i. v. APML
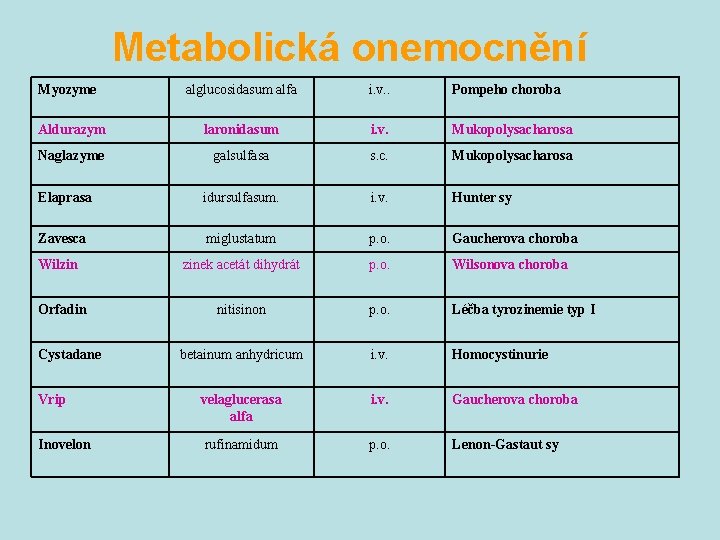
Metabolická onemocnění Myozyme alglucosidasum alfa i. v. . Pompeho choroba Aldurazym laronidasum i. v. Mukopolysacharosa Naglazyme galsulfasa s. c. Mukopolysacharosa Elaprasa idursulfasum. i. v. Hunter sy Zavesca miglustatum p. o. Gaucherova choroba zinek acetát dihydrát p. o. Wilsonova choroba nitisinon p. o. Léčba tyrozinemie typ I betainum anhydricum i. v. Homocystinurie Vrip velaglucerasa alfa i. v. Gaucherova choroba Inovelon rufinamidum p. o. Lenon-Gastaut sy Wilzin Orfadin Cystadane
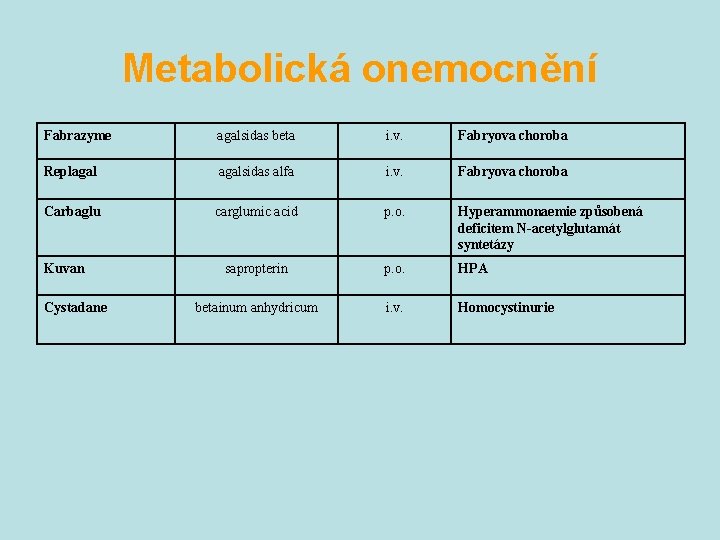
Metabolická onemocnění Fabrazyme agalsidas beta i. v. Fabryova choroba Replagalsidas alfa i. v. Fabryova choroba Carbaglu carglumic acid p. o. Hyperammonaemie způsobená deficitem N-acetylglutamát syntetázy sapropterin p. o. HPA betainum anhydricum i. v. Homocystinurie Kuvan Cystadane
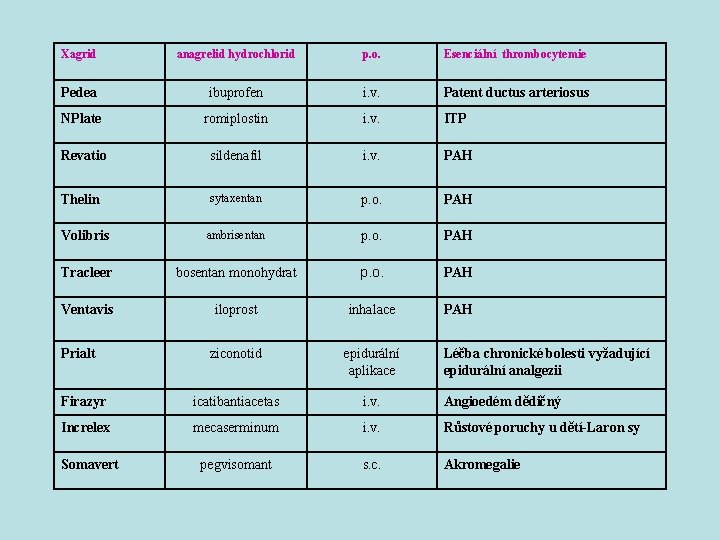
Xagrid anagrelid hydrochlorid p. o. Esenciální thrombocytemie Pedea ibuprofen i. v. Patent ductus arteriosus NPlate romiplostin i. v. ITP Revatio sildenafil i. v. PAH Thelin sytaxentan p. o. PAH Volibris ambrisentan p. o. PAH Tracleer bosentan monohydrat p. o. PAH Ventavis iloprost inhalace PAH ziconotid epidurální aplikace Firazyr icatibantiacetas i. v. Angioedém dědičný Increlex mecaserminum i. v. Růstové poruchy u dětí-Laron sy pegvisomant s. c. Akromegalie Prialt Somavert Léčba chronické bolesti vyžadující epidurální analgezii
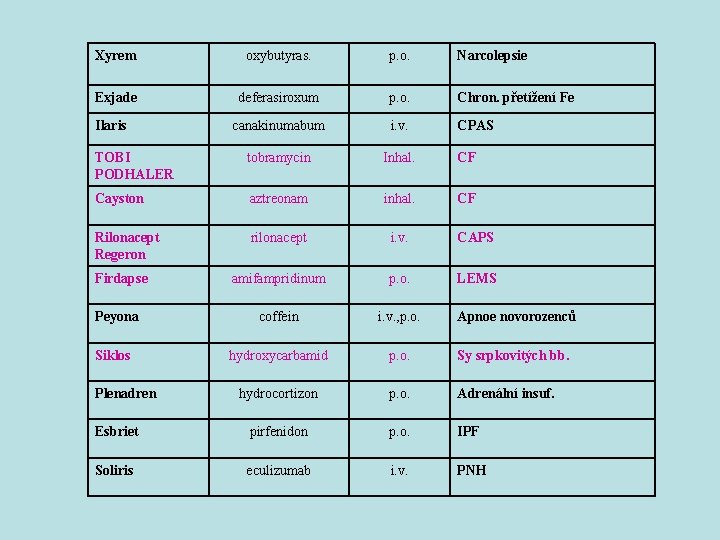
Xyrem oxybutyras. p. o. Narcolepsie Exjade deferasiroxum p. o. Chron. přetížení Fe canakinumabum i. v. CPAS TOBI PODHALER tobramycin Inhal. CF Cayston aztreonam inhal. CF Rilonacept Regeron rilonacept i. v. CAPS amifampridinum p. o. LEMS Peyona coffein i. v. , p. o. Apnoe novorozenců Siklos hydroxycarbamid p. o. Sy srpkovitých bb. hydrocortizon p. o. Adrenální insuf. Esbriet pirfenidon p. o. IPF Soliris eculizumab i. v. PNH Ilaris Firdapse Plenadren

Dostupnost - ale Ø Legislativa hrazené péče a stanovení cen - nezná „orphans“ Ø Nezohledněn parametr závažnosti a chybění alternativní léčby Ø Stejné posuzování jako standardní léčivé přípravky Ø Jak hodnotit nákladovou efektivitu

Zákon č. 378/2007 Sb. § 11 zákona o léčivech • činit opatření za účelem zajištění dostupnosti léčivých přípravků významných pro poskytování zdravotní péče a přijímá opatření na podporu výzkumu, vývoje a dostupnosti léčivých přípravků pro vzácná onemocnění a léčivých přípravků, které mohou být jako takové stanoveny, jakož i léčivých přípravků pro použití v dětském lékařství,

„Technická novela“ zákon č. 48/1997 Sb Dočasná úhrada § § Není znám dostatek údajů o nákladové efektivitě- jak ji stanovit Nejsou výsledky použití v klinické praxi- risk/ benefit- EU, EMA, COMP Dočasná úhrada na dobu 12 měsíců, a to až třikrát Poté úhrada podmíněna stanovením „trvalé“ úhrady standardním procesem, ve kterém bude muset prokázat mj. o jeho terapeutická účinnost a bezpečnost o závažnost onemocnění, k jejímuž léčení je určen- statut orphan léku o nákladová efektivita a náklady o předpokládaný dopad úhrady na finanční prostředky zdravotního pojištění o doporučené postupy odborných institucí a odborníků, a to vždy z hlediska nákladové efektivity a s ohledem na dopad na finanční prostředky zdravotního pojištění

§ 16 • Vymezení pro neregistrované léky, indikace s nedostatečnými daty o bezpečnosti a účinnosti • Administrativní zátěž • Prodlužování přístupu inovativních léků k pacientům
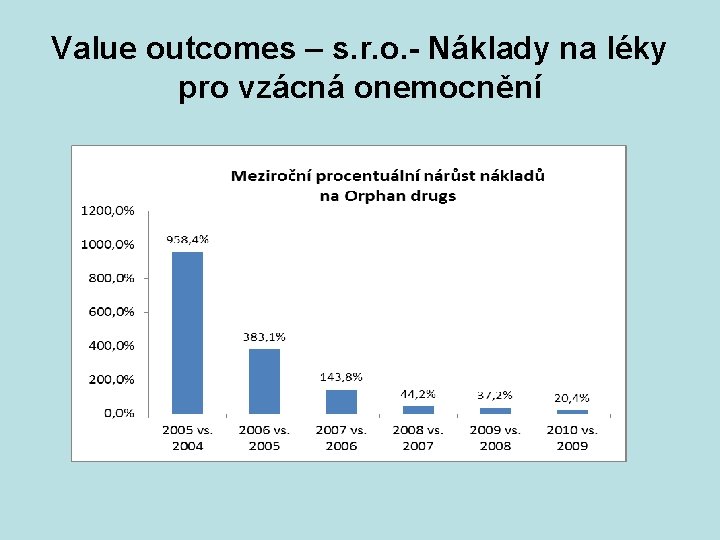
Value outcomes – s. r. o. - Náklady na léky pro vzácná onemocnění
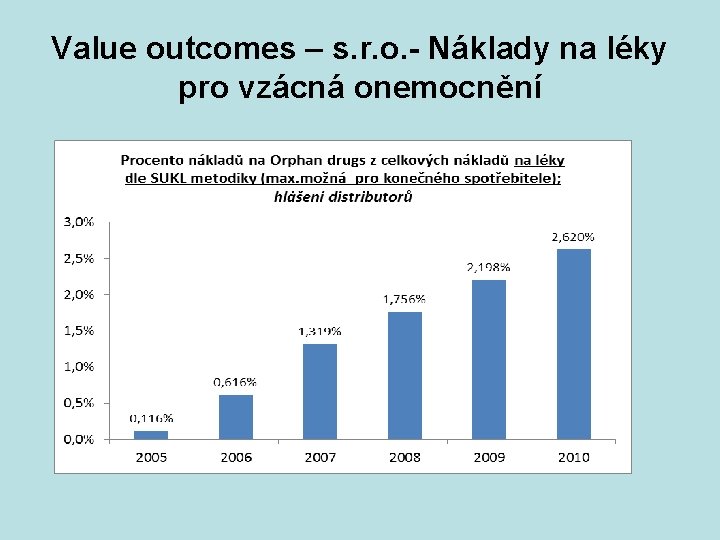
Value outcomes – s. r. o. - Náklady na léky pro vzácná onemocnění
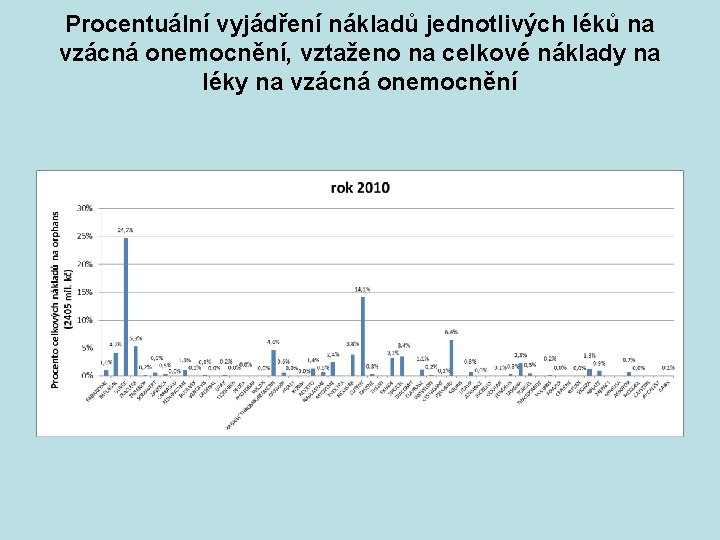
Procentuální vyjádření nákladů jednotlivých léků na vzácná onemocnění, vztaženo na celkové náklady na léky na vzácná onemocnění

CAVOD- Clinical Added-Value ( Relative Effectiveness) of Orphan Drug

www. orpha. net Encyklopedie a klasifikace • Orphan drugs Klinická pracoviště Laboratoře Pacientské skupiny Výzkumné projekty a studie


vzacna-onemocneni. cz/pdf/zpravodaj_cavo_2012_01. pdf

Pacientské organizace • Czech Republic lays groundwork for the Czech Association for Rare Diseases

Společné prohlášení pacientských organizací ke dni vzácných onemocnění 29. února 2012 Toto společné prohlášení zástupců organizací pacientů se vzácnými onemocněními poukazuje na oblasti a témata, která jsou z pohledu pacientů nejdůležitější a měla by být zohledněna při další práci na národním plánu pro vzácná onemocnění i při tvorbě národní legislativy v oblasti vzácných onemocnění. Když člověk onemocní vzácnou chorobou, je v podstatně složitější situaci než člověk s chorobou častou, ať už jde o diagnostiku, možnosti léčby nebo informace o nemoci. Přitom by měl mít stejná práva jako ostatní pacienti. Aby bylo možné napravit znevýhodnění, které takové diagnózy znamenají, je zapotřebí kategorii vzácných onemocnění zakotvit v příslušných předpisech a standardizovat specifický přístup tak, jak je tomu například ve většině zemí Evropy a USA a jak to předpokládá Nařízení rady Evropy z roku 1999/2000. • Diagnostika, léčba a péče o pacienty se vzácným onemocněním je v České republice na rozdílné úrovni. Většina případů je řešena ad hoc: nejsou zavedeny standardy léčby ani odpovídající legislativa. Aby bylo možné kvalitu péče do budoucna garantovat, považujeme za nezbytné zakotvit v odpovídajících normách především včasnou diagnostiku, rovný a včasný přístup k léčbě, a rozvoj sítě specializovaných center. Tyto cíle zmiňuje m. j. Národní strategie pro vzácná onemocnění a doporučení rady EU o vzácných onemocněních a měl by z nich vycházet i Národní plán pro vzácná onemocnění. • K dosažení těchto cílů je podle našeho názoru zapotřebí učinit následující kroky: • vymezení specifické kategorie vzácných onemocnění v české legislativě • standardizace léčebných postupů pro jednotlivé diagnózy v souladu s doporučenými evropskými standardy • legislativní zakotvení zvláštního režimu orphan drugs (léků na vzácná onemocnění) • usnadnění přístupu pacientů k novým lékům a léčebným postupům • zakotvení statusu specializovaných léčebných center a rozvoj sítě těchto center (pro některé nemoci dosud neexistuje odpovídající pracoviště) • posílení přeshraniční spolupráce při léčbě a výzkumu • rozvoj diagnostiky tak, aby co nejméně pacientů zůstávalo bez správné diagnózy • stanovení pevného časového harmonogramu uskutečňování jednotlivých cílů v rámci národního plánu, který bude naplňovat národní strategii vyhlášenou vládou v roce 2010 • zohlednění specifik vzácných onemocnění v oblasti sociální politiky • Národní plán pro vzácná onemocnění by měl obsahovat přesný postup, jak těchto cílů dosáhnout. • Toto společné prohlášení vzniklo v rámci přípravy založení a formulace cílů platformy na podporu činnosti sdružení pacientů se vzácnými onemocněními.


The importance of patient input for the work of the European Medicines Agency • Adapted from presentations by Juan Garcia Burgos • Head of Public Information and Stakeholder Networking – Medical Information • European Medicines Agency (EMA)

Přidaná hodnota pacientů v EMA ( Evropská Léková Agentura) – Přináší unikátní a kritický pohled z reálného života o chorobách a ze současného prostředí zdravotních služeb. – Zvýšení transparentosti a vytváření důvěry v regulačním procesu. – Zastupují zájmy pacientů a poskytují „ pacientských pohled“, jednotlivců, kterých se bezprostředně týká regulační rozhodnutí

Přidaná hodnota zainteresovaných pacientů – EMA( Evropská Léková Agentura) – Aktivně přispívat k informovanosti pacientů a komunikace o léčivých přípravcích. – Kominukovat výstupy jednání jednotlivých komisí na veřejnosti; předávat informace jiným pacientům a pacientským organizacím. – Radit a podporovat regulátory při jednání s průmyslem a ostatními zainteresovanými stranami při identifikaci oblastí výzkumu cílené terapie

Přidaná hodnota zainteresovaných pacientů – EMA – Připravenost pacientů doporučovat a podporovat regulátora v proveditelnosti plánu klinického výzkum( klinické studie pro dětskou populaci (PIP), designace léků pro vzácné onemocnění, risk-management plán etc. ) – Přispívat k obecnému zdraví ( zvyšovat povědomost o vlivu regulačních rozhodnutí) v rámci pacientských organizací – Kontinuálně přispívat a žádat změny v systému zvyšujících jeho funkčnost

Účast pacientů s aktivitách EMA Plné členství: Ø Management Board, 2005 Ø Committee for Orphan Medicinal Products (COMP), 2000 Ø Paediatric Committee (PDCO), 2008 Ø Committee for Advance Therapies (CAT), 2009 Ø Pharmacovigilance Working Party (Ph. VWP), 2010 Ø Pharmacovigilance Risk Assessment Committee (PRAC)

Výzvy – Nedostatek zdrojů v organizacích – Potřeba vzdělání k pochopení regulačního prostřdí – Potřeba definování úlohy pacientů v aktivitách Agentury a vědeckých výborech – Obtížnost získání vhodných expertů (např. jazykové bariéry)

©European Medicines Agency 2011. Reproduction and/or distribution of this document is possible for non-commercial purposes provided that EMEA is always acknowledged as the source in each copy. Citations may be made, provided the source is always acknowledged. See: http: //www. emea. europa. eu/htms/technical/dm p/copyritel. htm Update 19 Sept 2011 ©European Medicines Agency

Cíle politiky „ ORPHAN“ 1) Zajistit dostupnost komplexní péče pro pacienty se vzácnými onemocněními (psychologická péče, sociální péče, léčebná péče) 2) Zajistit jasný zákonný status (podmínky a výhody) specializovaných léčebných center 3) Do budoucna zajistit přístup pacientů k novým lékům pro vzácná, dosud neléčitelná onemocnění.

Spolupráce, multidisciplinarita
- Slides: 57