Prise en charge de lhpatite chronique B en

Prise en charge de l’hépatite chronique B en 2009 Recommandations EASL et AASLD (J Hepatol, GCB, Hepatology 2009) F. Lunel CVV 2009

Hépatite chronique B Définition n n Ag HBs + > 6 mois Ag HBe + ou – ADN VHB >20 000 UI/ml (Hbe +), >2000 (Hbe-) Transaminases élevées de façon persistante ou intermittente PBH: lésions variables (score nécro-inflammatoire) Evolution en 4 à 5 phases Lok, Hepatology 2001
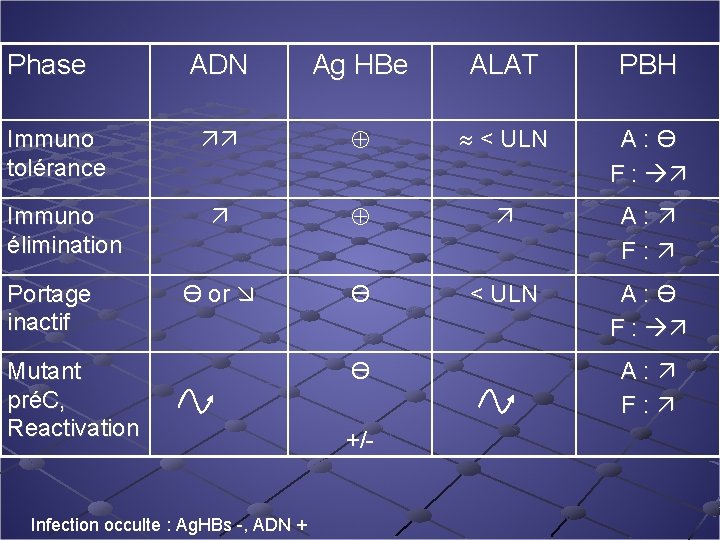
Phase Immuno tolérance Immuno élimination Portage inactif ADN Ag HBe ALAT PBH < ULN A : Ө F : A : F : Ө or Ө < ULN A : Ө F : Mutant préC, Reactivation Infection occulte : Ag. HBs -, ADN + Ө +/- A : F :

IMMUNOTOLERANCE Ag. HBe+ UI 2000 Titre g/ml 9 HBV DNA 6 Sérum 30 Log 3 Ig. M anti-HBc ALAT • Immunotolérance Temps • Multiplication virale active • Contagiosité maximale • absence d ’anomalies hépatiques ou lésions minimes

IMMUNOELIMINATION : Hépatite chronique active Ag Hbe + et ADN VHB + ALAT élevées Activité Fibrose/cirrhose Evolution : n n Clairance Ag HBe Séroconversion anti HBe Mutant pré C Séro-réversion
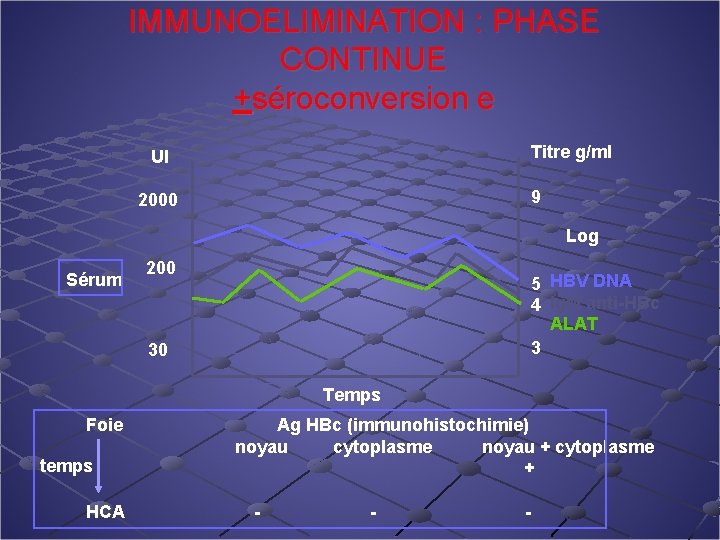
IMMUNOELIMINATION : PHASE CONTINUE +séroconversion e Titre g/ml UI 9 2000 Log Sérum 5 HBV DNA 4 Ig. M anti-HBc ALAT 3 200 30 Temps Foie Ag HBc (immunohistochimie) noyau cytoplasme noyau + cytoplasme temps + HCA -
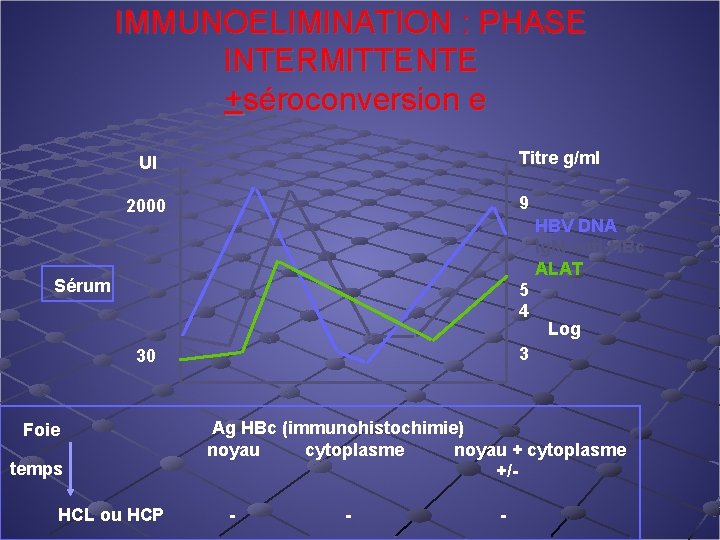
IMMUNOELIMINATION : PHASE INTERMITTENTE +séroconversion e UI 2000 Sérum 30 Titre g/ml 9 HBV DNA Ig. M anti-HBc ALAT 5 4 Log 3 Foie Ag HBc (immunohistochimie) noyau cytoplasme noyau + cytoplasme temps +/HCL ou HCP -

Mutants pré C Décrits pour la première fois en 1981 en Italie (Bonino); plus fréquents dans certaines régions n Pourtour méditerranéen n Asie du Sud Est n Étude multicentrique en cours en France n Pb sélectionnés par la réponse immune au moment de la clairance de l’Ag. HBe Mutation au niveau du codon 1896 - absence de synthèse de l ’Ag HBe, sujets Ac anti-HBe + Maladie plus sévère ? Niveau de réplication plus faible (4 à 5 Log UI/ml)
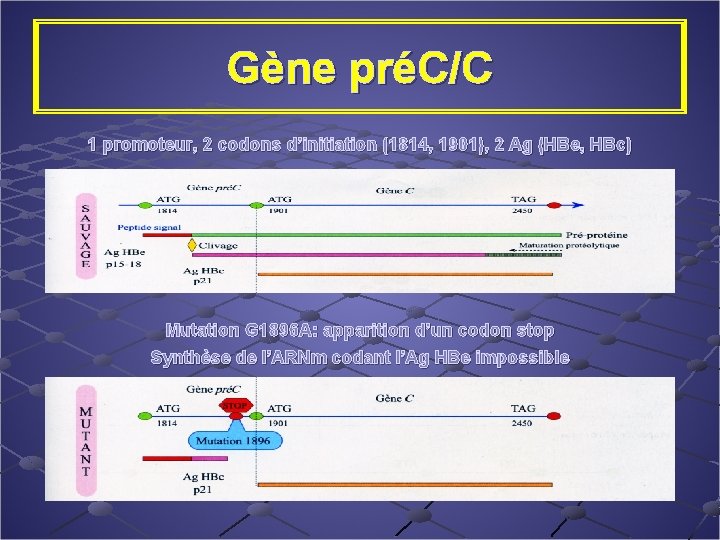
Gène préC/C 1 promoteur, 2 codons d’initiation (1814, 1901), 2 Ag (HBe, HBc) Mutation G 1896 A: apparition d’un codon stop Synthèse de l’ARNm codant l’Ag HBe impossible

Porteur « inactif » Définition n Ag HBs + > 6 mois Ag HBe – et Ac HBe+ ADN VHB <2000 UI/ml n Transaminases normales de façon persistante n n n PBH: lésions minimes (score nécroinflammatoire<4) Lok, Hepatology 2009
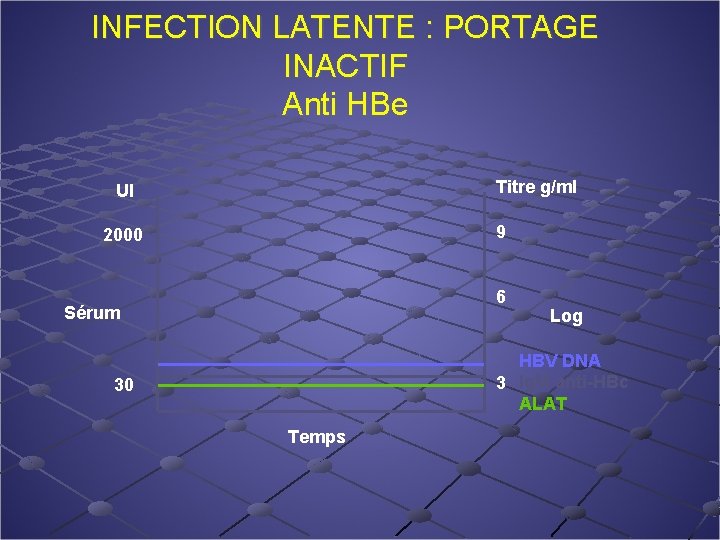
INFECTION LATENTE : PORTAGE INACTIF Anti HBe Titre g/ml UI 9 2000 6 Sérum Log HBV DNA 3 Ig. M anti-HBc ALAT 30 Temps

Porteur « inactif» Évolution n en règle bénigne n 4 risques théoriques réactivation virale: risque faible lié à la persistance d’une multiplication virale à minima (PCR) Surinfection delta: toxicomanes++ Carcinome hépatocellulaire: risque très faible Contagiosité: risque potentiel mais très faible

Réactivation Définition Réapparition de lésions nécrotico inflammatoires en général chez un porteur inactif 20 à 50 % après chimiothérapie ou immunosuppression ou anti. TNFalpha Mortalité sans traitement : 30% YEO W et al. Hepatology , 2006, 43, 209 -20 JANG JW et al. Hepatology , 2006 , 43, 233 -40
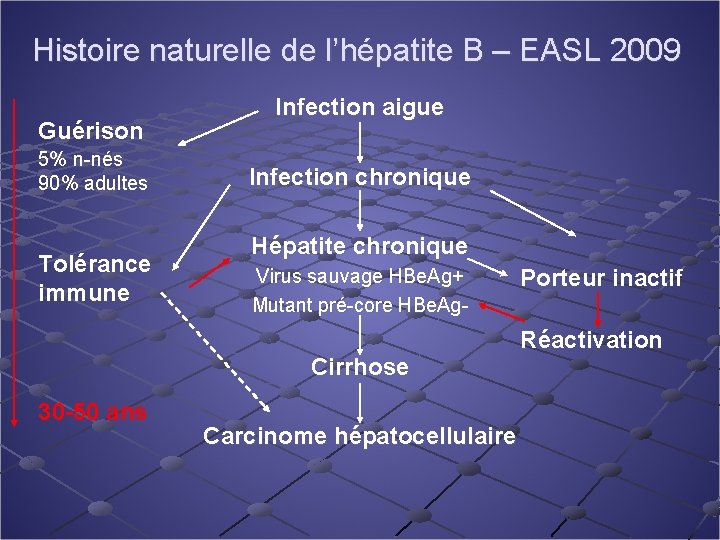
Histoire naturelle de l’hépatite B – EASL 2009 Guérison 5% n-nés 90% adultes Tolérance immune Infection aigue Infection chronique Hépatite chronique Virus sauvage HBe. Ag+ Mutant pré-core HBe. Ag- Cirrhose 30 -50 ans Carcinome hépatocellulaire Porteur inactif Réactivation
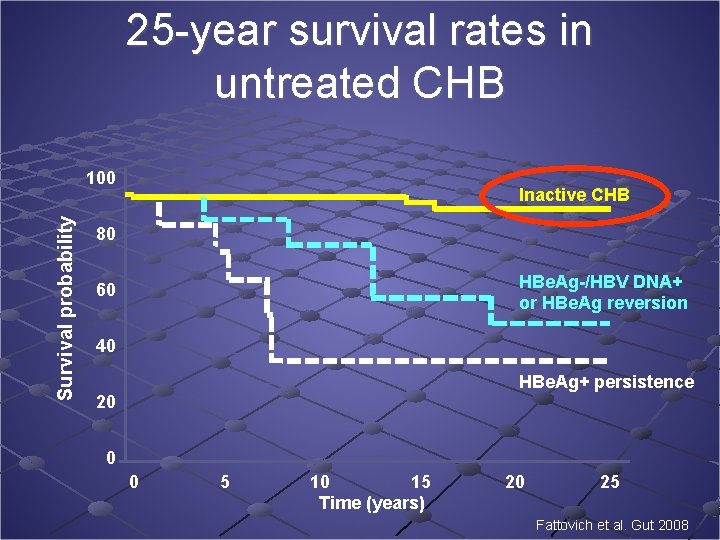
25 -year survival rates in untreated CHB Survival probability 100 Inactive CHB 80 HBe. Ag-/HBV DNA+ or HBe. Ag reversion 60 40 HBe. Ag+ persistence 20 0 0 5 10 15 Time (years) 20 25 Fattovich et al. Gut 2008
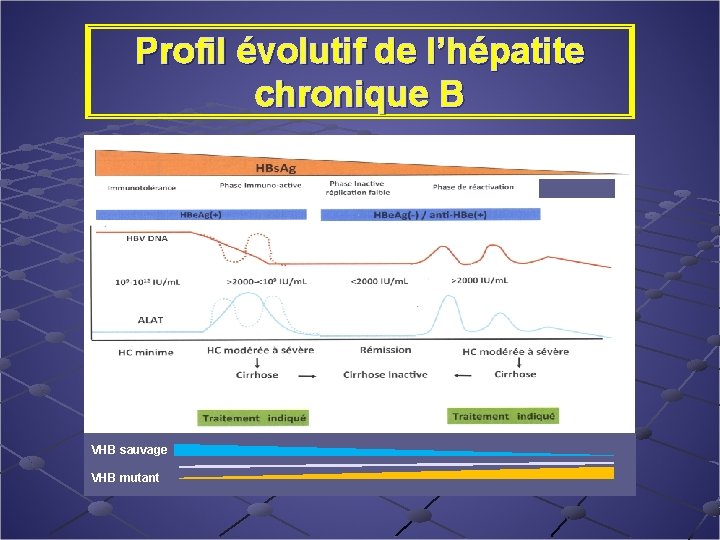
Profil évolutif de l’hépatite chronique B VHB sauvage VHB mutant

• Les 10 questions posées au panel d’experts EASL n n n n n Comment évaluer la maladie hépatique avant le traitement ? Quels sont les buts et les objectifs du traitement Quelle est la définition de la réponse à un traitement? Quelle est l’approche optimale du traitement de premier intention ? Quelles sont les critères prédictifs d’une réponse ? Quelle est la définition de la résistance au traitement et comment la prendre en charge ? Comment suivre le traitement ? Quand arrêter un traitement ? Comment traiter les populations particulières ? Quelques sont les points non- résolus ?

Comment évaluer la maladie hépatique avant le traitement ? Biochimie: n n Transaminases ASAT et ALAT, GGT, phosphatases alcalines, TP Albumine NFS plaquettes Ag HBe Echographie hépatique

ADN du Virus B PCR quantitative en temps réél À exprimer en UI/ml Toujours le même test
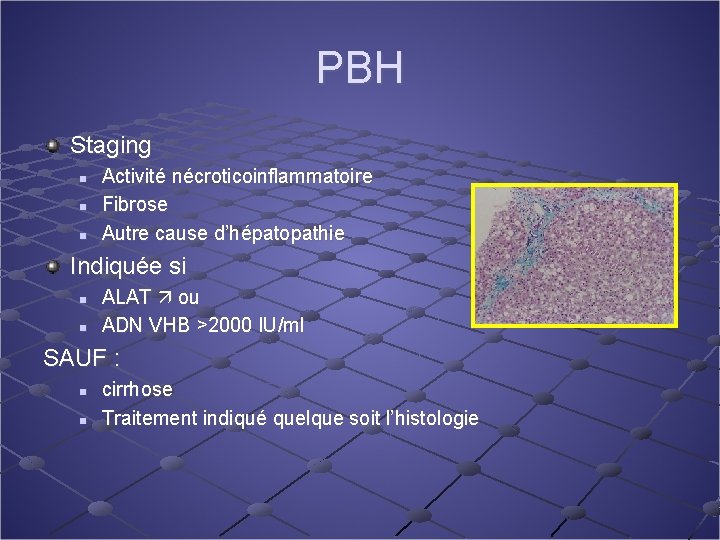
PBH Staging n n n Activité nécroticoinflammatoire Fibrose Autre cause d’hépatopathie Indiquée si n n ALAT ou ADN VHB >2000 IU/ml SAUF : n n cirrhose Traitement indiqué quelque soit l’histologie

Tests non invasifs de fibrose Utilisation de marqueurs non invasifs (tests sanguin, fibroscan) : intéressant pour compléter ou éviter une PBH Fibromètre, fibrotest validés dans l’hépatite B Variable continue (0 -1) pb intéressant dans le suivi de patient non traité

Evaluation des patients avec infection chronique par le VHB Evaluation initiale 1) 2) 3) 4) 5) 6) 7) Examen physique et antécédents Antécédents familiaux de maladie du foie, CHC Tests de laboratoire pour évaluer la maladie du foie – numérations sanguines complètes avec plaquettes, panel hépatique et temps prothrombine Tests de réplication du VHB – Ag. HBe/anti-HBe, ADN VHB Tests pour exclure des co-infections virales – VHC, VHD (chez les personnes de pays où l’infection par le VHD est courante et chez ceux avec des antécédents d’injection de drogues) et VIH chez ceux à risque Tests pour dépister CHC (AFP) et, chez les patients à haut risque échographie Considérer la biopsie du foie pour classer et évaluer la maladie du foie – chez les patients qui ont répondu aux critères d’hépatite chronique AASLD

Buts du traitement de l’hépatite B chronique Améliorer la qualité de vie et la survie en diminuant le risque de progression vers la cirrhose, le CHC, l’insuffisance hépatique en Réduisant au maximum le taux d’ADN du VHB, dans l’idéal au-dessous du seuil de détection (10 -15 UI/ml), ce qui réduit l’activité histologique Mais le virus B ne peut complètement être éradiqué en raison du ccc DNA Chez les patients Ag. HBe positif et Ag. HBe négatif But idéal = négativation de l’Ag. HBs A défaut : ADN VHB indétectable Chez les patients Ag. HBe positifs But satisfaisant = séroconversion HBe A défaut : ADN VHB indétectable

Objectifs du traitement Ag HBe + - AASLD 2007 EASL et AASLD 2009 Séroconversion e e Ag HBs - ADN -/Ag HBs-

Définitions de la réponse au traitement Non réponse primaire n INF α et NUC : définie comme une décroissance <1 log 10 UI/ml de l’ADN VHB après 3 mois de traitement par rapport à la valeur initiale Réponse virologique n INF α : définie comme une concentration d'ADN VHB < 2000 UI/ml à 24 sem de traitement Analogues : définie comme une concentration d’ADN VHB non détectable après 48 sem de traitement

Définitions de la réponse au traitement Réponse virologique partielle n Analogues : définie comme une diminution de l’ADN VHB > 1 log 10 UI/ml, mais non jusqu’à une valeur indétectable Modifier le traitement après 24 semaines pour lamivudine et telbivudine Modifier le traitement après 48 semaines pour produits hautement puissants, entécavir, et ténofovir Echappement virologique / biochimique n Analogues : définie comme une augmentation confirmée de l'ADN VHB > 1 log 10 UI/ml au dessus du nadir (plus basse valeur sous traitement) , après une période de réponse virologique ou ALAT > ULNM après normalisation Rebond virologique Augmentation de l’ADN VHB > 20000 UI/ml ou > valeur prétraitt après une période de réponse virologique
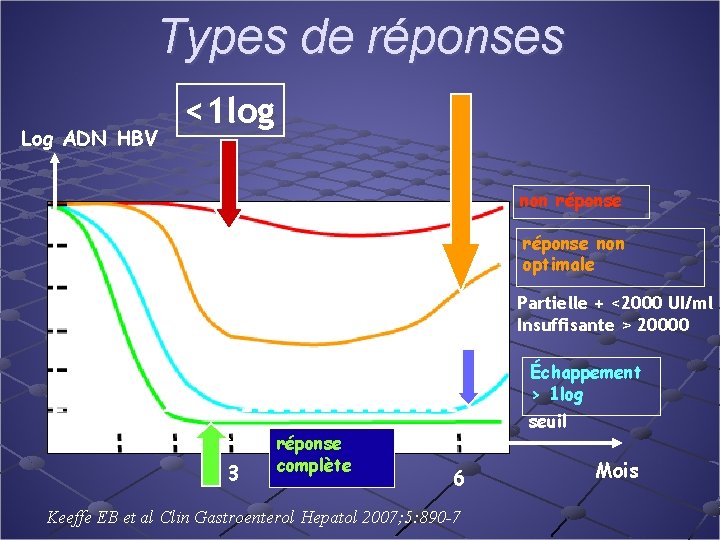
Types de réponses Log ADN HBV <1 log non réponse non optimale Partielle + <2000 UI/ml Insuffisante > 20000 Échappement > 1 log 3 réponse complète seuil 6 Keeffe EB et al Clin Gastroenterol Hepatol 2007; 5: 890 -7 Mois

Indication des traitements Identique pour Ag. HBe positif et Ag. HBe négatif ADN VHB > 2000 UI/ml ou 3, 3 log UI (environ 10 000 copies/ml ou 4 log copies) Et/ou ALAT > LSN Et PBH ou marqueurs non invasifs quand validés : A 2 ou F 2 (Métavir)

Critères d’indication de traitement Ag HBe + ou ADN UI/ml ALT AASLD 2007 >20 000 4 log > 2 N APASL 2008 >20 000 4 log > 2 N EASL 2009 >2 000 3, 3 log > N
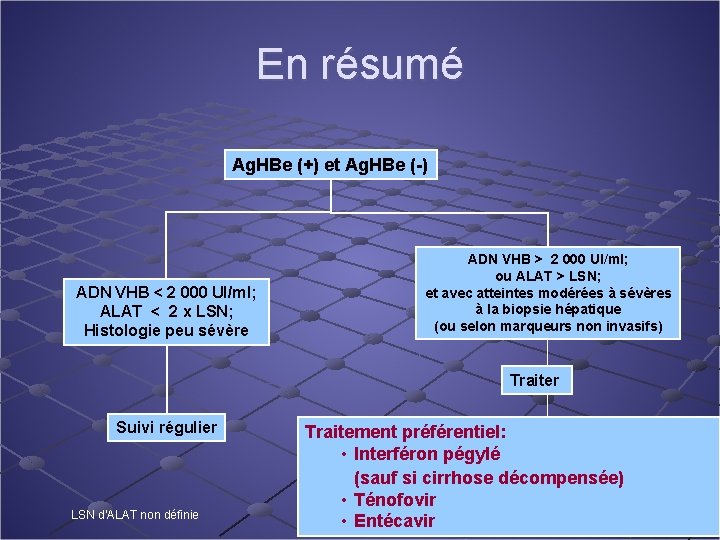
En résumé Ag. HBe (+) et Ag. HBe (-) ADN VHB < 2 000 UI/ml; ALAT < 2 x LSN; Histologie peu sévère ADN VHB > 2 000 UI/ml; ou ALAT > LSN; et avec atteintes modérées à sévères à la biopsie hépatique (ou selon marqueurs non invasifs) Traiter Suivi régulier LSN d’ALAT non définie Traitement préférentiel: • Interféron pégylé (sauf si cirrhose décompensée) • Ténofovir • Entécavir
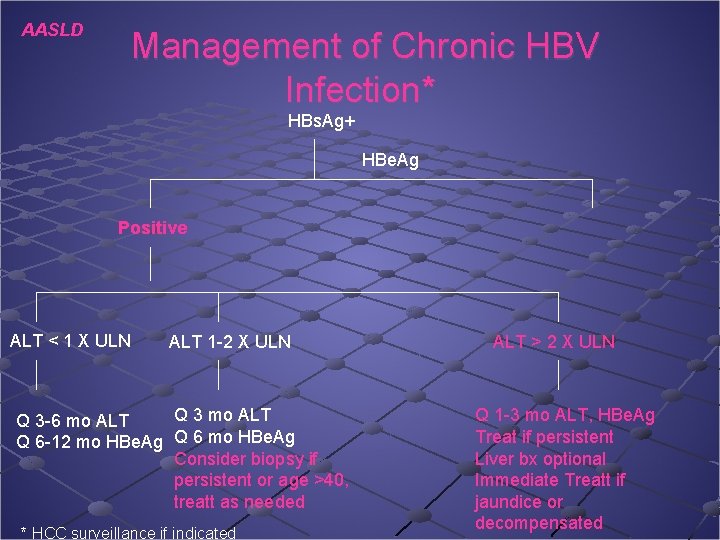
AASLD Management of Chronic HBV Infection* HBs. Ag+ HBe. Ag Positive ALT < 1 X ULN ALT 1 -2 X ULN Q 3 mo ALT Q 3 -6 mo ALT Q 6 -12 mo HBe. Ag Q 6 mo HBe. Ag Consider biopsy if persistent or age >40, treatt as needed * HCC surveillance if indicated ALT > 2 X ULN Q 1 -3 mo ALT, HBe. Ag Treat if persistent Liver bx optional Immediate Treatt if jaundice or decompensated
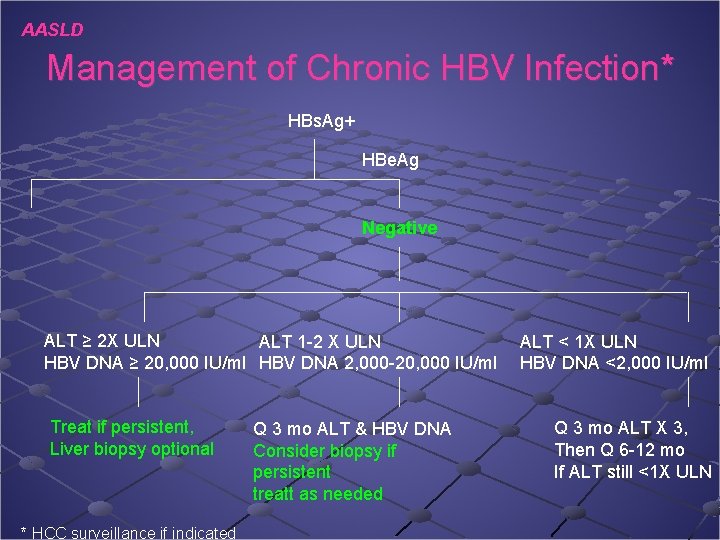
AASLD Management of Chronic HBV Infection* HBs. Ag+ HBe. Ag Negative ALT ≥ 2 X ULN ALT 1 -2 X ULN HBV DNA ≥ 20, 000 IU/ml HBV DNA 2, 000 -20, 000 IU/ml Treat if persistent, Liver biopsy optional * HCC surveillance if indicated Q 3 mo ALT & HBV DNA Consider biopsy if persistent treatt as needed ALT < 1 X ULN HBV DNA <2, 000 IU/ml Q 3 mo ALT X 3, Then Q 6 -12 mo If ALT still <1 X ULN
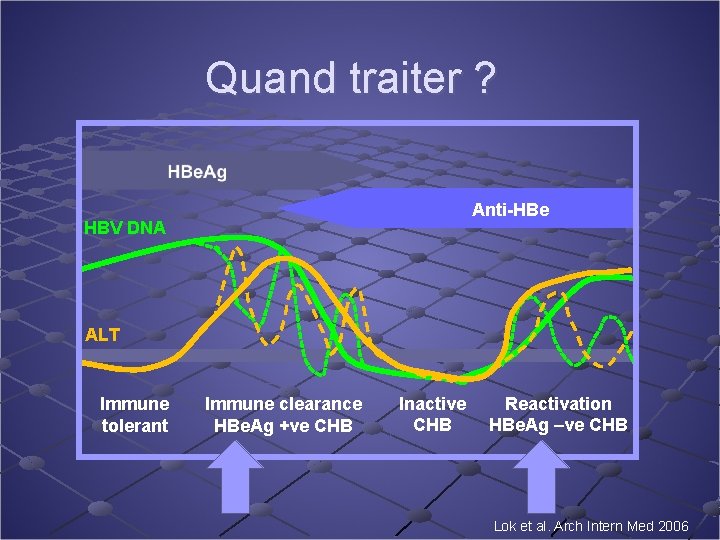
Quand traiter ? Anti-HBe HBV DNA ALT Immune tolerant Immune clearance HBe. Ag +ve CHB Inactive CHB Reactivation HBe. Ag –ve CHB Lok et al. Arch Intern Med 2006

Les options thérapeutiques 7 molécules commercialisées à ce jour n Interféron α remplacé aujourd’hui par l’Interféron Pégylé α n lamivudine n adéfovir dipivoxil n Entecavir n Telbivudine (AMM USA + Suisse) n Ténofovir, n Emtricitabine Des molécules en développement
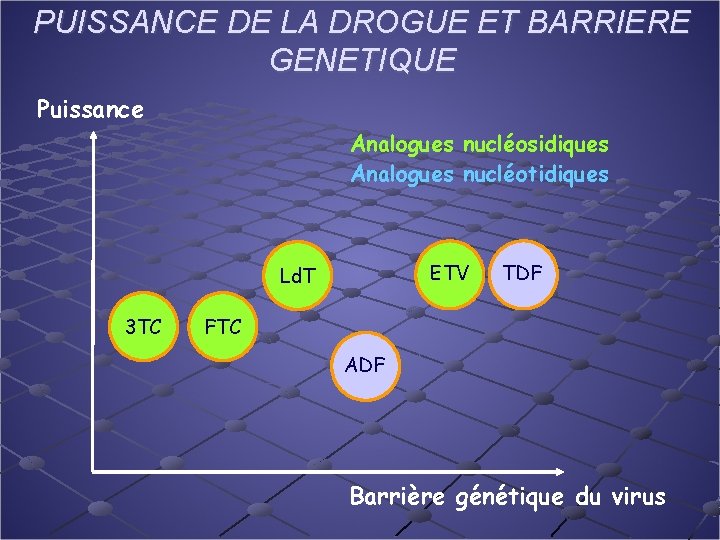
PUISSANCE DE LA DROGUE ET BARRIERE GENETIQUE Puissance Analogues nucléosidiques Analogues nucléotidiques ETV Ld. T 3 TC TDF FTC ADF Barrière génétique du virus
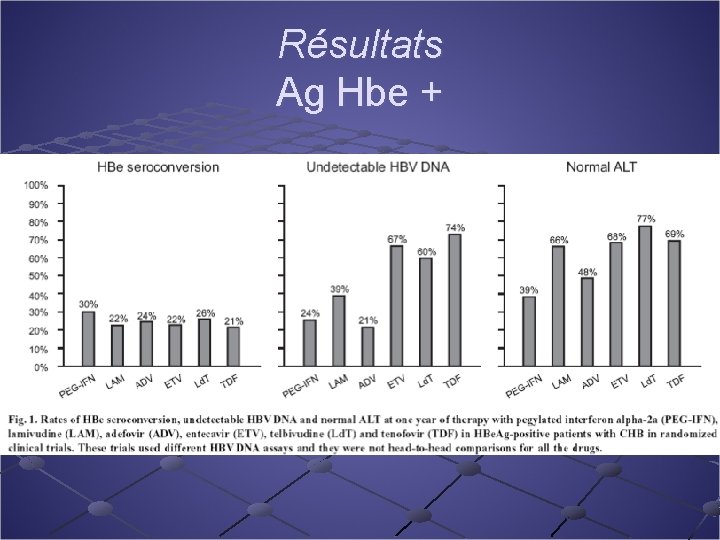
Résultats Ag Hbe +
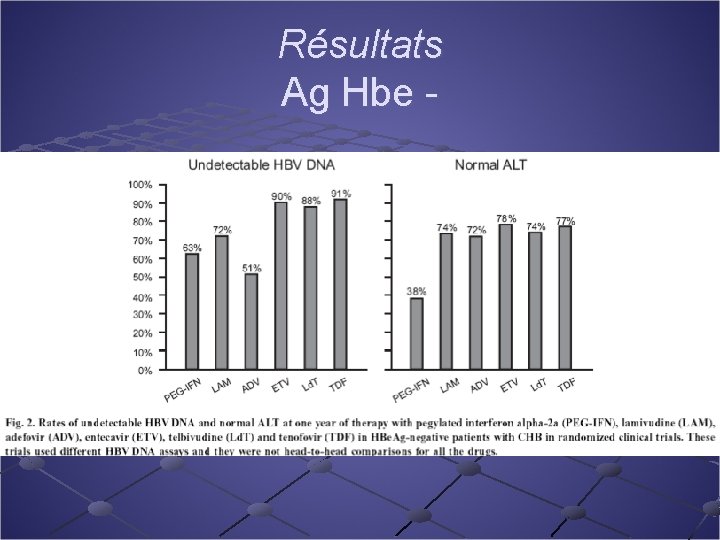
Résultats Ag Hbe -

Interferon Facteurs prédictifs de séroconversion e, patient Ag. HBe + Traitement Avant Pendant ADN Autres < 107 IU/ml or 7 log 10 IU/ml ALT > 3 ULN A 2 < 20, 000 UI/ml à S 12 (50% chance) -
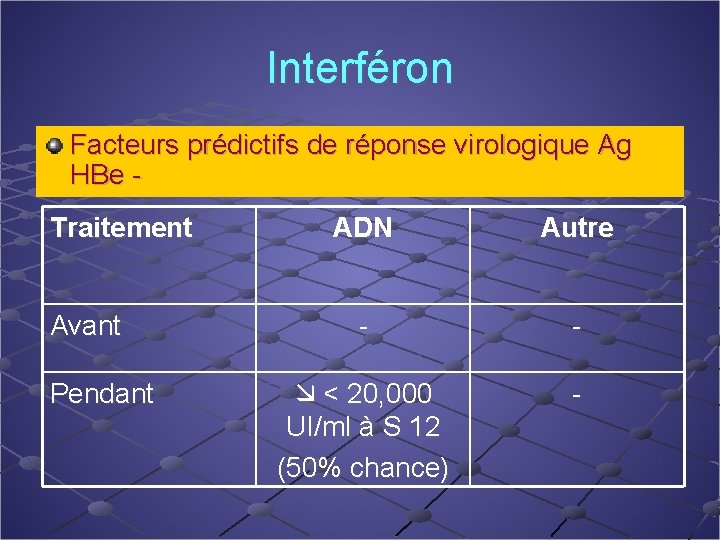
Interféron Facteurs prédictifs de réponse virologique Ag HBe Traitement Avant Pendant ADN Autre - - < 20, 000 UI/ml à S 12 (50% chance) -
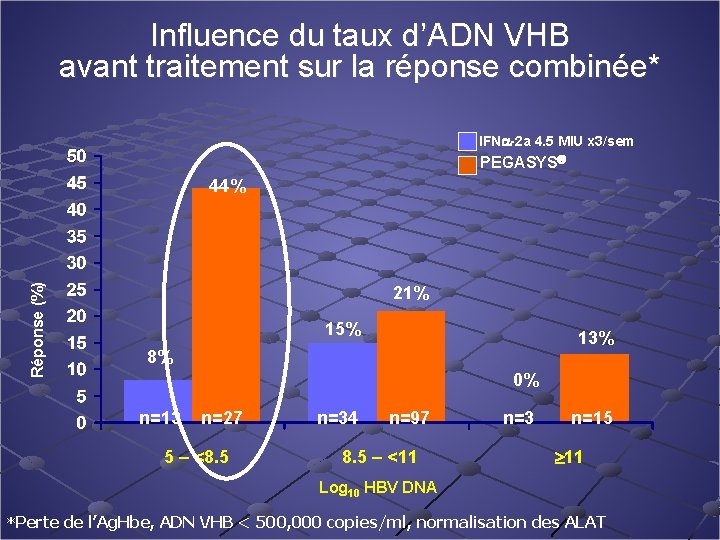
Influence du taux d’ADN VHB avant traitement sur la réponse combinée* IFN -2 a 4. 5 MIU x 3/sem PEGASYS Réponse (%) 44% 21% 15% 13% 8% 0% n=13 n=27 5 – <8. 5 n=34 n=97 8. 5 – <11 n=3 n=15 11 Log 10 HBV DNA *Perte de l’Ag. Hbe, ADN VHB < 500, 000 copies/ml, normalisation des ALAT

Cinétique ADN VHB sous Pegasys et séroconversion HBe 12 ADN VHB moyen (log 10 cp/ml) Traitement Période de Survenue séroconversion HBe Suivi 10 Pas de séroconversion HBe à S 72 (n = 184) 8 6 -3, 8 log 10 cp/ml Séroconversion HBe à S 72 (n = 87) 4 10 000 cp/ml -5, 84 log 10 cp/ml 2 33 % 0 0 12 29 % 24 36 48 Semaine 38 % 60 2, 30 log 10 cp/ml Séroconversion HBe et HBs à S 72 (n = 8) 72 Cinétique de l’ADN VHB sous Pegasys en monothérapie En fonction de la séroconversion HBe et HBs EASL 2006 – T. Piratvisuth, abstract 49
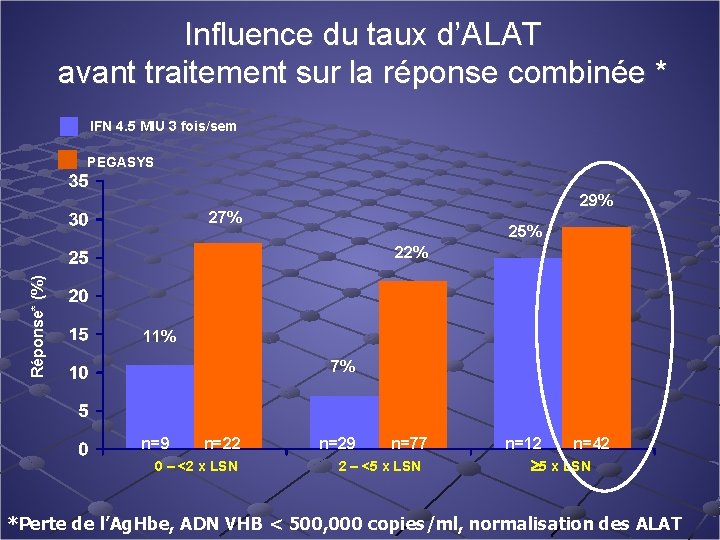
Influence du taux d’ALAT avant traitement sur la réponse combinée * IFN 4. 5 MIU 3 fois/sem PEGASYS 29% 27% 25% Réponse* (%) 22% 11% 7% n=9 n=22 0 – <2 x LSN n=29 n=77 2 – <5 x LSN n=12 n=42 5 x LSN *Perte de l’Ag. Hbe, ADN VHB < 500, 000 copies/ml, normalisation des ALAT
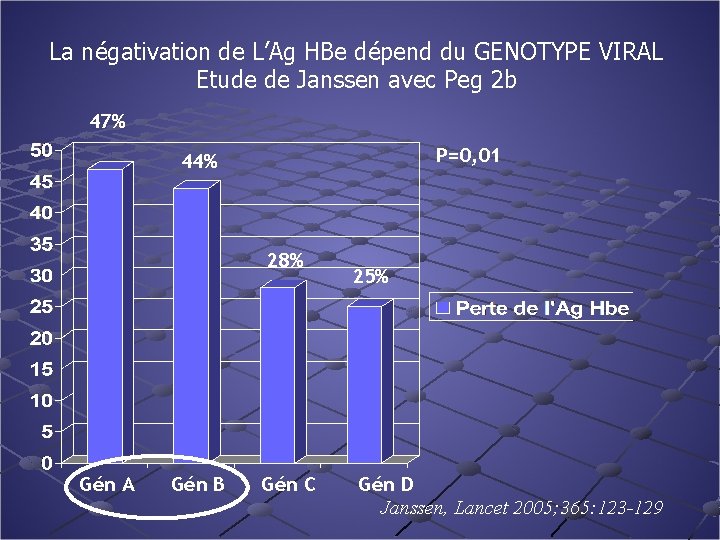
La négativation de L’Ag HBe dépend du GENOTYPE VIRAL Etude de Janssen avec Peg 2 b 47% P=0, 01 44% 28% Gén A Gén B Gén C 25% Gén D Janssen, Lancet 2005; 365: 123 -129

Génotype du VHB Une meilleure réponse à l'interféron alpha a été rapportée pour les génotypes A et B du VHB par rapport aux génotypes C et D mais le génotype seul n’est pas un élément suffisant pour recommander l’interféron Pas d’influence du génotype pour la réponse aux analogues

Analogues Facteurs prédictifs de séroconversion e, patient Ag. HBe + Traitement HBVDNA Autres Avant Pendant (L, A, T) < 107 IU/ml or 7 ALT > 3 ULN log 10 IU/ml A 2 indétectable à S 24 or 48 * -
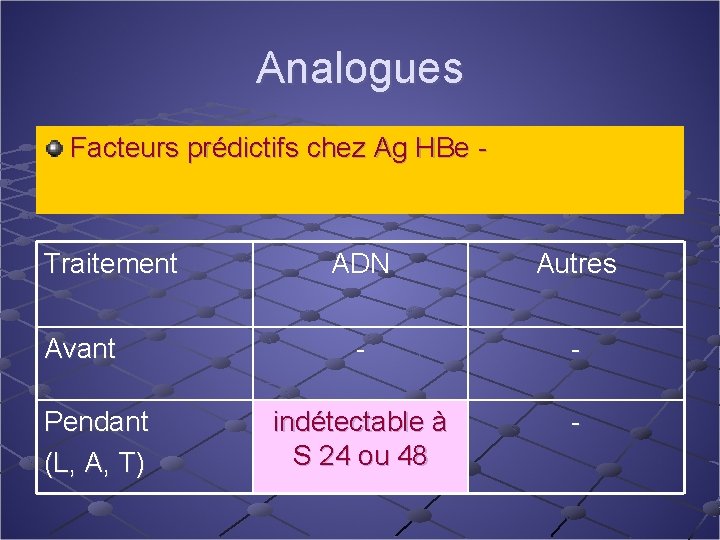
Analogues Facteurs prédictifs chez Ag HBe - Traitement Avant Pendant (L, A, T) ADN Autres - - indétectable à S 24 ou 48 -

TRAITEMENT DE L’HÉPATITE CHRONIQUE B DEUX STRATEGIES • INTERFERON Action antivirale et immunomodulatrice • ANALOGUES Action antivirale Durée limitée Durée indéfinie RÉPONSE PROLONGÉE RÉPONSE MAINTENUE Perte de l’Ag HBs non négligeable Perte de l’Ag HBs faible Pas de résistance Résistance avec perte du bénéfice ttt Constitution de réservoirs de virus multirésistants Rôle du génotype Tolérance médiocre Pas de Rôle du génotype Tolérance bonne
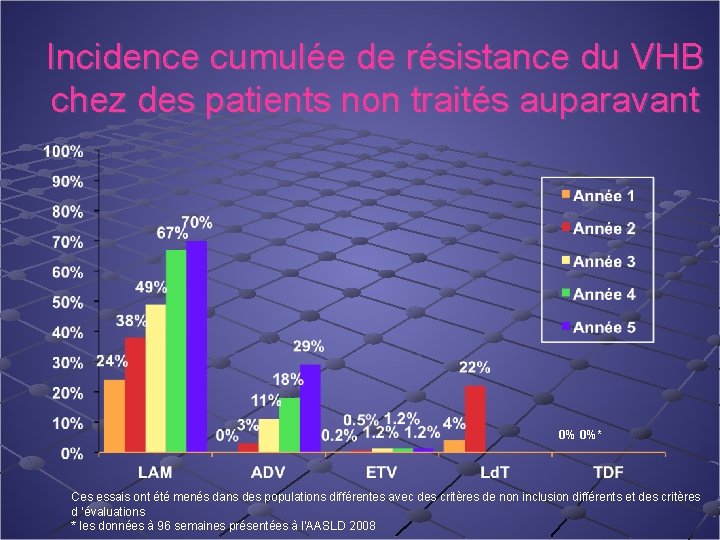
Incidence cumulée de résistance du VHB chez des patients non traités auparavant 0% 0%* Ces essais ont été menés dans des populations différentes avec des critères de non inclusion différents et des critères d ’évaluations * les données à 96 semaines présentées à l’AASLD 2008
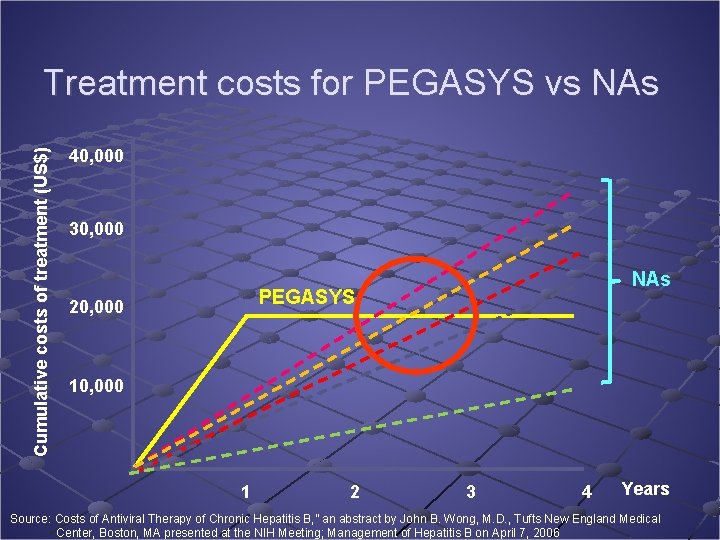
Cumulative costs of treatment (US$) Treatment costs for PEGASYS vs NAs 40, 000 30, 000 NAs PEGASYS 20, 000 1 2 3 4 Years Source: Costs of Antiviral Therapy of Chronic Hepatitis B, ” an abstract by John B. Wong, M. D. , Tufts New England Medical Center, Boston, MA presented at the NIH Meeting; Management of Hepatitis B on April 7, 2006
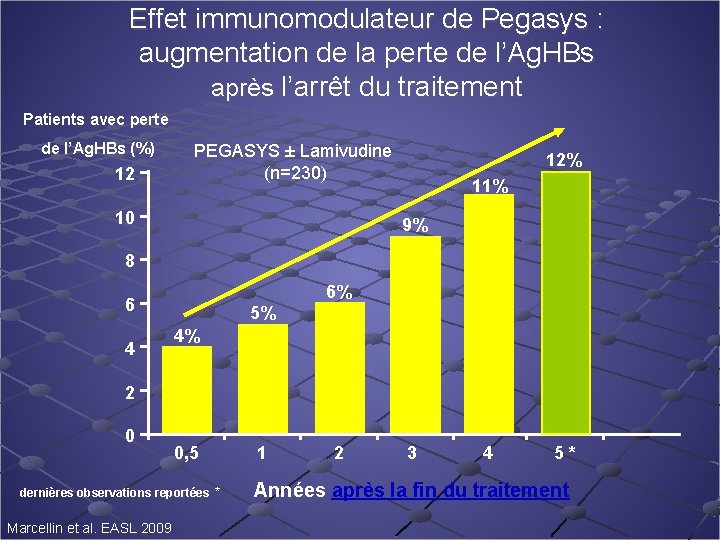
Effet immunomodulateur de Pegasys : augmentation de la perte de l’Ag. HBs après l’arrêt du traitement Patients avec perte de l’Ag. HBs (%) 12 PEGASYS ± Lamivudine (n=230) 10 12% 11% 9% 8 6% 6 4 5% 4% 2 0 0, 5 dernières observations reportées * Marcellin et al. EASL 2009 1 2 3 4 5 * Années après la fin du traitement

En pratique Patients Naïfs, jeunes, sans cirrhose n n Traitement par interféron alpha 2 a de première intention (car tt de durée définie), surtout si génotype A Analogues Si patient ne souhaitant pas l’interféron Si échec de l’interféron Si contre indication ou mauvaise tolérance de l’IFN

Critères d’arrêt du traitement Par interféron alpha pégylé : durée limitée 48 semaines n Ag. HBe(+) Objectif souhaité = séroconversion HBe avec ALAT< LSN et ADN VHB < 2000 UI/ml (si possible indétectable) Anti-HBe à vérifier à S 24 et S 48 puis 24 semaines après l’arrêt du traitement. Ag. HBs à vérifier tous les 6 mois après séroconversion HBe si l’ADN VHB est indétectable n Ag. HBe(-) Objectif souhaité = ADN VHB < 2000 UI/ml (si possible indétectable) L’efficacité et la tolérance doivent être vérifiées de la même façon pendant 48 semaines de traitement Ag. HBs doit être vérifié tous les 6 mois si l'ADN VHB est indétectable

Critères d’arrêt du traitement Par analogue n Ag. HBe(+) Indétectabilité ADN VHB et séroconversion HBe consécutive sont associées à des réponses biochimiques et histologiques. Le traitement par analogue peut être arrêté 6 à 12 mois après séroconversion HBe. Ag. HBs doit être vérifié tous les 6 mois après séroconversion HBe

Critères d’arrêt du traitement Par analogue n Ag. HBe(-) ?

Échec thérapeutique et recommandations Non réponse primaire (< 1 log à 12 sem) n Adéfovir : → remplacer par Ténofovir ou Entécavir n Lamivudine, Telbivudine, Entécavir ou Ténofovir : →vérifier l’observance →chez les patients observants, recher des mutations du VHB conférant une résistance
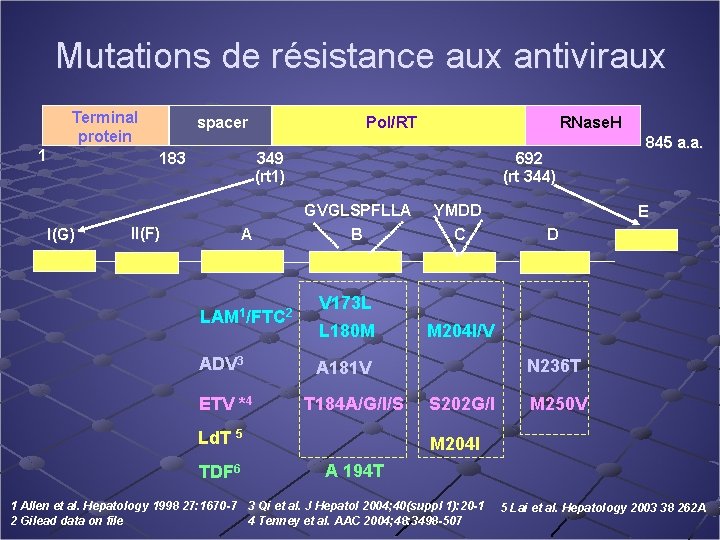
Mutations de résistance aux antiviraux Terminal protein 1 I(G) spacer 183 Pol/RT RNase. H 349 (rt 1) II(F) A LAM 1/FTC 2 ADV 3 ETV *4 692 (rt 344) GVGLSPFLLA B E D V 173 L L 180 M M 204 I/V N 236 T A 181 V T 184 A/G/I/S S 202 G/I M 250 V Ld. T 5 TDF 6 YMDD C 845 a. a. M 204 I A 194 T 1 Allen et al. Hepatology 1998 27: 1670 -7 3 Qi et al. J Hepatol 2004; 40(suppl 1): 20 -1 2 Gilead data on file 4 Tenney et al. AAC 2004; 48: 3498 -507 5 Lai et al. Hepatology 2003 38 262 A

Échec thérapeutique et recommandations Réponse virologique partielle ( ADN du VHB non indétectable à 24 sem) →Vérifier l’observance n Lamivudine, Adéfovir ou Telbivudine (24 sem) Remplacer par Ténofovir ou Entécavir Ou Ajouter Ténofovir à Lamivudine Ténofovir à Telbivudine Entécavir à Adéfovir

Échec thérapeutique et recommandations Echappement virologique n n Risque chez patients traités par adéfovir ou lamivudine avec ADN avant traitement élevé , Diminution lente de la charge virale B Un échappement virologique chez un patient observant est lié à une résistance virale La résistance doit être identifiée dès que possible avant un échappement clinique (augmentation d’ALAT) au moyen d’une surveillance de l’ADN VHB Le traitement doit être adapté dès la remontée de la charge virale.

Résistance du VHB aux antiviraux : Recommandations de traitement Résistance Lamivudine-R Traitement de sauvetage ajouter Ténofovir Remplacer par Ténofovir et ajouter : - Lamivudine, Entécavir ou Telbivudine Adéfovir-R si N 236 T - Entécavir si A 181 T/V Remplacer par Ténofovir/Emtricitabine Telbivudine-R ajouter Ténofovir Entécavir-R ajouter Ténofovir-R (non observé à ce jour) ajout Entécavir, Telbivudine, Lamivudine ou Emtricitabine

Cas particuliers

Pas de traitement Patients immunotolérants (pas de PBH) Patients avec hépatite B minime n ALAT < 2 N et PBH (< A 2 F 2)

Suivi suggéré chez les patients non considérés pour un traitement Ag. HBe+, ADN VHB >20, 000 IU: ml et ALT normale • ALT q 3 -6 mois, plus souvent si ALT devient élevée • Si les niveaux de ALT sont entre 1 -2 X ULN, revérifier ALT q 1 -3 mois; considérer la biopsie du foie si âge>40 ans, ALT limite ou un peu élevée sur des tests répétés Envisager un traitement si la biopsie montre une inflammation modérée/sévère ou une fibrose significative • Si ALT>2 X ULN >6 mois et Ag. HBe+, ADN VHB > 20, 000 IU/ml, envisager une biopsie du foie et un traitement • Envisager un dépistage du CHC chez les populations concernées AASLD

Suivi des porteurs inactifs du VHB • • • ALT q 3 mois pendant 1 an, si normal, ALTq 6 -12 mois Si ALT >1 -2 X ULN, vérifier le niveau ADN VHB et exclure les autres causes de maladie du foie Envisager une biopsie du foie si ALT limite ou un peu élevée sur des tests répétés ou si ADN du VHB persistant ≥ 2, 000 IU/ml. Envisager un traitement si la biospie montre une inflammation sévère/modérée ou une fibrose significative Envisager un dépistage du CHC chez les populations concernées AASLD

Cirrhose compensée Et ADN du VHB détectable Doivent être traités Entécavir ou ténofovir Même si : n n ALAT < N et/ou ADN < 2000 IU/ml (i. e. 10, 000 copies/ml)

Cirrhose décompensée Traitement anti viral B urgent Envisager une tranplantation Traitement par entécavir ou ténofovir

Association ? Recommandations de quelques experts en cas de cirrhose décompensée ou chez des patients ayant des charges virales B hautes Pas de preuve scientifique Tenofovir plus Lamivudine, ou Tenofovir plus Emtricitabine (Truvada)

Populations particulières Femme enceinte : possibilité de diminuer la charge virale B dernier trimestre n n n Lamivudine, adéfovir et entécavir sont listés dans la catégorie C de la classification de la FDA relative à la grossesse mais études uniquement sur lamivudine Ténofovir et telbivudine sont listés en catégorie B données sur la sécurité d’emploi chez des femmes enceintes infectées par le VIH ayant reçu ténofovir et/ou lamivudine ou emtricitabine

Recommandations AASLD pour le traitement des patients avec co-infection VHB/VIH Les patients qui ont répondu aux critères de l’Hépatite B chronique devraient être traités La biopsie du foie devrait être envisagée chez les patients avec ALT fluctuante ou peu élevée (1 -2 X normal) Les patients qui ne sont pas sous HAART et pour lesquels il n’est pas prévu de HAART dans le futur proche devraient être traités par une thérapie antivirale qui ne cible pas le VIH, telle que peg. IFN-α ou adefovir. Bien que la telbivudine ne cible pas le VIH, elle ne devrait pas être utilisée dans ce cas. AASLD

Recommandations AASLD pour le traitement des patients avec co-infection VHB/VIH Les patients chez qui le traitement à la fois pour le VHB et le VIH est planifié devraient recevoir 1 traitement efficace contre les 2 virus : lamivudine + tenofovir ou emtricitabine + tenofovir sont préconisées. Chez les patients avec une résistance à la lamivudine, le tenofovir sera ajouté. Quand les traitement ARV sont changés, les médicaments qui sont efficaces contre le VHB ne devraient pas être arrêtés sans remplacement par un autre médicament actif sur le VHB, à moins que le patient ait fait une séroconversion HBe et ait eu un traitement de consolidation AASLD

Populations particulières Traitement pré-emptif d ‘une réactivation (avant immunosuppresseurs ou chimiothérapie) n n screening de tout patient candidat à un traitement (Ag HBs, Ac HBc) Vaccination anti VHB recommandée si patients séronégatifs Ag. HBs+ : dosage ADN VHB et traitement par analogue à débuter avant puis 12 mois après arrêt de la chimio ou immunosuppresseurs Si charge virale B peu élevée: Lamivudine Si charge virale B élevée: Ténofovir ou entécavir Si patients anti-HBc isolé et ADN indétectable, surveillance des transaminases et ADN du VHB

Recommandations AASLD pour le traitement des patients avec Hépatite B symptomatique aigue Le traitement est seulement indiqué chez les patients avec hépatite B fulminante et ceux avec hépatite B sévère aigue, prolongée La lamivudine ou telbivudine doivent être utilisées quand la durée anticipée du traitement est courte; sinon l’entécavir est recommandé Le traitement devrait être prolongé jusqu’à confirmation de la clairance de l’ Ag. HBs ou indéfiniment chez ceux qui ont subi une transplantation L’IFN-α est contre-indiqué

Recommandations pour Dépistage CHC (AASLD) Porteurs du VHB à haut risque de CHC : 1. Hommes de type asiatique de plus de 40 ans et femmes asiatiques de plus de 50 ans, 2. personnes avec une cirrhose, 3. personnes avec des antécédents familiaux de CHC, 4. Africains de plus de 20 ans, 5. tout porteur de plus de 40 ans avec une élévation ALT intermittente ou persistante et/ou niveau élevé ADN VHB >2, 000 IU/ml devraient être dépistés avec examen US tous les 6 -12 mois. (II-2) Pour les porteurs du VHB à haut risque de CHC qui vivent dans des zones où l’echographie n’est pas facilement disponible, un dépistage périodique avec AFP devrait être étudié. (II-2)

C’EST FINI !

Hépate B « résolutive» Définition n HC connue Ag HBs + > 6 mois ou Ac HBc+, anti HBs +/Ag HBs– ADN VHB indetectable n Transaminases normales de façon persistante n n Lok, Hepatology 2009

Hépatites B « occultes » Définition : Réplication virale VHB en l’absence d’Ag HBs détectable Pathogénicité ? Transmission : Transfusion Mère enfant Greffon* Risque de réactivation en cas d’immunodépression (formes réactivées : le plus souvent Ag. HBs se positive) Hoofnagle et al, NEJM, 1978

Ag HBe + : IFN réduit le risque de cirrhose et de CHC Etude prospective cohorte 233 pts traités par IFN vs 233 contrôles non traités Suivi 11 ans (médiane 6, 8 ans 1, 1 -16, 5 ans) 30 Cirrhose 40 p = 0, 04 33, 7 % Groupe contrôle 30 17, 8 % 20 Groupe IFN 10 Incidence cumulée de CHC (%) Incidence cumulée de cirrhose (%) 50 CHC p = 0, 01 20 12, 5 % Groupe contrôle 10 2, 7 % Groupe IFN 0 0 0 48 96 144 Mois 192 216 0 48 96 144 192 216 Mois EASL 2006 – S. M. Lin, abstract 48

La séroconversion HBe réduit le risque de cirrhose et de CHC Etude prospective cohorte 233 pts traités par IFN vs 233 contrôles non traités Suivi 11 ans (médiane 6, 8 ans 1, 1 -16, 5 ans) CL NSC vs CL SC p = 0, 031 vs IFN SC p = 0, 023 vs IFN NSC p = 0, 065 40 30 Groupe contrôle sans séroconversion HBe 30 Groupe IFN sans Séroconversion HBe 20 Groupe contrôle avec séroconversion HBE 10 Groupe IFN avec séroconversion HBe Incidence cumulée de CHC (%) Incidence cumulée de cirrhose (%) 50 0 CL NSC vs CL SC p = 0, 009 vs IFN SC p = 0, 003 IFN SC vs IFN NSC p = 0, 014 Groupe contrôle sans séroconversion HBe 20 Groupe IFN sans Séroconversion HBe 10 Groupe contrôle avec séroconversion HBE 0 Groupe IFN avec séroconversion HBe -5 0 48 96 144 Mois 192 216 0 48 96 144 192 216 Mois EASL 2006 – S. M. Lin, abstract 48
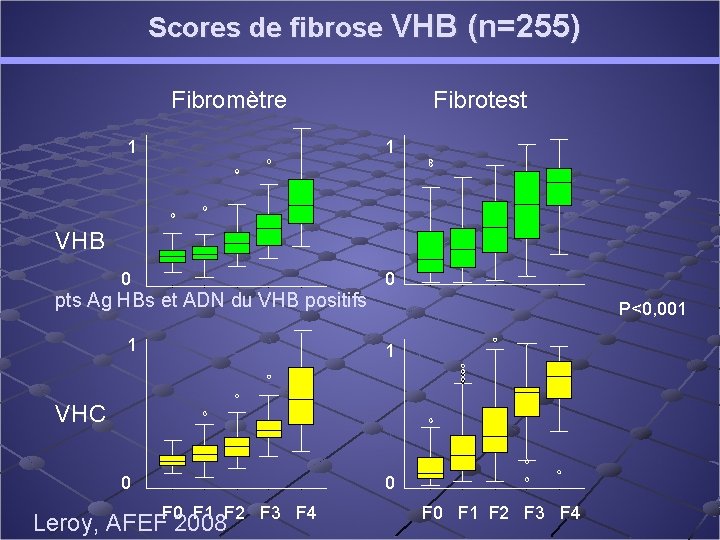
Scores de fibrose VHB (n=255) Fibromètre 1 Fibrotest 1 VHB 0 pts Ag HBs et ADN du VHB positifs 1 0 P<0, 001 1 VHC 0 0 F 1 F 2 F 3 F 4 F 0 F 1 F 2 F 3 F 4 Leroy, AFEF 2008

Compteurs des Fibro. Mètres Fibro. Mètre score F virus Fibro. Mètre aire virus
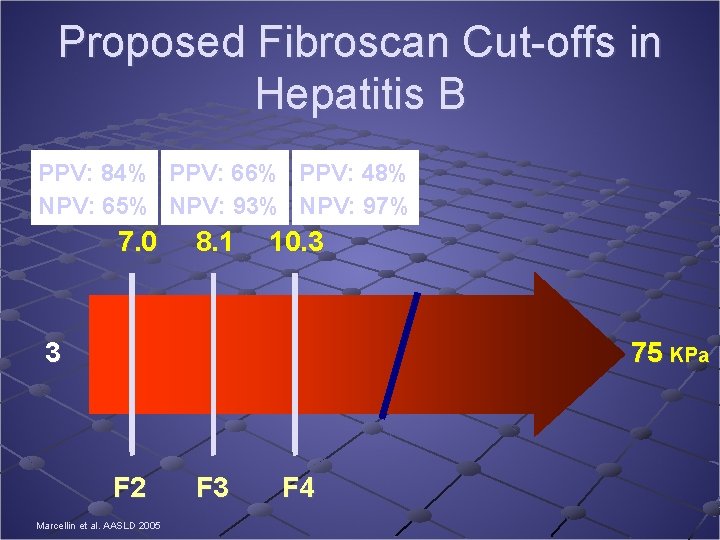
Proposed Fibroscan Cut-offs in Hepatitis B PPV: 84% PPV: 66% PPV: 48% NPV: 65% NPV: 93% NPV: 97% 7. 0 8. 1 10. 3 3 75 KPa F 2 Marcellin et al. AASLD 2005 F 3 F 4
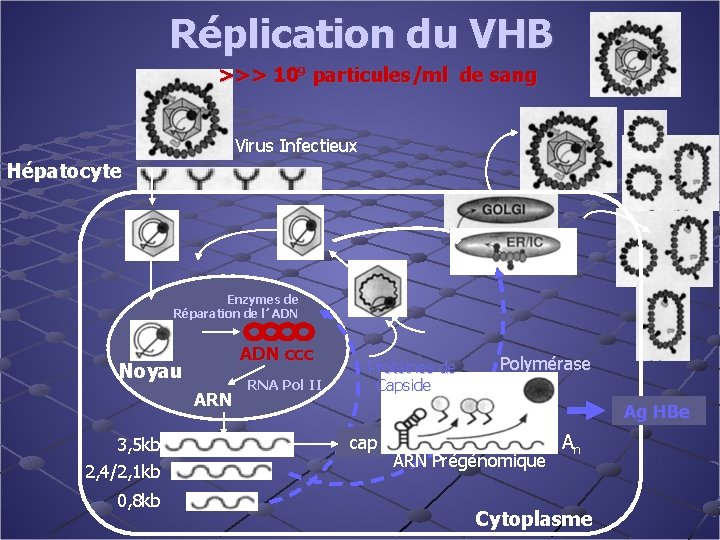
Réplication du VHB >>> 109 particules/ml de sang Virus Infectieux Hépatocyte Enzymes de Réparation de l’ ADN ccc Noyau ARN 3, 5 kb 2, 4/2, 1 kb 0, 8 kb RNA Pol II Protéines de Capside Polymérase cap Ag HBe ARN Prégénomique An Cytoplasme

Groupes à haut risque d’une infection par le AASLD VHB qui devraient être dépistés (1) Les individus nés dans des zones de taux de prévalence haute* ou intermédiaire† du VHB incluant les immigrants et les enfants adoptés‡§ - Asie : tous les pays Afrique : tous les pays Iles du Sud Pacifique : tous les pays Moyen Orient (sauf Chypre et Israël) Méditerranée (Europe) : Malte et Espagne Arctique (indigènes d’Alaska, du Canada et du Groenland) Amérique du Sud : Equateur, Guyane, Suriname, Venezuela et régions amazones de Bolivie, Brésil, Colombie et Pérou) - Europe de l’Est : tous les pays sauf la Hongrie - Caraïbes : Antigua et Barbude, République Dominicaine, Granada, Haïti, Jamaïque, St Kitts and Nevis, Ste Lucie, Turks and Caicos - Amérique centrale : Guatemala et Honduras *Prévalence Ag. HBs 8% †Prévalence Ag. HBs 2 -7% ‡Si personnes Ag. HBs positives sont trouvées dans la première génération, les générations suivantes devront être testées §Ceux qui sont séronégatifs devront recevoir le vaccin de l’hépatite B

AASLD Groupes à haut risque d’une infection par le VHB qui devraient être dépistés (2) - Autres groupes recommandés pour le dépistage Personnes nées aux Etats-Unis non vaccinées telles que les enfants dont les parents sont nés dans des régions de forte endémie du VHB (≥ 8%) Contacts familials et sexuels de personnes positives Ag. HBs§ Personnes qui ont déjà eu des injections de médicaments§ Personnes avec de multiples partenaires sexuels ou antécédent de maladie sexuellement transmissible§ Hommes homosexuels§ détenus Individus avec ALT ou AST chroniquement élevés§ Individus infectés par le VHC ou le VIH§ Patients sous dialyse rénale§ Toutes les femmes enceintes Personnes nécessitant une thérapeutique immusuppressive *Prévalence Ag. HBs 8% †Prévalence Ag. HBs 2 -7% ‡Si personnes Ag. HBs positives sont trouvées dans la première génération, les générations suivantes devront être testées §Ceux qui sont séronégatifs devront recevoir le vaccin de l’hépatite B

Recommandations pour les personnes infectées concernant la prévention de la transmission du VHB Les personnes qui sont Ag. HBs positives devraient : - Avoir des rapports sexuels avec des personnes vaccinées - Utiliser une protection lors des rapports sexuels si le partenaire n’est pas vacciné ou naturellement immunisé - Ne pas partager de brosses à dents ou rasoirs - Nettoyer les blessures avec un détergent ou eau de javel - Ne pas donner leur sang, organes ou sperme Les enfants et les adultes qui sont Ag. HBs+ : - Peuvent participer à toutes les activités y compris les sports de contact - Ne devraient pas être exclus des crèches ou de l’école et ne devraient pas être isolés des autres enfants - Peuvant partager des aliments, ustensiles et embrasser les autres AASLD

Recommandations pour le suivi et la prévention de l’Hépatite B des individus avec infection chronique par le VHB (1) Les porteurs devraient être suivis ( prévention de la transmission du VHB) Les contacts familials et sexuels des porteurs, négatifs pour les marqueurs du VHB devraient être vaccinés Les nouveaux-nés des mères infectées par le VHB devraient recevoir le vaccin +HBIG à la naissance et effectuer les rappels recommandés Les personnes qui restent à risque pour l’infection du VHB telles que les enfants de mères Ag. HBs+, le personnel de santé, les patients dialysés et les partenaires sexuels de porteurs devraient être testés en terme de réponse à la vaccination

Recommandations pour les personnes infectées concernant la prévention de la transmission du VHB (2) Le test de post vaccination devrait être réalisé entre 9 et 15 mois chez les enfants de mères porteuses et 1 à 2 ans après la dernière dose chez les autres personnes Le test de suivi de réponse au vaccin est recommandé annuellement chez les patients sous hémodialyse chronique L’abstinence ou l’usage seulement limité d’alcool est recommandé chez les porteurs de l’hépatite B Les personnes qui sont seulement anti-HBc positives et qui sont dans une zone de faible endémie sans facteurs de risque du VHB devraient recevoir une vaccination anti VHB AASLD

Recommandations AASLD pour le traitement des porteurs de l’hépatite B qui nécessitent un traitt immunosuppresseur ou cytotoxique Les tests Ag. HBs et anti-HBc devraient être réalisés chez les patients à haut risque d’infection par le VHB , avant le début d’une chimiothérapie ou thérapie immunosuppressive Une thérapie antivirale prophylactique est recommandée chez les porteurs du VHB au début de la chipiothérapie pour cancer ou à la fin d’une thérapie immunosuppressive a. b. c. d. e. Les patients avec ADN VHB <2, 000 IU/ml devraient continuer le traitement pendant 6 mois après réalisation de la chimiothérapie ou de la thérapie immusuppressive Les patients avec ADN VHB élevé (<2, 000 IU/ml) devraient continuer le traitement jusqu’à ce qu’ils atteignent les objectifs du traitement comme pour les patients immunocompétents La lamivudine ou telbivudine peuvent être utilisées si la durée anticipée du traitement est courte (≤ 12 mois) et ADN VHB du sérum n’est pas détectable Le tenofovir ou entecavir est recommandé pour un traitement de longue durée L’IFN-α devrait être évité en raison de l’effet sur la moelle osseuse

Recommandations pour le traitement de l’Hépatite chronique B

Recommandations pour le traitement de l’Hépatite chronique B (1) Ag. HBe ADN VHB(PCR) ALT Stratégie de traitement + >20, 000 IU/ml ≤ 2 X ULN Efficacité lente avec traitement actuel Observer; envisager un traitement quand ALT devient élevé Envisager une biopsie chez les personnes de plus de 40 ans, ALT élevé persistant 2 X ULN normal, ou avec antécédents familiaux de CHC Envisager un traitement si ADN VHB >20, 000 IU/ml et si la biopsie montre une inflammation modérée/sévère ou une fibrose significative + >20, 000 IU/ml >2 X ULN Observer pendant 3 -6 mois et traiter si pas de perte Ag. HBe spontanée Envisager une biopsie du foie avant le traitement si compensé Traitement immédiat si ictère ou décompensation clinique IFNα/peg. IFNα, LAM, ADV, ETV, TDF ou Ld. T peuvent être utilisé comme thérapie initiale ADV non recommandé dû à une activité antivirale faible et un fort taux de résistance après la 1ère année LAM et Ld. T non recommandés dû à un fort taux de résistance au médicament Critère de traitement – Séroconversion de Ag. HBe à anti. HBe Durée de la thérapie :

Recommandations pour le traitement de l’Hépatite chronique B (2) Ag. HBe - ADN VHB(PCR) >2, 000 IU/ml ALT > 2 X ULN Stratégie de traitement IFNα non répondeurs/ contre-indications à IFNα TDF/ETV IFN-α/peg IFN-α, LAM, ADV, ETV, TDF ou Ld. T peuvent être utilisés comme thérapie initiale LAM et Ld. T non recommandés dû à un fort taux de résistance au médicament ADV non recommandé dû à une activité antivirale faible et un fort taux de résistance après la 1ère année Critère de traitement – Non défini Durée de la thérapie : - IFN-α/peg. IFN-α : un an - LAM/ADV/ETV/Ld. T/TDF : > 1 an IFNα non répondeurs / contre-indications à IFN-α TDF/ETV Envisager une biopsie du foie et traiter si la biopsie du foie montre une nécroinflammation modérée/sévère une fibrose significative - <2, 000 IU/ml 1 ->2 x ULN - ≤ 2, 000 IU/ml ≤ ULN Observer, traiter si ADN VHB ou si ALT devient élevé +/- détectable Cirrhose Compensé ADN VHB >2, 000 IU/ml-traiter, LAM/ADV/ETV/Ld. T/TDF peuvent être utilisés comme thérapie initiale
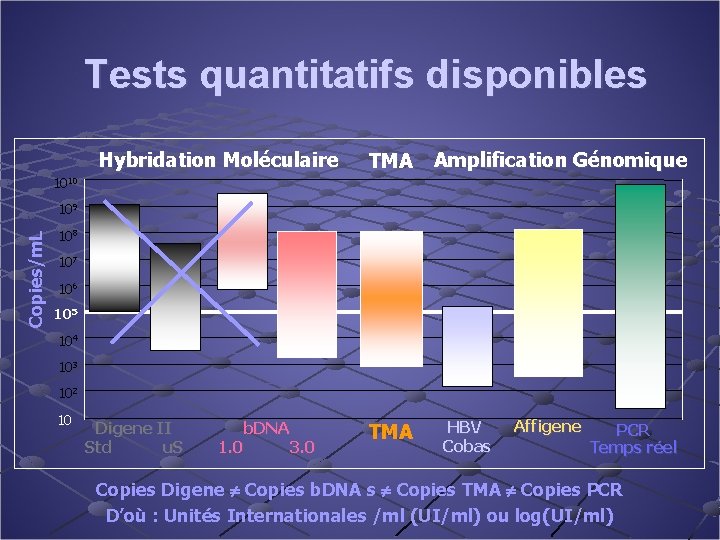
Tests quantitatifs disponibles Hybridation Moléculaire TMA Amplification Génomique 1010 Copies/m. L 109 108 107 106 105 104 103 102 10 Digene II Std u. S b. DNA 1. 0 3. 0 TMA HBV Cobas Affigene PCR Temps réel Copies Digene Copies b. DNA s Copies TMA Copies PCR D’où : Unités Internationales /ml (UI/ml) ou log(UI/ml)
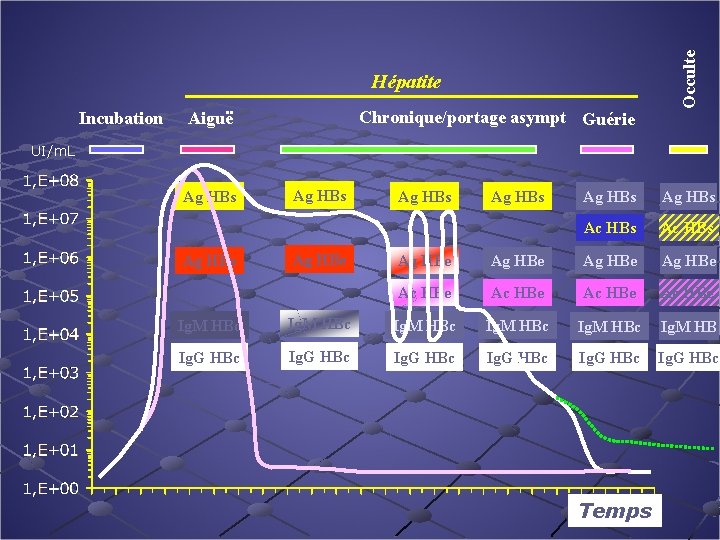
Incubation Chronique/portage asympt Guérie Aiguë Occulte Hépatite UI/m. L Ag HBs Ag HBe Ag HBs Ac HBs Ag HBe Ac HBe Ig. M HBc Ig. M HB Ig. G HBc Temps

Vaccination VHB : prévention du CHC 3 855 485 nouveaux nés vaccinés et suivis à Taiwan entre 1984 -2000 Suivi : 43 134 217 personnes/années 158 carcinomes hépatocellulaires (CHC) Garçons Filles Nb sujets Suivi Per/années Nb CHC Incidence CHC /100. 000 Nb sujets Suivi Per/années Nb CHC Incidence CHC /100 000 2 009 182 22 467 671 98 0, 44 1 846 303 20 666 547 60 0, 29 217 768 2 015 345 15 0, 74 197 921 1 851 005 8 0, 43 3 doses > 1992 0 -1 -6 1 061 759 9 671 294 49 0, 51 979 213 8 919 756 33 0, 37 4 doses < 1992 0 -1 -2 -12 729 655 34 0, 31 669 19 0, 19 Total Vaccin VHB 1 -2 doses - 58 % 10 781 032 - 56 % 9 895 786 EASL 2006 – Y. C. Chien et al abstract 247
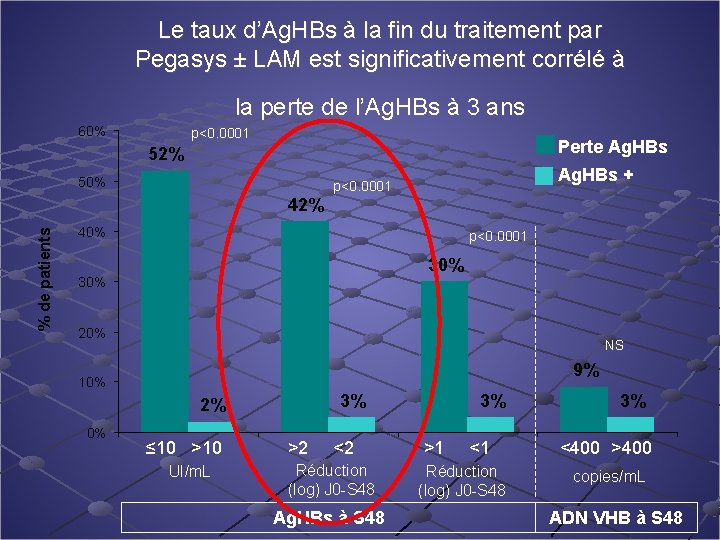
Le taux d’Ag. HBs à la fin du traitement par Pegasys ± LAM est significativement corrélé à la perte de l’Ag. HBs à 3 ans 60% p<0. 0001 Perte Ag. HBs 52% 50% Ag. HBs + p<0. 0001 % de patients 42% 40% p<0. 0001 30% 20% NS 9% 10% 3% 2% 0% ≤ 10 >10 UI/m. L >2 <2 Réduction (log) J 0 -S 48 Ag. HBs à S 48 3% >1 <1 Réduction (log) J 0 -S 48 3% <400 >400 copies/m. L ADN VHB à S 48
- Slides: 94