PRISE EN CHARGE DE LETHYLISME CHEZ LES PATIENTS































- Slides: 36

PRISE EN CHARGE DE L’ETHYLISME CHEZ LES PATIENTS AGÉS AVEC TROUBLES COGNITIFS EN HDJ Anne LORENZ – DESC de Gériatrie Pierre ANTHONY – PH Centre pour Personnes Agées Hôpitaux Civils de Colmar S

Les questions à l’origine de la présentation S « Docteur, que peut-on faire pour que la maladie d’Alzheimer évolue moins vite ? » Influence de l’éthylisme dans les troubles du comportement. S Le Baclofène chez la personne âgée. Intérêt du traitement à 10 ou 20 mg par jour ? S Bière et vin sans alcool, une solution à envisager chez les patients avec troubles cognitifs ?

Epidémiologie S

Prévalence de l’alcoolodépendance SPrévalence chez la personne âgée en France : aucune donnée SEtudes étrangères > 65 ans : 16 à 17, 7% homme, 2 à 4, 2 % femme Addiction in the elderly (T. Wetterling et Al. 2002), Alcoholism in older Korean men (JM. Kim et Al. 2002) S 1/3 de l’alcoolo-dépendance apparait après 60 ans Alcoholism in the elderly (JAMA 1996) SFréquence *1, 5 chez patients avec troubles cognitifs Catchement Aera Study (A. Regier et Al. 1990)

Hospitalisation et Mortalité S L‘Alcool une des toutes premières causes d‘hospitalisation en France (F. Paille et M. Reynaud 2015) : Séjours en 2012 : Ø 2, 2 % MCO - 10, 4% psychiatrie - 5, 6 % SSR Ø 10 % hommes et 5 % femmes S 3ème cause de mortalité (HTA et tabac) dans la population : 49 000 décès/an en France (INPES 2009) S > 65 ans près de 30 000 décès/an seraient dus à l’alcool (SFA –SFGG Recommandations 2013)

Alcool et démence L’alcoolo-dépendance est un facteur de risque de développer tout type de démence : SReprésenterait 10% des démences Liverpool - PA. Saunders et al 1991 , Finlayson et al 1998, Mayo Clin SCofacteur de démence dans 21 à 24% des cas Alcoholism and dementia – DM. Smith et Al 1995

Contribution of alcohol use disorders to the burden of dementia in France 2008 -13 : a nationwide retrospective cohort study. M. Schwarzinger et al. Lancet Public Health - Mars 2018 S Etude Française multicentrique S Cohorte rétrospective sur 31 624 156 patients hospitalisés plus de 20 ans S 1 109 343 patients diagnostiqués déments inclus S Alcool premier facteur de risque modifiable : 3, 44 (IC à 95% 3, 28 -3, 41) pour les femmes et de 3, 36 (3 31 -3, 41) pour les hommes

Alcool et démence ? ? A contrario : S 60 ans, consommation d’alcool modérée : rôle protecteur sur fonctions cognitives Etudes longitudinales : Herbert et al. 1993, PAQUID (S. Leweshow et al. 1998), Honolulu Heart Programm (DJ. Galanis et al. 2000) Etudes transversales : Hendrie et al. 1998, Dufouil et al. 1997 SHypothèses : fréquence lésions ischémiques cérébrales / stimulation libération Ach hyppocampique SRésultats inconstants et biais importants …

Moderate alcohol consumption as risk factor for adverse brain outcomes and cognitive decline: longitudinal cohort study A. Topiwala et al. BMJ 2017 A. S Cohorte suivie sur 30 ans (1985 -2015) S 550 patients, âge moyen à l’inclusion : 43 ans S Etude des structures cérébrales par IRM S Résultats -> Atrophie hippocampique dose-dépendante > 30 unités/semaine : OR 5, 8 ( IC 95% 1, 8 à 18, 6 – p < 0, 001) S Aucun effet protecteur pour une consommation légère ou modérée (OR 3, 4 – IC 95% 1, 4 à 8, 1 – p = 0, 007)

Cas Clinique M. B. 77 ans – novembre 2017 à mai 2018 S

Anamnèse S Patient de 77 ans, veuf depuis 4 mois. S Hospitalisé pour chute sur alcoolisation aigue S Ethylisme chronique difficile à quantifier mais signe physique présent : cytolyse, hépatomégalie S Troubles cognitifs avec atteinte de la mémoire épisodique décrit par l’entourage et constatés dans le service. S Sevrage avec supplémentation en vit B 1 -B 6 + Seresta

Evaluation neuropsychologique à 4 semaines S MMS 18/30 S Mémoire : au RL/RI 16 Rappel immédiat 15/16 Rappel libre aux 3 essais 16/48 * Rappel indicé aux 3 essais 43/48 Rappel libre différé 3/16 * Rappel libre indicé 13/16 * S Fonction exécutives BREF = 7/18 * TMT A = 2 min 20 * TMT B = impossible S Langage : décousu, fuite des idées mais pas de manque du mot – DO 29/30

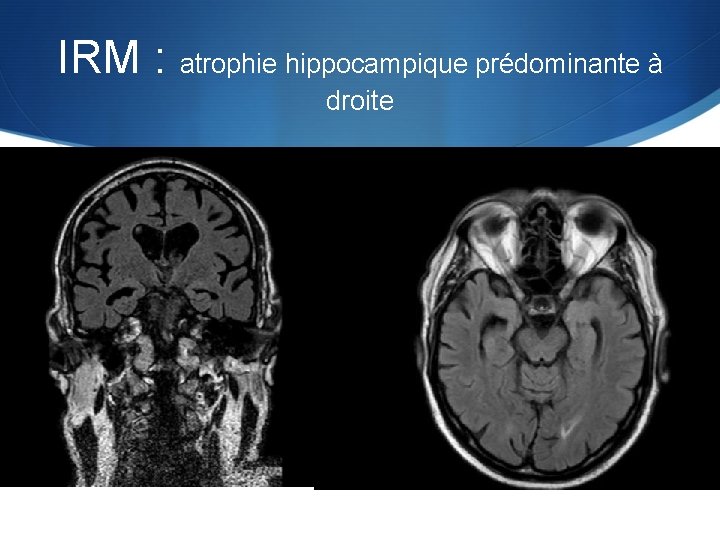
IRM : atrophie hippocampique prédominante à droite

Hypothèses diagnostiques ? A vous de voter S 1 ) Maladie d’Alzheimer S 2 ) Syndrome de Korsakoff S 3 ) Troubles liés à l’éthylisme chronique S 4 ) Autre proposition

Propositions de réponses Ø Syndrome de Korsakoff : NON Pas de fausses reconnaissances, pas de signes à l’IRM Ø Comment distinguer les conséquences de l’éthylisme chronique et un début de maladie d’Alzheimer ? - Réévaluation 6 mois après le sevrage complet - Biomarqueurs du LCR

Biomarqueurs du LCR : Pas en faveur d’une maladie d’Alzheimer S AB 42 = 598 * ng/ml (N>700) S Tau = 227 ng/ml (N<400) S p. Tau = 29 ng/ml (N<60) S Iati = 1, 18 Normes selon Lehmann et al, Impact of harmonisation of collections tubes on Alzheimer’s Disease diagnosis, in Alzheimer and Dementia 2013

Réévaluation 6 mois après le sevrage S Patient en EHPAD S Amélioration comportementale S MMS 25/30 + 7 points S Mémoire : au RL/RI 16 Rappel immédiat 15/16 Rappel libre aux 3 essais 16/48 * Rappel indicé aux 3 essais 44/48 Rappel libre différé 5/16 Rappel libre indicé 14/16 * S Fonction exécutives BREF = 12/18 * + 5 points

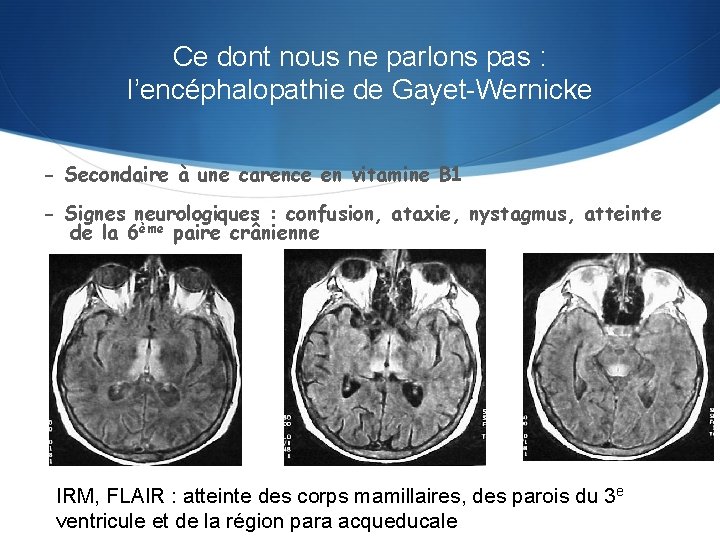
Ce dont nous ne parlons pas : l’encéphalopathie de Gayet-Wernicke - Secondaire à une carence en vitamine B 1 - Signes neurologiques : confusion, ataxie, nystagmus, atteinte de la 6ème paire crânienne IRM, FLAIR : atteinte des corps mamillaires, des parois du 3 e ventricule et de la région para acqueducale

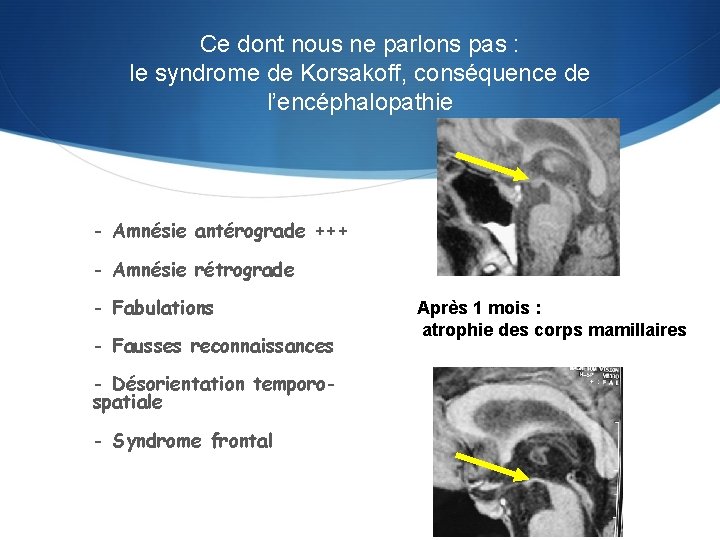
Ce dont nous ne parlons pas : le syndrome de Korsakoff, conséquence de l’encéphalopathie - Amnésie antérograde +++ - Amnésie rétrograde - Fabulations - Fausses reconnaissances - Désorientation temporospatiale - Syndrome frontal Après 1 mois : atrophie des corps mamillaires

Les conséquences de l’éthylisme chronique sur la cognition S Physiopathologie : - Neurotoxicité directe de l’alcool - Effet de la carence en thiamine (vit B 1) S Controverse sur la notion de démence alcoolique S Hétérogénéité des troubles S Notion de continuum entre les troubles liés à l’alcoolodépendance et le Sd de Korsakoff S Sous diagnostic des Encéphalopathies de Gayet. Wernicke

Les conséquences de l’éthylisme chronique sur la cognition Neuropsychologie : SAtteinte des fonctions exécutives et attentionnelles STroubles de la mémoire épisodiques – diagnostic différentiel parfois difficile avec la MA STroubles émotionnels : Déficit d’encodage des émotions qui aggrave les problèmes relationnels et l’isolement social Imagerie : SAtrophie à prédominance frontale SAtrophie cérébelleuse et du corps calleux SAtrophie hippocampique Effet positif du sevrage : Spreuve de la récupération à la volumétrie hippocampique en IRM à 6 mois de sevrage

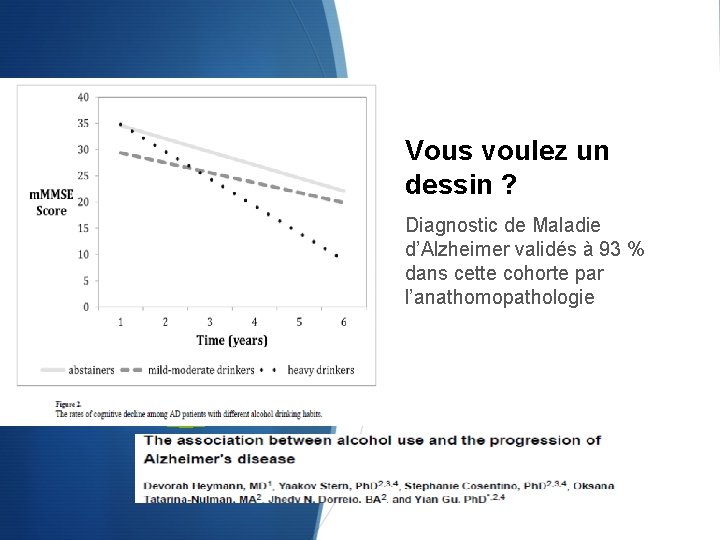
S Etude de cohorte avec 360 patients, suivi biannuel, informations auprès de l’aidant. S 3 catégories : - gros buveurs ˃ 8 unités semaines - buveurs légers à modérés 17 ui/sem - abstinents S

Vous voulez un dessin ? Diagnostic de Maladie d’Alzheimer validés à 93 % dans cette cohorte par l’anathomopathologie

Dépistage S

Nouvelles recommandations Adultes – Santé publique France 2017 S Homme = femme S 10 verres / semaine, 2 verres max/j S Deux jours d’abstinence / semaine Personnes âgées – SFA et SFGG 2014 S 7 verres / semaine, 1 verre max/j S 3 verres lors d’occasion

Parler d’alcool Quand ? Comment ? u Troubles cognitifs u Interventions brèves u Post-aigu : chute, syndrome u Questionnaire AUDIT-C (intérêt > confusionnel, troubles du comportement, dépression, carence nutritionnelle 65 ans), FACE … u Importance de l’entourage (famille, aides humaines à domicile) -> Répéter régulièrement -> Osez poser la question

Prise en charge 1. Le sevrage et l’abstinence 2. La réhabilitation cognitive 3. Les possibilités en HDJ S

Le sevrage classique S Personne âgée = sevrage hospitalier -> risque DT, troubles hydro-électrolytiques, épilepsie S Benzodiazépine de demie vie courte (Oxazepam) S Thiamine (vit B 1) 250 mg - Faible risque : pas de dénutrition ni comorbidité, 250 mg per os - Fort risque : dénutrition / hépatopathie / synd. de sevrage, 250 mg IV 5 j S Antidépresseur ? Non systématique S Suivi possible en HDJ hebdomadaire

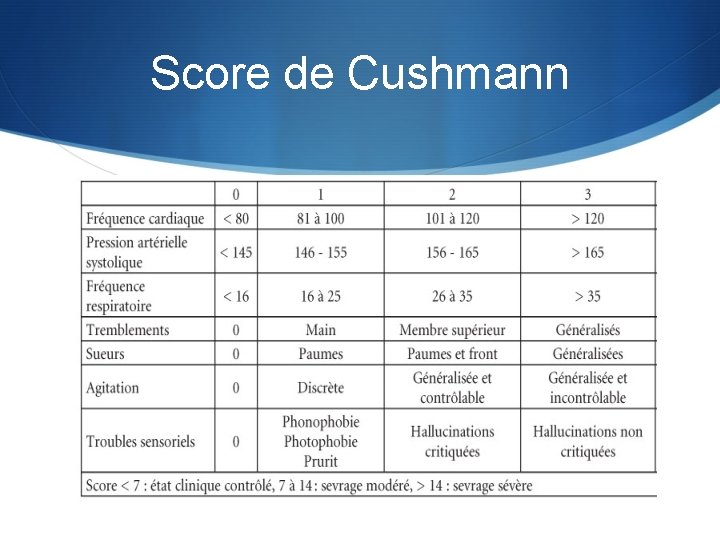
Score de Cushmann

La réduction de consommation = réduction des risques Sen ambulatoire STraitement : Baclofène (Lioseral®) : agoniste réc. GABA Nalméfène (Selincro®) : antagoniste opioïde Sassocié à un accompagnement psycho-social + -> Difficulté principale : observance

Un point sur le Baclofène Controverse actuelle : Efficace vs Dangereux à forte dose Alpadir (M. Reynaud et al. 2017), Bacloville (JR. Le Gall et al. 2018), données INSERM 2017 S Posologie : 15 mg jusqu’à Pas de recul chez la personne âgée, à savoir : S EI fréquents : somnolence, SAbaissement du seuil 80 mg confusion, asthénie, troubles thymiques épileptogène SAssociation L-Dopa : majoration syndrome Parkinsonien

Et le Nalméfène ? S Posologie : 1 cp/j (18 mg) avant besoin de consommation S Efficacité : réduction consommation 3 j /mois vs placebo Karhuvaara S et al. Targeted nalmefene with a simple medical management in the treatment of heavy drinkers: a randomized double-blind placebo. Alcohol Clin Exp Res 2007 S EI : Nausées, insomnies, vertiges S Contre indication : Insuffisance rénale / hépatique sévère En association avec antalgique opiacé

La réhabilitation cognitive → Récupération spontanée incomplète six mois après sevrage S Deux approches : Ø Restauration des fonctions exécutives (mémorisation, attention) Ø Techniques de compensation (notes, agenda), aménagement de l’environnement, aides extérieures S Lieux : FAM, CSAPA avec hébergement, EHPAD (lieu de vie sans alcool pour l’ensemble des résidents)

Les possibilités de prise en charge en HDJ S Collaboration avec le service d’Addictologie : - entretien avec IDE - psychologue S S Bilan somatique : - nutritionnel - cirrhose - épilepsie - iatrogénie ? Les particularité du patient avec troubles cognitifs : - anosognosie - perte d’autonomie dans les IADL (courses) - ISOLEMENT

La « substitution » : une possibilité de réduction du risque S Une solution à proposer : - pas de changement des habitudes - plus facile si le patient ne fait pas les courses

Conclusion S Evaluation de la consommation lors du recueil d’information S Etre convaincu de l’utilité de la réduction du risque S Collaboration avec le service d’addictologie