PRINCIPALI ALTERAZIONI DELLA MEMBRANA PLASMATICA ALTERAZIONI GROSSOLANE DI
PRINCIPALI ALTERAZIONI DELLA MEMBRANA PLASMATICA ALTERAZIONI GROSSOLANE DI STRUTTURA ALTERAZIONI DEL TRASPORTO ALTERAZIONI DI ESPRESSIONE/FUNZIONI RECETTORIALI

ALTERAZIONI NELL’ESPRESSIONE DI RECETTORI 1. Difetti di espressione su base genetica: u. Difetti di espressione o internalizzazione del recettore per LDL (LDL-receptor) u. Difetti di espressione per recettori adesivi: ü Leukocyte Adhesion Deficiency Syndromes (LADs) (Leucociti) ü Sindrome di Bernard-Soulier (Piastrine) ü Tromboastenia di Glanzmann (Piastrine) u. Difetti di espressione per recettori per ormoni 2. Difetti di espressione (down-modulation) su base acquisita: u. Ridotta espressione LDL-receptor per eccessivo accumulo di colesterolo intracellulare u“Down-modulation” di recettori adrenergici nello scompenso cardiaco u“Down-modulation” di trombomodulina sull’endotelio nel corso di risposte infiammatorie 3. Aumentata espressione (up-modulation): u. Aumentata espressione di recettori adesivi su endotelio e leucociti nella flogosi u. Aumentata espressione di recettori per citochine/recettori per patogeni in cellule dell’immunità innata e adattativa u. Aumentata espressione di Fattore tessutale in cellule endoteliali e infiammatorie u. Aumentata espressione di recettori per fattori di crescita in cellule proliferanti o neoplastiche

ALTERAZIONI NELLA FUNZIONE DI RECETTORI 1. Difetti di FUNZIONE su base genetica: u Geni mutati codificano per recettori che trasducono il segnale anche in assenza/basse concentrazioni di ligandi u Geni mutati codificano per proteine citoplasmatiche fanno parte dei sistemi di trasduzione del segnale con guadagno di funzione (gain-of-function) di funzione u Geni mutati codificanti per proteine ad attività di regolazione negativa di componenti della trasduzione del segnale hanno una ridotta attività inibitoria (loss-of-function) 2. Difetti di FUNZIONE su base acquisita: u Fattori esogeni (tossine batteriche, sostanze tossiche) o endogeni (ormoni, molecole biologicamente attive, risposte dell’ospite a danni di diversa natura) alterano la trasduzione del segnale da parte di recettori modificando la funzione di componenti della trasduzione del segnale
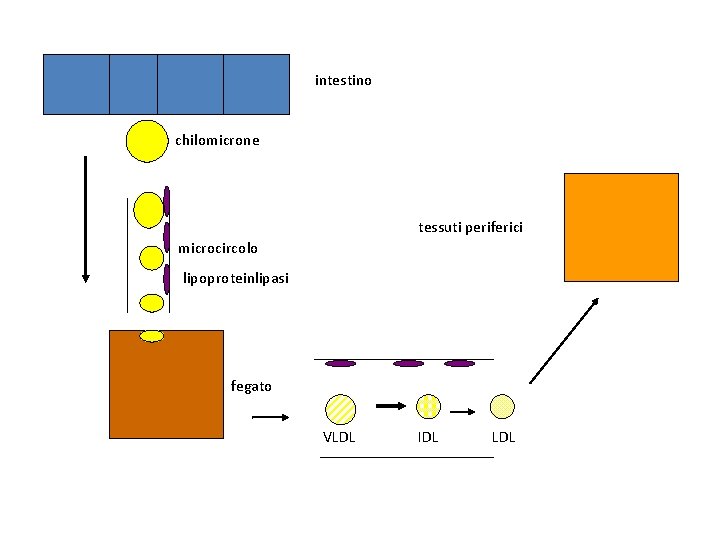
intestino chilomicrone tessuti periferici microcircolo lipoproteinlipasi fegato VLDL IDL LDL

IPERCOLESTEROLEMIE SU BASE GENETICA DOVUTE AD ALTERAZIONI REETTORIALI I. IPERCOLESTEROLEMIA FAMIGLIARE (AD): * eterozigote (1/500). . . 300 mg/dl LDL-colesterolo * omozigote (1/1. 000). . . 650 mg/dl LDL-colesterolo Gene mutato: LDLReceptor II. DIFETTO FAMIGLIARE DI APOB-100 (AD): * eterozigote (1/1000). . . 270 mg/dl LDL-colesterolo * omozigote (1/1. 000). . . 320 mg/dl LDL-colesterolo Gene mutato: Apo. B-100 III. IPERCOLESTEROLEMIA AUTOSOMICA RECESSIVA (AR): omozigote (<1/10. 000). . . 470 mg/dl LDL-colesterolo Gene mutato: ARH (regola internalizzazione/localizzazione LDLR)
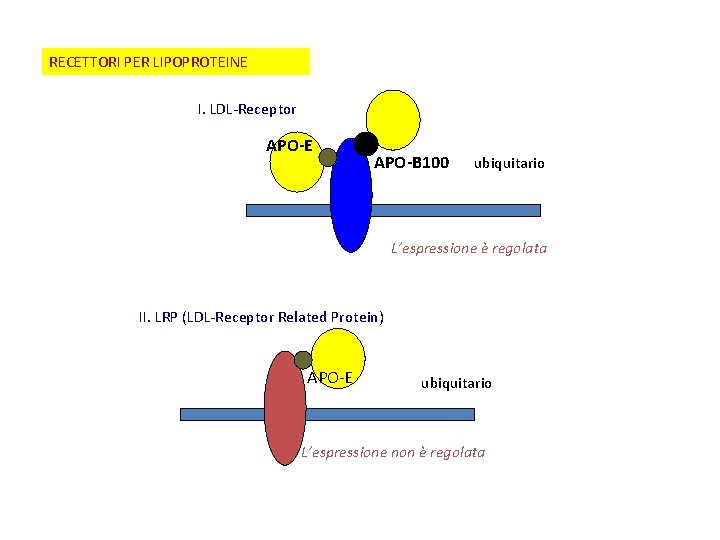
RECETTORI PER LIPOPROTEINE I. LDL-Receptor APO-E APO-B 100 ubiquitario L’espressione è regolata II. LRP (LDL-Receptor Related Protein) APO-E ubiquitario L’espressione non è regolata
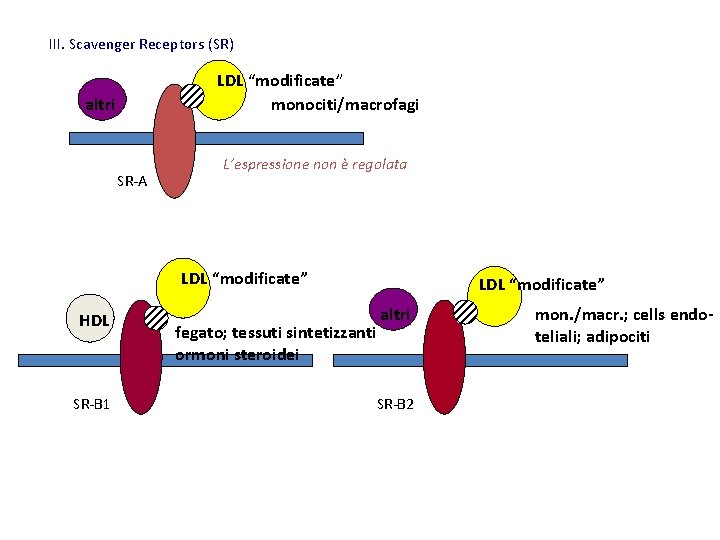
III. Scavenger Receptors (SR) LDL “modificate” monociti/macrofagi altri SR-A L’espressione non è regolata LDL “modificate” HDL SR-B 1 LDL “modificate” fegato; tessuti sintetizzanti ormoni steroidei altri SR-B 2 mon. /macr. ; cells endoteliali; adipociti
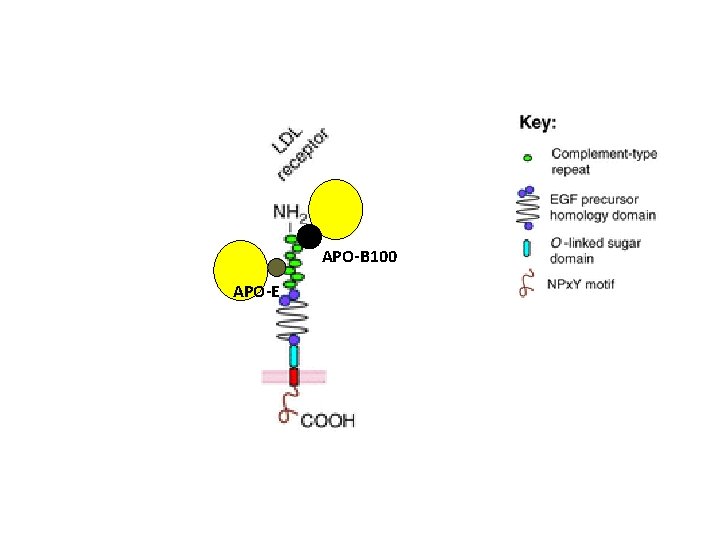
APO-B 100 APO-E
![The low-density lipoprotein (LDL) receptor (apolipoprotein [apo] B/E receptor). The LDL receptor is a The low-density lipoprotein (LDL) receptor (apolipoprotein [apo] B/E receptor). The LDL receptor is a](http://slidetodoc.com/presentation_image_h2/766b469f8f4eff3cedceaea3598e77ed/image-11.jpg)
The low-density lipoprotein (LDL) receptor (apolipoprotein [apo] B/E receptor). The LDL receptor is a single protein with five functional domains. The carboxyl terminal of 50 amino acids provides a cytoplasmic domain that is believed to play an important role in the internalization of the lipoprotein. The membrane-spanning domain has 22 amino acids. The third domain of 58 amino acids is rich in serine and threonine residues (18 residues) and has several O-linked sugars. The largest domain has over 400 amino acids and is 35% homologous to the precursor of epidermal growth factor (EGF). The cysteinerich N-terminal domain consists of 292 amino acids that include several negatively charged amino acids that generate regions for binding to either a single apo E molecule or an apo B-100 molecule. the requirements for apo B-100 binding are more stringent than for apo E binding.
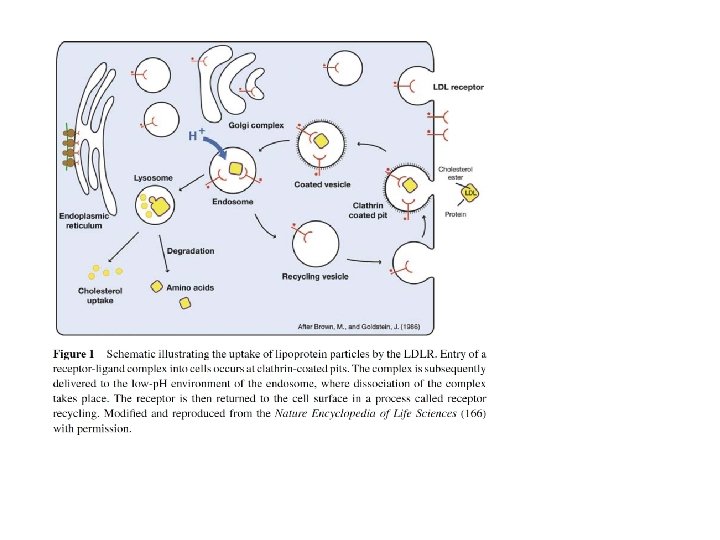
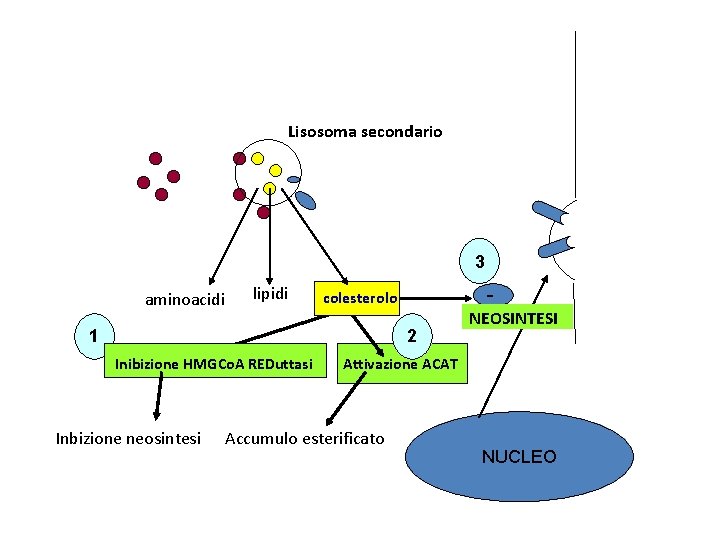
Lisosoma secondario 3 aminoacidi lipidi - colesterolo 1 2 Inibizione HMGCo. A REDuttasi Inbizione neosintesi NEOSINTESI Attivazione ACAT Accumulo esterificato NUCLEO
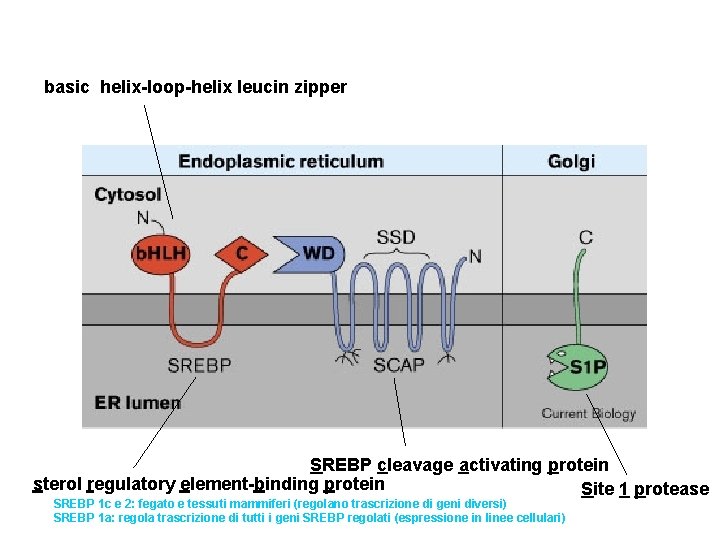
basic helix-loop-helix leucin zipper SREBP cleavage activating protein sterol regulatory element-binding protein Site 1 protease SREBP 1 c e 2: fegato e tessuti mammiferi (regolano trascrizione di geni diversi) SREBP 1 a: regola trascrizione di tutti i geni SREBP regolati (espressione in linee cellulari)
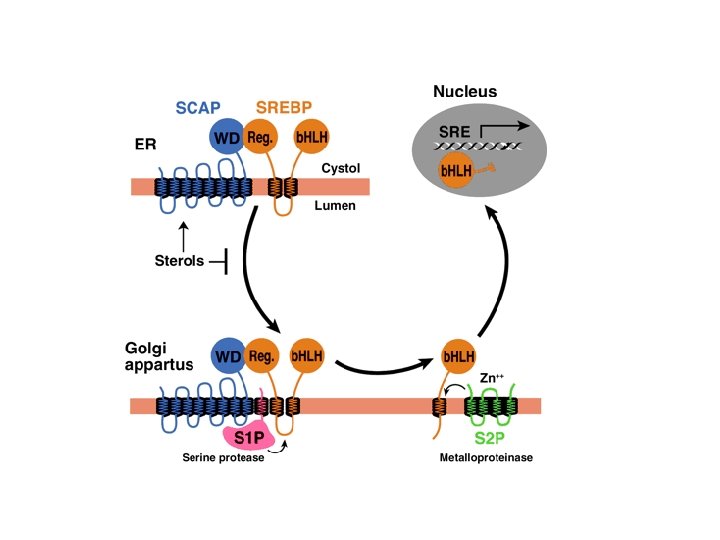
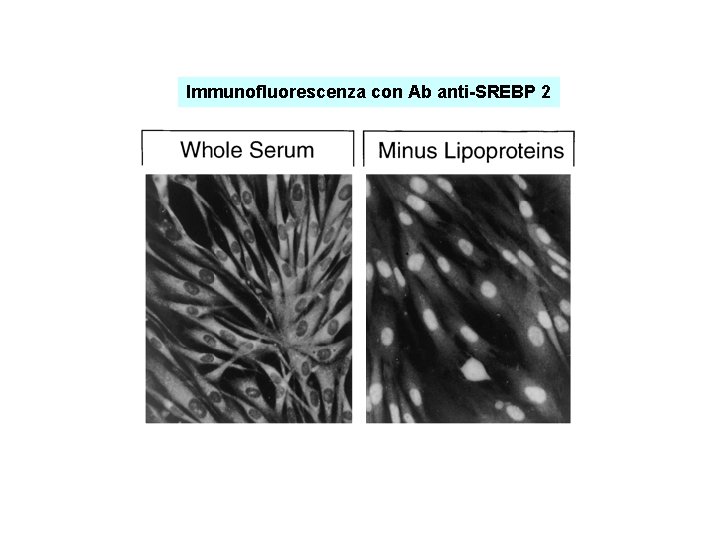
Immunofluorescenza con Ab anti-SREBP 2

Classification of LDL Receptor Mutations Class I These "null" alleles (R-O) fail to produce detectable receptors; this mutation is very common. Class II The synthesized receptors do not undergo proper posttranslational modification and are degraded, never to reach the cell surface. Class III Receptors are produced and processed at normal rates but are unable to bind LDL efficiently. Class IV Receptors have defective internalization and do not localize at the coated pits. Class V Receptors internalize but do not recycle.
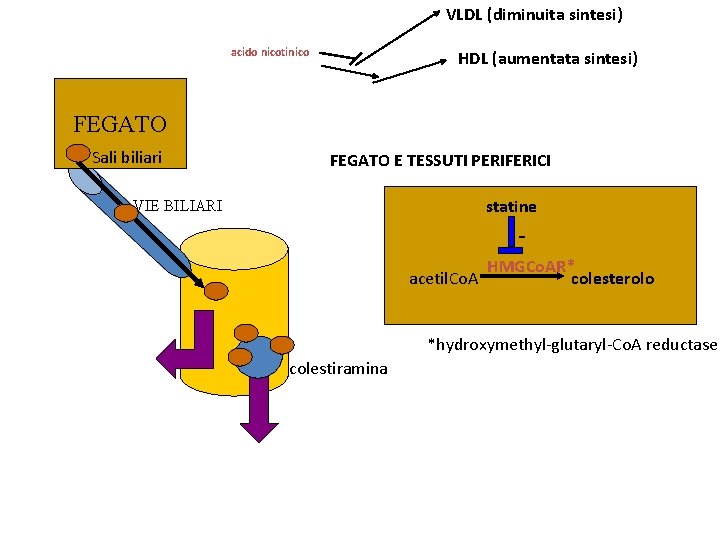
VLDL (diminuita sintesi) acido nicotinico HDL (aumentata sintesi) FEGATO Sali biliari FEGATO E TESSUTI PERIFERICI statine VIE BILIARI acetil. Co. A HMGCo. AR* colesterolo *hydroxymethyl-glutaryl-Co. A reductase colestiramina
Nuovi farmaci inibitori dell’assorbimento di colesterolo ezetimibe esteri dello stanolo
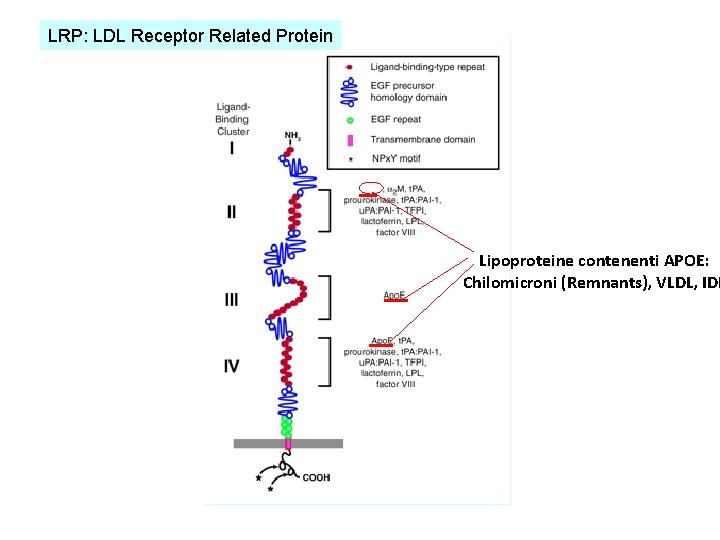
LRP: LDL Receptor Related Protein Lipoproteine contenenti APOE: Chilomicroni (Remnants), VLDL, IDL
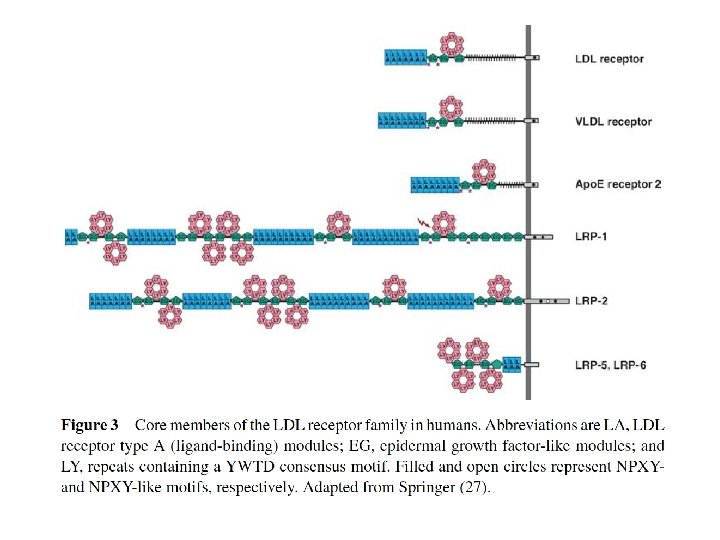
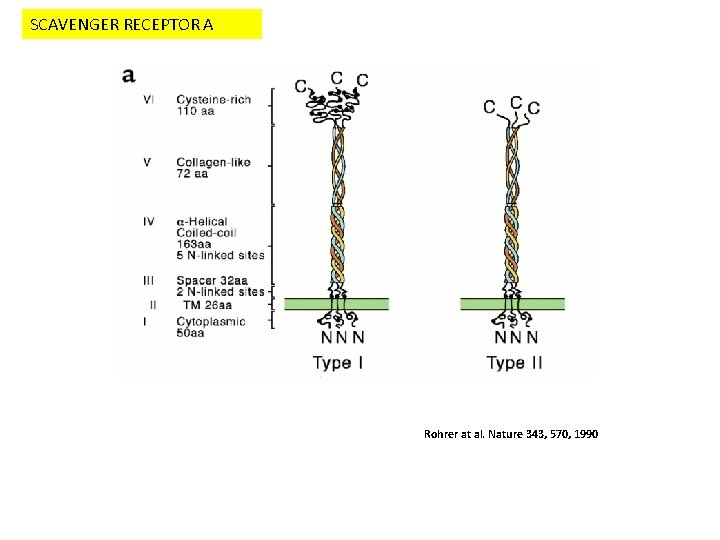
SCAVENGER RECEPTOR A Rohrer at al. Nature 343, 570, 1990
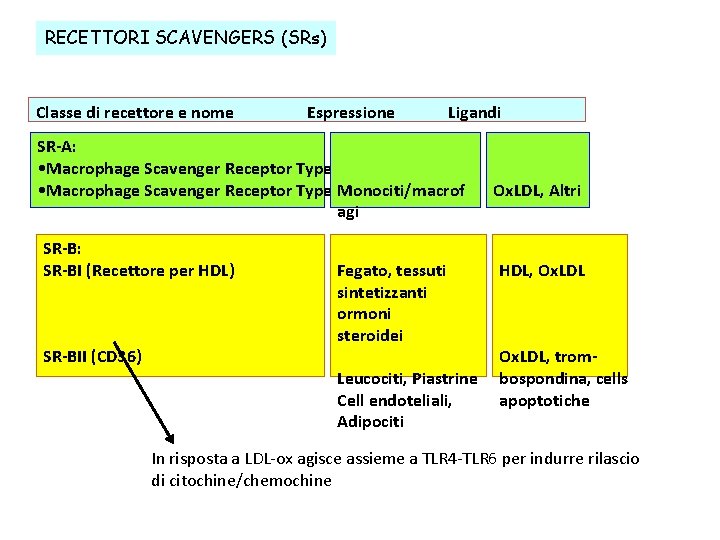
RECETTORI SCAVENGERS (SRs) Classe di recettore e nome Espressione Ligandi SR-A: • Macrophage Scavenger Receptor Type IMonociti/macrof agi SR-B: SR-BI (Recettore per HDL) SR-BII (CD 36) Fegato, tessuti sintetizzanti ormoni steroidei Leucociti, Piastrine Cell endoteliali, Adipociti Ox. LDL, Altri HDL, Ox. LDL, trombospondina, cells apoptotiche In risposta a LDL-ox agisce assieme a TLR 4 -TLR 6 per indurre rilascio di citochine/chemochine

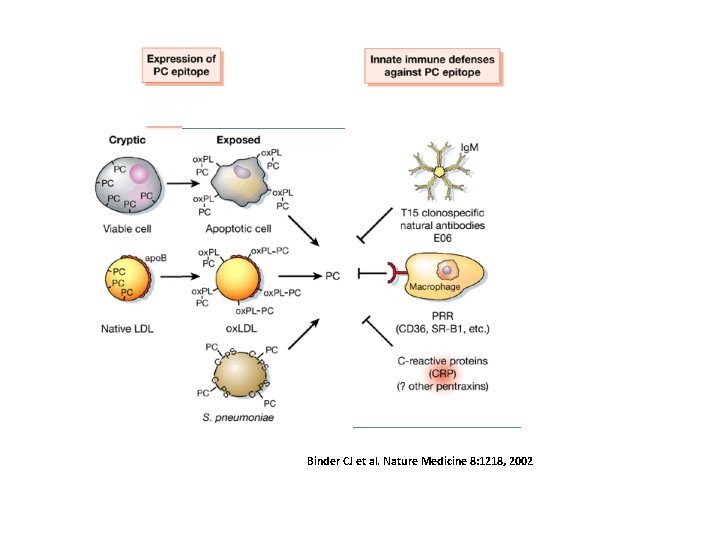
Binder CJ et al. Nature Medicine 8: 1218, 2002
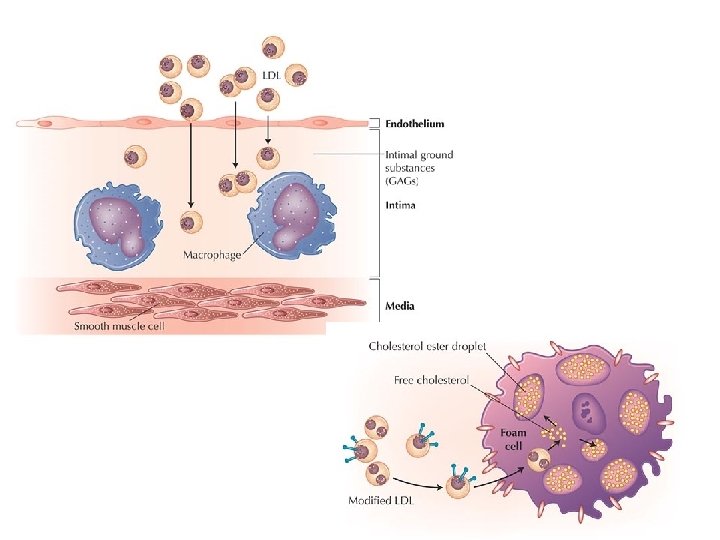
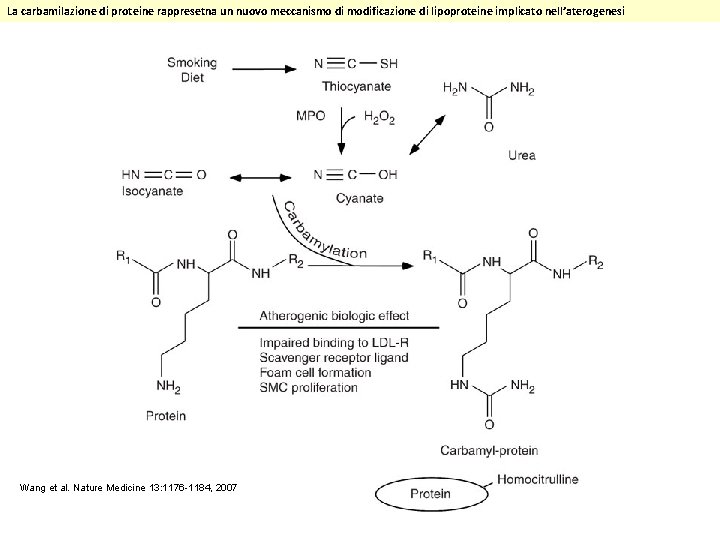
La carbamilazione di proteine rappresetna un nuovo meccanismo di modificazione di lipoproteine implicato nell’aterogenesi Wang et al. Nature Medicine 13: 1176 -1184, 2007
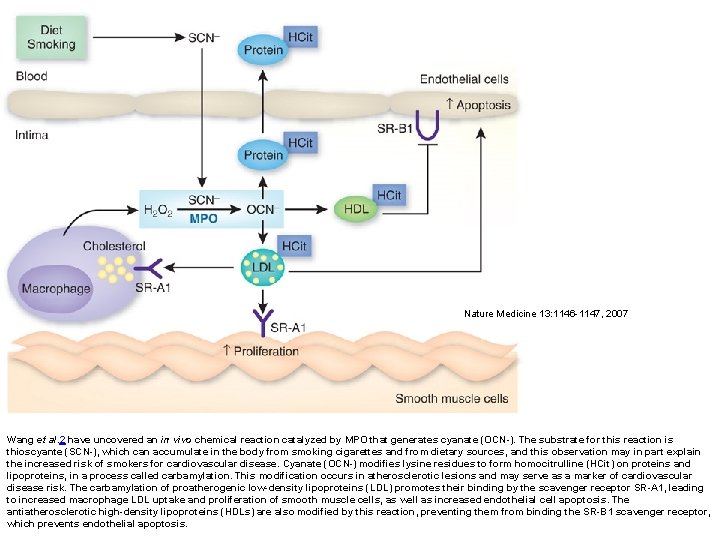
Nature Medicine 13: 1146 -1147, 2007 Wang et al. 2 have uncovered an in vivo chemical reaction catalyzed by MPO that generates cyanate (OCN-). The substrate for this reaction is thioscyante (SCN-), which can accumulate in the body from smoking cigarettes and from dietary sources, and this observation may in part explain the increased risk of smokers for cardiovascular disease. Cyanate (OCN-) modifies lysine residues to form homocitrulline (HCit) on proteins and lipoproteins, in a process called carbamylation. This modification occurs in atherosclerotic lesions and may serve as a marker of cardiovascular disease risk. The carbamylation of proatherogenic low-density lipoproteins (LDL) promotes their binding by the scavenger receptor SR-A 1, leading to increased macrophage LDL uptake and proliferation of smooth muscle cells, as well as increased endothelial cell apoptosis. The antiatherosclerotic high-density lipoproteins (HDLs) are also modified by this reaction, preventing them from binding the SR-B 1 scavenger receptor, which prevents endothelial apoptosis.
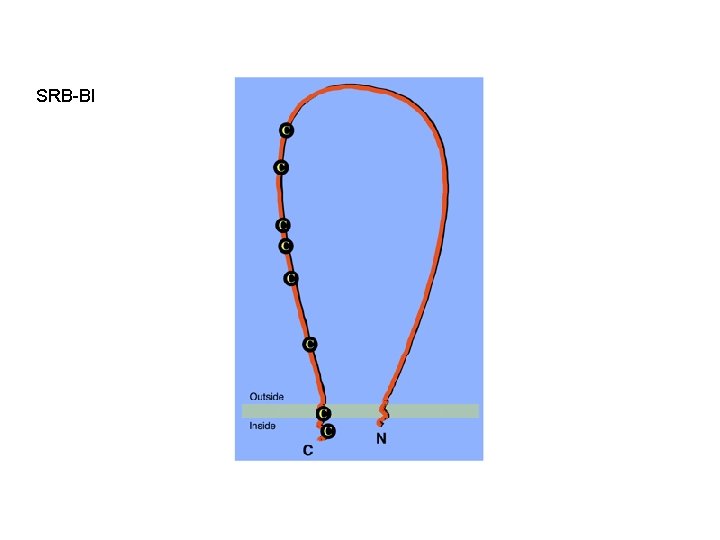
SRB-BI
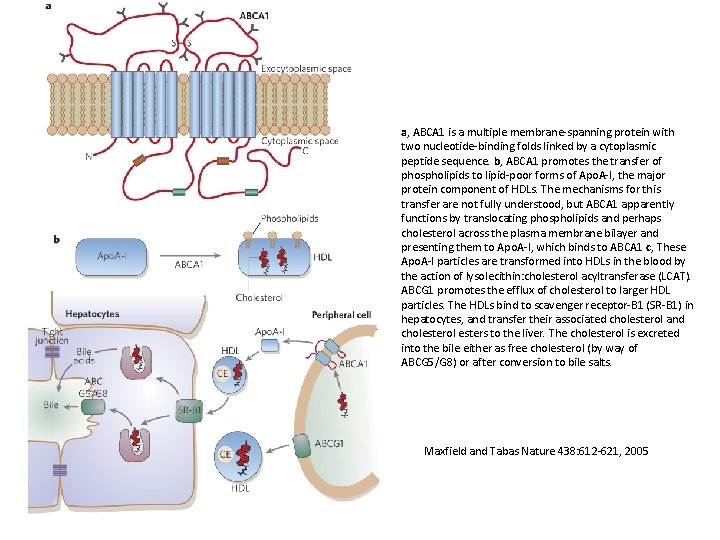
a, ABCA 1 is a multiple membrane-spanning protein with two nucleotide-binding folds linked by a cytoplasmic peptide sequence. b, ABCA 1 promotes the transfer of phospholipids to lipid-poor forms of Apo. A-I, the major protein component of HDLs. The mechanisms for this transfer are not fully understood, but ABCA 1 apparently functions by translocating phospholipids and perhaps cholesterol across the plasma membrane bilayer and presenting them to Apo. A-I, which binds to ABCA 1 c, These Apo. A-I particles are transformed into HDLs in the blood by the action of lysolecithin: cholesterol acyltransferase (LCAT). ABCG 1 promotes the efflux of cholesterol to larger HDL particles. The HDLs bind to scavenger receptor-B 1 (SR-B 1) in hepatocytes, and transfer their associated cholesterol and cholesterol esters to the liver. The cholesterol is excreted into the bile either as free cholesterol (by way of ABCG 5/G 8) or after conversion to bile salts. Maxfield and Tabas Nature 438: 612 -621, 2005
- Slides: 31