PREVENZIONE ED EPIDEMIOLOGIA DELLE INFEZIONI OSPEDALIERE DEFINIZIONE Per























































































































































- Slides: 159

PREVENZIONE ED EPIDEMIOLOGIA DELLE INFEZIONI OSPEDALIERE

DEFINIZIONE Per infezione acquisita in Ospedale si definisce un’infezione contratta durante il ricovero in ospedale, che non era manifesta clinicamente né in incubazione al momento dell’ammissione, ma che compare durante o dopo il ricovero e da questo è determinata. Le infezioni acquisite in ospedale comprendono anche le infezioni che il personale ospedaliero può contrarre nell’assistenza ai malati. L’infezione va distinta dalla "colonizzazione", definita come la moltiplicazione a livello locale di microrganismi senza apparenti reazioni tessutali o sintomi clinici. (Circolare Ministero Sanità n. 52/1985 )

Definizione di infezione ospedaliera (NNIS 1988) Una condizione localizzata o sistemica risultante da una reazione avversa alla presenza di un agente infettivo o di sue tossine che rientra nei seguenti criteri: si presenta in un paziente ricoverato nell’ambito della rete di sorveglianza, non vi è evidenza di infezione e di una sua incubazione al momento dell’ammissione a meno che non sia correlata ad un precedente ricovero, deve rientrare nei criteri specifici che definiscono i siti di infezione.

Definizione di infezione ospedaliera Con il termine I. O. sia scientificamente che operativamente oggi si intende un campo più vasto che include tutte le infezioni riconducibili a momenti assistenziali, anche non strettamente ospedalieri, e la prevenzione del rischio biologico per il personale sanitario. Oggi più correttamente si parla di INFEZIONI CORRELATE ALLE PRATICHE ASSISTENZIALI (ICPA).

CENNI STORICI Nella metà del 1800 I. Semmelweiss e J. Simpson furono i pionieri di una raccolta sistematica dei tassi di infezione ospedaliera: Semmelweiss dimostrò efficacemente che l’ospedale poteva rappresentare un rischio per i pazienti (le donne che non partorivano in ospedale avevano un rischio di sepsi puerperale ed una mortalità molto più bassa rispetto a quelle che partorivano in ospedale), che tale rischio era di origine infettiva (i patogeni erano trasmessi dai medici e dagli studenti che, prima di assistere le partorienti, effettuavano riscontri autoptici), che tale evento era prevenibile (lavando le mani con cloruro di calcio). Simpson evidenziò una correlazione diretta tra la mortalità per infezione, dopo amputazione degli arti, e la grandezza dell’ospedale, condizione associata al sovraffollamento, che favoriva la trasmissione delle infezioni da paziente.

L’impulso decisivo fu dato da una pandemia causata da S. Aureus resistente alla penicillina sia in ospedali europei che statunitensi. 1955: Colebrook propose rilevazioni di infezioni in ogni grande ospedale. 1959: Moore istituì la figura professionale dell’infermiera addetta al controllo delle infezioni nel suo ospedale, esempio seguito da altri 1970: si delinea una popolazione di pz a ↑ rischio di IO Pz sottoposti a pratiche invasive durante la degenza. Stati Uniti: istituirono i CDC ( Center for Disease Control and Prevention) e la Divisione Infezioni Ospedaliere e ne svilupparono le definizioni standard con l’avvio di un sistema di sorveglianza attiva National Nosocomial Infections Survillance System(NNIS) tutt’oggi funzionante

1980 ü In Italia: l’Istituto Superiore di Sanità (ISS) elabora il programma italiano di controllo delle IO. (SIPIO/1984) Emanazione delle circolari del Ministero della Sanità N° 52/1985 e N° 8/1988 § 1990: ü In Italia vengono emanati i decreti legislativi 502/92 e 517/93 per la riorganizzazione delle strutture ospedaliere. ü Negli Stati Uniti vengono pubblicati i documenti contenenti linee guida tra cui quelle del Hospital Infection Control Practice Advisory Committee (HICPAC) dei CDC

§ 2005: Nell’era del controllo delle infezioni, l’obiettivo da raggiungere è il cambiamento migliorativo dell’intero processo e non della singola attività. Infatti in una situazione di aperta competizione tra le varie aziende solo quelle capaci di differenziarsi in termini di conoscenza di livelli di rischio al loro interno, di bassa incidenza delle IO e di attuazione di misure di sicurezza, potranno raggiungere elevati livelli di qualità

DATI EPIDEMIOLOGICI Le infezioni ospedaliere si manifestano con alti tassi di MORBOSITA’ ed incremento della MORTALITA’, contribuendo anche all’aumento dei COSTI di degenza, dei pazienti ospedalizzati. Nonostante la riduzione della durata e del numero dei ricoveri e le ampie conoscenze disponibili in materia, in termini sia di fattori di rischio, sia di metodi appropriati di prevenzione, la frequenza delle infezioni ospedaliere non è generalmente in declino.

Frequenza 5%-10% dei pazienti ricoverati in ospedale sviluppa un infezione (Burke Jp, 2003) Il rischio per giornata di degenza è aumentato negli ultimi decenni (Wenstein, 1988): l’ 8%-12% la presenta in un giorno Il 90% delle infezioni si presenta in forma endemica, il 6% fa parte di cluster epidemici (Wenzel RP, 1987) ed il 4% di epidemie (Wenzel RP, 1983)

Localizzazioni più frequenti di infezioni ospedaliere L’ 80% di tutte le infezioni asssociate all’assistenza si localizza in quattro siti

§OMS 1983 -1985: Studio condotto su 47 ospedali di 13 paesi prevalenza 9. 9% §Stati Uniti 1998: Classificazione e raccolta sui reparti a maggiore rischio: -UTI -Reparti di chirurgia (particolare attenzione alle infezioni della ferita chirurgica)

Studio effettuato nel 1979 Svezia Danimarca Norvegia Inghilterra Galles Belgio Spagna Cecoslovacchia La prevalenza oscillava da 6. 1% in Cecoslovacchia a 12. 3% in Danimarca

Studi di Prevalenza Nazioni/Siti di infezione Germania (1994) Galles (1980) UK – Eire (1993 - 94) IVU 42. 1% 30. 3% 23. 8% FC 15. 8% 18. 9% 10. 7% Basse Vie Respiratorie 20. 6% 16. 8% 22. 9% Cute - 13. 5% 9. 6% Batteriemie 8. 3% - -

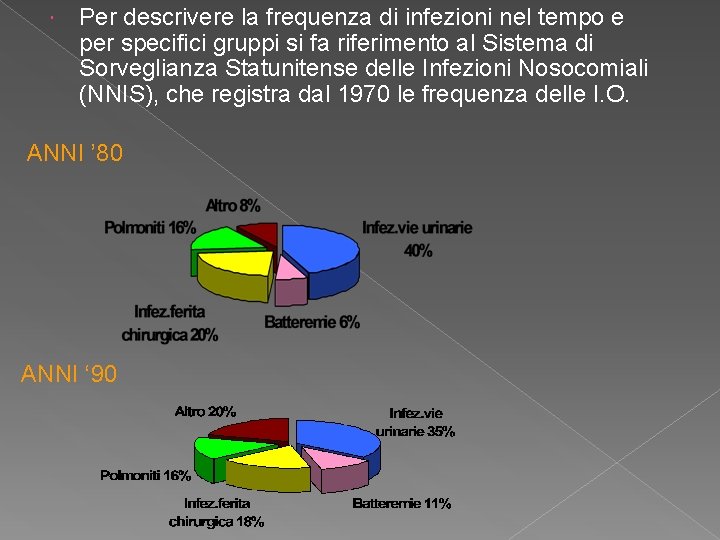
Per descrivere la frequenza di infezioni nel tempo e per specifici gruppi si fa riferimento al Sistema di Sorveglianza Statunitense delle Infezioni Nosocomiali (NNIS), che registra dal 1970 le frequenza delle I. O. ANNI ’ 80 ANNI ‘ 90

In Italia, nel 1983, fu effettuato lo Studio Italiano Prevalenza Infezioni Ospedaliere (SIPIO) che coinvolse 142 ospedali (36000 letti) ed evidenziò: - una prevalenza di I. O. del 6, 8%. - il 12, 3% dei pazienti entra in ospedale già infetto. Tali dati sono stati ulteriormente confermati da successivi studi d’incidenza condotti in alcuni ospedali italiani. La stima numerica annua d’infezioni ospedaliere oltrepassa le 600 mila unità l’anno; tali infezioni prolungano ovviamente la degenza ospedaliera, con un aggravio di costi.

. Nel 2000 uno studio di prevalenza condotto in Italia dalla Dott. ssa Moro fornì i seguenti dati: - prevalenza: 5 -8% dei ricoverati - 400. 000 -700. 000 infezioni ……di cui 30% prevenibile=135. 000 -210. 000 Le epidemie di I. O. sono per lo più attribuibili ad errori nelle pratiche assistenziali e, pertanto, EVITABILI!!!

Gli studi più recenti confermano una prevalenza di infezioni che va dal 5, 9% all’ 8, 3% L’indagine conoscitiva svolta dal ISS e dall’ Ospedale Spallanzani, è pubblicata nei rapporti Istisan, in tutti gli ospedali italiani con più di 300 posti letto e su 50% di quelli più piccoli, ha rilevato che solo la metà ha un comitato di controllo attivo, anche se qualche misura di sorveglianza e/o di rilevazione è stata comunque messa in atto in numerosi altri presidi. Nonostante l’esistenza di protocolli scritti di prevenzione, nella maggior parte degli ospedali analizzati mancano misure applicate di controllo e sorveglianza

Eziologia e patogenesi delle infezioni ospedaliere

Agenti patogeni tradizionali, quali per esempio il virus influenzale, i virus dell’epatite, le Salmonelle, etc… che, oltre ai pazienti, possono colpire anche il personale di assistenza. Agenti opportunisti, vale a dire tutti quei microrganismi che aggrediscono l’ospite solo quando si determinano condizioni tali da consentire il loro impianto in distretti normalmente sterili e/o quando si verifica una diminuzione a vario livello delle difese dell’ospite.

Modalità di trasmissione Il serbatoio di questi microrganismi (habitat naturale e sede di moltiplicazione) è costituito dall’uomo (pz infetti/colonizzati e/o portatori) e dall’ambiente. Affinchè avvenga la trasmissione del m. o. è necessario che vi sia un veicolo. Un veicolo di importanza determinante è costituito dalle MANI degli operatori sanitari, sulle quali colonizzano un numero e una varietà non indifferente di potenziali patogeni. L’importanza di tale veicolo è sottolineato dal fatto che le misure di controllo più efficaci della maggior parte delle I. O. si basano sul lavaggio frequente delle mani.

Classificazione Le infezioni ospedaliere relativamente alla provenienza dell’agente eziologico, si distinguono in: 1. ENDOGENE , quando l’infezione è sostenuta da un agente già da tempo presente nell’organismo del soggetto in causa, in veste di ospite abituale non patogeno, ma che ha acquistato patogenicità e virulenza in seguito a una grave compromissione delle difese dell’organismo; 2. ESOGENE , sono le infezioni in cui il germe arriva al pz trasmesso da un altro pz (infezione crociata) o dall’ambiente ospedaliero, secondo due principali modalità: Contatto diretto , in cui il pz viene a diretto contatto con la fonte di infezione ( ad es. goccioline di saliva); Contatto indiretto , in cui il m. o. è trasportato dalla fonte di infezione all’ospite recettivo da un veicolo animato o inanimato (per es. endoscopi, strumenti chirurgici, etc…).

DEFINIZIONE DI CASO Deve avere un valore predittivo positivo, quindi, deve essere dotata di alta sensibilità ed elevata specificità Si parla di caso quando la sintomatologia sia insorta a partire dal terzo giorno di degenza, oppure la sintomatologia è presente anche prima del terzo giorno ma il paziente è stato ricoverato nuovamente meno di 2 giorni prima in un ospedale per acuti. Viene considerato caso quando vi è infezione anche prima del giorno 3 ma è presente un dispositivo invasivo il giorno 1 o il giorno 2

DEFINIZIONE DI CASO Si parla di caso quando un paziente viene ricoverato con una infezione da C. Difficile essendo stato dimesso meno di 28 giorni da un ospedale per acuti

Localizzazioni più frequenti VIE URINARIE : per parlare di infezioni delle vie urinarie sintomatiche è necessario che vi sia la presenza di almeno uno dei seguenti sintomi/segni, in assenza di altri possibili cause: - febbre (>38°C); -urgenza a urinare; - pollachiuria; - disuria; - tensione sovrapubica.

I microrganismi causa di infezione delle vie urinarie possono avere accesso alla vescica in questo modo: Al momento dell’inserzione del catetere 2. Attraverso il lume del catetere 3. Sulla superficie esterna del catetere 4. Dopo la rimozione del catetere 1.

Tra i principali fattori che favoriscono lo sviluppo di I. V. U. associate a cateterismo vi è la suscettibilità intrinseca del catetere alla contaminazione. Negli ultimi anni, inoltre, è stato messo in evidenza come alcuni patogeni urinari, quali Pseudomonas e Proteus, abbiano la capacità di produrre una matrice extracellulare di glicocalice batterico che consente loro di aderire alla superfice plastica del catetere.

Polmonite nosocomiale, secondo il protocollo HELICS 1997 la polmonite definita o probabile deve corrispondere al seguente criterio: 1. Presenza di infiltrato polmonare nuovo (progressivo) o persistente, 2. Secrezioni tracheali purulente; 3. Almeno uno dei seguenti: - evidenza radiografica di ascesso polmonare e coltura positiva dell’agoaspirato dell’ascesso; - evidenze patologiche di polmonite all’esame istologico ottenuto con biopsia del polmone a cielo aperto o durante il riscontro autoptico subito dopo il decesso, che dimostrino la formazione di un ascesso , oppure un’area di consolidamento con intenso accumulo di leucociti PNM, in associazione a coltura quantitativa positiva del parenchima polmonare; - coltura quantitativa positiva di un campione di secrezioni del tratto respiratorio inferiore; - emocoltura positiva, non correlata ad alcuna fonte di infezione ottenuta entro 48 h dall’isolamentodello stesso ceppo dalle secrezioni del tratto respiratorio inferioree mediante aspirato tracheale; - isolamento dello stesso ceppo da campioni di liquido pleurico e tratto respiratorio inferiore. Non deve essere stata effettuata alcuna procedura invasiva precedente sulla pleura; - isolamento di Legionella dall’espettorato e sierologia specifica positiva.

I batteri possono invadere il tratto respiratorio inferiore attraverso quattro meccanismi: Aspirazione di batteri colonizzanti il tratto orofaringeo o gastrico. Inalazione di aerosol contenenti batteri. Diffusione ematogena di batteri da una localizzazione remota (meno frequente rispetto agli altri); Traslocazione batterica dal tratto gastrointestinale (ipotesi più recente!).

Infezioni del sito chirurgico, L’infezione si sviluppa entro 30 gg dall’intervento; L’infezione interessa soltanto la cute o il tessuto sottocutaneo dell’incisione SSI-S (incisionale superficiale) e si mnoifesta entro 30 giorni L’infezione coinvolge i tessuti molli e si manifesta entro 30 giorni o entro un anno in caso di impianto di protesi SSI-D (incisionale profonda) L’infezione si manifesta entro 30 giorni o un anno in caso di protesi e coinvolge un qualsiasi distretto anatomico, organo o spazio, che sia stato inciso durante l’intervento SSI-O Naturalmente in tutti e tre i casi vi è secrezione purulenta che nel caso di SSI-O è da tubo di drenaggio.

La maggior parte delle infezioni della ferita chirurgica viene acquisita durante l’intervento: se una ferita è pulita e asciutta, infatti, nell’arco di poche ore dall’intervento non è più suscettibile all’aggressione da parte di m. o.

In fase postoperatoria, le infezioni possono essere acquisite attraverso i drenaggi chirurgici o, nel caso di infezioni non ancora rimarginate al momento della medicazione. Le più comuni fonti per l’infezione chirurgica sono: flora cutanea del pz; tessuti dell’ospite infetti o contaminati nel corso di interventi; mani del personale; drenaggi chirurgici.

Importante!! I m. o. patogeni responsabili di I. O. sono nel 70% dei casi resistenti a uno o più antibiotici.

Sistemi di tipizzazione epidemiologica E’ un metodo importante per controllare la diffusione di m. o. resistenti agli antibiotici, sia a livello intraospedaliero che interospedaliero.

Perché è importante la tipizzazione? Per confermare e delineare i profili di trasmissione di uno o più cloni epidemici, per identificare le fonti e i veicoli di trasmissione di questi cloni e per monitorare i serbatoi dei m. o. epidemici.

INFEZIONE CATETERE CORRELATA Infezione locale correlata a catetere a CVC o PVC. Infezione sistemica correlata a CVC o PVC.

FATTORI DI RISCHIO

Definizione Per fattore di rischio si intende: una condizione generica che: provoca (fattore causale) o, più spesso, facilita (concausa) l’instaurarsi di una malattia.

I fattori causali possono essere: - necessari (conditio sine qua non) - sufficienti (quando producono inevitabilmente un particolare effetto) Le concause si dividono in: -predisponenti; -precipitanti; -rinforzanti.

Per definire se un fattore è causale nei confronti di una patologia, deve possedere una serie di criteri: üSequenza temporale üPlausibilità biologica üForza o grado üConsistenza üRelazione dose risposta

Classificazione fattori intriseci (associati alle condizioni del paziente) fattori estrinseci -associati a procedure invasive e assistenziali -associati alla mancata adozione delle misure generali di prevenzione -associati a caratteristiche organizzative dell’ospedale

Fattori di rischio intrinseci • Età

INCIDENZA PER FASCE DI ETA’ Le fasce al di sotto dei 10 anni ed oltre i 65 anni sono quelle maggiormente colpite Il neonato pretermine presenta un rischio d'infezione particolarmente elevato in ragione dell'immaturità del suo sistema immunitario e di diversi organi, come pelle, polmoni o tratto intestinale. Sono, nello stesso tempo veicolo di infezione per altri pazienti (abbondanza di secrezioni respiratorie, l'incontinenza di feci o urina, contatti fisici stretti durante il gioco o nel corso di cure mediche).

L’over 65 presenta, un rischio d'infezione particolarmente elevato in ragione della frequente coesistenza di affezioni degenerative (es. apparato respiratorio), riduzione delle difese immunitarie.

UOMINI DONNE 66, 7% 33, 3% “Sorveglianza delle infezioni del sito chirurgico in Cardiochirurgia INCIDENZA E FATTORI DI RISCHIO” 4 maggio 2004. AZIENDA OSPEDALIERA “SANTA MARIA DELLA MISERICORDIA” DI RILIEVO NAZIONALE E DI ALTA SPECIALIZZAZIONE – UDINE

-Obesità • Stato nutrizionale -Denutrizione (stati carenziali) proteine, immunoglobuline, complemento) Aumentano il rischio infettivo di 2 -3 volte. Determinano un ritardo nella guarigione delle ferite, conseguente aumento dell’ospedalizzazione e incremento delle complicanze chirurgiche.

• Gravi malattie di base • Endocrinopatie • BPCO • Neoplasie • Splenectomizzati • Ustioni estese • IRC • Deficit immunitari(leucemie) • Politraumatismi USO IMPROPRIO DI FARMACI Antibiotici, chemioterapici, immunosoppressori

Cause di deficit immunitario Diminuzione di Neutrofili linfociti T (CD 4+) linfociti B macrofagi alveolari fagociti piastrine

Fattori di rischio estrinseci Associati a procedure invasive e assistenziali • Presenza di cateteri intravascolari

Si ricorre al loro impianto, nel corso della degenza, nel 30 -50% dei pazienti ospedalizzati. Perché sono considerati fattori di rischio… • corpo estraneo per l’organismo. Rappresentano, un substrato ideale per la colonizzazione microbica ; • materiale: Cateteri polietilene (flebite purulenta e flogosi del sito di inserzione: eritema edema dolore e vena palpabile). Oggi vengono usati cateteri in poliuretano (>biocompatibilità, <colonizzazione microbica, < trombogenicità ). • Manipolazione e tempo di permanenza in sede Il rischio di infezioni è basso se il catetere subisce poche manipolazioni ed è mantenuto in situ per meno di tre giorni.

- Presenza e durata della permanenza del catetere urinario (UVI)

Applicare il catetere solo in presenza di precise indicazioni cliniche -Rimuovere il catetere appena l’indicazione cessa di esistere -Corretto lavaggio antisettico delle mani prima di applicare o rimuovere il catetere -Corretta detersione dei genitali prima della disinfezione -Utilizzare sempre sacche di drenaggio a circuito chiuso e non scollegare mai la sacca -Utilizzare catetere di calibro il più piccolo possibile (12 o 14 CH) -Garantire una scrupolosa igiene ai pazienti portatori di catetere vescicale.

Respirazione assistita con intubazione endotracheale, VAM Indagini invasive a scopo diagnostico (broncoscopie)

• Accertati: tricotomia durata dell’intervento (la frequenza di infezione si raddoppia per ogni ora di intervento) tipo di intervento (pulito, contaminato, sporco) classe ASA (ASA score 1 -5) • Probabili: Interventi chirurgici interventi chirurgici combinati entità del trauma chirurgico uso di materiali estranei (protesi) emotrasfusioni • Possibili: non effettuare la doccia prima dell’intervento d’urgenza uso di drenaggi.

TRICOTOMIA Contenere l’area da tricotomizzare alla sola area di incisione chirurgica • Eseguire la procedura con strumenti monouso evitando di lesionare la cute • Praticare in stretta connessione temporale con l’intervento chirurgico (entro 2 -4 ore dall’inizio della procedura chirurgica).

Durata dell’intervento Esiste un rapporto diretto tra durata dell’intervento e incidenza di infezione postoperatoria. Tra i vari meccanismi, ipotizzati, responsabili ricordiamo: 1)progressiva riduzione della resistenza locale dei tessuti a causa delle manipolazioni chirurgiche, dell’essiccamento e dell’esposizione all’aria; 2) complicanze (anemia, shock, …) dirette responsabili della maggiore durata dell’intervento, in grado di compromettere i meccanismi di resistenza generali.

Tipo di intervento % Infezioni Tipo di intervento Interventi sul colon 7, 1 Chirurgia vascolare 2, 9 trapianti d'organo 6, 9 Nefrectomia 2, 5 vie biliari, fegato, pancreas 6, 2 Chirurgia toracica 2, 5 Amputazione di arto 6, 1 Protesi articolare 2, 4 Chirurgia gastrica 5, 8 Craniotomia 2, 3 Intestino tenue 5, 8 Appendicectomia 2, 2 Taglio cesario 4, 1 Colecistectomia 2, 2 Shunt ventricolare 4, 1 Fusione spinale 2, 1 Isterectomia addominale 3, 8 Mastectomia 1, 9 Cardiochirurgia 3, 7 Isterectomia vaginale 1, 9 Bypass aorta coronarico 3, 6 Chirurgia testa collo 1, 8 Trapianto di cute 3, 4 Riduzione frattura 1, 7 Laparotomia 3, 1 Ernioraffia 1, 2 Splenectomia 3 Prostatectomia 1, 2 % Infezioni


Entità del trauma chirurgico Una tecnica chirurgica impeccabile in grado di minimizzare il trauma chirurgico, viene considerata di fondamentale importanza per limitare il rischio infettivo e per una corretta guarigione della ferita. • Mantenere un’adeguato apporto di sangue • Effettuare un’emostasi corretta • Allontanare i tessuti devitalizzati • Irrigare il campo operatorio con soluzione fisiologica negli interventi di lunga durata • Usare appropriati materiali per sutura cercando di non determinare eccessiva tensione dei margini.

Associati alla mancata adozione di misure generali di prevenzione Carenze strutturali, organizzative, igieniche Lavaggio accurato e metodico delle mani Doccia o bagno preoperatorio (clorexidine) Misure di igiene personale del paziente e del personale Corrette politiche di disinfezione e sterilizzazione (superfici, tute e camici dell’equipe, teli) Ventilazione dell’ambiente operatorio. Il livello di contaminazione microbica nell’aria delle sale è direttamente proporzionale al numero di persone che si muovono nella stanza (calcolo della cubatura).

Il lavaggio delle mani rappresenta da solo il mezzo più importanti ed efficace per prevenire la trasmissione delle infezioni. Lavaggio sociale delle mani -bagnare mani e polsi con acqua corrente. -Applicare uniformemente 5 ml di soluzione antisettica con detergente -frizionare accuratamente unghie, dita, palmi e dorsi delle mani, polsi e parte degli avambracci per almeno 1 -2 minuti -Sciacquare accuratamente sotto l’acqua corrente -Asciugare con salviette monouso (tamponando) -Se non c’è rubinetto a gomito o pedale con la salvietta chiudere il rubinetto.

Lavaggio antisettico delle mani - bagnare uniformemente mani e avambracci fino a 2 dita al di sopra della piega dei gomiti, tenendo le mani più alte rispetto ai gomiti; - distribuire uniformemente 5 ml di soluzione antisettica, premendo la leva del diffusore con il gomito - strofinare accuratamente facendo particolare attenzione agli spazi ungueali ed interdigitali per 2 minuti, procedere in un unico senso dalle mani ai gomiti; - risciacquare prima le mani e dopo gli avambracci avendo cura di tenere le mani al disopra del livello dei gomiti per evitare che l’acqua dagli avambracci coli sulle mani. - spazzolare le unghie 30 secondi per mano e ripetere il lavaggio per altre due volte. - risciacquare mani -Asciugare mani e avambracci con un panno sterile.

Associati a caratteristiche organizzative dell’ospedale Durata della degenza Carenza del personale Mancanza di informazione e formazione del personale ospedaliero Norme comportamentali

SORVEGLIANZA

DEFINIZIONE Raccolta sistematica e progressiva, analisi ed interpretazione di dati sulla salute essenziali alla pianificazione, al miglioramento, alla valutazione di attività in Sanità Pubblica, strettamente integrati con una periodica diffusione a quanti ne hanno necessità. L’obbiettivo finale è l’uso di questi dati per la prevenzione ed il controllo. WHO, 1968; CDC, 1986

La circolare ministeriale n. 8/1988 descrive i principali sistemi di sorveglianza adottabili dai singoli ospedali seconda dei problemi presenti e delle risorse disponibili: - sorveglianza basata sul laboratorio - sorveglianza attraverso studi di prevalenza - sistemi di sorveglianza continuativa di reparti ad alto rischio - sorveglianza orientata per problemi

OBIETTIVI -1 Dovrebbe garantire informazioni correnti ed accurate sulla distribuzione delle infezioni nella popolazione di pazienti studiata e sui fattori che contribuiscono significativamente all’insorgenza delle infezioni per poterli contenere al fine di poter predisporre ed orientare interventi di prevenzione e controllo

OBIETTIVI -2 Determinare l’ andamento delle IO nel tempo (definizione dei livelli di endemia) Individuare precocemente le epidemie o comunque eventuali scostamenti rispetto ai livelli endemici Identificare specifici fattori di rischio rispetto a categorie di individui, a procedure/pratiche assistenziali

OBIETTIVI -3 Informare il personale sanitario sui rischi esistenti rispetto alle procedure che vengono erogate Verificare il raggiungimento degli obiettivi ovvero valutare l’utilità e l’efficienza dei programmi adottati

OBIETTIVI –conclusioni Descrivere la frequenza delle infezioni ospedaliere Formulare ipotesi sui fattori di rischio Valutare le misure di controllo adottate Sensibilizzare/coinvolgere gli operatori sanitari Generare ipotesi per specifici progetti di ricerca

METODI PER CONDURRE LA SORVEGLIANZA Sorveglianza orientata sul paziente Sorveglianza basata sui dati di laboratorio

SORVEGLIANZA ORIENTATA AL PAZIENTE viene svolta in reparto attraverso la revisione di documenti sanitari ed il colloquio con il personale del reparto Si attua attraverso studi di prevalenza ed incidenza

SORVEGLIANZA ORIENTATA AL PAZIENTE Estensione § Tutto l’ospedale § Solo reparti a rischio § Per obiettivi Tipo di eventi sotto sorveglianza § Tutte le infezioni § Infezioni selezionate § Variabili di processo Frequenza temporale § Continuativa § Periodica § In relazione all’obiettivo

PREVALENZA Si ottiene esaminando i pazienti ricoverati ad un dato momento e rilevando le infezioni presenti La popolazione esaminata è rappresentata dai ricoverati presenti ad un dato momento in ospedale

PREVALENZA VANTAGGI § Facile sul piano organizzativo § Rapida ed economica § Identifica le aree di maggiore rischio SVANTAGGI § Ridotti periodi di osservazione § Le stime ottenute non rappresentano indicatori clinici che consentano il confronto tra ospedali/reparti nel tempo § Rischia di offrire una immagine distorta

INCIDENZA Si ottiene seguendo i pazienti nel corso del ricovero ospedaliero e, in alcuni casi, anche dopo la dimissione Registra tutti i nuovi casi di infezione insorti La popolazione esaminata è rappresentata dai pazienti che si ricoverano in un determinato periodo di tempo (ad es. , 6 mesi)

INCIDENZA VANTAGGI § Più accurata § Possibile stima della frequenza di infezioni in pazienti esposti a procedure invasive § Utile ad effettuare confronti nello spazio e nel tempo tra i vari reparti/ospedali SVANTAGGI § Tempo § Risorse umane § Costi

SORVEGLIANZA BASATA SUI DATI DI LABORATORIO Consente di descrivere accuratamente le infezioni in termini qualitativi Non è strumento per la rilevazione quantitativa di indicatori specifici indirizzati a gruppi di pazienti e alla esposizione alle procedure a rischio

SORVEGLIANZA BASATA SUI DATI DI LABORATORIO OBIETTIVI Identificare microrganismi “pericolosi” (“alert organism”) Identificare epidemie sostenute da un unico microrganismo Monitorare le resistenze

SORVEGIANZA BASATA SUI DATI DI LABORATORIO SVANTAGGI § Fornisce un andamento § Non può essere utilizzata da sola periodico degli monitorare isolamenti e delle l’andamento delle resistenze infezioni § Permette di avere delle § Identifica solo i casi per soglie di riferimento i quali sia stato chiesto rispetto agli isolamenti l’esame colturale § Se disponibili alcune § Identifica le IO solo se tecniche di biologia nella richiesta è molecolare specificato il sospetto identificano le vie di trasmissione

SORVEGLIANZA BASATA SUI DATI DI LABORATORIO PROCEDURE DA STANDARDIZZARE Protocolli di prelievo e trasporto dei campioni Protocolli di indagine microbiologica, da richiedere in presenza di segni/sintomi di infezione Moduli di richiesta esami che contengano alcuni dati di base (data del ricovero, data di insorgenza dei sintomi) Controlli di qualità degli esami di laboratorio

FONTI UTILIZZATE PER I DATI Esame del paziente Colloqui con operatori Cartelle cliniche Referti di laboratorio Referti di diagnostica per immagini SDO, DRG, referti ambulatoriali, ecc. Denunce obbligatorie Dati amministrativi Registri interni Medico competente Consumi di farmacia (farmaci e presidi)

FLUSSO INFORMATIVO Evento Intervento preventivo o di controllo ICI, DS CIO - reparti Rilevatore Segnalazione al sistema (passiva/attiva) Raccolta ed analisi dati Risultati

SORVEGLIANZA PASSIVA Si aspetta che i dati, le notifiche, le informazioni, arrivino senza sollecitazioni dirette § I dati vengono ottenuti normalmente tramite segnalazione a chi gestisce la sorveglianza da parte degli addetti all’assistenza §

SORVEGLIANZA PASSIVA VANTAGGI Economica Costante Richiede meno tempo I dati possono mostrare il trend delle IO SVANTAGGI Identifica il 14 -34% delle IO È legata alla sensibilità culturale È poco controllabile Può non essere in grado di evidenziare possibili epidemie Può non essere rappresentativa

SORVEGLIANZA ATTIVA I dati e le informazioni vengono prese dagli operatori che si occupano della sorveglianza, in modo più o meno particolareggiato e ad intervalli di tempo prefissati. I dati vengono ottenuti contattando regolarmente da parte di chi gestisce la sorveglianza quanti, singoli e/o istituti, rappresentano le probabili fonti di informazione sull’evento I metodi utilizzabili in reparto sono le indagini di INCIDENZA e PREVALENZA

SORVEGLIANZA ATTIVA VANTAGGI Identifica l’ 85 -100% delle IO Tempestiva Qualitativa (completezza ed affidabilità) Controllabile Permette di agire SVANTAGGI Maggiore costo Maggiore tempo Maggiore dispendio energetico

PIANIFICARE UNA SORVEGLIANZA Stabilire gli obiettivi Sviluppare la definizione di caso Sviluppare il sistema di raccolta dei dati Sviluppare gli strumenti di raccolta dei dati

PIANIFICARE UNA SORVEGLIANZA Sviluppare i metodi di valutazione Sviluppare l’analisi dei dati Determinare il feed-back dei dati Determinare i metodi per la valutazione del sistema

Lo studio SENIC ha dimostrato come una frazione pari al 30% di tutte le IO sia prevenibile in presenza di alcuni requisiti organizzativi come un buon sistema di sorveglianza

In Italia non esiste un sistema di sorveglianza standardizzato ed applicato in tutti i presidi ospedalieri. A tal riguardo, il PSN 98 -00 rifacendosi alle linee guida dello statunitense NNIS System, ha stabilito delle indicazioni operative per ridurre del 25% le infezioni ospedaliere nel nostro sistema sanitario

INDICAZIONI OPERATIVE PSN 98 -00 Introdurre misure efficaci Attivare i comitati di controllo delle IO (CIO) Sorvegliare le IO Definire procedure e protocolli condivisi Formare gli operatori Curare l’aggiornamento continuo

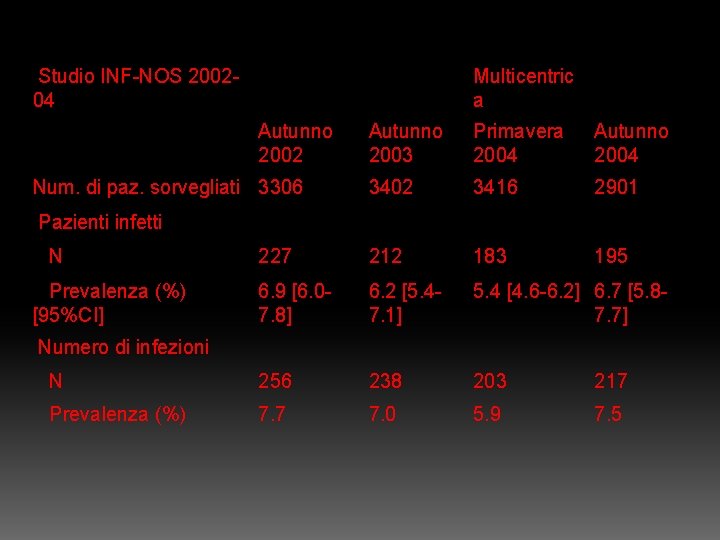
Studio INF-NOS 200204 Multicentric a Autunno 2002 Num. di paz. sorvegliati 3306 Autunno 2003 Primavera 2004 Autunno 2004 3402 3416 2901 195 Pazienti infetti N 227 212 183 Prevalenza (%) [95%CI] 6. 9 [6. 07. 8] 6. 2 [5. 47. 1] 5. 4 [4. 6 -6. 2] 6. 7 [5. 87. 7] N 256 238 203 217 Prevalenza (%) 7. 7 7. 0 5. 9 7. 5 Numero di infezioni

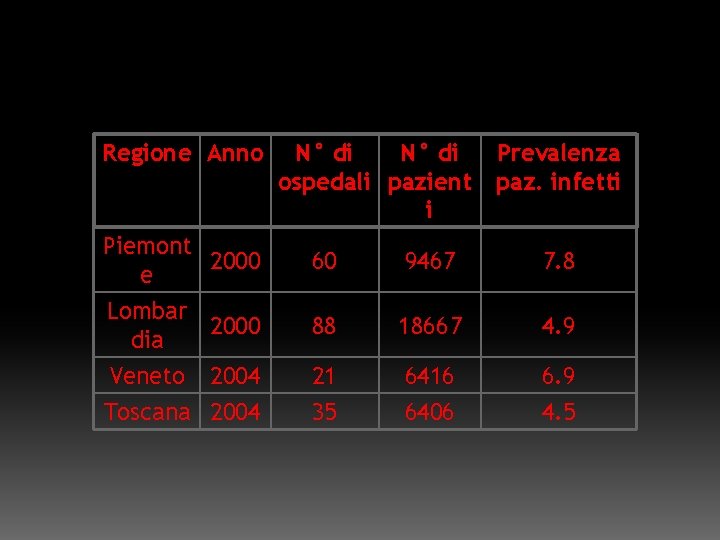
Regione Anno N° di ospedali pazient i Prevalenza paz. infetti Piemont 2000 e 60 9467 7. 8 Lombar 2000 dia 88 18667 4. 9 Veneto 2004 Toscana 2004 21 35 6416 6406 6. 9 4. 5

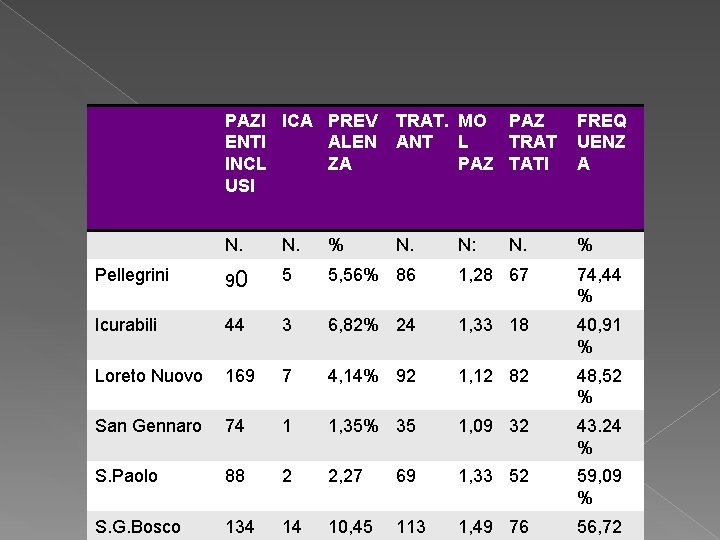
PAZI ICA PREV ENTI ALEN INCL ZA USI TRAT. MO PAZ ANT L TRAT PAZ TATI FREQ UENZ A N. % Pellegrini 90 5 5, 56% 86 1, 28 67 74, 44 % Icurabili 44 3 6, 82% 24 1, 33 18 40, 91 % Loreto Nuovo 169 7 4, 14% 92 1, 12 82 48, 52 % San Gennaro 74 1 1, 35% 35 1, 09 32 43. 24 % S. Paolo 88 2 2, 27 69 1, 33 52 59, 09 % S. G. Bosco 134 14 10, 45 113 1, 49 76 56, 72 N: N.

Sorveglianza delle infezioni del sito chirurgico in Campania Nel periodo gennaio 2011 -dicembre 2014 in 21 ospedali della Campania sono stati sorvegliati 9063 interventi relativi a 31 categorie chirurgiche per interventi non protesici Per l’asl Napoli 1 hanno partecipato il P. O. San Paolo, Il P. O. Loreto Nuovo, il P. O. San Gennaro, Il P. O. San Giovanni Bosco e il P. O. Pellegrini

Sorveglianza delle infezioni del sito chirurgico in Campania Nella popolazione sorvegliata il tasso di infezione è stato pari allo 1, 2% determinato da 112 infezioni Il 38. 4% delle infezioni è sto rilevato nel follow-up post dimissione

Sorveglianza delle infezioni del sito chirurgico in Campania La mediana del tempo di latenza per l’insorgenza delle infezioni è stata complessivamente pari a 10 giorni Il 25% delle infezioni è risultato di tipo non superficiale; in particolare il 13, 4% erano profonde e il 11, 6% coinvolgeva organi e spazi

Sorveglianza delle infezioni del sito chirurgico in Campania Nel periodo gennaio 2011 -dicembre 2013 in 8 ospedali della Campania sono stati sorvegliati 754 interventi relativi a 12 categorie chirurgiche con utilizzo di materiale protesico Nella popolazione sorvegliata il tasso di infezionee è stato pari allo 0, 3% determinato da 2 infezioni rilevate

La Governance del rischio infettivo Le infezioni correlate all’assistenza sono da considerarsi come indicatori della qualità del servizio offerto ai pazienti Le infezioni possono essere considerate di fatto come “errori in medicina” L’integrazione tra gruppi operativi dei cio e servizio qualità/rischio clinico può migliorare l’efficacia del governo della problematica del rischio infettivo

La Governance del rischio infettivo In una asl Abruzzese sono stati portati avanti interventi applicando il modello PDCA e del Risk Assessment Il primo intervento è stato valutare il livello di sicurezza dei pazienti in ospedale relativamente al rischio infettivo

La Governance del rischio infettivo Sono stati individuati due infermieri specialisti sul rischio infettivo come coordinatori, dieci infermieri part time per le attività di sorveglianza e un referente per P. O. Come riferimento locale Le unità operative sono state coinvolte attraverso i referenti per il rischio clinico

La Governance del rischio infettivo Indagini conoscitive: Sono stati utilizzati questionari e audit per rilevare criticità e sono state effettuate indagini di prevalenza e analisi osservazionali per rilevare l’adesione all’igiene delle mani Azioni: Revisione di tutte le procedure esistenti e implementazione di quelle mancanti

La Governance del rischio infettivo Sono stati scelti sei bundle come strategia di prevenzione: SSI, Inf. da catetere intravascolare e catetere urinario, inf. Da C: D: , controllo germi multiresistenti. Per ogni bundle è stata predisposta una checklist da inserire in cartella

La Governance del rischio infettivo La sorveglianza delle infezioni è stata effettuata in sede di ricovero e con follow-up telefonico Individuazione pazienti con germi multiresistenti su cui applicare misure di controllo Omogenizzazione reportistica sui patogeni sentinella, sui consumi di antibiotici e di gel idroalcolico

La Governance del rischio infettivo Analisi delle richieste di risarcimento per problemi di ica Realizzare poster sui diversi aspetti della prevenzione Molta enfasi è stata data ai corsi di formazione e ai percorsi di audit

La Governance del rischio infettivo Esempio di Bundle per la prevenzione delle polminiti: Sollevare la testata del letto di 30°- 45° Valutare ogni giorno ka sospensione della sedazione farmacologica Eseguire igiene del cavo orale con clorexedina Eseguire l’aspirazione continua delle secrezioni subglottidee

La Governance del rischio infettivo E’ stata fatto successivamente una intensa attività di verifica e monitoraggio con report condivisi in audit effettuati sempre in collaborazione con il servizio Qualità/Rischio Clinico

La Governance del rischio infettivo Risultati: Variazione dell’incidenza delle ISC Diminuzione della spesa totale per antibiotici Incremento dell’uso della cefazolina in profilassi perioperatoria

La Governance del rischio infettivo Incremento di utilizzo di gel alcolico Aumento della compliance degli operatori al lavaggio delle mani Decremento degli isolamenti di patogeni santinella

ANTIBIOTICO RESISTENZA E’ la capacità dei batteri di essere o di diventare resistenti nei confronti degli antibiotici e rappresenta sicuramente il maggior problema dell’antibiotico-terapia, problema di grande attualità e di profondo impatto pratico, in quanto condiziona la scelta, l’impiego e il futuro della chemioterapia stessa. Inizia con la nascita di quest'ultima e ne segue costantemente il decorso.

ANTIBIOTICO RESISTENZA Resistenza naturale (origine naturale): Insensibilità costituzionale di un microrganismo verso un determinato antibiotico: Immutabile nel tempo, geneticamente determinata Si manifesta in tutti i ceppi di una stessa specie

ANTIBIOTICO RESISTENZA Dipende: caratteristiche dell’antibiotico strutture del microrganismo mancata penetrazione del farmaco attraverso le strutture esterne del microrganismo Es. insensibilità degli enterobatteri per la penicillina o dei batteri Gram negativi per i glicopeptidi

ANTIBIOTICO RESISTENZA Resistenza acquisita: Comparsa di ceppi che, nell’ambito di una specie microbica originariamente sensibile ad un chemioterapico, hanno perduto la sensibilità verso concentrazioni del farmaco terapeuticamente raggiungibili in vivo. E’ favorita dall’elevata velocità con cui i batteri si dividono. Si divide in cromosomica (o endogena) ed extracromosomica (o esogena)

ANTIBIOTICO RESISTENZA Resistenza cromosomica: Costituisce solo il 10 -15% di tutte le resistenze acquisite (bassa frequenza di insorgenza) Si realizza tramite un’alterazione mutazionale spontanea dell’informazione genetica cromosomica

ANTIBIOTICO RESISTENZA L’antibiotico esercita un’azione selettiva (seleziona i mutanti resistenti, inibendo le cellule sensibili) Tale resistenza interessa solo l’antibiotico verso il quale sono stati isolati i mutanti resistenti Gli stessi mutanti possono essere resistenti anche ad altri antibiotici con caratteristiche simili (resistenza crociata o crossresistenza)

ANTIBIOTICO RESISTENZA Si trasmette verticalmente tramite la discendenza (da cellula madre a cellula figlia) Può essere: multi-step sono necessarie più mutazioni perché possa instaurarsi (es. beta-lattamine, macrolidi, cloramfenicolo) one-step è sufficiente una sola mutazione per determinare la comparsa di ceppi totalmente resistenti (es. rifamicine, chinoloni)

ANTIBIOTICO RESISTENZA Resistenza extracromosomica: Costituisce il 90% di tutte le resistenze (alta frequenza di insorgenza) Si origina per acquisizione di nuova informazione genetica che deriva da altri microrganismi e che penetra nella cellula mediante i meccanismi di coniugazione, trasformazione e traduzione)

ANTIBIOTICO RESISTENZA Riguarda più antibiotici contemporaneamente (resistenza multipla) E’ a trasmissione orizzontale (tramite lo scambio genetico) Può essere trasferita anche a microrganismi appartenente a specie differenti (resistenza contagiosa) E’ dovuta a geni presenti su plasmidi o trasposoni (elementi genici mobili)

ANTIBIOTICO RESISTENZA I meccanismi attraverso i quali può instaurarsi una resistenza antibiotica sono: ridotta permeabilità cellulare aumentato efflusso alterazione del bersaglio produzione di enzimi inattivanti

ANTIBIOTICO RESISTENZA Ridotta Permeabilitò Cellulare: la penetrazione di un antibiotico può essere ridotta da cambiamenti strutturali negli involucri superficiali della cellula. Nei Gram- la resistenza può essere dovuta ad alterazione delle porine. (proteine di membrana attraverso le quali penetrano molti antibiotici)

ANTIBIOTICO RESISTENZA Aumentato efflusso: l’antibiotico penetrato nella cellula batterica è allontanato da sistemi di efflusso. Nei Gram- le pompe di efflusso operano accoppiate a ” proteine canale” che provocano l’espulsione diretta del farmaco

ANTIBIOTICO RESISTENZA Alterazione del bersaglio: il bersaglio dell’antibiotico è alterato e non è più riconosciuto dall’antibiotico. Tale strategia si realizza tramite: · ridotta affinità per il bersaglio (si produce un cambiamento che, pur non variando l’attività biologica del bersaglio, ne riduce la capacità di legame con l’antibiotico)

ANTIBIOTICO RESISTENZA · iperproduzione del bersaglio (si realizza un’aumentata sintesi del bersaglio che elude l’azione dell’antibiotico) · sostituzione del bersaglio (la resistenza è dovuta ad acquisizione di un gene che codifica per un bersaglio per il quale l’antibiotico non ha affinità) · modifica enzimatica del bersaglio (il bersaglio è modificato enzimaticamente e non è più riconosciuto dall’antibiotico)

ANTIBIOTICO RESISTENZA Produzione di enzimi inattivanti: l’antibiotico perde la sua attività biologica, poiché viene inattivato da enzimi specifici. (beta-lattamasi, acetiltransferasi, fosfotransferasi, adeniltransferasi)

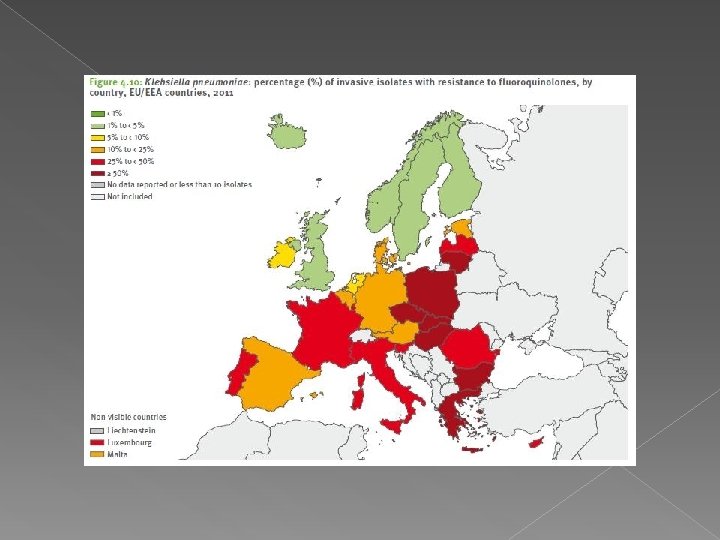
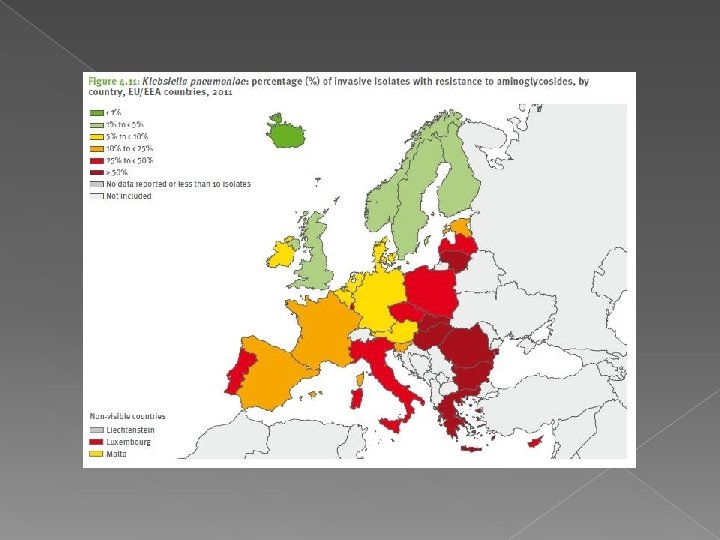
ANTIBIOTICO RESISTENZA Secondo la sorveglianza dell’antibioticoresistenza coordinata dall’Istituto superiore di sanità , in Italia la resistenza agli antibiotici si mantiene purtroppo tra le più elevate in Europa e quasi sempre al di sopra della media europea. Nel quadriennio 2010 -2013 nelle specie Gram-negative si è osservato un trend prevalentemente in aumento.

ANTIBIOTICO RESISTENZA Questo incremento è relativo soprattutto ai Fluorochinoloni, cefalosporine di III generazione e aminoglicosidi in E. coli, K. pneu. L’aumento è stato rilevato per Pse. aeru. pepiparacillina+tazobactam, ceftazidime, aminoglicosidi. Drammatico è stato l’aumento della resistenza ai carbapenemici in K. pneumoniae che in 6 anni è aumentata da meno dell’ 1% delle Klebsielle resistenti nel 2008 al 34% nel 2013.

ANTIBIOTICO RESISTENZA I dati di resistenza per i patogeni Gram positivi sono invece tendenzialmente stabili, ma sempre elevati: in S. pneumoniae la non sensibilità alla penicillina (14% del 2013) è in leggero aumento rispetto gli anni precedenti mentre la resistenza ai macrolidi (25% nel 2013) è in leggero calo rispetto agli anni precedenti; in S. aureus la resistenza alla meticillina (36% nel 2013) è stabile.

ANTIBIOTICO RESISTENZA La sorveglianza ha confermato, inoltre, che i livelli di resistenza sono più alti al Centro- Sud rispetto al Nord Italia, dato in relazione con il maggior consumo di antibiotici registrato in queste aree geografiche. I cambiamenti nei dati italiani vanno interpretati con cautela a causa della variabilità dei laboratori partecipanti che negli ultimi due anni includono un maggior numero di laboratori del Sud Italia.

ANTIBIOTICO RESISTENZA Molti di questi dati sono contenuti nel rapporto “Antimicrobial resistance surveillance in Europe 2013” , pubblicato a novembre 2014 dallo European Centre for Disease Prevention and Control (Ecdc). Il documento presenta le informazioni raccolte dalla sorveglianza europea Ears-Net coordinata dall’Ecdc a cui l’Istituto superiore di sanità fornisce i dati italiani che provengono da circa 40 ospedali partecipanti alle reti Ar-Iss

ANTIBIOTICO RESISTENZA Il rapporto fornisce i dati sulla resistenza agli antibiotici di sette patogeni invasivi, di grande importanza per la sanità pubblica (Escherichia coli, Klebsiella pneumoniae, Pseudomonas aeruginosa, Streptococcus pneumoniae, Staphylococcus aureus, Acinetobacter ed enterococchi) presentando per il 2013 le informazioni segnalate da 30 Paesi.

ANTIBIOTICO RESISTENZA Di fronte all’aumentata resistenza ai carbapenemi, che sono gli antibiotici di ultima linea per le infezioni da patogeni multiresistenti, le alternative terapeutiche sono estremamente scarse. Una possibilità è rappresentata dall’utilizzo di colistina, un vecchio antibiotico con problemi di tossicità, verso il quale, però, i ceppi di K. pneumoniae stanno sviluppando resistenza.

ANTIBIOTICO RESISTENZA Infine, nonostante i dati europei mostrino mostrano una riduzione della percentuale di Mrsa (Staphylococcus aureus resistente alla meticillina) tra il 2010 e il 2013 in tutti i Paesi Ue/See, nel 2013, 7 Paesi su 30 hanno segnalato percentuali di Mrsa superiori al 25% e in Italia questo valore ancor

ANTIBIOTICO RESISTENZA I microrganismi resistenti agli antimicrobici, compresi quelli multiresistenti, sono spesso all’origine delle infezioni associate all’assistenza sanitaria ma anche delle infezioni di pazienti non ricoverati e possono essere presenti nella normale flora batterica di tutte le persone sane, negli animali da compagnia e nell’ambiente

ANTIBIOTICO RESISTENZA I microrganismi resistenti sono responsabili di infezioni e sono presenti anche negli animali destinati alla produzione alimentare, e a volte anche negli alimenti. D’altra parte, molte infezioni associate all’assistenza sanitaria sono causate da microrganismi che non sono resistenti agli antimicrobici.

ANTIBIOTICO RESISTENZA Per resistenza antimicrobica si intende la capacità di un microrganismo di resistere all’azione di un farmaco antimicrobico. Il fenomeno costituisce un adattamento del microrganismo all’ambiente. In presenza di un antimicrobico, il microrganismo è costretto ad adattarsi oppure muore.

ANTIBIOTICO RESISTENZA Sono i microrganismi che colonizzano e talvolta infettano uomini e animali che sviluppano resistenza agli antimicrobici e non l’essere (uomo o animale) colpito. Né l’uomo né l’animale sviluppano resistenza al trattamento antimicrobico, che è invece un fenomeno che riguarda batteri e altri microrganismi.

ANTIBIOTICO RESISTENZA La resistenza antimicrobica comporta una riduzione o la totale perdita di efficacia del farmaco antimicrobico usato per curare o prevenire l’infezione da quel microrganismo. Per multiresistenza si intende la contemporanea resistenza di un microrganismo a più farmaci antimicrobici.

ANTIBIOTICO RESISTENZA Il problema della multiresistenza riguarda tutti i microrganismi, compresi i batteri responsabili delle infezioni associate all’assistenza sanitaria, i microrganismi responsabili delle infezioni trasmesse da acqua e alimenti, la tubercolosi e i microrganismi responsabili delle malattie a trasmissione sessuale, ad esempio gonorrea e HIV.

ANTIBIOTICO RESISTENZA I microrganismi multiresistenti costituiscono un problema particolarmente importante in quanto le terapie alternative sono limitate o addirittura inesistenti. Esempi di batteri multiresistenti più comuni:

ANTIBIOTICO RESISTENZA Staphylococcus aureus resistente alla meticillina (MRSA) Enterococchi resistenti alla vancomicina (VRE) Enterobacteriaceae che producono betalattamasi a spettro esteso (ESBL) (esempi più comuni: Escherichia coli e Klebsiella pneumoniae) Pseudomonas aeruginosa Clostridium difficile

ANTIBIOTICO RESISTENZA I due maggiori fattori causali della resistenza antimicrobica sono: l’uso di antimicrobici, che esercita una pressione ecologica sui microrganismi e contribuisce alla comparsa e alla selezione di microrganismi resistenti agli antimicrobici in varie popolazioni; la diffusione e la trasmissione crociata di microrganismi resistenti agli antimicrobici uomo-uomo, animale-animale e uomoanimale-ambiente.

ANTIBIOTICO RESISTENZA I due maggiori settori di intervento per la gestione, il controllo e la prevenzione della resistenza antimicrobica sono pertanto: uso prudente di antimicrobici (ovvero solo nei casi i cui è realmente necessario, rispettando le dosi, gli intervalli e la durata del trattamento);

ANTIBIOTICO RESISTENZA precauzioni igieniche per il controllo della trasmissione crociata dei microrganismi resistenti agli antimicrobici (controllo delle infezioni) compresa l’igiene delle mani. Gli antibiotici impiegati per trattare e prevenire le infezioni negli animali appartengano alle stesse classi delle sostanze usate in medicina umana, pertanto gli animali possono trasmettere batteri resistenti agli stessi antibiotici.

ANTIBIOTICO RESISTENZA Tuttavia la causa principale di resistenza antimicrobica nei microrganismi che interessano l’uomo rimane l’uso degli antimicrobici in medicina umana, in comunità, in ospedale nonché in altre strutture di assistenza sanitaria. l’assunzione di antibiotici comporta sempre una modificazione della flora batterica normalmente presente, spesso con effetti collaterali (ad es. diarrea) e con la comparsa e/o selezione di batteri antibiotico-resistenti;

ANTIBIOTICO RESISTENZA questi batteri resistenti possono persistere, in generale senza causare infezioni, per un periodo di sei mesi e talvolta oltre; i pazienti colonizzati da batteri resistenti o che ne sono portatori hanno in genere un maggior rischio di sviluppare infezioni da questi batteri piuttosto che da varianti sensibili degli stessi batteri;

ANTIBIOTICO RESISTENZA gli antibiotici non vanno usati quando non sono necessari, ovvero in caso di infezioni virali come il raffreddore o l’influenza; se un antibiotico si rende necessario, esso andrà utilizzato in modo appropriato, ovvero rispettando le dosi, gli intervalli tra una somministrazione e l’altra e la durata del trattamento, in modo da ottimizzare l’efficacia terapeutica e ridurre al minimo la comparsa di resistenza;

ANTIBIOTICO RESISTENZA anche quando gli antibiotici vengono usati correttamente è comunque possibile la comparsa di antibiotico-resistenza, dato che questo fenomeno rappresenta un naturale meccanismo di adattamento dei batteri. In caso di comparsa o proliferazione di batteri resistenti è essenziale adottare precauzioni per il controllo delle infezioni, per evitare la trasmissione dei batteri dai pazienti già infetti ad altri pazienti o altre persone.

ANTIBIOTICO RESISTENZA esistono ampie variazioni da uno Stato dell’UE all’altro per quanto riguarda le percentuali dei batteri resistenti. È tuttavia riconoscibile un gradiente da nord a sud per quanto riguarda la maggior parte dei batteri resistenti osservati dal sistema europeo di sorveglianza della resistenza antimicrobica (EARSS);

ANTIBIOTICO RESISTENZA esistono inoltre ampie variazioni nell’uso degli antibiotici da uno Stato membro all’altro, come emerge dai dati del progetto di sorveglianza europea sul consumo degli antimicrobici (ESAC); in rapporto alla popolazione, gli Stati membri con il più alto uso di antibiotici per la cura dei pazienti ambulatoriali (Grecia e Cipro) usano circa il triplo di antibiotici per abitante/anno rispetto allo Stato membro che ne usa di meno, ovvero i Paesi Bassi;

ANTIBIOTICO RESISTENZA esiste una correlazione costante tra consumo di antibiotici e livelli di resistenza agli antibiotici; in altri termini più gli antibiotici vengono usati in una determinata popolazione, maggiore sarà la resistenza agli antibiotici dei batteri responsabili delle infezioni in quella popolazione.

ANTIBIOTICO RESISTENZA Ai sensi della direttiva 2001/83/CE e delle normative vigenti negli Stati membri, gli antimicrobici per uso sistemico (cioè non locale) vanno distribuiti solo in farmacia dietro presentazione di ricetta medica. Nonostante questo in vari Stati membri accade ancora che in farmacia si possano ottenere antimicrobici anche senza ricetta medica.







 Infezioni anergizzanti
Infezioni anergizzanti Tetrade di sabin toxoplasmosi
Tetrade di sabin toxoplasmosi Prescrizioni normative sistemi controllo fumo
Prescrizioni normative sistemi controllo fumo Ufficio prevenzione infortuni
Ufficio prevenzione infortuni Dipartimento prevenzione asl viterbo
Dipartimento prevenzione asl viterbo Forum prevenzione incendi
Forum prevenzione incendi L'esperienza delle cose moderne e la lezione delle antique
L'esperienza delle cose moderne e la lezione delle antique Esperienza delle cose moderne e la lezione delle antique
Esperienza delle cose moderne e la lezione delle antique La nascita delle lingue e delle letterature romanze
La nascita delle lingue e delle letterature romanze Investigación epidemiológica de campo
Investigación epidemiológica de campo Epidemiologia clinica
Epidemiologia clinica Nom preeclampsia
Nom preeclampsia Epidemiologia
Epidemiologia Mesangiocapilar
Mesangiocapilar Trascendencia epidemiologia
Trascendencia epidemiologia Epidemiologia laboral
Epidemiologia laboral Epidemiologia
Epidemiologia Epidemiologia
Epidemiologia O que é epidemiologia
O que é epidemiologia Medidas de asociación
Medidas de asociación Autotocne
Autotocne Prevalencia de periodo ejemplo
Prevalencia de periodo ejemplo Ampigenta
Ampigenta Epidemiología analítica
Epidemiología analítica Epidemiología analítica
Epidemiología analítica Parkinson epidemiologia
Parkinson epidemiologia Bulimia n
Bulimia n Vies de aferição
Vies de aferição Que es un factor protector
Que es un factor protector Taenia solium
Taenia solium Medidas de frecuencia en epidemiología
Medidas de frecuencia en epidemiología Odds ratio epidemiologia
Odds ratio epidemiologia Validade interna e externa epidemiologia
Validade interna e externa epidemiologia Epidemiologia clinica
Epidemiologia clinica Tipos de estudos científicos
Tipos de estudos científicos Romero sandoval erika andrea
Romero sandoval erika andrea Ferinan
Ferinan Formula de la incidencia
Formula de la incidencia O que é prevalencia
O que é prevalencia Traguardi per lo sviluppo delle competenze irc
Traguardi per lo sviluppo delle competenze irc Per stirpes v per capita
Per stirpes v per capita 186 282 miles per second into meters per second
186 282 miles per second into meters per second Multās per gentēs et multa per aequora vectus
Multās per gentēs et multa per aequora vectus Coop per te
Coop per te Multas per gentes et multa per aequora vectus
Multas per gentes et multa per aequora vectus Cantico dei cantici una voce il mio diletto
Cantico dei cantici una voce il mio diletto 1/60 of a minute
1/60 of a minute Longum iter est
Longum iter est 4 km + 3 hm + 2 dam =
4 km + 3 hm + 2 dam = Eina per ugni nedega eina per vandeni neskesta
Eina per ugni nedega eina per vandeni neskesta Per capita vs per stirpes
Per capita vs per stirpes Moltiplicazioni con numeri periodici
Moltiplicazioni con numeri periodici Gli ambienti europei
Gli ambienti europei Definizione di prisma
Definizione di prisma Proprietà tecnologiche fusibilità
Proprietà tecnologiche fusibilità Paranoia definizione
Paranoia definizione Definizione turismo unwto
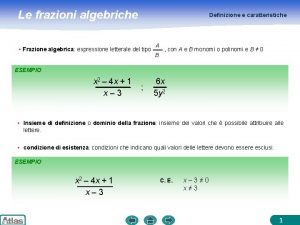
Definizione turismo unwto Semplificazione frazioni algebriche
Semplificazione frazioni algebriche Rescissione
Rescissione Definizione equazione pura
Definizione equazione pura Marketing del targeting
Marketing del targeting Massimi e minimi vincolati definizione
Massimi e minimi vincolati definizione Struttura trasversale nave
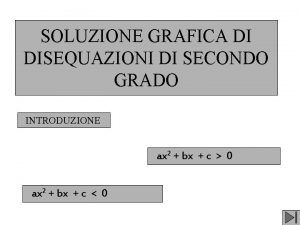
Struttura trasversale nave Risoluzione grafica disequazioni secondo grado
Risoluzione grafica disequazioni secondo grado Esterocezione e interocezione
Esterocezione e interocezione Category management definizione
Category management definizione Etnocentrismo definizione
Etnocentrismo definizione Lembo di dufourmentel
Lembo di dufourmentel Definizione di arrhenius
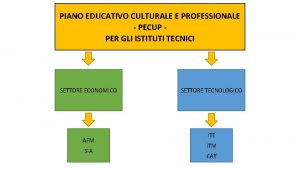
Definizione di arrhenius Pecup definizione
Pecup definizione Sali poco solubili tabella
Sali poco solubili tabella Planos de guedel
Planos de guedel Definizione di insieme matematico
Definizione di insieme matematico Statistica cosa studia
Statistica cosa studia Coping definizione
Coping definizione Ingegnere definizione
Ingegnere definizione Numeri relativi definizione
Numeri relativi definizione Disoccupazione frizionale definizione
Disoccupazione frizionale definizione Luogo geometrico definizione
Luogo geometrico definizione Potenza elettrica definizione
Potenza elettrica definizione Business intelligence knowledge management
Business intelligence knowledge management La moneta definizione
La moneta definizione Ossigeno numero ossidazione
Ossigeno numero ossidazione Poligoni irregolari definizione
Poligoni irregolari definizione Factoring notes algebra 1
Factoring notes algebra 1 Sessadecimale a centesimale
Sessadecimale a centesimale Musica pop definizione
Musica pop definizione Esempi grandezze direttamente proporzionali
Esempi grandezze direttamente proporzionali Problemi con le frazioni risolti
Problemi con le frazioni risolti Angoloide definizione
Angoloide definizione Selezione clonale vite
Selezione clonale vite Sistema informativo aziendale definizione
Sistema informativo aziendale definizione Isometrie
Isometrie Come si calcola massa molecolare
Come si calcola massa molecolare Asse di simmetria parabola
Asse di simmetria parabola Teoria della detenzione del segnale
Teoria della detenzione del segnale Momento d'inerzia quadrato
Momento d'inerzia quadrato Private equity definizione
Private equity definizione Personalita definizione
Personalita definizione Un programma è un insieme di
Un programma è un insieme di Valori mobiliari definizione
Valori mobiliari definizione Polinomi e monomi
Polinomi e monomi Mobilizzazione atraumatica
Mobilizzazione atraumatica Sistema di disequazioni lineari
Sistema di disequazioni lineari Scienze umane cos'è
Scienze umane cos'è Formule inverse corona circolare
Formule inverse corona circolare Poligoni irregolari immagini
Poligoni irregolari immagini Definizione di angoli
Definizione di angoli Mcd definizione
Mcd definizione Rangeability definizione
Rangeability definizione Definizione di bene pubblico
Definizione di bene pubblico Energia meccanica scuola primaria
Energia meccanica scuola primaria Definizione rette perpendicolari
Definizione rette perpendicolari Arrhenius acido
Arrhenius acido Esempio di risk management plan
Esempio di risk management plan Definizione di informazione
Definizione di informazione Sport integrato definizione
Sport integrato definizione Enti fondamentali della geometria
Enti fondamentali della geometria Definizione di numeri decimali
Definizione di numeri decimali Trasformare frazioni apparenti in numeri naturali
Trasformare frazioni apparenti in numeri naturali Multicomponenziale
Multicomponenziale Euclide biografia
Euclide biografia Assonometria isometrica misure
Assonometria isometrica misure Definizione di autoefficacia
Definizione di autoefficacia Adhocrazia esempio
Adhocrazia esempio Maturity factoring definizione
Maturity factoring definizione Definizione numeri interi
Definizione numeri interi Teorema delle probabilità composte
Teorema delle probabilità composte Walter lorenz
Walter lorenz Frazioni equivalenti definizione
Frazioni equivalenti definizione Escatologia definizione
Escatologia definizione Trauma emicostato significato
Trauma emicostato significato Oscilloscopio definizione
Oscilloscopio definizione Glomerulosclerosi definizione
Glomerulosclerosi definizione Stile cognitivo definizione
Stile cognitivo definizione Definizione di competenza
Definizione di competenza Misurare una grandezza significa
Misurare una grandezza significa Concetto di primitiva
Concetto di primitiva Equazioni incomplete pure
Equazioni incomplete pure Piede neuropatico immagini
Piede neuropatico immagini House organ significato
House organ significato Definizione di agente chimico
Definizione di agente chimico Teorema di fattorizzazione
Teorema di fattorizzazione Economie di scala esempio
Economie di scala esempio Uni cei env 13005
Uni cei env 13005 Percezione sincretica
Percezione sincretica I complementi avverbiali
I complementi avverbiali Come si risolve equazione pura
Come si risolve equazione pura Learning by doing definizione
Learning by doing definizione Definizione di informazione in informatica
Definizione di informazione in informatica Principio di le chatelier
Principio di le chatelier Avverbi
Avverbi Bunsen fiamma ossidante e riducente
Bunsen fiamma ossidante e riducente Prodotto della somma di due monomi per la loro differenza
Prodotto della somma di due monomi per la loro differenza Enti primitivi definizione
Enti primitivi definizione Controdado antisvitamento
Controdado antisvitamento Tax smoothing definizione
Tax smoothing definizione Il romanzo greco
Il romanzo greco Veicolo isolato
Veicolo isolato Asse di simmetria della parabola
Asse di simmetria della parabola